高效液相色谱法测定分析原料药氟胞嘧啶中有关物质的方法验证
(精华制药集团南通有限公司,江苏南通 226407)
5-氟胞嘧啶(5-Flμcylosine) (简称5-FC),化学名为4-氨基-5-氟-2(1H)-嘧啶酮,对隐球菌属和念珠菌属等具有较高抗菌活性,对着色真菌、少数曲霉菌属有一定抗菌活性,其抗菌作用在临床上得到广泛应用,其药用机制是替代尿嘧啶进入DNA 分子中,阻断核酸合成,也是抗癌原料药卡培他滨、氟西他滨关键中间体[1]。
5-氟胞嘧啶的杂质控制方法在中国药典中已有摘录,但应对国外市场,必须符合欧洲以及美国药典的要求。为此,本实验室为更好地控制产品质量,在中国药典的基础上,结合欧洲及美国药典的要求,对测试方法进行了专题研究和一定程度的优化。
1 探讨与分析
1.1 检测方法的选择
美国药典采用薄层色谱法(TLC)检测5-氟胞嘧啶的有关物质,中国药典和欧洲药典都采用高效液相色谱法(High Performance Liquid Chromatography HPLC)检测5-氟胞嘧啶的有关物质。高效液相色谱法用作定量分析时,较薄层色谱法更为准确,且精确度和灵敏度高。因此,选择HPLC 测定5-氟胞嘧啶的有关物质。
1.2 流动相的选择
为选取最优的流动相体系,分别考察了中国药典方法流动相A(甲醇-水)、欧洲药典方法流动相B(甲醇-磷酸二氢钾水溶液)、流动相C(甲醇-磷酸二氢钠水溶液)3 种流动相体系,在同一浓度下进行峰面积比较。结果表明,当选取流动相C 时,其灵敏度和峰形达到最佳,相邻峰之间的分离度较好,因此最终选择流动相C 作为最优流动相体系。
1.3 检测波长的确定
为选取最合适的检测波长,用加有杂质的氟胞嘧啶溶液在200 ~ 380 nm 进行波长扫描。测试结果表明,在260 nm 处,氟胞嘧啶和其杂质均有较大吸收,故选择260 nm 作为检测波长。
2 改进后的方法学验证
2.1 验证参数
专属性、重复性、中间精密度、准确度、检出限、定量限、线性范围、耐用性[2-5]。
2.2 仪器与试剂
岛津LC-20AT 高效液相色谱仪及Labsolution CS工作站、色谱柱C18(4.6×250 mm×5μm)、氟胞嘧啶标准品(R03100)、氟尿嘧啶标准品(R009T0)、氟胞嘧啶原料药(自制)等。甲醇为色谱纯,其余试剂为分析纯。
2.3 色谱条件
流动相:称取2.72 g 磷酸二氢钠溶于1 800 mL纯化水中,用磷酸调节pH 至3.0,然后加入一定量的甲醇,使溶液的甲醇浓度为5%,用0.45μm 过滤膜过滤,脱气即得。流速0.8 mL/min,检测波长260 nm,进样量20 μL,柱温25 ℃。
进样次序:第一针进空白,接着进系统适应性试液、氟尿嘧啶对照液、标准溶液稀释液各一针,然后进五针标准液(第一份),再进一针标准液(第二份),再进两针平行样品,最后再进一针标准液(第一份)。连续进样品的针数不得超过十针,超过十针需每十针间隔进一针标准液(第一份)。标准液(第二份)用于计算回收率。
系统适应性要求:重复进6 针标准溶液,在所得的色谱图中,要求6 针标准溶液氟胞嘧啶峰面积的RSD ≤2.0%,系统适应性溶液中氟胞嘧啶与氟尿嘧啶的分离度R≥2。按照外标法以峰面积进行计算,即得含量。
2.4 样品与对照制备
2.4.1 标准对照溶液配置
标准溶液:准确称取10 mg 氟胞嘧啶标准品于100 mL 容量瓶中,加入80 mL 水,用超声波完全溶解后定容。
标准溶液稀释液:精密吸取1 mL 标准溶液用超纯水稀释至100 mL,再吸取1 mL 前溶液用超纯水稀释至10 mL。
氟尿嘧啶对照液:精密称取取氟尿嘧啶标准品10 mg,加超纯水使溶解成200 mL,准确吸取该溶液1.0 mL 稀释至100 mL,再准确吸取稀释液 1.0 mL 稀释至 10 mL,即得。
加杂测试液:准确称取10 mg 样品于100 mL 容量瓶中,加入100 μL 氟尿嘧啶对照液中配制过程中的0.05 mg/mL 的高浓度溶液,加适量的水超声溶解后定容。
2.4.2 样品测试溶液
准确称取10 mg 样品于100 mL 容量瓶中,加入80 mL 水,用超声波完全溶解后定容,即得。
3 实验结果
3.1 专属性
将氟尿嘧啶对照液、标准溶液稀释液、系统适应性溶液、标准溶液、样品测试溶液、加杂测试液,分别进样。检测结果见表1。

表1 专属性的检测结果Tab.1 Test results of specificity
对比所测试的每张色谱图,样品、杂质、对照的出峰时间没有重叠或交叉,且峰型近似于对称形正态分布曲线,不拖尾,不前伸。样品溶液中氟胞嘧啶与相邻杂质峰分离度为10.01,系统适应性溶液中氟胞嘧啶与氟尿嘧啶的分离度为10.13。测试结果表明空白溶剂不干扰本品的有关物质的检查,样品对杂质出峰无干扰,各峰之间能有效分离,该方法专属性强。
3.2 重复性
分别配制6 份标准溶液,每份各进样1 针,六次测定的氟胞嘧啶峰面积RSD 为0.02%。
分别配制6 份加杂测试溶液,每份溶液进样1针,用氟尿嘧啶对照液中氟尿嘧啶的峰面积计算杂质的回收率,六次测定主峰氟胞嘧啶平均回收率为101.03%,回收率的相对标准偏差RSD 为0.01%;杂质氟尿嘧啶平均回收率为100.66%;回收率的相对标准偏差RSD 为0.31%。从该项测试的RSD 结果可知,该方法具有良好的重复性。
3.3 中间精密度
由不同的分析员在不同的时间用另外一台仪器,按照重复性项的方法进行测试。两组12 次测定结果,杂质氟尿嘧啶平均回收率为102.12%,回收率相对标准偏差RSD 为1.66%;氟胞嘧啶平均回收率为101.50%,回收率相对标准偏差RSD 为0.48%;证实该方法中间精密度良好。
3.4 检出限
在选定的色谱条件下,以信噪比(S/N)约为3时相应的试样浓度来确定,杂质氟尿嘧啶的检出限为0.003 5 μg/mL,氟胞嘧啶的检出限为0.007 0 μg/mL。
3.5 定量限
把已知浓度样品溶液稀释到低浓度的试样,测出的信号与空白处的信号(基线噪音)进行比较,算出能被可靠检测出的最低浓度或百分比。以信噪比(S/N)约为10 时相应的试样浓度来确定,杂质氟尿嘧啶定量限为0.01 μg/mL,氟胞嘧啶定量限为0.02 μg/ mL。
3.6 线性及范围
在LOQ 浓度至不低于120%指标浓度的范围内取6 个浓度点进行研究。线性关系以测得的响应信号(峰面积)对被分析物浓度的函数作图,用最小二乘法进行线性回归,要求线性相关系数r≥0.996。测得杂质氟尿嘧啶线性回归方程y= 84 059x+ 13.206,相关系数r= 0.999 9(见图1);测得氟胞嘧啶线性回归方程y= 48 522x+ 17.194,相关系数r= 0.999 8(见图2)。测试结果表明,杂质氟尿嘧啶质量浓度在0.01 ~ 0.06 μg/mL 范围内,氟胞嘧啶质量浓度在0.02 ~ 0.12 μg/mL 范围内,具有良好的线性关系。
3.7 准确度
准确度测定:加入浓度为样品配置浓度,检出浓度为样品通过液相色谱检测出峰面积然后换算成浓度,回收率=检出浓度/加样浓度×100%。
在不含氟胞嘧啶的空白溶剂(超纯水)中,加入氟胞嘧啶标准品,配置成标准溶液浓度的80%、100%、120% 三种溶液,分别进样。测得杂质氟尿嘧啶回收率在99.65%~100.08%,定量限处回收率在99.30%~100.30%,氟胞嘧啶回收率在97.75%~97.91%,定量限处回收率在97.84%~97.87%,符合验证要求。

图1 杂质氟尿嘧啶线性关系图Fig.1 Linear relationship of impurity fluorouracil

图2 氟胞嘧啶线性关系图Fig.2 Linear relationship of fluorocytosine
测试结果表明,此方法测得的结果与真实值之间较为接近,且在同一水平浓度上有较高的精确度,该测试方法准确度高。检测结果见表2、表3。
3.8 耐用性的测定
3.8.1 溶液的稳定性
通过配制标准溶液、样品测试溶液、加杂测试溶液,在自然常温环境下,将容量瓶中的溶液放置0 h、8 h、12 h、24 h 和48 h 后进行测试,计算峰面积RSD。测试结果(见表4),供试品溶液在自然常温条件下放置48 h 内稳定性良好。
3.8.2 流速的影响
配制加杂测试溶液,在不改变其他色谱条件的前提下,分别设定流动相流速为0.7 mL/min、0.8 mL/ min、0.9 mL/min,评估测定条件参数微小变动时,主峰氟胞嘧啶和杂质氟尿嘧啶峰面积的回收率。测试结果(见表5)表明,三种流速下对样品的测试结果影响不大。

表2 杂质氟尿嘧啶准确度的测试结果Tab.2 Test results of accuracy of impurity fluorouracil

表3 氟胞嘧啶准确度的测试结果Tab.3 Test results of accuracy of fluorocytosine

表4 溶液的稳定性测试结果Tab.4 Stability test results of solution
3.8.3 柱温的影响
配制加杂测试溶液,在不改变其他色谱条件的前提下,分别设定色谱柱温度为23 ℃;25 ℃;27 ℃分析,评估测定条件参数微小变动时,主峰氟胞嘧啶和杂质氟尿嘧啶峰面积的回收率。测试结果(见表6)表明,柱温在23 ~ 27 ℃范围内,对样品的测试结果影响不大。

表5 流速对测试结果的影响Tab.5 Effect of flow rate on test results

表6 柱温对测试结果的影响Tab.6 Effect of column temperature on test results
3.8.4 色谱柱的影响
配制加杂测试溶液,在不改变其他色谱条件的前提下,分别采用同一生产商两个不同批号的色谱柱分析,评估测定条件参数微小变动时,主峰氟胞嘧啶和杂质氟尿嘧啶峰面积的回收率。测试结果(见表7)表明,同一生产商不同批号的色谱柱对样品的测试结果影响不大。
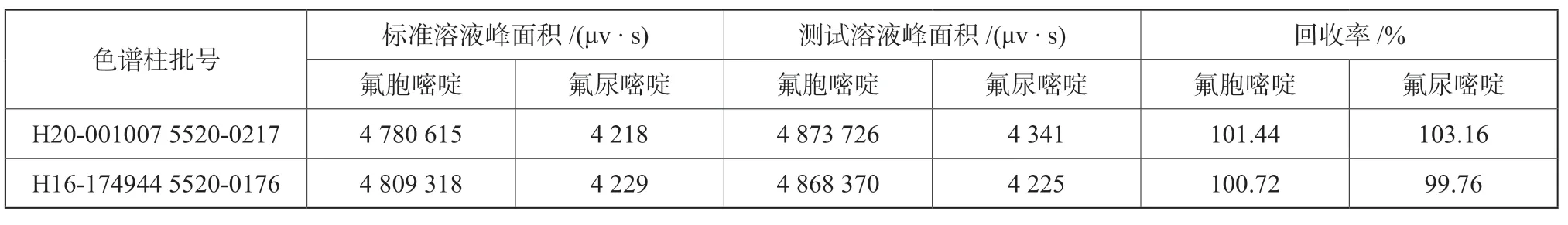
表7 色谱柱对测试结果的影响Tab.7 Influence of chromatographic column on test results
3.8.5 流动相pH 值的影响
配制加杂测试溶液,在不改变其他色谱条件的前提下,调节流动相的pH 值分别为2.8、3.0、3.2,评估测定条件参数微小变动时,主峰氟胞嘧啶和杂质氟尿嘧啶峰面积的回收率。测试结果(见表8)表明,流动相pH 值在2.8 ~ 3.2 范围内,对样品的测试结果影响不大。

表8 流动相pH 值对测试结果的影响Tab.8 Influence of pH value of mobile phase on test results
3.9 样品测试
分别称取FLC2020001、FLC2020002、FLC2020003 三个批号的样品进行测试,结果显示该三批样品中杂质氟尿嘧啶和未知杂质均未检出。
4 结论
本文对现有5-氟胞嘧啶中有关物质的质量控制方法进行了研究与探讨,建立了更为严格、准确的检测方法,即在本实验室确立的条件下,采用高效液相色谱法测定氟胞嘧啶中的有关物质,并对线性试验、精密度试验、准确度试验、耐用性试验进行方法验证。
测试结果表明空白溶剂不干扰本品的有关物质的检查,样品对杂质出峰无干扰,样品溶液中氟胞嘧啶与相邻杂质峰分离度为10.01,专属性强。重复性项下的测试结果RSD 为0.02%。中间精密度项下,杂质氟尿嘧啶平均回收率为102.12%,RSD 为1.66%;氟胞嘧啶平均回收率为101.50%,RSD 为0.48%。杂质氟尿嘧啶的检出限为0.003 5 μg/mL,氟胞嘧啶的检出限为0.007 0 μg/mL。杂质氟尿嘧啶定量限为0.01 μg/mL,氟胞嘧啶定量限为0.02 μg/mL。杂质氟尿嘧啶质量浓度在0.01 ~ 0.06 μg/mL,氟胞嘧啶质量浓度在0.02 ~ 0.12 μg/mL,具有良好的线性关系。耐用性测试结果表明,样品溶液在自然常温条件下放置48 h 内稳定性良好;流动相流速为(0.8 ± 0.1) mL/ min、色谱柱温度为(25 ± 2) ℃、流动相pH 值为2.8 ~ 3.2,对样品的测试结果影响不大。表明该控制方法重复性好,专属性强,检测结果准确、可控,可以有效控制该产品的质量。

