R-EBUS和VBN联合ROSE诊断肺外周病变对医疗资源消耗的影响
吴智,洪彩霞,叶煜铭,汪铁柱,胡妙芬
(福建医科大学附属漳州市医院,福建 漳州 363000)
肺部外周型病变在气管镜检查时无法进行直视下活组织检查(以下简称活检),导致诊断阳性率存在波动,首次活检阴性的情况下再次气管镜活检阳性率也低,经常需要采用其他方法进行2~3次活检,导致患者确诊时间延长,医疗资源消耗增多,也更容易产生医疗纠纷。目前肺癌进入靶向及免疫治疗时代,随着二代基因检测(NGS)等技术的开展,感染性病变也即将进入精准治疗时代,组织样本能否进行分子基因检测对临床医生极为重要。经气管镜肺活检及经皮肺穿刺是目前最常用的两种方案。在取样组织体积及阳性率方面,经皮肺穿刺活检具有一定的优势,但大咯血、气胸及活检后转移的风险相对较大,所以经气管镜肺活检技术仍然非常重要。如何在保证活检阳性率的基础上缩短确诊时间、减少医疗资源消耗成为临床医生极为关注的问题。本研究针对无法应用气管镜进行直视下活检的肺外周型病变,在环形超声支气管镜(R-EBUS)和虚拟导航(VBN)基础上联合快速现场检测技术(ROSE)对活检阳性率、首次活检至确诊医疗费用、首次活检至确诊时间进行对比,报告如下。
1 资料与方法
1.1 一般资料
选择2018年11月—2019年3月我院经胸部CT确诊的100 例肺外周型病变患者,采用随机数字表法,将组号及随机数字装进信封进行随机化隐匿,分为观察组(联合ROSE)和对照组(非ROSE),每组50 例。
1.2 纳入及排除标准
纳入标准:胸部CT显示病变为肺外周型,位于胸腔的外1/3,支气管镜下无法直视观察到病灶;术前完善凝血时间、心电图、血常规、肺功能、血气分析等检查,胸部增强CT排除血管瘤,无相关禁忌证;患者及其家属同意气管镜检查,术前签署知情同意书。排除标准:气管镜下可直视病灶;术前未完善胸部增强CT;纯磨玻璃性结节;伴有并发症:3 个月内发生的心肌梗死、不稳定心绞痛、严重心律失常、急性心力衰竭、气胸、重症哮喘、大咯血、呼吸衰竭;存在凝血功能障碍;孕妇;不能配合气管镜操作或因其他原因不能耐受检查者;考虑气管镜肺活检阳性率低,可采取CT引导下经皮肺穿刺或者行淋巴结等其他远处转移病灶活检确诊。
1.3 仪器与方法
观察组:常规检查各个段级支气管后,将支气管镜退至气管下段水平,根据虚拟电子导航系统引导气管镜到达目标部位,卡住管腔后注入1:10 000去甲肾上腺素,收缩远端气道黏膜,减少出血。将超声探头送入检查部位,进入远端后开启超声探头,探查到异常回声后评估病灶径向长度。将探头固定在最佳成像位置,然后使用定位卡扣定位,固定气管镜位置,抽出探头,根据定位卡扣确定刷检及活检深度后进行刷检,来回抽刷5次,将刷检成分涂片,立即进行ROSE检查。过程如下:如ROSE阳性,即在该部位活检4~5块肺组织。如初次ROSE为阴性,但超声显像见软组织回声明显,则于同一部位进行再次刷检和ROSE检查;如初始部位连续三次ROSE结果均为阴性,则用R-EBUS在可能性大的其他管腔部位进行探查,如均未探及异常图像,则仍在首次刷检部位活检4~5块肺组织;如在其他管腔部位探及异常图像,则更换毛刷在新的管腔部位进行刷检和再次ROSE检查。如果新的管腔部位ROSE为阳性,则于该阳性部位进行活检;如新的管腔部位ROSE仍为阴性,则选择在R-EBUS成像最佳部位活检4~5块肺组织。如多次R-EBUS探查未见异常,则按导航部位采取盲检,行刷检及活检,并行ROSE检查。对照组:R-EBUS探查后直接刷检涂片,然后活检4~5块肺组织;如R-EBUS探查未见异常,则按导航采取盲检,行刷检及活检。ROSE由同一位经验丰富的细胞学医师处理。
1.4 观察指标
ROSE阳性判断标准:ROSE见到癌细胞或高度核异质细胞;影像学考虑炎症,ROSE见到中性粒细胞,经抗感染治疗后病灶吸收;影像学考虑炎症,ROSE见到淋巴细胞等炎症细胞,经穿刺、手术病理等与ROSE特点相符。ROSE假阴性判断标准:ROSE未见到癌细胞或高度核异质细胞,经术后病理或二次活检证实为肿瘤;ROSE见到炎症细胞,病灶经抗感染无法吸收或经过其他方法确诊后与ROSE特点不相符。首次活检至确诊时间定义:从开始行气管镜检查之日起计算。如ROSE见到肿瘤细胞,确诊时间计为1天;如ROSE为非特异性改变,则至确诊之日为止(比如经术后病理或二次活检确诊肿瘤,经治疗后或其他相关检查诊断为炎症)。
1.5 统计学方法
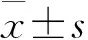
2 结 果
两组临床基本特征比较差异无统计学意义(见表1)。观察组50 例,诊断阳性率84.00%(42/50),对照组50 例,诊断阳性率74.00%(37/50),两组诊断活检阳性率比较,差异有统计学意义(χ2=8.7,P<0.05)。观察组首次活检至确诊医疗费用为1 425.75 元,首次活检至确诊时间为(3.84±4.28)d。对照组首次活检至确诊医疗费用为5 162.00元,首次活检至确诊时间(6.46±3.66)d。两组医疗费用及首次活检至确诊时间比较,差异有统计学意义(P<0.05)。虽然在直径≤3 cm占位患者中两组刷检、活检及整体阳性率比较差异无统计学意义,但直径>3 cm占位患者中两组刷检及整体阳性率比较差异有统计学意义(P<0.05)(见表2)。提示联合ROSE可以提高VBN和R-EBUS对肺外周病灶的诊断阳性率,降低医疗费用,缩短确诊时间。

表1 两组患者临床基本特征的分析结果
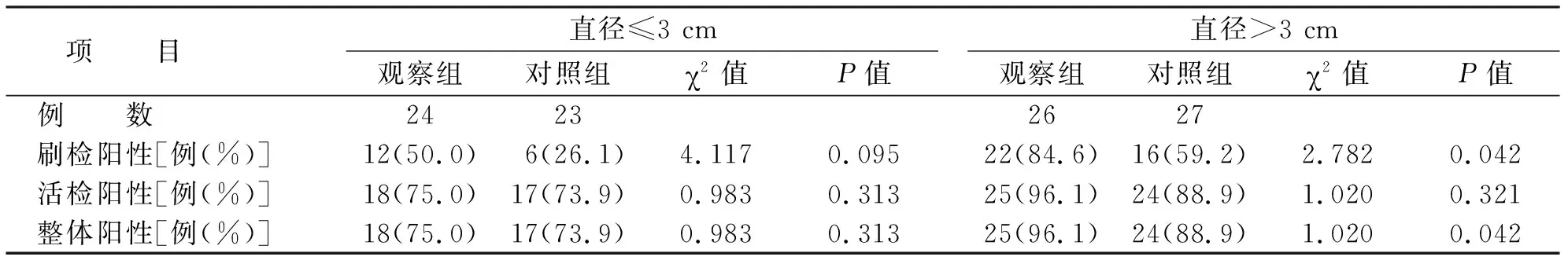
表2 ROSE在直径≤3 cm及>3 cm占位患者中的阳性率比较
3 讨 论
缩短住院时间、降低医疗费用是目前医疗的一个发展趋势,而肺癌是目前我国发病率最高的恶性肿瘤,病死率居恶性肿瘤的首位[1]。呼吸科、胸外科、肿瘤科住院患者中,肺癌患者占比较大,如何应用有限的医疗资源为更多的患者服务是目前研究的方向。目前肺活检方法主要是气管镜活检或经皮肺穿刺活检。经皮肺穿刺阳性率可达74%~98%[2-4],但存在较大的气胸发生率(9%~44%)[5-8],且需要在彩超或CT辅助下实施,需占用一定的医疗资源。因此,气管镜活检的诊断地位不可替代。外周型病灶气管镜活检的经典办法是透视下活检,对于直径2.0~4.0 cm的病灶活检阳性率可达73.2%,但对于直径<2.0 cm的病灶阳性率降至60.0%[9],且操作者和患者均需暴露于X射线下,病灶越小,操作时间越长,射线暴露剂量越大,目前已逐步被大部分医院淘汰。新引导技术的出现在保证阳性率的同时解决了暴露射线的问题,R-EBUS联合经支气管镜肺活检(TBLB)阳性率可达66.7%~77.0%[10-11]。如果联合虚拟导航技术,直径<2.0 cm病灶阳性率可达81.1%,直径2~3 cm的病灶阳性率可达83.3%[12]。单用电磁导航技术的阳性率大约为59%,如果联合R-EBUS,阳性率可达到88%[13],但电磁导航设备极为昂贵,目前拥有这项技术的医院不多,难以在基层广泛开展。因此如何高效率地活检、减少二次活检次数、缩短确诊时间成为临床医生极为关注的问题。基于引导鞘(GS)在很多地区为非医保耗材,R-EBUS和VBN应用经济成本及技术难度门槛相对不高,大多数医院开展难度不大等特点,本研究探讨在不使用引导鞘(GS)的情况下,应用R-EBUS和VBN联合ROSE的医疗经济学意义。
本研究提示应用ROSE技术能够提高肺外周病灶活检阳性率,与Steinfort等[14]和Chen等[15]进行的R-EBUS联合ROSE的前瞻性队列研究及随机对照研究结论一致。龙发等[16]对R-EBUS联合刷检现场细胞学的前瞻性研究提示,不论直径≤3 cm或者>3 cm的病灶,刷检联合ROSE的诊断阳性率与联合活检总阳性率对比差异无统计学意义,但该研究并未设置对照组。本研究在设置随机对照的同时对比ROSE技术的介入对不同直径病灶诊断阳性率的差异,ROSE组诊断阳性率虽明显高于对照组,但仅直径>3 cm组的刷检阳性率及整体阳性诊断率比较差异有统计学意义,考虑可能与入组病例相对较少有关。Asano等[17]对VBN联合R-EBUS及X线透视对直径<2 cm的外周型肺结节的诊断阳性率进行研究,结果提示联合VBN可将诊断阳性率提升至67.4%,而本研究提示对于外周肺结节,ROSE联合VBN和R-EBUS对直径<3 cm病灶活检的阳性率为75.00%,提示VBN联合ROSE有可能进一步提升诊断阳性率。本研究因入组病例数较少,进一步分VBN组及非VBN组后可能导致亚组病例数进一步减少,分析时偏倚过大,故未进一步分组,期待以后的研究加大入组病例数进一步进行亚组分析。
在保证阳性率的同时应用ROSE技术可以缩短首次活检至确诊时间,考虑原因如下。第一,我院细胞学检查回报时间为3个工作日,活检病理回报时间为5个工作日,ROSE阳性可立即确诊;第二,在活检阴性的情况下需二次活检或进行手术冰冻检查,时间一般增加5~7 d,而观察组的整体活检阳性率高于对照组,因此ROSE组需进行二次活检或进行手术的病例数降低,导致总体确诊时间缩短。目前检索到的关于ROSE对首次活检至确诊时间影响程度的相关文献较少,未来可通过增加样本量及更严谨的研究设计来进一步验证结论。目前针对ROSE费用方面的研究主要是单次检查的病理诊断费用[18],但差异仅100余元,对医疗资源的影响不大。本研究针对首次活检至确诊医疗费用进行分析,提示ROSE技术可以减少医疗费用,原因可能为:观察组的整体活检阳性率高于对照组,因此需进行二次活检或手术的病例数降低,从而降低费用;部分肺炎型肺癌病例,当刷检结果阳性后可减少不必要的抗感染治疗,减少费用;确诊时间缩短,可降低住院费。
R-EBUS联合VBN的经济成本及技术难度门槛相对不高。R-EBUS和VBN联合ROSE在保证检查阳性率的基础上可以缩短确诊时间,降低医疗费用,可在大多数医院开展。

