星状神经节阻滞对慢性心力衰竭病人肾上腺素能受体表达及临床效果的影响
黄晓莉,郝君锋
心力衰竭抑制是医学领域研究的重点,病人可因心脏收缩能力不全引起一系列临床表现,且随着病程的延长导致心脏结构异常[1]。心室重构发生后,可对病人心功能造成严重负面影响,为多种心血管疾病晚期最常见症状,也是导致病人死亡的主要原因[2]。心力衰竭病人随着病程的进展,其可作为脱离诱因的独立疾病而导致机体出现病理生理改变。治疗上,多以药物控制临床症状,延缓疾病进展为主,如强心、利尿、扩血管、药物等,同时还应维持血糖、血压稳定,降低血脂等处理,虽然以上药物治疗具有一定临床意义但病死率仍较高[3]。
目前针对慢性心力衰竭的药物选择多种,且各有临床优势,但长期应用药物不良反应与药物治疗后耐受性不容忽视[4]。星状神经节症状主要是针对颈胸部交感神经节使用局部刺激,具有一定的抑制交感活性传导,扩张心脑血管的作用[5]。本研究探讨左侧星状神经节阻滞对慢性心力衰竭病人肾上腺素能受体表达及临床效果的影响。
1 资料与方法
1.1 临床资料 选取2016年6月—2018年6月西安市中医医院收治的慢性心力衰竭病人80例为研究对象,以2015年中华医学会关于慢性心力衰竭的诊治指南为标准,入组前签署入组同意书,并申报医院伦理委员会批准,纽约心功能分级在Ⅲ级以上,血浆心房脑钠肽(BNP)水平超过500 pg/L,年龄>60岁。排除标准:存在肝肾功能不全、明确精神异常、肺部感染、免疫系统疾病、缺血性脑卒中,文化程度为文盲,听力和语言表达能力障碍者。按照随机数字表法分为两组。观察组40例,男21例,女19例;年龄60~79(69.1±3.1)岁;病程3~13(6.1±0.5)年;合并高血压30例,糖尿病19例,慢性阻塞性肺疾病18例,高脂血症23例。对照组40例,男20例,女20;年龄60~79(69.2±3.2)岁;病程3~14(6.0±0.5)年;合并高血压31例,糖尿病18例,慢性阻塞性肺疾病19例,高脂血症24例。两组性别、年龄、病程及合并常见内科疾病等比较差异无统计学意义(P>0.05)。
1.2 方法 对照组给予药物强心、利尿及扩血管治疗,维持血压、血糖稳定,定时吸氧,适当锻炼,调节饮食、加强心理调节,对症支持处理。观察组实施超声引导下左侧星状神经节阻滞,每间隔2 d行1次,连续5次为1个疗程。操作方法:开放静脉通道行持续心电监护,选择左侧颈部穿刺,病人取仰卧位,肩下稍垫高,头偏向对侧。应用索诺声MicroMaxx P17型超声引导(探头频率8~13 MHz),定位胸部第C6神经根及其横突基底部,明确颈长肌、颈动静脉位置,操作时避开甲状腺和气管,采用平面内穿刺进针,针尖到达颈长肌前方星状神经节位置,回抽无血及脑脊液,注入0.2%罗哌卡因5 mL,嘱病人卧床休息15 min,以出现霍纳综合征、超声提示头面部皮肤血流增加≥50%、皮肤温度升高≥34 ℃为穿刺成功标准。
1.3 观察指标 比较两组干预前后血清α受体蛋白和β受体蛋白水平、心脏彩色多普勒超声指标变化情况,统计两组干预过程中出现的并发症及救治成功率,分析干预过程中BNP水平变化趋势,且随访1年,统计两组生存情况。
1.4 评定标准 ①肾上腺受体水平检测以实时荧光定量PCR法进行,先提取1 pg总量的目标RNA,依据所使用试剂盒严格按照操作说明进行反转录,获取cDNA,随后采用实时荧光定量PCR仪针对目标蛋白(α受体蛋白及β受体蛋白)进行定量分析。实验条件与步骤分别为95 ℃ 5 min,95 ℃ 30 s,55 ℃ 30 s,72 ℃ 20 s,所有操作均由具有5年以上实验室操作经验医师严格按照试剂说明书进行,定量水平为连续测定3次取平均值。②心脏彩色多普勒超声指标:左心室舒张末期内径(LVEDD)、左心室收缩末期内径(LVESD)、左室射血分数(LVEF)。③并发症主要包括:室性心律失常、房室传导阻滞、低血压及心肌梗死发生情况。④BNP水平正常值为≤200 pg/mL,如≥500 pg/mL提示心力衰竭。
2 结 果
2.1 两组干预前后血清α受体蛋白和β受体蛋白水平比较 干预前两组α受体蛋白表达量和β受体蛋白表达量比较差异无统计学意义(P>0.05);干预后两组α受体蛋白表达量和β受体蛋白表达量均较干预前差异有统计学意义(P<0.05),且干预后观察组α受体蛋白表达量和β受体蛋白表达量与对照组比较差异有统计学意义(P<0.05)。详见表1。
表1 两组干预前后血清α受体蛋白和β受体蛋白水平比较(±s) 单位: ng/L
2.2 两组干预前后心脏彩色多普勒超声指标比较 干预前两组LVEDD、LVESD及LVEF水平比较差异无统计学意义(P>0.05);干预后两组LVEDD和LVESD水平低于干预前(P<0.05),LVEF水平高于干预前(P<0.05),且干预后观察组LVEDD和LVESD水平低于对照组(P<0.05),LVEF水平高于对照组(P<0.05)。详见表2。
表2 两组干预前后心脏彩色多普勒超声指标比较(±s)
2.3 两组干预过程中BNP水平变化趋势 两组干预前BNP水平比较差异无统计学意义(P>0.05);干预后1 d、干预后10 d及随访1个月时,观察组BNP水平均低于同期对照组(P<0.05)。详见表3。
表3 两组干预过程中BNP水平变化趋势(±s) 单位: pg/mL
2.4 两组干预过程中并发症及救治成功率比较 干预过程中观察组发生室性心律失常、房室传导阻滞、低血压及心肌梗死比例均低于对照组(P<0.05),救治成功率高于对照组(P<0.05)。详见表4。
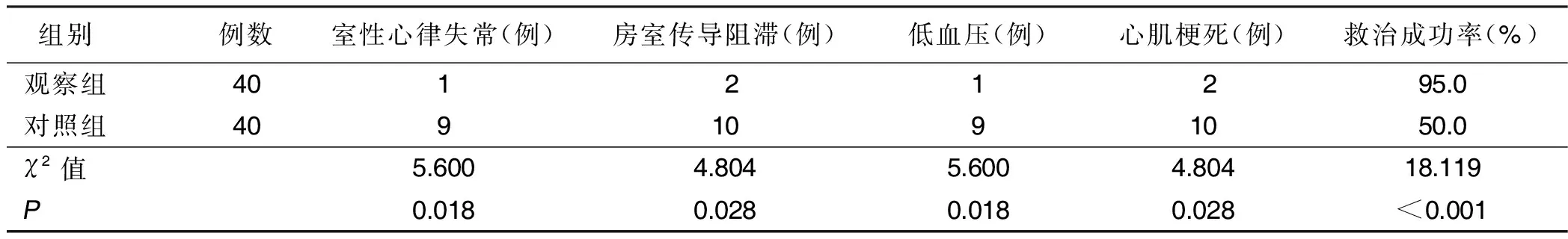
表4 两组干预过程中出现的并发症及救治成功率比较
2.5 两组随访1年生存时间比较 观察组生存36例(90.0%),对照组生存19例(47.5%)。两组1年生存曲线见图1。
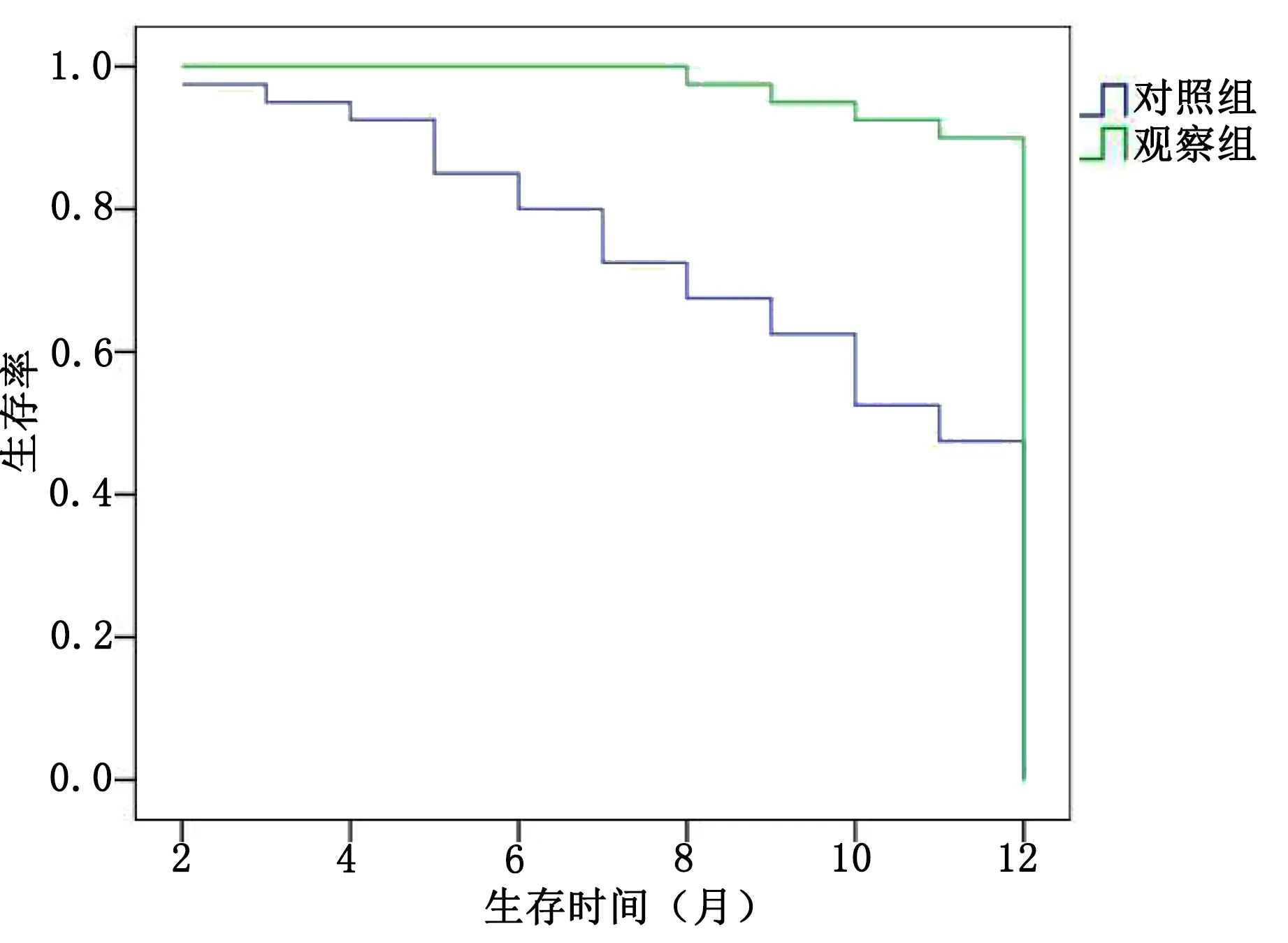
图1 两组1年生存曲线
3 讨 论
慢性心力衰竭为多种心血管疾病中晚期表现,研究提示其病理生理变化以心交感系统兴奋增高,导致大量儿茶酚胺类激素分泌与活性增高为主[6]。病人存在心肌负担加重、能量代谢紊乱、自律性伸缩性减弱等[7]。如合并心肌氧耗量增加,则可导致心肌细胞损伤进一步加重,甚至诱发恶性心律失常而导致心搏骤停[8]。病人多存在有支配心脏的交感与副交感神经水平功能失衡,冠状动脉阻力增高、心肌灌注不足、血小板活性增强、钙离子超载、血栓形成风险加大[9]。针对慢性心力衰竭,降低交感活性对改善心室功能,治疗心力衰竭有重要价值。星状神经节阻滞能有效地抑制心交感活性,降低心脏前后负荷,对改善冠状动脉血供,抑制心室重构均有一定价值[10]。
本研究针对慢性心力衰竭病人,对照组行常规药物等干预,观察组则在对照组基础上联合使用超声引导下左侧星状神经节阻滞治疗方案,比较两组干预前后血清α受体蛋白和β受体蛋白水平发现,干预后两组α受体蛋白表达量和β受体蛋白表达量均较干预前差异有统计学意义,且干预后观察组α受体蛋白表达量和β受体蛋白表达量与对照组差异有统计学意义。提示联合使用超声引导下左侧星状神经节阻滞,可降低体内肾上腺素能受体水平,对降低心脏交感神经支配有一定价值。另外,针对两组干预前后心脏彩色多普勒超声指标比较发现,干预后两组LVEDD和LVESD水平低于干预前,LVEF水平高于干预前,且干预后观察组LVEDD和LVESD水平低于对照组,LVEF水平高于对照组。提示针对慢性心力衰竭联合使用超声引导下左侧星状神经节阻滞,对促进心脏收缩与舒张功能恢复,逆转心室重构有一定价值。同时分析干预过程中BNP水平变化趋势发现,干预后1 d、干预后10 d及随访1个月,观察组BNP水平均低于同期对照组。证明针对慢性心力衰竭,联合使用超声引导下左侧星状神经节阻滞,可更有效地减少心力衰竭导致的心肌损伤,降低体内心力衰竭指标水平。两组干预过程中观察组发生室性心律失常、房室传导阻滞、低血压及心肌梗死比例低于对照组,救治成功率高于对照组。同时随访1年比较两组生存率发现,观察组生存率达到90.0%,对照组生存率仅为47.5%。针对慢性心力衰竭在常规药物治疗基础上联合使用超声引导下左侧星状神经节阻滞,对减少治疗期间并发症,提高救治成功率,延长病人生存时间有重要价值。
本研究中观察组针对慢性心力衰竭病人使用的超声引导下左侧星状神经节阻滞方法,首先可通过调节下丘脑自主神经调控活性[11]、调节肾上腺素能受体活性并减少其分泌[12],同时还可引起颈胸部交感神经支配区血管扩张[13],提高其顺应性,加快心肌相关血管尤其是各冠状动脉血流速度与血流量。抑制脊髓侧角神经元与前角神经元兴奋性,进一步降低交感传出神经纤维活性[14],从而起到针对性的扩张冠状动脉,解除血管痉挛,改善心肌血供,并且还能降低机体炎症反应,提高抗氧化能力[15]。
综上所述,针对慢性心力衰竭联合使用超声引导下左侧星状神经节阻滞,可降低体内肾上腺素能受体水平,改善心肌收缩与舒张能力,降低心肌损伤,延长病人生存时间。

