低温共沉淀法制备ZnMn2O4微纳米材料及其电化学性能
许雪棠,龙俊禧,刘素英,苏海艳,王凡
(广西大学 化学化工学院, 广西 南宁 530004)
近年来,尖晶石型复合金属氧化物ZnMn2O4作为无机功能半导体材料,因具有成本低、无毒、光电活性较高等特点,越来越受到科研工作者的关注[1-6]。例如,XIAO等[7]在低温下制备得到的花球状ZnMn2O4超级结构纳米材料,该材料具有很好的电化学储锂性能,经过一次电化学循环过程后,库伦效率达到98 %以上,在电流密度为100 mA/g下,经过50圈电化学循环后仍有626 mAh/g的高比容量。ZHANG等[8]采用共沉淀法制备得到具有核-壳结构的多孔ZnMn2O4纳米颗粒,研究结果表明,经过600 ℃高温煅烧的样品,作为锂电池材料具有较高的可逆容量,在100 mA/g的电流密度下,经过50次循环充放电后,样品电极的电容量仍保持为999 mAh/g。YANG等[9]利用静电纺丝法制备一维ZnMn2O4纳米纤维,用于锂电池材料的研究,经过35次电化学循环后,放电容量为658 mAh/g。目前ZnMn2O4在电化学方面有较多的研究报道,但是大多数集中在锂电池电极材料的应用上,作为超级电容器电极材料的应用仍研究不多。锰是广西的优势资源,保有储量达到2.23×108t,占全国的39.8 %,居全国之首。研究开发尖晶石型锰基电化学材料,将有利于提高锰产品的附加值,拓宽锰材料的应用范围。
低温共沉淀法一般指在室温以下温度(如: -20~20 ℃),采用共沉淀的原理制备得到目标材料的方法。在低温条件下,沉淀粒子的成核和生长速度变慢,生长习惯也会改变,从而使得沉淀产物的结构特征与常温共沉淀产物有非常大的不同[10-11]。采用低温共沉淀法制备材料,金属盐的种类、沉淀剂的种类、反应液的浓度、共沉淀的温度等,不同的制备工艺条件都会影响到材料的结构与性能[12]。
本文采用低温共沉淀法,制备出具有较大比表面积的ZnMn2O4微纳米材料,对材料进行结构表征,并测试了其电荷存储的电化学性能。
1 实验
1.1 试剂和仪器
Zn(NO3)2·6H2O、MnCl2·4H2O、Na2CO3、KOH、乙二醇、丙酮、N-甲基吡咯烷酮等均为分析纯试剂。
采用瑞士的PANalytical X’Pert PRO型X-ray粉末衍射仪进行XRD分析;采用日本日立公司的S-3400N型扫描电镜进行SEM分析;采用美国FEI公司的Tecnai G2 F30型透射电子显微镜进行TEM分析;采用PHI 5000 Versa Probe型X射线光电子能谱进行XPS分析,并以C1s峰(284.8 eV)校正结合能峰;采用TriStar Ⅱ 3020型比表面积和孔径分析仪进行BET、BJH分析。
主要实验在上海方瑞仪器有限公司的DC-6506低温恒温槽中进行;电化学测试采用上海辰华仪器有限公司的CHI660D电化学工作站。
1.2 低温共沉淀法制备ZnMn2O4
在30 mL乙二醇中,加入1.115 5 g Zn(NO3)2·6H2O和1.484 3 g MnCl2·4H2O,磁力搅拌30 min。将完全溶解的反应液转移至三颈烧瓶(250 mL)中,将三颈烧瓶置于-10 °C恒温槽中,一直保持N2氛围,机械搅拌30 min,再滴加100 mL Na2CO3溶液(0.225 mol/L),滴加速度为1.2 mL/min。调慢搅拌速度,反应液陈化1 h。对陈化后的反应液进行离心分离,得到的沉淀依次用去离子水(60 °C)洗涤5次、无水乙醇洗涤2次。经过60 °C烘干10 h之后,将产物研磨成粉末,置于马弗炉中,以1 °C/min的速率升至相应温度,煅烧4 h,自然冷却至室温,则可得到目标产物。
1.3 电化学测试
本测试以Hg/HgO电极作为参比电极、涂有待测样品的镍网作为工作电极、铂电极作为辅助电极,三电极体系进行电化学性能测试。电解液为6 mol/L KOH,测试温度30 ℃。采用循环伏安法测CV曲线、恒流充放电法测CP曲线、电化学阻抗法测EIS曲线,电压窗口设定为(-0.05~0.45 V),测试频率区间为0.1~100 kHz,扰动电压振幅为(± 5.0)mV。
2 结果与讨论
2.1 ZnMn2O4样品的XRD分析
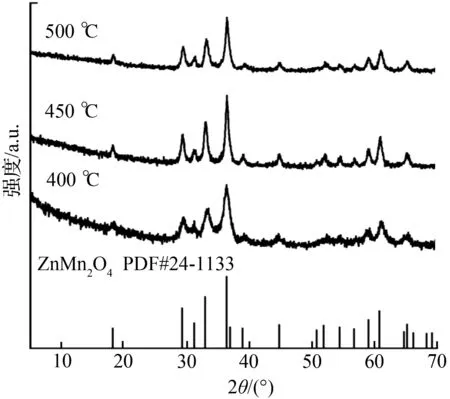
图1 ZnMn2O4样品在不同煅烧温度下的XRD谱图
图1是ZnMn2O4样品在不同煅烧温度下的XRD谱。由图1可见,在400 ℃、450 ℃、500 ℃下煅烧所得样品的XRD衍射峰均与尖晶石型ZnMn2O4的JCPDS标准谱(PDF # 24-1133)一致,谱图中没有杂相峰,表明所得样品的纯度较高。与标准谱相比,三个样品的各衍射峰的相对强度大致相同,由此表明样品没有特定的某一快速生长晶面,即样品在乙二醇的水溶液环境下是以各向同性方式生长的。
2.2 ZnMn2O4样品的形貌分析
在400 ℃下煅烧所得的ZnMn2O4样品的SEM和TEM图谱如图2所示。图2(a)是ZnMn2O4样品的SEM,从图2(a)可见,样品颗粒均匀,粒径大小为200~500 nm的小微球。图2(b)是ZnMn2O4样品的高倍数SEM,可以看到,每个小微球是由更小的颗粒堆积而成,颗粒之间有一定的空隙,使得小微球表面粗糙,呈现多孔结构。图2(c)是ZnMn2O4样品的TEM,很清晰看到,样品的小微球颗粒是多孔结构,孔道尺寸约为10 nm。图2(d)的高分辨TEM进一步证实了小微球的多孔结构实际是由更小的无规则纳米晶颗粒堆积而成,纳米颗粒边缘光滑,晶格条纹清晰可见。纳米颗粒的堆垛并不非常紧凑,因此就形成了很多无规则的堆积孔。

(a) ZnMn2O4样品的SEM图
2.3 ZnMn2O4样品的比表面及孔径分析
ZnMn2O4样品的N2吸附-脱附等温线和BJH孔径分布曲线如图3所示。从图3(a)的N2吸附-脱附等温线可以看出,在400 ℃、450 ℃、500 ℃下煅烧获得的ZnMn2O4样品的等温线的变化趋势基本一致。以400 ℃煅烧获得的ZnMn2O4样品为例,当相对压力P/Po<0.8,基本没有吸附;当P/Po达到0.8时,开始出现毛细凝聚现象,随着相对压力增大,等温线急剧上升;当P/Po接近0.98,出现拐点,这与多层吸附的特点相符合。脱附部分的曲线基本属于H1型回滞环类型。由图3(b)可见,ZnMn2O4样品的孔径范围在2~20 nm。多孔结构的产生主要来源于两个方面:无规则纳米小颗粒的堆积孔、碳酸盐转化为氧化物所产生的气体通道。由此可知,图中较小孔径主要由碳酸盐分解所形成气体通道,而较大孔径分布则对应于无规则纳米小颗粒颗粒的堆积孔。从比表面数据可知,在400 ℃、450 ℃、500 ℃下煅烧,样品的比表面积依次为95.8、52.3、49.6 m2/g,比表面呈减小趋势,原因主要是样品颗粒的团聚。在450 ℃、500 ℃的煅烧温度下样品的比表面积接近,也可说明由无规则纳米颗粒堆积而成的ZnMn2O4样品具有一定的结构热稳定性。
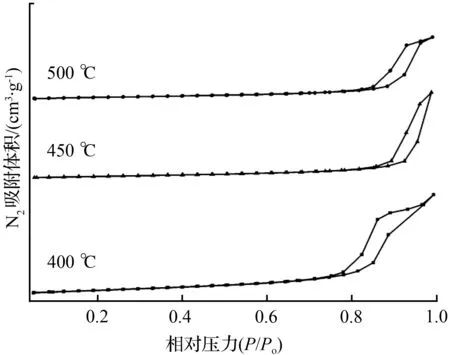
(a) N2吸附-脱附等温线
2.4 ZnMn2O4样品的XPS分析
对400 ℃煅烧得到的ZnMn2O4样品进行XPS表征,以此获得样品中各元素的价态信息(图4)。图4(a)是样品的XPS全谱图,从中可见,样品中只含有Zn、Mn和O三种元素(C元素是引进的校准)。图4(b)则是Zn 2p的区域高分辨图,1 044.4 eV和1 021.3 eV附近的结合能峰分别对应于Zn 2p1/2和Zn 2p3/2的结合能峰,这是Zn2+的特征结合能。图4(c)是Mn 2p的区域高分辨图,653.4 eV和642.2 eV附近的结合能峰分别对应于Mn 2p1/2和Mn 2p3/2的结合能峰。由于锰的化合价有多种,Mn 2p1/2和Mn 2p3/2峰间的能量间隔为11.4 eV,由此可推测Mn元素主要是以+3价存在的。图4(d)是O 1s的区域高分辨图,531.0 eV的峰对应于ZnMn2O4样品内的Mn—O—O峰,529.9 eV的峰则对应于ZnMn2O4样品内的Mn—O—Mn峰[13-14]。
2.5 ZnMn2O4样品的电化学性能分析
由前文可知,采用低温共沉淀法,可以制备得到具有较大比表面积的微纳米ZnMn2O4样品。由于锰氧基化合物常用作电极材料,因此将所制备的ZnMn2O4样品制成电极,进行电化学性能测试,以此探究其在电化学方面的应用前景。
以400 ℃煅烧得到的ZnMn2O4样品为例,图5为ZnMn2O4电极依次在10、20、50、100 mV/s的不同扫速、电压窗口为-0.05~0.45 V的条件下的循环伏安(CV)曲线。从图5可见,在0.25~0.40 V,CV曲线有一对氧化还原峰,这对应于Mn3+/Mn4+离子对的氧化还原峰(0.25 V为还原峰,0.40 V为氧化峰)。而0.40 V以上出现的氧化峰,猜测是金属Mn的氧化过程。图5中显示,随着扫速的增加,氧化峰和还原峰的位置分别向高、低电压方向移动而相互远离,且响应电流也随着增大,由此说明这主要是由离子迁移控制的表面电化学行为。
图6为ZnMn2O4电极的充放电曲线。由图6可见,在0.5、1、2、5 A/g的电流密度下,0.3~0.4 V区间,曲线存在着充放电平台,与CV曲线所反映的情况一致。电极存在着双电层行为,从而充放电平台长度并不明显,曲线接近于三角形形状。利用相关公式可以算出样品电极在0.5、1、2、5 A/g电流密度时对应的质量比电容分别为53.7、39.9、28.0、16.8 F/g,也就是随着电流密度的增大,质量比电容呈明显的减小趋势。
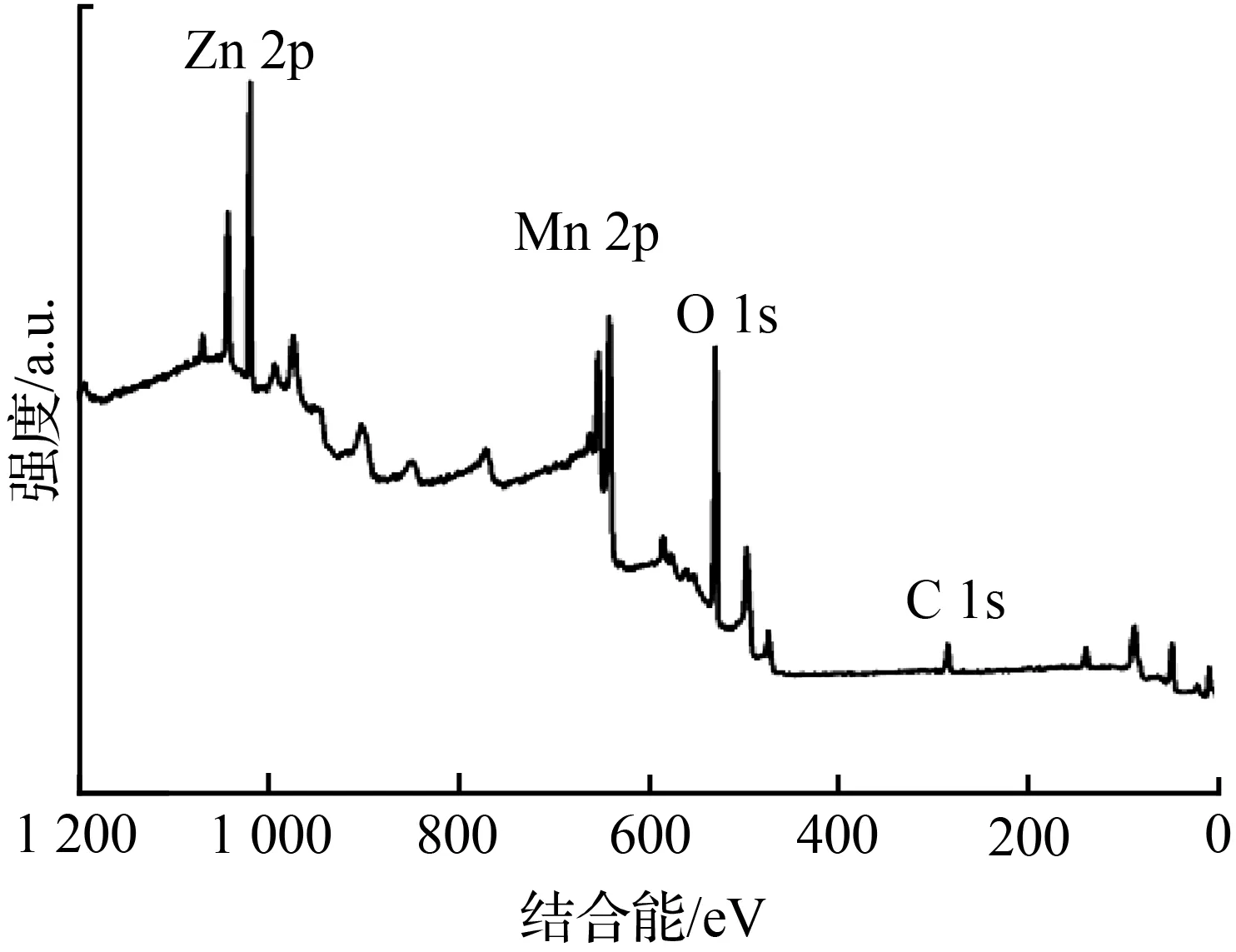
(a) 全谱

图5 ZnMn2O4电极的循环伏安曲线

图6 ZnMn2O4电极的充放电曲线
ZnMn2O4电极的电化学阻抗谱(EIS)见图7。Nyquist曲线与实部Z′的交点等于内部电阻(Rs)数值大小,图7中约为1.48 Ω,由此表明电极系统的内阻较小,原因可能是ZnMn2O4样品的多孔结构造成的。此外,在低频区,曲线的斜率较大,说明所制备的样品电极的扩散阻抗较小。而在高频区,曲线没有出现半圆弧形,说明可忽略样品电极界面的电荷传递电阻(RCt)。
图8为在5 A/g的电流密度下ZnMn2O4电极的的循环寿命曲线图。从图8可见,经过3 000圈循环充放电后,与初始容量相比,样品电极的电容量仍有77.3 %的保留率。
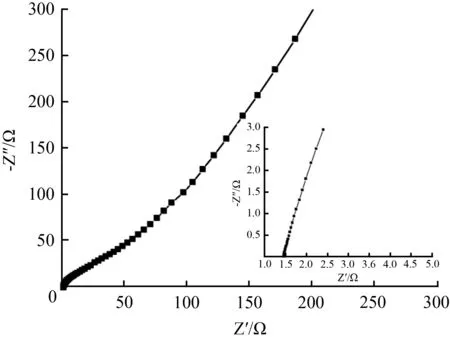
图7 ZnMn2O4电极的Nyquist曲线

图8 ZnMn2O4电极的循环寿命曲线
Fig.8 Cycling behaviors of ZnMn2O4electrode
3 结论
本实验采用低温共沉淀法,制备得到尖晶石型ZnMn2O4微纳米材料。实验结果表明,所制备的尖晶石型ZnMn2O4微纳米材料为微纳米颗粒堆积的多孔结构,孔道尺寸约为10 nm,属于介孔材料。400 ℃煅烧得到的ZnMn2O4样品的比表面积可达95.8 m2/g,具有一定的结构热稳定性。样品的电化学性能(CV、CP、EIS、循环寿命)分析结果表明,制备的ZnMn2O4样品电极具有较好的电荷存储性能。

