白内障超声乳化联合IOL植入术治疗PACG的有效性及影响因素分析
李继英,潘旭方,崔宏宇,张志宏,郭黎霞
0引言
原发性闭角型青光眼(primary angle-closure glaucoma,PACG)以眼压急剧上升为临床表现,存在特征性眼前节解剖结构,约占所有类型青光眼的80%,是仅次于白内障的致盲性眼病[1]。PACG的病因至今尚未能完全阐明,研究指出,PACG的发生或是基于浅前房、房角狭窄的病理基础,瞳孔阻滞或非瞳孔阻滞导致周边虹膜突然或缓慢进行性阻塞小梁网,使前房排水受阻而导致眼压突然或缓慢进行性升高,若病情得不到有效控制便可引起视神经损伤,最终失明[2-3]。传统内引流术、外引流术虽可有效降低眼压,但术后白内障、眼内炎、恶性青光眼风险高[4]。白内障超声乳化联合人工晶状体(IOL)植入治疗闭角型青光眼可从根本上解除闭角型青光眼的瞳孔阻滞,并重新开放全部或部分房水流出通道,达到降低眼压、改善视功能的目的[5]。但在适应证选择、术后疗效评价上仍存在一定争议[6-7]。鉴于此,现回顾性分析2017-01/2018-12在本院接受白内障超声乳化联合IOL植入术治疗的PACG患者的临床资料,着重探究白内障超声乳化联合IOL植入术治疗的有效性,并对疗效的相关影响因素进行分析,以期为PACG的临床治疗提供参考依据。
1对象和方法
1.1对象选取2017-01/2018-12在本院接受白内障超声乳化联合IOL植入术治疗的PACG患者75例75眼,其中男45例,女30例;年龄47~72(平均50.95±11.36)岁;晶状体混浊分级系统(Lens Opacity Classification System,LOCS)Ⅱ级40例40眼,Ⅲ级35例35眼;急性PACG 59例59眼,慢性PACG 16例16眼;术前前房深度1.80±0.25mm;房角黏连<150°30例30眼,150°~159° 38例38眼,>160° 7例7眼;晶状体厚度4~5mm 44例44眼,>5~10mm 24例24眼,>10mm 7例7眼;入院眼压44.05±8.08mmHg,术前眼压24.69±2.58mmHg。纳入标准:(1)符合PACG诊断标准[8];(2)LOCS分级Ⅱ~Ⅳ级;(3)角膜水肿消退,动态房角镜检查前房角黏连关闭≤1/2房角;(4)最佳矫正视力(best corrected visual acuity,BCVA)<0.5;(5)病程<6mo;(6)知晓手术内容及手术相关风险,并自愿签署手术知情同意书。排除标准:(1)继发性青光眼;(2)患有PACG以外的眼部疾病;(3)眼部外伤史;(4)既往有眼部手术史。本研究通过医院伦理委员会审核。
1.2方法
1.2.1手术方法所有患者均严格完善视力、眼压、裂隙灯等术前检查,对眼压≥25mmHg的患者给予局部或全身降眼压药物,将眼压控制25mmHg以下。术前1d生理盐水冲洗泪道,左氧氟沙星滴眼液滴术眼。术前60min按每次间隔10min给予复方托吡卡胺滴眼液散瞳,盐酸奥布卡因滴眼液行术眼表面麻醉,生理盐水冲洗结膜囊。常规铺消毒巾,开睑器开睑,于角膜缘3∶00位作1.5mm辅助透明角膜切口,前房内注入弥散型黏弹剂,角膜缘12∶00位作3mm宽透明角膜切口,前房注入聚合型黏弹剂加深前房深度,部分黏连或固定小瞳孔采用虹膜拉钩分离黏连,牵拉瞳孔至瞳孔直径≥5mm,作连续环形撕囊。囊膜下充分水分离至晶状体浮起,并可在囊袋内转动。再次输入聚合型黏弹剂,囊袋内十字劈裂法分裂晶状体后超声乳化吸除,包括残留晶状体皮质,再次注入聚合型黏弹剂,抛光后囊膜、囊膜袋内注满黏弹剂,囊袋内置入折叠式IOL,并将其调整至最佳位置,吸出前房及囊袋内黏弹剂。术毕取出开睑器,结膜囊内涂地塞米松眼膏,包扎术眼。术后第1d常规抗感染,并给予复方托吡卡胺滴眼液、地塞米松眼膏等药物,术后给予持续随访,定期复查。
1.2.2观察指标以查阅临床病历、手术资料方式统计患者术后眼压(IOP)、视力(LogMAR)改善情况,记录术后超声生物显微镜(ultrasound biomicroscope,UBM)、裂隙灯前节光学相干断层成像(slit lamp optical coherence tomography,SL-OCT)检查结果,包括中央前房深度(central anterior chamber depth,ACD)、房角开放距离(angle opening distance,AOD500)、小梁虹膜夹角(trabecular iris angle,TIA500)、房角隐窝面积(angle recess area,ARA),统计术中及术后并发症发生情况。
临床疗效评价标准:参照文献[9],依据术后3mo眼压改善情况将临床疗效分为成功、条件成功及失败三个等级,术后无需用降眼压药物眼压<21mmHg视为成功;术后需使用降眼压药物眼压<21mmHg视为条件成功;局部使用降眼压药物后眼压仍≥21mmHg,需行二次抗青光眼手术治疗视为失败。
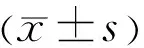
2结果
2.1临床疗效所有患者均顺利完成手术,无虹膜损伤、后囊破裂、玻璃体脱出等并发症发生。随访至术后3mo,手术成功45例45眼,条件成功20例20眼,失败10例10眼。
2.2术后眼压及视力情况术后1wk,1、3mo时本组患者IOP均低于术前(t=7.462、9.959、11.671,均P<0.05),BCVA(LogMAR)均较术前明显改善(t=19.610、19.966、19.200,P<0.001),见表1。
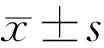
表1 手术前后眼压及视力情况
2.3术后眼前节情况术后3mo,UBM、SL-OCT检查均可见ACD、AOD500、TIA500、ARA较术前显著改善(P<0.01),见表2。
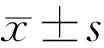
表2 手术前后眼前节情况
2.4影响PACG患者手术疗效的危险因素分析
2.4.1单因素分析手术成功、条件成功视为有效,失败视为无效,将患者分为有效组(65例65眼)和无效组(10例10眼)。两组患者性别、年龄、晶状体核硬度及厚度比较差异均无统计学意义(P>0.05),但有效组患者术前BCVA优于无效组,急性PACG占比、术前ACD显著高于无效组,术前IOP、房角黏连>160°患者占比均显著低于无效组(P<0.05),见表3。
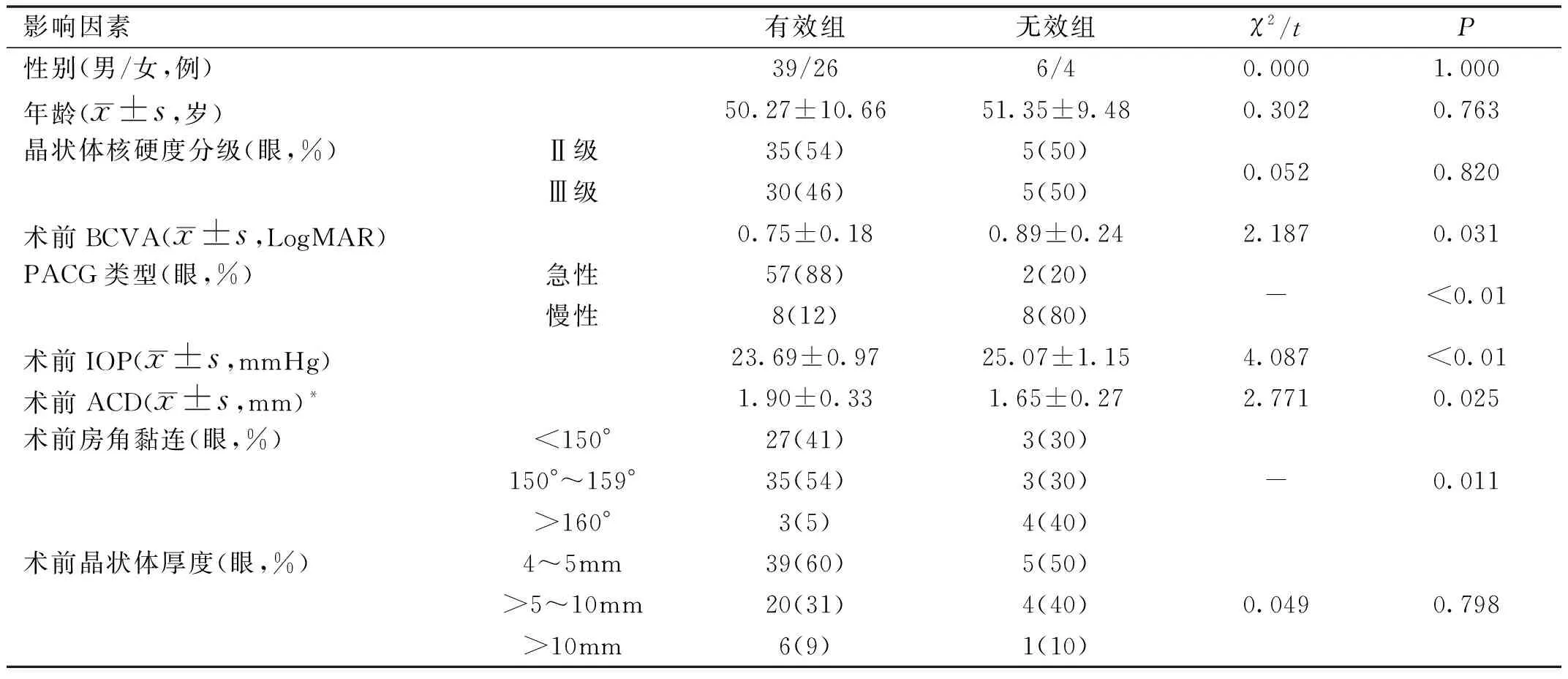
表3 PACG患者手术疗效的影响因素分析
2.4.2多因素Logistic回归分析将单因素分析差异有统计学意义的变量[术前BCVA(原值输入)、PACG类型(急性PACG=0、慢性PACG=1)、术前IOP(原值输入)、术前ACD(原值输入)、术前房角黏连(<150°=0、150°~159°=1、>160°=2)]作为为协变量,疗效(有效=0、无效=1)作为因变量,经多因素Logistic回归分析,结果显示,慢性PACG、术前IOP是PACG患者白内障超声乳化联合IOL植入术疗效的危险因素(均P<0.05),见表4。
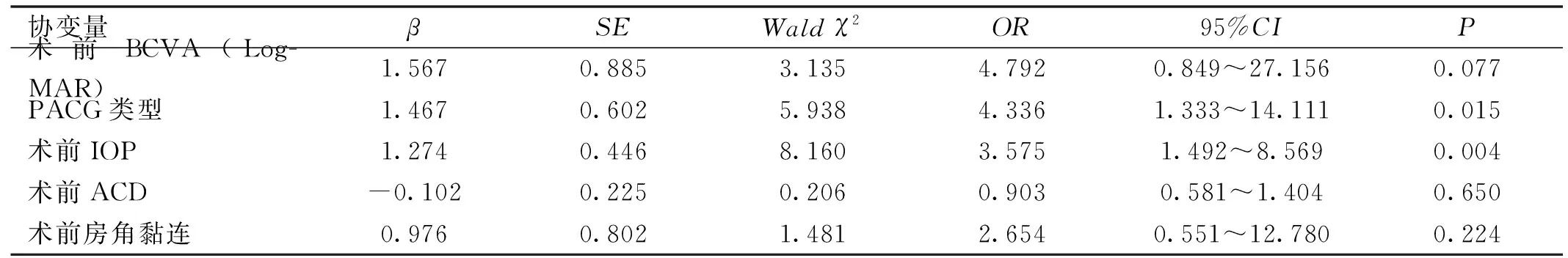
表4 多因素Logistic回归分析
3讨论
目前,多数学者认为PACG的发病因素与晶状体、虹膜、小眼球、小角膜、眼前容积小等因素有关。既往报道指出,多数PACG患者晶状体较厚,晶状体厚度增加可直接导致周边虹膜前移,引起房角关闭;再者,晶状体悬韧带松弛,扩大其与虹膜的接触面,增加瞳孔阻滞力,最终引起房角关闭[10-11]。而眼轴短、角膜小则可直接导致前房拥挤,眼内容量变化使晶状体-虹膜隔前移,导致瞳孔阻滞,引起房角关闭,这也是PACG多见于远视、小眼球患者的原因之一[12-13]。超声乳化吸出术治疗PACG是通过将具备超声振荡功能的乳化针小切口深入眼球内,利用乳化针规则的高频振荡震碎病变的晶状体组织并吸出,可加深前房,增宽房角,改善周边虹膜黏连,打开房水通道,且术中超声乳化头前液体与晶状体间的撞击作用所产生的冲击力、灌注液在前房形成的压力还可再度开放房角,减少黏连,缓解PACG症状,临床应用相对广泛[14-15]。
本研究纳入患者术中及术后均未见不良反应,提示白内障超声乳化联合IOL植入术安全性良好。PACG患者术后眼压均下降,BCVA均改善,与术前比较差异均有统计学意义,这与潘兰香等[16]报道结论相符,均提示白内障超声乳化联合IOL植入术治疗PACG可有效改善患者视功能,降低眼压。曾招荣等[17]报道超声乳化联合IOL植入术可有效增加前房深度、改善房角结构,这与本研究结果相似,本研究术后采用UBM、SL-OCT检查均可见ACD、AOD500、TIA500、ARA较术前显著上升。但本研究75例患者中,仍有10例患者术后局部使用降减压药物后最终眼压≥21mmHg,需行二次抗青光眼手术治疗,提示治疗失败。进一步分析手术疗效的影响因素,结果显示慢性PACG、术前眼压是PACG患者白内障超声乳化联合IOL植入术疗效的危险因素。
本研究中发现,慢性PACG患者较急性PACG患者白内障超声乳化联合IOL植入术无效的风险增加4.336(1.333~14.111)倍。目前,临床针对慢性PACG患者是否可行白内障超声乳化联合IOL植入术,主要参考其青光眼病史、房角是否关闭、房角是否黏连情况而定,一般病程超过6mo的PACG患者接受白内障超声乳化联合IOL植入术治疗后,在开放黏连房角、降低眼压上获益不显著[18]。本研究虽排除病程超过6mo患者,但可能存在病程不精确计算现象。同时,慢性PACG患者在疾病早期、中期时无明显特异性临床症状,多数出现症状就诊时已为病程晚期,多数患者不能准确描述病程,也不能理解房角黏连概念。这也提示临床或应规范、加强慢性PACG的早期诊断,这对提升慢性PACG患者白内障超声乳化联合IOL植入术治疗成功率有益。此外,本研究结果显示,术前眼压是白内障超声乳化联合IOL植入术疗效的危险因素,且术前眼压越高,手术无效风险越高。这与张鹏程等[19]报道结论相似,其指出术前眼压与术后眼压呈显著正相关关系,直接关系术后眼压水平。但考虑本研究的局限性,如样本量少,无效组仅10例患者,可能存在一定统计学误差,因此认为白内障超声乳化联合IOL植入术治疗PACG的安全性、有效性及影响其有效性的危险因素等仍有极大深入探究空间。
综上所述,白内障超声乳化联合IOL植入术治疗PACG疗效佳,可显著降低眼压,提升视力,改善视功能;积极控制术前眼压、慎重评估慢性PACG患者开展白内障超声乳化联合IOL植入术的可行性或是进一步提升治疗疗效的关键。

