R语言在分析化学教学中的应用
谭巧国
厦门大学环境与生态学院,福建 厦门 361102
分析化学由于其定量属性,涉及大量的计算和统计分析,并常需借助可视化手段展示复杂概念、过程和方法。因此,在分析化学的教学中,兼具计算和绘图功能的 Excel软件成为广泛采用的教学辅助工具。分析化学的经典教材也普遍结合Excel进行教学[1,2],而且有专著专门讲解Excel在分析化学中的应用[3,4]。此外,也有文献零星地介绍其他计算机软件在分析化学中应用,所介绍软件包括Matlab[5-7],Origin[8]等。
R语言是近年来兴起的一门计算机语言,在生物学、生态环境科学、经济学、社会科学等各领域都得到了广泛的应用,成为当前最受欢迎的编程语言之一[9,10]。R有比Excel更卓越的数据处理和可视化能力,理论上非常适用于分析化学的教学。然而,与其在科学研究中的热度形成鲜明对比,目前尚未见论文和书籍介绍将R用于包括分析化学在内的课程教学。本文列举数例,说明R可以在分析化学教学的多个方面得到应用。
1 R语言简介
R语言是一款开源免费的编程语言,主要用于统计分析和数据可视化。R最初是由两位统计学家罗斯·伊哈卡和罗伯特·杰特曼基于S语言开发而成。由于两位开发者名字的首字母都是R,R因此得名。目前R由“R开发核心团队”负责维护和开发[9]。
R的功能可以通过程序包得到扩展。例如本文中绘图用到了ggplot2程序包,数据整理用到了reshape2程序包,而这两个程序包与其他多个常用的程序包一起又包括在tidyverse程序包中。初次使用时,需运行以下代码安装:
install.packages("tidyverse")
除了以上提及的统计分析和绘图功能,R用于分析化学教学还具有以下几方面的优势:
R以代码形式实现计算和作图,操作过程完整地体现在代码中。代码具有自释性,理论上无需另外的解释性文字。代码可以纯文本的形式储存和传播,操作过程能够通过代码精确重现。与此相比,Excel计算过程的展示则必须用到图片(甚至视频)结合繁琐的步骤说明[11],不仅占用大量储存空间,而且也不利于教学中的传播、分享和交流。
R有广阔的应用场景。R作为以数据分析和可视化见长的编程语言,是科学研究的有力工具。R借助扩展程序包,不断发展出新的功能满足科研需求。在分析化学的教学中使用R,为学习者接触掌握这项科研利器提供良好契机,可提高学习者的知识获得感和实际收益。
R软件免费,轻便。在写作本文时,最新版本R 4.0.0的安装文件仅84 MB。因此便于在不同的场合(如教室、师生的个人电脑等)随时安装使用R。与此相比,Matlab等收费软件不仅价格昂贵,而且需要5-8 GB的安装空间。
2 R应用于分析化学教学举例
2.1 R应用于分析化学计算
在学习化学平衡和滴定分析时,常涉及复杂的计算。例如,一元弱酸溶液 pH值的计算式是一元三次方程,多元弱酸和其他溶液还会涉及更高次的方程。高次方程不一定存在公式解,即使存在其公式也极为复杂。因此,直接解高次方程缺乏可操作性。目前教材中常采用忽略次要组分,忽略方程中的次要项等做法,以损失一定的准确度为代价,将高次方程简化成二次或一次方程进行求解[12]。简化中涉及多个判别式,判别式因溶液体系而异。这部分内容因此记忆负担较大,常成为学习分析化学的障碍。
R语言可看成一个功能全面的计算器,能执行各类科学计算,能用于解决分析化学中的高次方程求解问题。下面举一例说明求解过程。例题取自柳青和王海水[13]的论文,关于磷酸溶液pH值的计算。柳青和王海水提出了简化多元弱酸溶液 pH值计算的新方法,但思路仍然是将高次方程简化为二次或一次方程。其方法改善了通用性,但过程仍然较为复杂,仍有较大的记忆负担。
例 1 已知磷酸(H3A)的 Ka1= 7.6 × 10−3,Ka2= 6.3 × 10−8,Ka3= 4.4 × 10−13,计算 0.20 mol·L−1磷酸溶液的pH。
以上例题可通过执行以下 R代码进行计算。需说明的是#号后是代码注释,用于说明代码的用途,注释不会被作为代码执行。本文中的代码在关键处添加了注释,便于读者理解。

以上代码中,起核心作用的是解方程函数uniroot()。在使用uniroot()时,所输入的f是H+浓度精确计算式,因溶液体系而异;参数interval是粗略预估的方程根的上下限;参数tol是所允许的误差。运行以上代码后,得到结果:1.45134,因此可知溶液pH值为1.45,与参考文献中的计算值一致。
运用该方法,除了计算准确,还可以将所有酸碱溶液的 pH值计算都转变为同一种方法。计算过程可分为三步:(1) 根据质子得失平衡写出质子条件式;(2) 将式中酸(碱)各型体的浓度都替换成酸(碱)的分析浓度与分布分数之积,得到关于[H+]([OH−])的一元高次方程,即以上所用的f;(3) 解高次方程。
此方法只用到质子条件式和分布分数这两个容易掌握的基本方法,避免了复杂的判别式和简化过程,便于理解和记忆。从而使学习者从复杂的公式和繁琐的计算中解脱出来,将更多精力用于学习分析化学知识本身。
2.2 R应用于分析化学绘图
R语言另一项特色功能是科学绘图。图在分析化学的教学中发挥着不可或缺的作用,可以将复杂的概念、溶液体系、反应过程等可视化,降低理解难度。例如,分布分数图之于化学平衡,滴定曲线图之于滴定原理,都是极为有效的教学工具。学习者若能自己绘制这些图,则更能提升学习效果,增加学习乐趣。
以下以多元酸的分布分数图和络合滴定图为例,演示如何用将R应用于分析化学绘图,并帮助理解其背后的化学原理。需要说明的是,为了节省篇幅,以下作图的R代码仅保留主干部分,图的细节修饰所需代码未给出。读者运行以下代码,可看到图的主体信息,但格式细节与文中所示的图略有区别。完整作图代码获取方式见文末说明。
2.2.1 分布分数图的绘制
三元弱酸磷酸经三级解离,得到四种型体。根据磷酸的三个Ka值,可得到四种型体分布分数的表达式,并据此绘制分布分数图。以下是绘图的R代码:


运行以上代码,可得到磷酸的分布分数图(图1)。该图可用于判断不同pH值条件下,磷酸的主要型体。例如,天然海水的pH约为8.2,因此可判断海水中的磷酸盐主要以型体存在。该图亦可反向用于估算磷酸或磷酸盐溶液的pH值。例如,可估算KH2PO4和K2HPO4溶液的pH值分别在5和10左右。例1中的问题亦可使用该图帮助简化。假设0.20 mol∙L−1的H3PO4溶于水后第一级电离发生了50% (此比例据经验粗略估算,无需准确),则溶液pH值为1左右。据图1判断,溶液中几乎不存在,因此可忽略H3PO4的第二、三级电离,可直接将磷酸当成一元弱酸来处理,大为简化了其pH值的计算。
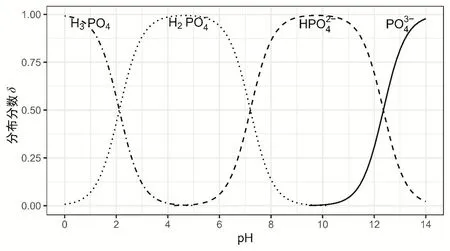
图1 用R绘制磷酸的分布分数图
除了一元、多元酸碱的分布分数图,其他分布分数图,如Cu(NH3)n逐级络合物的分布分数图,EDTA各型体的分布分数图等,亦可按照以上方法绘制。学习者若改变作图参数(如Ka值),便可即时看到图的变化。这样的过程可以帮助理解稳定常数、解离常数等如何决定了曲线的形状,进而理解这些常数的内涵。
2.2.2 滴定曲线的绘制
以下以EDTA络合滴定金属离子M为例,演示如何用R绘制络合滴定曲线。络合滴定曲线是滴定过程中金属离子浓度(pM')与滴定分数(a)之间关系的曲线,由络合滴定曲线方程描述:

在此例中,假设用0.1000 mol∙L−1的EDTA滴定同浓度的金属离子M,EDTA络合M的条件稳定常数K'MY为1.0 × 1014L∙mol−1。绘制其滴定曲线图的R代码如下:

运行以上代码,得到络合滴定曲线(图2)。曲线中包含了络合滴定的多项信息,这些信息在曲线绘制过程中均得到求解。例如,化学计量点的pM'即滴定分数a等于1时的pM',为7.65;滴定突跃范围是滴定分数a为(100.0 ± 0.1)%对应的pM'范围,为4.30-11.00。通过调整K'MY和cM的取值,观察曲线形状的变化,有助于理解络合稳定常数以及金属离子浓度对于滴定突跃的影响。

图2 用R绘制的络合滴定曲线
此例中所用的方程可以定量描述络合滴定的各个阶段。对于其他滴定,也能建立类似的方程用于绘制滴定曲线,英文教材中将这类方程称为“master equation”[14]。此外,还可将滴定过程分为滴定前、化学计量点前、化学计量点、化学计量点后四个阶段,将问题简化,分别计算 pM'和滴定分数的关系,并进而绘制曲线。滴定曲线绘制充分运用了化学平衡与滴定的知识,同时使用了R的解方程和绘图两项主要功能,适用于教学中的知识讲解,但也因此步骤较多。若在日常教学科研中需频繁绘制滴定曲线,还可所采用R扩展程序包“titrationCurves”一步完成曲线绘制[15]。
2.3 R应用于分析化学中的统计分析
定量分析中的误差不可避免,计算和评估误差则需要用到统计分析方法。统计分析的理论和方法较为抽象,对其理解有赖于扎实的数学和统计学基础,因此常成为教和学的难点。分析化学中统计分析的教学应有别于数学、统计学类课程,目标应当是准确理解,正确使用,可以淡化数学推导。R最初是由统计学家开发,其统计学功能齐全而严谨,且容易使用。将R运用于分析化学中统计方法的教学,不仅可以帮助学习者掌握数据处理的正确方法,还有助于更好地理解相关的理论和方法。
以下以t检验为例,演示如何将R用于分析化学中的统计分析,并结合可视化的方法帮助学习者理解统计学概念。例题取自武汉大学《分析化学(上册)》[12]。
例2 采用一种新方法测定基准明矾中铝的质量分数,9次测定结果为10.74%,10.77%,10.77%,10.77%,10.81%,10.82%,10.73%,10.86%,10.81%。已知明矾中铝含量的标准值(以理论值代替)为10.77%。采用新方法后,是否引起系统误差(置信度95%)?
教材上介绍的是常规方法:由于测定次数较少,判断随机误差符合t分布。计算t值得到1.43,查t值表得到临界值t(0.05,8)= 2.31。t值小于临界值,从而判断无显著系统误差。
运用R语言,无需查表,进行单样本t检验直接得到结果。具体操作如下:

输出结果如下(为节省篇幅,部分信息省略):
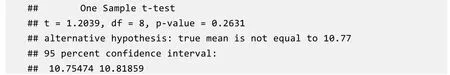
结果显示p值为0.2631,大于显著性水平0.05,因而可判断新方法的测定值与理论值无显著差异,亦即新方法未导致显著的系统误差。结果中还给出了测定值的95%置信区间,即(10.755,10.819),此区间内包含理论值10.77,也表明新方法无显著系统误差。
在此基础上,还可将以上结果可视化,显示9次测定值、置信区间、理论值在坐标轴上的位置(图3),帮助学习者理解t检验及置信区间的含义。以下是绘制图3a的代码:

从图上可看到各次测定值的位置决定了置信区间的位置和宽度;置信区间若将理论值包含在内,则表明测定值的均值与理论值无显著差异。为了进一步理解,另外生成一组有系统误差的数据作为对比。将例题中的测定值均减去0.05,并针对这组新数据做t检验:

结果显示p值为0.04266,小于0.05;95%置信区间为(10.705, 10.768),不包含理论值10.77。表明存在显著的系统误差(图3b)。若将显著性水平调为99%,再进行t检验:
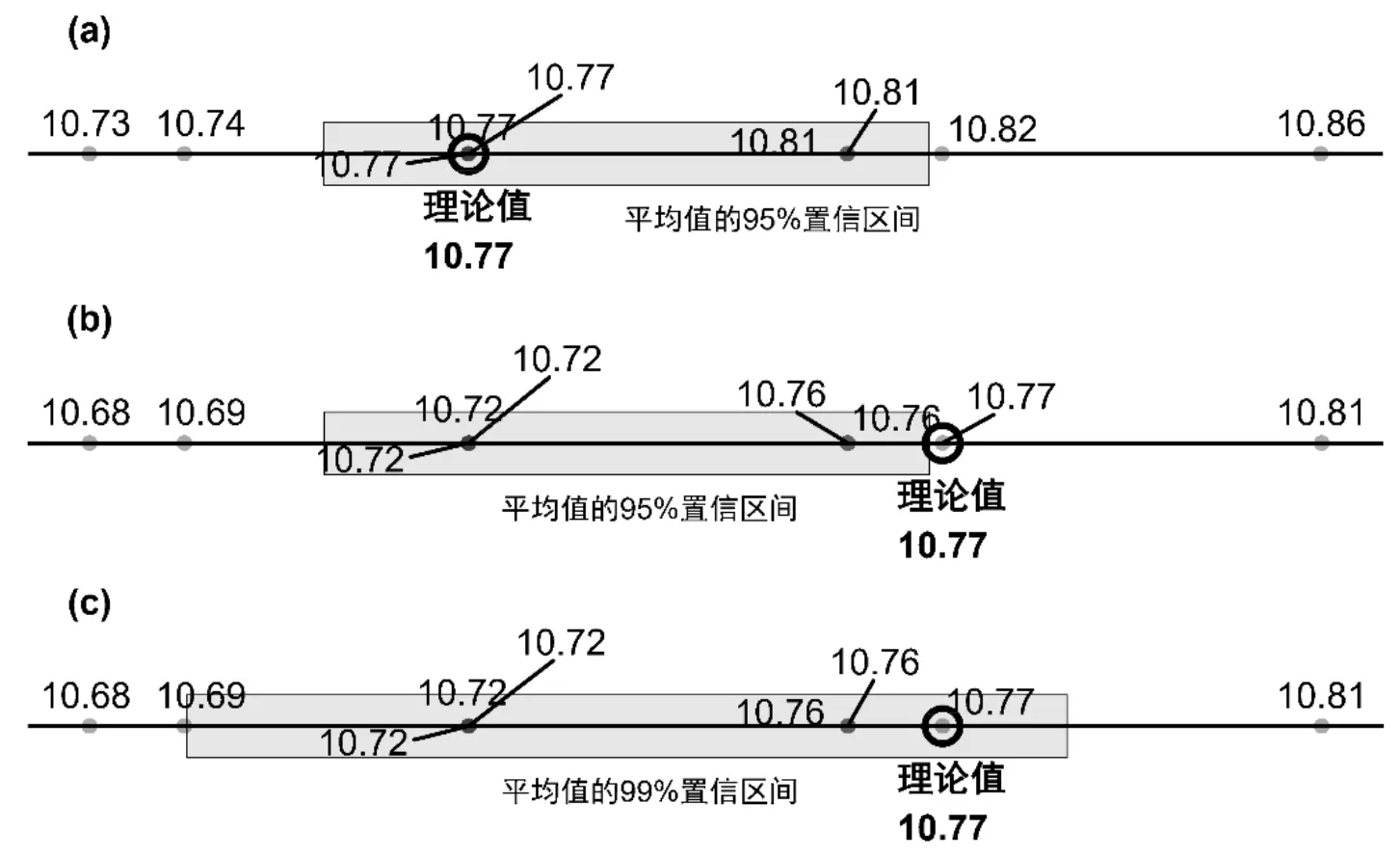
图3 用R绘图对比测定值及其均值的95%置信区间与理论值
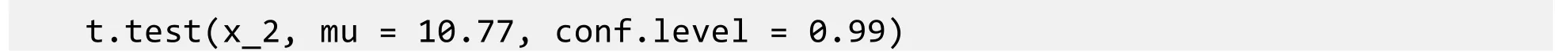
得到结果 p值仍为 0.04266,虽小于 0.05,但大于新采用的显著性水平 0.01;99%置信区间为(10.690, 10.783),比95%置信区间更宽,包含理论值10.77,表明不存在显著系统误差。因此可知,关于是否存在系统误差的结论与置信度的选择有密切相关。
除以上的t检验外,分析化学教学中涉及正态分布、t分布、置信区间的估计、F检验、可疑值的取舍、回归分析等统计分析内容均可借助R进行教学。
2.4 R数值模拟用于解释复杂概念
R作为编程语言,有生成符合特定分布的随机数,进行随机抽样等功能,因而可以进行数值模拟,帮助解释分析化学中一些复杂的概念和方法,以下举一例说明。
例3 测量值m1= 0.00 ± 0.10,测量值m2= 2.00 ± 0.10,则m2与m1之差m的值和标准差是多少?
按照误差传递公式,可以算得m的标准差是(0.102+ 0.102)1/2,即0.14,因此m = 2.00 ± 0.14。误差传递计算并不难,但是误差传递公式的推导过程较为复杂,学习和理解的难度较高。因此,学习者虽然能够按照公式算出误差,但未必能理解误差传递的真正含义。借助R的数值模拟和可视化,可以帮助学习者克服这一困难。以下针对例题3,进行数值模拟,得到图4。
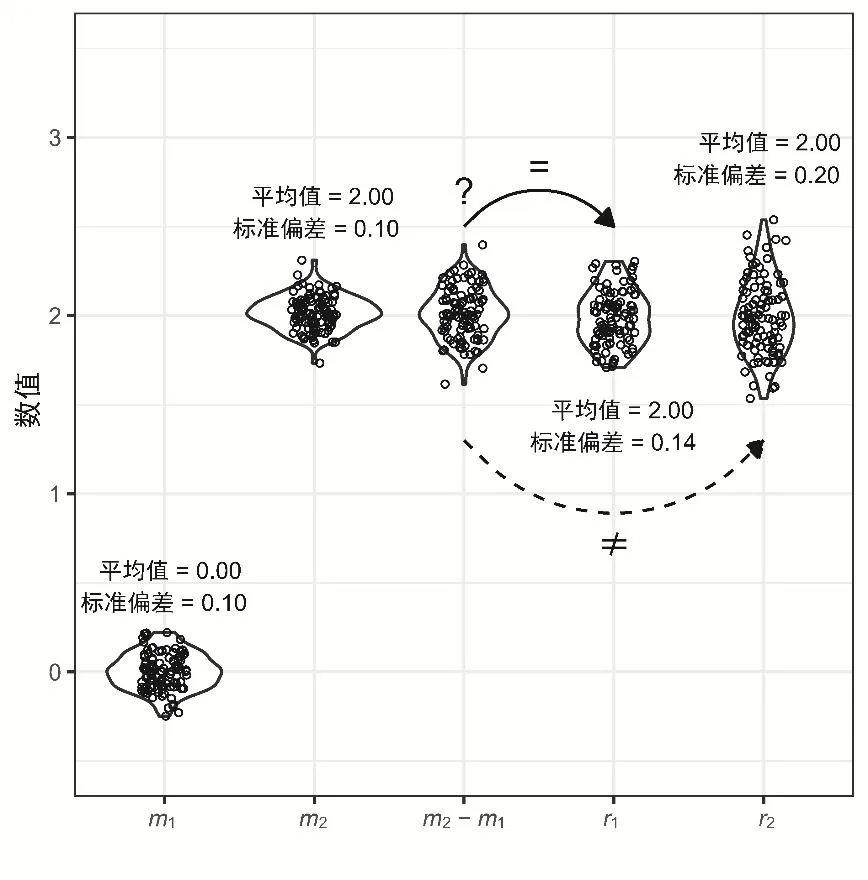
图4 用R做数值实验帮助理解误差传递的原理

从图4中可知,差值(m2− m1)的离散程度大于m1和m2,但是小于r2,而与r1接近。从R代码中可知,r2的标准差为m1和m2标准差之和(即0.20);r1的标准差为0.1414,与误差公式的计算结果吻合。通过数值模让学习者“眼见为实”,验证了误差传递公式。类似的模拟还可用于其他概念的解释,如置信区间、标准偏差的计算公式等[16]。
3 结语
以上举例展示了R在分析化学教学中的应用。R兼具计算、绘图、统计、模拟等功能,因此,分析化学中凡是涉及这些功能的内容,不限于以上所举的例子,均可用R辅助教学。R通过代码实现各项功能,操作过程均体现在文本化的代码中,便于信息的传播交流。因此R不仅适用于课堂演示,还便于学习者课后自学。相比于Excel,R在初学时有较为陡峭的学习曲线。考虑到本科生通常在低年级学习过C语言等更为复杂的编程语言,学习R已经有了较好的基础。目前在高校和学术界有人数众多气氛活跃的R学习群体,互联网上有丰富且优质的R学习资料,这也为自学R营造了良好的环境。将R用于分析化学的教与学,也让学习者有机会在应用实践中学习R,反过来促进R的学习。从分析化学课上学到R的技能,也将有助于其他课程的学习和日后的科学研究。
本文中计算、绘图等所涉及R代码的完整版本均可在此链接(http://tinyurl.com/y9hh36zq)下载或通过联系作者获取。

