Co-g-C3N4/La-TiO2复合材料光催化降解废水中乙基黄药
张亚宣 姚振龙 汪遵盛 汪存会 欧阳二明
(1.南昌大学建筑工程学院,江西南昌330031;2.南昌大学际銮书院,江西南昌330031;3.南昌大学资源环境与化工学院,江西南昌330031)
黄药作为最常用的捕收剂,大量存在于硫化矿的浮选废水中[1]。黄药具有较强的生理毒性,对人体的肝脏和中枢神经系统会造成严重的伤害。黄药分解产生的CS2会使人感到肌肉疼痛,甚至引发大脑神经系统病变[2]。光催化氧化技术是一种新兴的降解污染物的技术,具有催化效率高、速率快、使用简单和绿色无污染等优点[3]。二氧化钛作为应用最广泛的光敏半导体,具有廉价易得、催化效果好等优点;石墨相氮化碳是一种非金属半导体材料,在降解水中有机污染物方面有广阔的发展前景[4]。然而这两种材料具有电子-空穴快速复合、禁带宽度较大和吸光范围较窄等缺点,光催化效率不高。金属掺杂可以使得TiO2和g-C3N4带隙变窄,光的响应范围变大,并提升其光催化性能[5-6]。通过构建金属氧化物和g-C3N4异质结构能够有效地降低带隙宽度,降低光生电子-空穴复合率,拓宽光的吸收范围,提高光催化效率[7]。本研究筛选出最佳催化效果的La掺杂TiO2和Co掺杂g-C3N4,并将其按不同质量比混合,制备出Co-g-C3N4/La-TiO2复合材料,在可见光下降解模拟废水中的乙基黄药。
1 材料与方法
1.1 试验试剂
乙基黄原酸钾(乙基黄药)、无水乙醇、钛酸四丁酯、尿素、三聚氰胺、乙酸钴、硝酸镧(六水)、冰乙酸、硝酸钠、盐酸、氢氧化钠、三乙醇胺、异丙醇、1,4-对苯醌均为分析纯。
1.2 试验仪器
紫外分光光度计、荧光分光光度计、马弗炉、磁力搅拌器、离心机、超声波清洗器、天平、扫描电子显微镜、X射线衍射仪等。
1.3 试验方法
1.3.1 Co-g-C3N4/La-TiO2复合材料的制备
(1)将10 mL钛酸四丁酯与20 mL无水乙醇混合,磁力搅拌30 min形成A液;将10 mL无水乙醇、5 mL冰乙酸和10 mL去离子水均匀混合,磁力搅拌30 min形成B液。将A液缓慢滴加到B液当中并进行剧烈搅拌,滴加完毕后继续搅拌3 h得到淡黄色的溶胶,溶胶在80℃的条件下静置12 h形成凝胶。凝胶经过陈化、烘干和研磨并在450℃的条件下煅烧3 h,再用去离子水和无水乙醇各清洗3次得到TiO2。在上述的B液中加入0.191 g的硝酸镧(六水),其余采用同样的方法步骤,得到La/Ti摩尔比为1.5%的La-TiO2。
(2)称取2份3.5 g三聚氰胺、3.5 g尿素放入烧杯中,分别加入100 mL去离子水,其中一份加入0.105 g的乙酸钴,搅拌3 h,然后放入旋转蒸发仪中进行浓缩并在60℃下干燥。将得到的样品进行研磨后放入马弗炉中,以3℃/min的速率升温到550℃,在550℃下保温4 h。将得到的样品再次进行研磨,经过3次水洗和3次醇洗后放入鼓风干燥箱内烘干。最终可分别得到粉末状的g-C3N4和Co-g-C3N4。
(3)称取0.470 g的Co-g-C3N4,加入(1)过程中的B液中,并在其中加入0.191 g的硝酸镧(六水),其余步骤与(1)中TiO2的制备相同。最终可得到两者质量比为1∶5的Co-g-C3N4/La-TiO2复合材料。
1.3.2 光催化降解试验
配制一定浓度的乙基黄药溶液作为模拟废水,使用盐酸和氢氧化钠调节溶液的pH值。在室温条件下,将一定量的催化剂和模拟废水加入到石英反应器中,在黑暗条件下搅拌30 min,实现吸附-脱附平衡。之后采用300 W的氙灯模拟可见光光源照射石英反应器中的模拟废水,每隔一段时间从反应器中取3 mL水样,用0.22 μm的水系膜进行过滤。用紫外-可见分光光度计测得其吸光度,并根据用标准溶液测得的标准曲线计算水样中乙基黄药的浓度和去除率。
1.3.3 活性自由基捕捉试验
采用三乙醇胺、异丙醇、1,4-对苯醌作为空穴(h+)、·OH、·O2-的捕获剂[8-9]。分别向不同反应器中加入三乙醇胺、异丙醇、1,4-对苯醌,并设置对照组,测定并记录不同反应时间下乙基黄药的浓度,计算其对应的去除率。
2 结果与讨论
2.1 材料表征结果分析
2.1.1 SEM及EDS能谱分析
为了对样品的表面形貌进行分析,使用扫描电子显微镜(SEM)分别对所制备的Co-g-C3N4、La-TiO2和Co-g-C3N4/La-TiO2进行了表征,结果如图1所示。

由图1(a)可知,Co-g-C3N4呈现二维烟状结构,表面具有丰富的褶皱,与普通的片状结构相比,具有大量褶皱的Co-g-C3N4拥有更大的比表面面积。这一独特的结构赋予了其出色的吸附性能[10]。由图1(b)可知,制备的La掺杂TiO2为粒状结构,且颗粒十分均匀,平均粒径小于100 nm。从图1(c)可以清晰地看到粒状结构的La-TiO2均匀地分散在Co-g-C3N4的褶皱中。Co-g-C3N4表面的褶皱可以将La-TiO2更好地包裹在空隙中,使得其与La-TiO2的结合更为紧密。
借助X射线能谱仪对样品中的各种元素的分布进行分析,结果如图2所示。从图中可以看出C元素的分布密度较大,这是由于承载样品的碳导电胶带造成的;C、N、O、Ti、Co、La等6种元素分布较为均匀,说明Co-g-C3N4/La-TiO2的复合情况较理想,而物质的有效结合则可以增强其在可见光下的催化性能[11]。

2.1.2 XRD表征分析
通过X射线衍射(XRD)光谱对复合材料中的物质组成和晶型结构进行了研究,结果如图3所示。

由图3可知,制备的g-C3N4样品在12.9°和27.5°处具有特征峰,分别对应(100)晶面和(002)晶面(标准卡 JCPDS87-1526)[12],与 g-C3N4材料标准卡上的特征峰相符,这说明所制备的物质为g-C3N4。制备出的 TiO2在 25.37°、37.03°、48.12°、53.97°、55.10°、62.74°、68.79°出现了7个特征峰,所对应的晶面分别为(101)、(103)、(004)、(112)、(200)、(105)、(211),这些特征峰均为锐钛矿相TiO2的特征峰,并不含有金红石相和板钛矿相TiO2的特征峰。由此可证实,所制备的TiO2为纯锐钛矿相TiO2。在Co-g-C3N4/La-TiO2的XRD图谱中,27.5°处存在一个较小的特征峰,这与g-C3N4的其中一个特征峰相对应。其他特征峰与锐钛矿相TiO2的特征峰基本保持一致。在Co-g-C3N4/La-TiO2的XRD图谱中并没有发现Co和La对应的特征峰,这可能跟Co元素和La元素含量较低有关[13]。
2.1.3 XPS分析
为了研究Co-g-C3N4/La-TiO2表面化学状态,利用X射线光电子能谱(XPS)对样品的元素组成进行了表征,结果如图4所示。
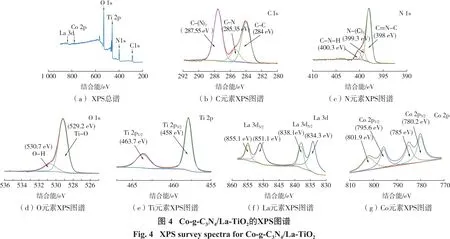
图4(a)为Co-g-C3N4/La-TiO2的XPS全谱,从图中可以观察到位于284 eV左右的C 1s峰,399 eV的N 1s峰,530 eV的O 1s峰,460 eV的Ti 2p峰以及842 eV的La 3d峰和788 eV的Co 2p峰。
图4(b)为C 1s的XPS能谱图。通过拟合分别在284 eV、285.35 eV和287.55 eV的位置呈现出3个特征峰,分别对应C—C、C—N和C—(N)3键[14]。
图4(c)为N 1s的XPS能谱图。可拟合为位于398 eV、399.3 eV和400.3 eV处的3个特征峰,分别代表C==N—C、N—(C)3和C—N—H基团[15]。
图4(d)的O 1s能谱中的2个特征峰则分别代表Ti—O键(529.2 eV)和O—H键(530.7 eV)。前者来源于TiO2中的氧元素,后者则可能来自于Co-g-C3N4/La-TiO2表面的水分子或羟基[16]。
图4(e)的Ti 2p能谱中,结合能为458 eV和463.7 eV的2个特征峰分别对应钛元素的Ti 2p3/2和Ti 2p1/2。这与纯TiO2的XPS能谱图一致[9]。
图4(f)的La 3d能谱可拟合为4个特征峰,其中位于834.3 eV处的峰对应La 3d5/2,而处于851.1 eV上的峰则对应La 3d3/2。838.1 eV与855.1 eV处,则为其携上卫星峰。有研究显示,这与金属镧形成的复合氧化物有关[17]。通过位于834.8 eV和851.1 eV的2个特征峰可以证实,Co-g-C3N4/La-TiO2中的镧元素是以La3+形式存在的[18]。与La2O3中La 3d5/2和La 3d3/2对应的特征峰(836.5 eV和853 eV)相比,Co-g-C3N4/La-TiO2的特征峰有一定程度的偏移,这表明镧元素在Co-g-C3N4/La-TiO2中并不是以La2O3的形式存在,La3+也并没有进入TiO2晶格,而是分布于TiO2晶体之间,形成Ti—O—La键[19],这赋予了其优异的催化性。
图4(g)为Co-g-C3N4/La-TiO2的Co 2p能谱,可观察到在780.2 eV和795.6 eV处的Co 2p3/2和Co 2p1/2特征峰以及位于785 eV和801.9 eV附近的卫星峰,这归因于 Co-Nx物质中的 Co2+[20-21]。
2.1.4 UV-Vis分析
使用紫外-可见光(UV-Vis)吸收光谱研究了g-C3N4、TiO2和 Co-g-C3N4/La-TiO2复合材料的光学性质,结果如图5所示。
从图5(a)可以看出,TiO2的光吸收范围较窄,对紫外光吸收较好;但是当光的波长大于400 nm时,TiO2的吸光度较低,这说明TiO2对可见光的利用率较低。g-C3N4对光的吸收范围较TiO2更宽,但是当光的波长大于450 nm时,g-C3N4的吸光度同样显著降低。而Co-g-C3N4/La-TiO2复合材料的光吸收相较于TiO2和g-C3N4发生了红移,增强了对可见光的吸收,拓宽了光的吸收范围,提高了光的利用率,这说明Co-g-C3N4/La-TiO2在可见光波段下的光的利用效率较高。
图5(b)为(Ahv)1/2对hv做的图,曲线切线与横坐标交点为样品的禁带宽度。由图(b)可知g-C3N4、TiO2和Co-g-C3N4/La-TiO2的禁带宽度分别为2.36 eV、2.95 eV和2.14 eV;Co-g-C3N4/La-TiO2复合材料的禁带宽度相对于g-C3N4和TiO2明显变窄,这也可以说明Co-g-C3N4/La-TiO2复合材料的可利用光的范围明显增大。

2.1.5 光致发光光谱分析
样品的荧光强度越高,光生电子-空穴对复合的概率就越高,光催化性能也就越低[22]。因此,可以通过对比样品的光致发光(PL)强度来比较其光催化性能的高低。有研究表明,在g-C3N4晶格中引入金属离子,可以加速电荷在g-C3N4表面迁移,减小能带带隙,增强g-C3N4吸光能力,进而改善g-C3N4的光催化性能[23]。
图6为g-C3N4和Co-g-C3N4的光致发光光谱,图7为 TiO2、La-TiO2和 Co-g-C3N4/La-TiO2的光致发光光谱。
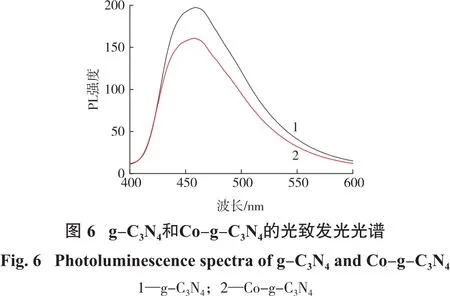
从图6可以看出,Co掺杂的g-C3N4的PL强度低于g-C3N4的强度。从图7可以看出,La掺杂的TiO2的PL强度也低于TiO2的PL强度,这可能是La掺杂后TiO2晶格发生畸变,原子间的键长及原子的电荷量也有所变化,导致TiO2体系中的八面体的偶极矩增大,增强了光生电子-空穴对的分离效率,从而提高TiO2在可见光范围的光催化活性[24]。而Co-g-C3N4/La-TiO2的PL强度最低,说明Co-g-C3N4/La-TiO2能够有效抑制光生电子-空穴对的复合,提高光催化效率。

2.2 光催化试验结果与分析
2.2.1 Co-g-C3N4/La-TiO2投加量对乙基黄药去除率的影响
向反应容器中加入50 mL乙基黄药模拟废水(浓度为60 mg/L),将Co-g-C3N4/La-TiO2的投加量分别控制在0.6 g/L、0.8 g/L、1.0 g/L和1.2 g/L,控制每个反应容器的pH=7。试验结果如图8所示。

由图8可知,经过30 min的吸附脱附后,乙基黄药的去除率在16%~19%,去除率随着催化剂投加量的增加而有所增加,但是增加幅度并不大。在光照射后,乙基黄药的去除率随着时间的增加而增加;同时乙基黄药的去除率也随着催化剂投加量的增加而变大,催化剂投加量为0.6 g/L、0.8 g/L、1.0 g/L和1.2 g/L的模拟废水在光催化60 min后,乙基黄药的去除率分别为94.7%、98.2%、99.1%和99.5%。催化剂投加量为1 g/L和1.2 g/L的催化效果较好,这两个投加量下乙基黄药的去除率非常接近,从经济角度考虑,Co-g-C3N4/La-TiO2的最佳投加量为1 g/L。
2.2.2 pH对乙基黄药去除率的影响
用盐酸和氢氧化钠来调节乙基黄药模拟废水的pH值。每个反应器中加入50 mL浓度为60 mg/L的乙基黄药模拟废水,Co-g-C3N4/La-TiO2的投加量为1 g/L,分别调节反应器内的模拟废水pH为4、5、7、9和10。试验结果如图9所示。

由图9可知,随着模拟废水的pH的升高,乙基黄药的降解率随之降低,这说明乙基黄药在酸性溶液中比较容易降解,但是在碱性溶液中也有较好的去除效果,在pH=10的模拟废水中,经过60 min的光催化,乙基黄药的降解率为98.8%。这证明Co-g-C3N4/La-TiO2可以应用于实际的乙基黄药废水的处理。
2.2.3 乙基黄药的初始浓度对乙基黄药去除率的影响
在实际生产中,黄药浮选废水的pH一般在10~11[25]。为了使得配制的废水更加接近实际情况,本组实验的模拟废水pH为10,Co-g-C3N4/La-TiO2的投加量为1 g/L,在此条件下,考察乙基黄药初始浓度对乙基黄药去除率的影响。试验结果如图10所示。
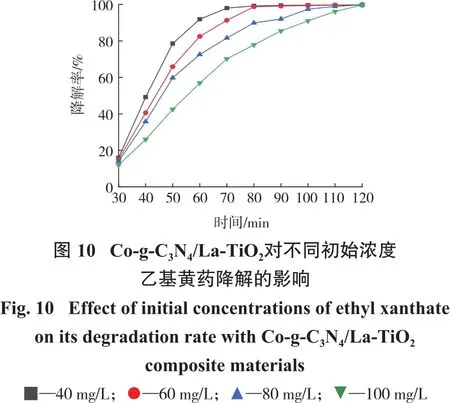
由图10可知,随着乙基黄药初始浓度的增加,其降解率的增长速率降低。当初始浓度为40 mg/L时,在光催化30 min后,其降解率可达91.9%;而乙基黄药初始浓度为60 mg/L、80 mg/L、100 mg/L的模拟废水降解率达到90%分别需要40 min、50 min、70 min。虽然浓度较高的乙基黄药废水的光催化降解需要更长的时间,但最终仍可达到预期效果。由于实际浮选废水中黄药的浓度一般为 5~50 mg/L[26],因此 Co-g-C3N4/La-TiO2在实际废水中具有理想的去除乙基黄药的效果。
2.3 光催化机理研究
为了研究光催化降解乙基黄药过程中起主要作用的活性自由基,对Co-g-C3N4/La-TiO2催化降解乙基黄药设计了活性自由基捕捉试验(参见1.3.3)。试验结果如图11所示。
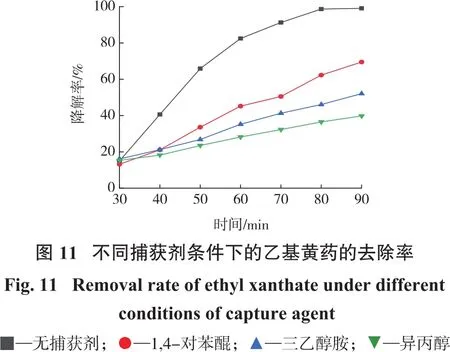
由图11可知,在光催化60 min后,无捕获剂的乙基黄药降解率达到了99.1%,而加入三乙醇胺、异丙醇、1,4-对苯醌的乙基黄药降解率仅达到了52.1%、39.8%和69.5%。由此可知,h+、·OH和·O2-都在Cog-C3N4/La-TiO2催化降解乙基黄药过程中起到了重要作用,对光催化的贡献程度·OH>h+>·O-2
。
3 结 论
(1)通过溶胶-凝胶法制备出一种具有较高可见光催化活性的复合型光催化材料Co-g-C3N4/La-TiO2。其禁带宽度明显减小、吸收带边红移,光催化效率较高。La是以La3+形式分布于TiO2晶体之间,形成Ti—O—La键,Co以Co2+形式与g-C3N形成Co-Nx键。
(2)Co-g-C3N4/La-TiO2可以对模拟选矿废水中乙基黄药进行高效降解。催化剂投加量、模拟废水pH、乙基黄药的初始浓度都对光催化效果均有一定影响;催化剂最经济的投加量为1 g/L;在酸性条件下,乙基黄药的降解速率最快。但考虑到实际的选矿废水的溶液pH为10~11,在催化降解乙基黄药时,调整pH为10,此时同样能使乙基黄药达到较好的去除效果。当乙基黄药初始浓度为40 mg/L时,在光催化30 min后其降解率就可以达到91.9%;当初始浓度为60 mg/L,光催化60 min时,乙基黄药的去除率可达到99.1%。
(3)对Co-g-C3N4/La-TiO2光催化降解乙基黄药设计了活性自由基捕捉试验,试验发现h+、·OH和·O2-都在Co-g-C3N4/La-TiO2催化降解乙基黄药过程中起到了重要作用,对光催化的贡献程度·OH>h+>·O2-。

