血必净注射液治疗脓毒症有效性的Meta 分析
刘静婷,曹学东,李会芳
(1.山西中医药大学,山西 晋中 030619;2.山西省中西医结合医院,山西 太原 030013)
脓毒症(sepsis)是由于感染引起宿主反应失调导致的危及生命的器官功能障碍,是严重创伤、烧伤、战伤以及休克、感染、外科大手术等过程中常见并发症,是因各类感染而引起的全身炎症性反应[1]。临床特征为寒战、高热或低热,起病急,发展快,神智淡漠或烦躁,昏迷,心率快,脉搏细数,呼吸急促或困难,肝脾大,甚至休克。脓毒症是重症监护的常见病,因发病率高、死亡率高、治疗费用高而引起大部分全球医学工作者的密切关注[2]。在脓毒症的治疗中,抗感染治疗是非常重要的环节之一,会使用到抗生素和中药注射剂。从红花、赤芍、当归、川芎、丹参五味中药中提取有效成分制成的血必净注射液具有活血化瘀、清热解毒、扶正祛邪等功效[1,3],目前已广泛应用于脓毒症的临床治疗并取得良好的辅助治疗效果,但对其有效性尚缺少系统的研究及评价。因此,本研究在常规治疗基础上对血必净注射液治疗脓毒症的有效性进行了系统评价,为今后血必净注射液的临床应用提供证据。
1 资料与方法
1.1 纳入标准
①研究类型为随机对照试验(RCT)的临床研究文献,无论是否采用盲法。②脓毒症诊断符合2001 年美国危重病医学会、欧洲重症监护学会、美国胸科医师协会、美国胸科学会及外科感染学会联席会议制定的脓毒症诊断标准[4]。研究对象为确诊脓毒症的患者。患者的种族、性别、年龄、疗程以及疾病严重程度不限,但用药途径相同。③干预措施:治疗组采用血必净注射液(剂量、产地、疗程不限)+常规治疗,对照组采用常规治疗(包括液体复苏、抗生素使用、持续血液净化和呼吸机支持等脓毒症指南中推荐的治疗方法)。④观察指标:主要指标包括总体有效率、28 d 病死率、白细胞计数(WBC)、中性粒细胞计数(N)、血小板计数(PLT)、凝血酶原时间(PT)、活化部分凝血活酶时间(APTT)、C 反应蛋白(CRP)、肿瘤坏死因子-α(TNF-α)和降钙素原(PCT);次要指标包括体温(T)、呼吸频率(R)、心率(HR)、白介素6/8(IL-6/8)、肌酐(Cr)、总胆红素(TBiL)、谷丙转氨酶(ALT/GPT)、谷草转氨酶(AST/GOT)、肌酸激酶(CK)、肌酸激酶同工酶(CK-MB)、乳酸脱氢酶(LDH)。
1.2 排除标准
①脓毒症诊断标准不明确的临床研究;②治疗组的观察药物只包含血必净注射液和常规治疗药物,凡治疗组出现其他药物的临床研究文献一律剔除;③重复文献只取1 篇;④原始数据不完整导致无法充分利用的文献;⑤排除对血必净注射液过敏的患者。
1.3 文献检索
计算机检索中国知网数据库(CNKI)、中国生物医学文献数据库(CBM)、维普数据库(VIP)、万方数据库、Cochrane 图书馆和PubMed,所有数据库均检索至2019 年8 月。中文检索词包括:血必净注射液、脓毒症、临床和随机对照试验;英文检索词包括:Xuebijing injection,seps is,clinical research,RCT,查阅所有检出论文的参考文献作为补充。
1.4 资料提取
由2 项研究者根据纳入和排除标准独立筛选符合的文献,并对入选的文献提取资料和质量评价。2 项研究者共同核对各自提取的信息,对有疑问的文献交给第三位研究者决定。
1.5 文献质量评价
文献质量评价主要参照Jadad 随机对照试验评分法[5]和Cochrane 评价手册5.1.0[6]中的随机对照试验风险评估工具评价纳入研究的质量,主要评价内容包括:随机方法是否采用随机数字表法;基线是否相似;是否实施分配隐藏;是否对受试者、干预提供者和结果评价者施盲法;结果数据是否完整,有无失访或退出,若有失访或退出时,是否采用意向治疗分析(ITT);是否存在其他偏倚来源。
1.6 Meta 分析
Meta 分析采用RevMan 5.3 软件进行异质性检验和疗效效应量统计学分析。用I2评估异质性大小,如果异质性检验结果提示I2<50%,表明各项研究之间异质性较小,故选用固定效应模型估计合并效应量;如果异质性检验结果提示I2≥50%,则应考查和分析异质性来源(如研究对象、研究质量、疗程剂量等),通过亚组分析或敏感性分析来降低异质性I2值。若I2值仍≥50%,则采用随机效应模型估计合并效应量。
疗效效应量统计学分析要进行假设检验(采用U 检验),用Z 和P 表示,当P<0.05 时疗效效应量的差异有统计学意义。疗效效应量分为计数资料和计量资料两类,计数资料采用比值比(OR),计量资料采用均差(MD),区间估计采用95%可信区间(CI)。异质性检验和疗效效应量假设检验的结果均显示在森林图中。疗效指标下的文献数≥10篇的要做漏斗图,分析是否有发表偏倚。
2 结果
2.1 纳入研究的一般情况
2.1.1 文献检索结果 6 个数据库一共检索到60篇文献,通过全文阅读文献,排除不符合要求的文献,最后有16 篇文献[7-22]纳入本次研究。
2.1.2 纳入研究的基本特征 纳入的16 项研究总共1423 例患者,所有患者均为中国人种,其中血必净注射液治疗组743 例,对照组680 例;最大样本数为182 例,最小样本数为16 例。研究中的血必净注射液均为国产静脉用药,用药剂量为30~100 mL/次不等,用药疗程为3~8 d 不等。纳入文献的特征见表1。
2.2 纳入研究的质量评价
筛选出的16 篇文献均为中文。根据Jadad 随机对照试验评分法,16 篇文献的Jadad 评分在1~3 分之间。所有纳入的文献均提及随机,其中有9篇[7,9,10,12,17,18,20-22]采用 随机数字表法 分组,其余文献均未提及具体的分组方法。纳入的所有文献均未报道实施分配隐藏、盲法和ITT 分析。3 篇文献[7,10,21]报道失访,其余均未报道失访。16 篇文献均未说明有其他偏倚的来源。纳入研究的方法学质量及Jadad 评分见表2,纳入的研究存在偏倚风险的项目情况见图1。
2.3 Meta 分析结果
2.3.1 总有效率 共有5 项研究[9-10,13,15,18]报道了总有效率,各研究间的异质性较大(I2=66%,P=0.02),采用随机效应模型进行Meta 分析,结果显示差异无统计学意义[OR=1.59,95%CI(0.73,3.48),P=0.25],提示联用血必净注射液治疗组较常规治疗组对脓毒症患者总有效率提高不明显。结果见图2。

表1 纳入研究的基本特征

表2 纳入研究的方法学质量及Jadad 评分

图1 纳入研究产生偏倚风险的项目所占百分比
2.3.2 28 d 病死率 共有5 项研究[8,11,14,16,19]报道了28 d 病死率,各研究之间的效应量异质性<50%(I2=0%,P=0.89),采用固定效应模型进行Meta 分析。结果显示差异有统计学意义[OR=0.35,95%CI(0.20,0.60),P=0.000 2],提示在降低脓毒症患者的28 d 病死率上,联用血必净注射液治疗组的效果优于常规治疗组。结果见图3。
2.3.3 WBC WBC 纳入11 项研究[7-9,11,13-14,16,18-20,22],各研究间的异质性较大(I2=97%,P<0.000 01),故采用随机效应模型进行Meta 分析,结果显示差异有统计学意义[MD=-1.95,95%CI(-3.62,-0.28),P=0.02],提示在降低脓毒症患者的WBC 指标时,联用血必净注射液治疗组的效果优于常规治疗组。结果见图4。
2.3.4 N 有5 项研究[7,11,13,18,20]报道了N,各研究间的异质性较大(I2=99%,P<0.000 01),故采用随机效应模型进行Meta 分析,结果显示差异有统计学意义[MD=-3.22,95%CI(-4.56,-1.88),P<0.000 01],提示在降低脓毒症患者的N 指标时,联用血必净注射液治疗组的效果优于常规治疗组。结果见图5。

图2 血必净注射液治疗脓毒症总有效率森林示意图

图3 血必净注射液治疗脓毒症28 d 病死率森林示意图

图4 血必净注射液治疗脓毒症WBC 森林示意图
2.3.5 PCT 有6 项研究[9,13,17,19,20,22]报道了PCT,各研究间的异质性较大(I2=78%,P=0.000 3),故采用随机效应模型进行Meta 分析,结果显示差异有统计学意义[MD=-1.29,95%CI(-1.97,-0.62),P=0.000 2],提示在降低脓毒症患者的PCT 指标时,联用血必净注射液治疗组的效果优于常规治疗组。结果见图6。
2.3.6 CRP 有8 项研究[9,11,13,16,18-20,22]报道了CRP,各研究间的异质性较大(I2=92%,P<0.000 01)。重查文献发现CRP 指标的单位不同,其中CRP 单位为mg/L 有5 篇,ng/L、ug/L、g/L 各1 篇,因此对CRP单位为mg/L 的5 篇进行亚组分析。5 篇研究[9,11,16,19,20]之间存在异质性(I2=68%,P=0.01),故采用随机效应模型进行Meta 分析,结果显示差异有统计学意义[MD=-19.26,95%CI(-29.50,-9.03),P=0.000 2],提示在降低脓毒症患者的CRP 指标时,联用血必净注射液治疗组的效果优于常规治疗组。结果见图7。
2.3.7 TNF-α 共有4 项研究[13,17,18,20]报道了TNFα,各研究之间的效应量异质性较小(I2=17%,P=0.31),故采用固定效应模型进行Meta 分析。结果显示差异有统计学意义[MD=-35.46,95%CI(-45.49,-25.44),P<0.000 01],提示在降低脓毒症患者的TNF-α 指标时,联用血必净注射液治疗组的效果优于常规治疗组。结果见图8。
2.3.8 PLT 有4 项研究[8,12,20,21]报道了PLT,各研究间的异质性较大(I2=99%,P<0.000 01),故采用随机效应模型进行Meta 分析,结果显示差异无统计学意义[MD=45.63,95%CI(-18.83,110.10),P=0.17],提示联用血必净注射液治疗组较常规治疗组对脓毒症患者的PLT 升高不明显。结果见图9。
2.3.9 PT 共有4 项研究[7,12,20,21]报道了PT,各研究之间的效应量异质性较小(I2=10%,P=0.35),故采用固定效应模型进行Meta 分析。结果显示差异有统计学意义[MD=-2.85,95%CI(-3.35,-2.35),P<0.000 01],提示在降低脓毒症患者的PT 指标时,联用血必净注射液治疗组的效果优于常规治疗组。结果见图10。
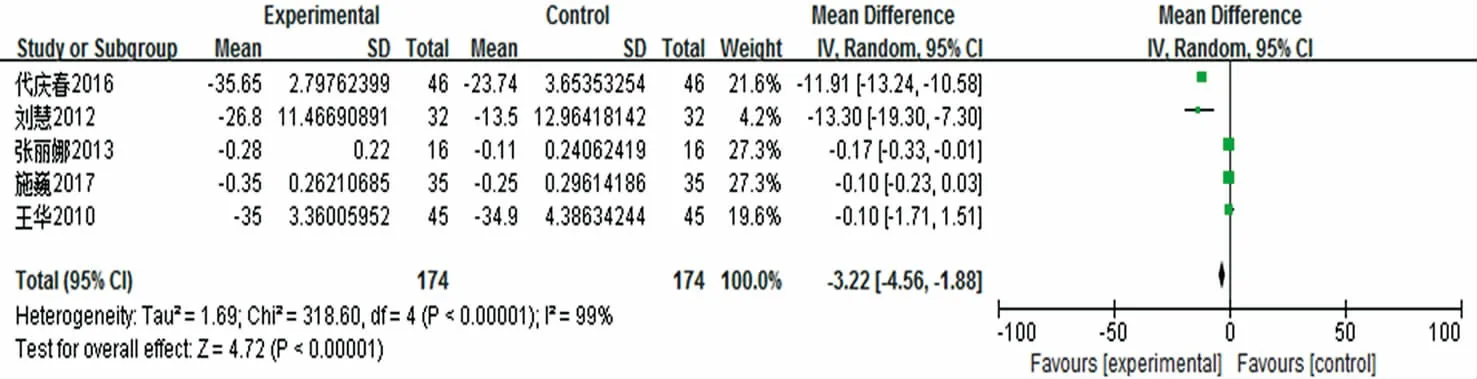
图5 血必净注射液治疗脓毒症N 森林示意图
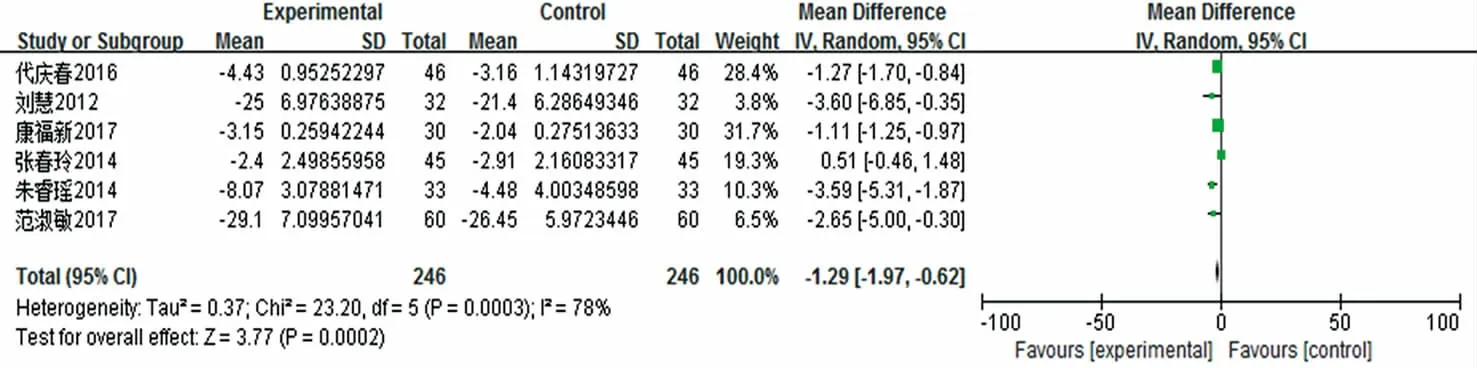
图6 血必净注射液治疗脓毒症PCT 森林示意图

图7 血必净注射液治疗脓毒症CRP 森林示意图
2.3.10 APTT 共有4 项研究[7,12,20,21]报道了APTT,各研究之间的效应量异质性<50%(I2=0%,P=0.53),故采用固定效应模型进行Meta 分析。结果显示差异有统计学意义[MD=-4.44,95%CI(-5.46,-3.42),P<0.000 01],提示在降低脓毒症患者的APTT 指标时,联用血必净注射液治疗组的效果优于常规治疗组。结果见图11。
2.3.11 发表偏倚 纳入WBC 的文献有11 篇(≥10 篇),故使用RevMan 5.3 软件做漏斗图进行文献发表偏倚的分析,大部分样本点分布在漏斗图的顶部,并且样本点分布在中心对称线上或其左右,呈现为一个对称的漏斗图,提示纳入WBC 的11 篇文献偏倚程度小,存在潜在的发表偏倚的可能性小。其他终点指标由于纳入文献数量较少,则不必做漏斗图分析,但存在发表偏倚的可能性非常大。结果见图12。
3 讨论
本次系统评价纳入的16 项研究包括1423 例脓毒症患者。Meta 分析结果表明,与常规治疗组比较,联用血必净注射液治疗组可以降低脓毒症患者的28 d 病死率、WBC、N、PCT、CRP、TNF-α、PT及APTT,但在总有效率、PLT 方面升高不明显。

图8 血必净注射液治疗脓毒症TNF-α 森林示意图

图9 血必净注射液治疗脓毒症PLT 森林示意图

图10 血必净注射液治疗脓毒症PT 森林示意图

图11 血必净注射液治疗脓毒症APTT 森林示意图

图12 血必净注射液治疗脓毒症对WBC 影响的漏斗图
从纳入研究的质量评价结果可以看出,纳入的16 篇文献质量总体不高,Jadad 评分3 分的文献3 篇,Jadad 评分2 分的文献6 篇,其余7 篇文献为1 分。16 篇文献中无1 篇采用分配隐藏、盲法和ITT(意向性分析)方案,这些因素都会导致研究中存在测量偏倚和实施偏倚。16 篇文献中有9 篇文献报道了采用随机数字表法分组,其余只提及随机分组,具体方法未说明,增加了整个研究中的选择偏倚。有3 篇文献报道了失访或退出,其余未明确描述,故对结局数据的完整性存在疑虑。并且多数研究样本量较小,降低了研究结果的可靠性。
血必净注射液具有活血化瘀、清热解毒、扶正固本、菌毒并治等功效。现代药理研究有抗炎、抗氧化应激、调节免疫和改善凝血等功能[23],用于治疗全身炎症反应综合征(SIRS)和多器官功能障碍综合征(MODS)[1]。血必净注射液对脓毒症的治疗表现出良好的临床疗效,得到广泛的认可。本研究中总有效率的疗效判定标准以中医证候积分和客观指标为主,一部分研究提到脓毒症发病率、MODS发生率和病死率,但总有效率Meta 分析所纳入的文献较少,目前结果提示常规治疗联用血必净注射液之后对脓毒症患者总体有效率提高不明显,需要纳入更多的包含总有效率终点指标的文献一同研究,以期得出更加真实和疗效明确的结论。
根据血必净注射液治疗脓毒症Meta 分析的结果,在常规治疗的基础上联用血必净注射液治疗脓毒症有一定的治疗效果。但由于纳入的文献质量总体不高,为进一步验证其有效性需要开展设计严格的大样本、多中心、双盲的随机对照临床试验[24]。

