糖皮质激素替代治疗对成人腺垂体功能减退症患者糖脂代谢的影响
贾文娟,冯志美,张莹,郑方平,黄启亚,杨彩娴
广州医科大学附属第六医院,清远市人民医院,广东 清远 511500
腺垂体功能减退症是由于垂体损伤引起的多种或单一的腺垂体激素分泌不足所导致的一组临床综合征。其中继发性肾上腺皮质功能减退导致促肾上腺皮质激素(ACTH)分泌的缺乏,是腺垂体功能减退症较为常见的一种,也是一种潜在威胁生命的疾病。继发性肾上腺皮质功能减退症均可导致心血管疾病、代谢疾病和感染性疾病的发生,从而引起死亡率的上升。最近有研究表明,不恰当的激素替代治疗(剂量或时间的不同)可能是引起上述疾病及死亡率增加的重要原因。高血压、胰岛素抵抗、体质量增加、腹型肥胖,以及体质量指数的增加、代谢综合征、糖耐量异常、糖尿病、血脂障碍可能都与糖皮质激素替代治疗过量有关,如果同时合并有生长激素、性腺激素等缺乏者,补充激素后上述表现尤为明显[1-2]。我国《内科学》(第9 版)教材关于腺垂体功能减退症章节中,对于确诊为继发性肾上腺皮质功能减退症后,必须尽快补充肾上腺皮质激素,采用氢化可的松(皮质醇,hydrocortisone,HC)最符合生理性,而醋酸可的松(皮质素)需在体内经肝脏转变为皮质醇才能发挥作用,对肝功能障碍者疗效较差。替代剂量需要依据临床情况而定,氢化可的松最大剂量不超过30 mg/d[3]。2016年美国内分泌学会临床实践指南关于成人垂体机能减退症激素补充治疗推荐:使用氢化可的松,通常每日总剂量为15~20 mg,单次或分多次给药。清晨睡醒后用一次,剂量最大,次剂量是下午给药(若两次给药);或午餐时、下午较晚的时间第二次和第三次给药(若三次给药)[4]。本研究主要探讨不同生理剂量糖皮质激素替代治疗对腺垂体功能减退症患者血糖、血脂代谢等的影响。
1 资料与方法
1.1 一般资料
收集2017 年6 月至2018 年6 月在广州医科大学附属第六医院内分泌科门诊和住院部就诊的18例成人腺垂体功能减退症患者为研究对象。
1.2 纳入和排除标准
纳入标准:(1)年龄大于18 岁;(2)结合病史(垂体瘤术后、产后大出血等)、症状(乏力、纳差、闭经、产后无乳等)、生化检查(反复低钠、低血压、低血糖等、促肾上腺皮质激素<100 nmol/L)等,明确诊断为成人腺垂体功能减退症;(3)合并甲状腺功能低下,但未补充性激素及生长激素。排除标准:(1)入组前已合并糖尿病者;(2)妊娠期妇女;(3)合并有严重心脑血管疾病、恶性肿瘤等;(4)精神障碍者;(5)同时口服其他影响血糖的药物。
1.3 病例脱落情况
由于成人腺垂体功能减退症患者病例数较少,收集的部分门诊患者在入组前已在外院诊断且治疗了半年至1 年,按照纳入标准,删除了基线资料不全的病例数,对符合条件的患者进行了随访及统计分析,故总的病例数仍较少。同时由于此病发病率不高,病例数较预期少,危象去除后很多患者在当地医院就诊或自行购药,依从性差,造成了较高的失访率。因此完成统计的仅18 例。
1.4 治疗方法
目前国内外“指南”[3-4]对糖皮质激素替代治疗成人腺垂体功能减退症有不同剂量推荐,具体根据医生的临床经验及患者病情,在患者充分知情同意下给予氢化可的松治疗。观察组:氢化可的松剂量为20 mg/d。对照组:氢化可的松剂量为30 mg/d。两组均长期服药,并定期随访。
1.5 观察指标
首次就诊时,采集患者基本信息、身高、体质量、生命体征、病程、用药,以及相关指标,如空腹血糖、血脂(胆固醇、三酰甘油、高密度脂蛋白胆固醇、低密度脂蛋白胆固醇)、肝功能(谷丙转氨酶、谷草转氨酶)、血钠、血钾、糖化血红蛋白等基线值,服药后每3 个月随访一次,监测上述指标。随访2 年,比较两组2 年后相关指标的变化。
1.6 统计学方法
采用SPSS 25.0 统计学软件分析数据。计量资料采用表示,数据对比采用配对t检验,当P<0.05 表示差异有统计学意义。
2 结果
氢化可的松治疗后2 年,观察组空腹血糖(FBG)、糖化血红蛋白(HbA1c)、总胆固醇(CHO)、三酰甘油(TG)、低密度脂蛋白胆固醇(LDL-CH)、高密度脂蛋白胆固醇(HDL-CH)、血钾与治疗前比较,差异无统计学意义(P>0.05);对照组FBG、TG 较治疗前升高,差异有统计学意义(P<0.05),CHO、LDL-CH、HDL-CH、HbA1c 较治疗前无明显变化,差异无统计学意义(P>0.05),见表1。
表1 不同剂量氢化可的松治疗成人腺垂体功能减退观察指标变化情况()
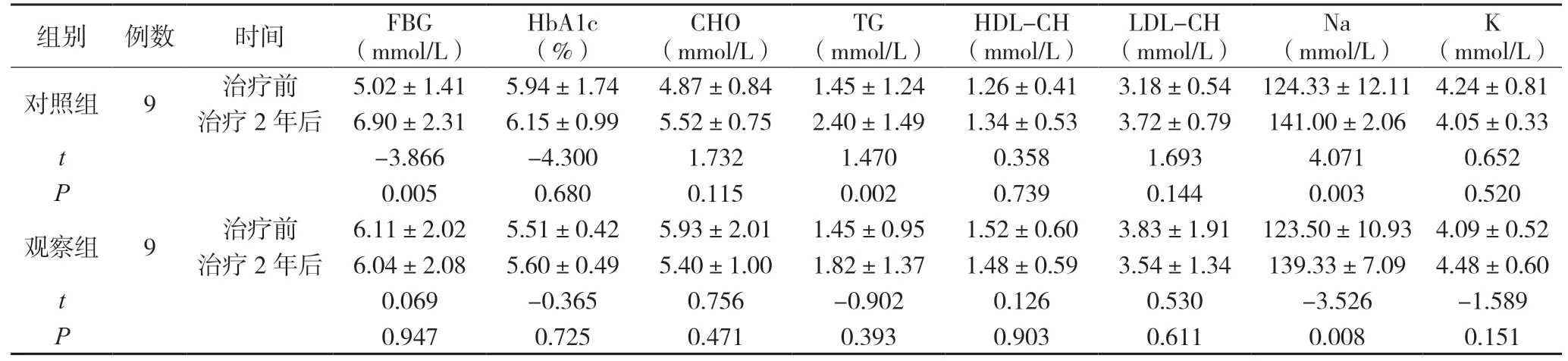
表1 不同剂量氢化可的松治疗成人腺垂体功能减退观察指标变化情况()
注:两组治疗前比较,差异无统计学意义(P>0.05)。
3 讨论
腺垂体功能减退是指垂体或下丘脑的多种病损可累及垂体的内分泌功能,当垂体的全部或绝大部分被毁坏后,可产生一系列内分泌腺功能减退的表现。主要累及的腺体为性腺、甲状腺及肾上腺皮质,多见于成年(21~40 岁)。成人腺垂体功能减退又称为Simmond 病,患病率为150~280 例/100 万,女性则更高[5]。最常见的病因为产后垂体缺血坏死(Sheehan 综合征、席汉综合征)及垂体腺瘤,还有颅咽管瘤术后。因垂体前叶病变所造成的各种激素分泌减少,其程度各有不同,其相对应的靶器官功能低下的临床表现则不完全平行,发病早晚不一,症状轻重不同。常见的临床表现为乏力、食欲减退、恶心、呕吐、腹泻、低血压及腹痛。一般起病较缓慢,症状随着时间逐渐出现。由于临床症状的不典型性,容易引起漏诊甚至误诊,常常延误了糖皮质激素替代治疗,7.4%的继发性肾上腺功能低下及10.6%的原发性肾上腺功能低下的患者经历过至少4次或更多次的肾上腺危象。本研究病例女性患者主要为席汉综合征。该病最早出现泌乳素及促性腺激素缺乏的表现,如产后无乳、闭经、体毛、性欲减退、乳房缩小、继发不孕等[6],后期多数有恶心、呕吐,经检查后发现“反复出现难以纠正的低钠血症”。由于起病症状不一,首诊科室有脑科、心血管科、消化科、血液科等,所以对于不明原因“乏力、恶性呕吐、意识障碍”就诊患者一定要排除该病,尽早做出处理,避免垂体危象出现[2]。
由于本研究主要病例均为18 岁以上成人,并未进行生长激素补充。女性均为已婚已育,由于未出现明显骨质疏松,且在告知患者可能出现子宫内膜癌等不良反应后,由于传统观念的影响及地区的特点,女性患者均未同意补充雌激素,但笔者仍建议50 岁以下女性可考虑补充雌激素。由于低促性腺激素性腺功能减退的患者均为中青年男性,就诊时在补充糖皮质激素的同时,均给予补充雄激素(如睾酮),对于有生育需求的男性,给予应用HCG(人绒毛膜促性腺激素)治疗。
皮质醇增多与高血糖及胰岛素抵抗相关,对胰腺造成不良影响[7]。磷脂酰肌醇-3-激酶(phosphatidylinositol 3-kinases,PI3K)通路在胰岛素信号减少NO 合酶激活和引起内皮损伤中发挥作用,最终增加心血管风险[8]。有文献报道,成人腺垂体功能减退症患者糖皮质激素替代治疗后,糖尿病的发生率明显升高。据“指南”推荐,临床常用剂量大小可能是影响糖耐量异常甚至进展到糖尿病的主要原因[4]。糖皮质激素引起糖耐量受损的机制是通过减少外周组织对葡萄糖的利用和通过加强糖异生,增加了肝糖原的输出[9]。
寻求合适的剂量对这类患者的治疗有重大意义。此研究由于总体病例数较少,可能存在未能准确反应生理剂量激素替代治疗的真实情况,故笔者在分析数据的同时,将既往3 年(2014—2017 年)在本院住院的44 例患者数据进行了分析,除去缺失的例数外,查阅随访至今的病例资料42 例,发现仅有5 例发生了糖代谢异常,2 例已明确为2 型糖尿病。此2 例糖尿病患者年龄均较大,1 例为大于70 岁的男性,1 例为大于50 岁的女性,故结合临床病例分析及此次数据分析均能表明,生理替代量糖皮质激素引起糖尿病的可能性不大[10]。
通过分析所选病例,结果仅2 例出现糖尿病。据《中国2 型糖尿病防治指南(2017 年版)》[11]资料,我国糖尿病发病率已达到11.3%,所以目前结果表明,生理剂量糖皮质激素替代治疗长期应用对糖耐量的影响不大,需继续随访观察。另外,给药时间一般是每天8 时、16 时,因为如果一天中太迟给药可引起夜晚更高的糖皮质激素暴露,这可能影响睡眠,并且可能对代谢有更多的不良反应。本研究结果显示,每天生理替代量20 mg 氢化可的松是安全的,对血糖、血脂影响不大,但30 mg/d 氢化可的松,可能引起空腹血糖及三酰甘油升高。同时,结合最新“指南”,建议补充20 mg/d 氢化可的松,对成人腺垂体功能减退症患者的糖皮质激素是安全的[4],当然临床医生也要根据患者的临床表现及电解质、血压等结果,采取个性化原则进行调整及给药。
综上所述,对于腺垂体功能减退症患者给予补充生理替代剂量糖皮质激素是相对安全的,也是必要的,但仍需监测血糖、血脂变化情况。同时,建议根据临床症状不同,采取个体化的原则。

