氟苯尼考及其代谢物氟苯尼考胺在鸡蛋中的残留消除规律
张静,周倩,高玉时,唐修君,陆俊贤,马丽娜,陈大伟,唐梦君
(江苏省家禽科学研究所,江苏 扬州225125)
氟苯尼考(florfenicol,FF)[1],又名氟甲砜霉素,是动物专用氯霉素类广谱抗菌药物,因其吸收好、体内分布广、安全高效,并且无再生障碍性贫血的特点,被广泛用于治疗猪、禽、牛以及水产等养殖动物的细菌性疾病[2]。然而,氟苯尼考对哺乳动物具有胚胎毒性,人体用药后会出现厌食、腹泻等不良症状。农业农村部在《食品安全国家标准 食品中兽药最大残留限量》(GB 31650—2019)中规定,氟苯尼考的最高残留限量为肌肉中不得超过100 μg/kg,产蛋期家禽禁用[3]。然而,目前蛋鸡生产中违规使用这些药物的情况仍时有发生。研究蛋鸡中氟苯尼考的残留消除规律,可为保证蛋鸡产品安全与有效检测监督提供技术依据。
氟苯尼考的残留不仅有原形药物,还有氟苯尼考胺(florfenicol amine,FFA)、氟苯尼考醇和一些尚不清楚的代谢物形式,但主要代谢产物为氟苯尼考胺,氟苯尼考和氟苯尼考胺均作为食品中氟苯尼考的标示性残留物。目前,国内外对氟苯尼考及其代谢物氟苯尼考胺的串联质谱残留检测方法研究较多[4-7],其残留规律研究主要集中在鸡和水产上[8-14],但关于产蛋期鸡蛋中氟苯尼考及其代谢物氟苯尼考胺残留消除规律的研究较少。本试验在国内常规饲养条件下,连续5 d 内按体质量以15 和30 mg/kg 剂量预拌料方式分别给海蓝褐壳蛋鸡喂药,测定给药期每天和停药后不同时间氟苯尼考及其代谢物氟苯尼考胺在全蛋、蛋黄和蛋清中的残留量,以获得药物残留消除规律,为蛋鸡产品安全监督提供科学依据。
1 材料与方法
1.1 试验动物及分组
选取90 只42 周龄健康海蓝褐壳蛋鸡,体质量为1.9~2.0 kg,随机分成3组:第1组为空白对照组;第2组为预防组,饲料中按体质量拌入15 mg/kg的氟苯尼考粉;第3 组为治疗组,饲料中按体质量拌入30 mg/kg 的氟苯尼考粉。每组30 只鸡,分为5 个重复,每个重复6 只鸡。饲养试验在国家家禽生产性能测定中心进行,试验鸡按每个重复进行笼养,给药前称量,试验前预饲阶段正常饲养和饮水,并保证喂药前不饲喂氟苯尼考。
1.2 主要试剂配制与材料
氟苯尼考(FF)标准品、氟苯尼考胺(FFA)标准品和氘代氯霉素(氯霉素-D5)均购自德国Dr.Eherenstorfer公司;氟苯尼考原粉(生产批号170103,规格10%),购自上海同仁药业股份有限公司上海兽药厂;乙腈、丙酮、正己烷、甲醇均购自德国Merck公司;甲酸(>98%)购自上海阿拉丁生化科技股份有限公司;氨水(分析纯)购自上海安谱实验科技股份有限公司;LC-Si 固相萃取柱,购自美国Supelco公司。
氟苯尼考标准品储备液:准确称取氟苯尼考标准品9.998 mg于100 mL棕色容量瓶中,用甲醇溶解并定容至刻度,即成0.1 mg/L 的氟苯尼考标准液,于-20 ℃冰箱中保存。氟苯尼考胺标准品储备液:准确称取氟苯尼考胺标准品9.996 mg 于100 mL 棕色容量瓶中,用甲醇溶解并定容至刻度,即成0.1 mg/L的氟苯尼考胺标准液,于-20 ℃冰箱中保存。
2 µg/mL 混合标准品储备液:分别量取2 mL 0.1 mg/L氟苯尼考和氟苯尼考胺标准品储备液于棕色容量瓶中,用甲醇定容至刻度,配制成2µg/mL的氟苯尼考和氟苯尼考胺混标储备液,于-20℃冰箱中保存。
氨水-乙腈(体积比1∶19)溶液:按体积比量取氨水和乙腈,混匀备用。丙酮-正己烷(体积比1∶9)和丙酮-正己烷(体积比4∶6)溶液:按体积比量取丙酮和正己烷,混匀备用。甲醇-0.1%甲酸(体积比1∶9)水溶液:按体积比先量取甲酸和氨水配置0.1%甲酸水溶液,再按体积比量取甲醇和0.1%甲酸水溶液,混匀备用。
1.3 主要仪器
TSQ MAX 质谱仪、ACCLEA 高效液相色谱仪(美国Thermo公司);RZ-218A搅拌机(安徽合肥荣事达电子科技有限公司);XS105 电子分析天平(瑞士Mettler Toledo 公司);3-30K 台式高速冷冻离心机(德国Sigma 公司);超声波清洗器(上海科导超声仪器有限公司);VTX-3000L 涡旋仪(比利时LMS 公司);VX-Ⅲ振荡器(北京踏锦科技有限公司);固相萃取装置(美国Supelco 公司);N-EVAP 112氮吹仪(美国Organomation公司)。
1.4 给药剂量、方式及样品采集
预防组和治疗组蛋鸡分别按体质量以15 和30 mg/kg 剂量拌料,根据鸡采食习惯采用拌料方式给药,试验期间每天一次性给药;对照组饲喂不含药的等量饲料。每只鸡日采食量150~200 g,连续饲喂5 d,分别收集给药期和停药后第1、2、3、5、7、10、12、15、18天的各组鸡蛋,每3枚鸡蛋混合成一个样品,每组重复5个样品。分别制备全蛋、蛋黄和蛋清样品,于-20 ℃冰箱中保存。
1.5 试验方法
1.5.1 色谱条件及参数
采用美国Waters XSelectR CSHTMC18 色谱柱(2.1 mm×150 mm,3.5 µm),流动相为0.1%甲酸水溶液(A)-甲醇(B)。梯度洗脱程序:0~0.5 min,流动相A 为90%,B 为10%,保持0.5 min;0.5~4.0 min,流动相A由90%降至10%,保持2.2 min;6.20~6.21 min,流动相A 由10%增至90%,保持至8.0 min。流速0.2 mL/min,柱温30 ℃,进样量10 μL。
1.5.2 样品提取与净化
称取试样5.00 g(精确至0.01 g),置于50 mL离心管中,加入100 μL 100 ng/mL 氯霉素-D5 工作溶液,并用10 mL 5%氨水-乙腈溶液提取,涡旋混匀后以6 000 r/min离心5 min。将上清液移入另一50 mL离心管中。重复提取一次,合并上清液。用45 ℃氮气吹干,加入5 mL 丙酮-正己烷(体积比1∶9)溶解残渣。
用5 mL 丙酮-正己烷(体积比1∶9)淋洗LC-Si固相萃取柱,弃去淋洗液,将残渣溶解液转移到固相萃取小柱上,弃去流出液,抽干,用5 mL丙酮-正己烷(体积比6∶4)洗脱。洗脱液用45 ℃氮气吹干后置于2 mL 甲醇-0.1%甲酸(体积比1∶9)中溶解,用正己烷去脂,过0.22 μm 滤膜,供高效液相色谱-串联质谱法(high performance liquid chromatographytandem mass spectrometry, HPLC-MS/MS)测定,用内标法定量。
1.5.3 标准曲线、检出限及定量限
由于氟苯尼考基质效应影响大,因此采用基质标准曲线内标法进行线性关系确定。参照1.5.2 节处理空白样品后,采用甲醇-0.1%甲酸(体积比1∶9)水溶液将2µg/mL氟苯尼考和氟苯尼考胺储备液稀释成质量浓度分别为2、4、10、20、100、160、200 和400 ng/mL 的系列标准工作液,采用HPLC-MS/MS分析。每个质量浓度点重复测定3 次,取平均值绘制质量浓度(x)和外标与内标色谱峰面积之比(y)的标准曲线。按1.5.2节的方法操作,向空白样品中添加一定质量浓度的氟苯尼考和氟苯尼考胺的标准溶液,进行HPLC-MS/MS 分析,并逐渐降低氟苯尼考和氟苯尼考胺的质量浓度,将样品检测的信噪比(signal to noise ratio,S/N)为3和10时的质量浓度分别作为药物在鸡蛋中的检出限和定量限。
1.5.4 样品回收率和精密度测定
准确称取5.00 g(精确至0.01 g)空白试样匀浆液于50 mL 离心管中,并添加不同质量浓度的标准工作液,使得空白匀浆液中FF和FFA添加量分别为1.0、2.0、5.0 μg/kg。每个添加量设6个平行,经1.5.2节的方法提取和净化后进样做HPLC-MS/MS 检测,用内标法定量,计算添加回收率。分别在1周内不同日相同时间点,6 次重复测定1.0、2.0、5.0 μg/kg这3 种添加水平下试样的回收率,并求日内和日间精密度。
1.5.5 全蛋、蛋黄和蛋清中氟苯尼考及其代谢物氟苯尼考胺残留量的测定
将全蛋、蛋黄和蛋清中所测得的氟苯尼考及其代谢物氟苯尼考胺色谱峰面积分别代入标准曲线,得到氟苯尼考及其代谢物氟苯尼考胺的残留量。
2 结果与分析
2.1 线性范围、决定系数、定量限和检出限
分别以氟苯尼考、氟苯尼考胺的外标与内标色谱峰面积之比(y)对氟苯尼考、氟苯尼考胺的质量浓度(x,ng/mL)作图,得到标准曲线。氟苯尼考的回归方程为y=6 234.61x+97 068.7,决定系数R2=0.990 1;氟苯尼考胺的回归方程为y=110 511x+108 858,决定系数R2=0.998 6。氟苯尼考和氟苯尼考胺在2~400 ng/mL质量浓度范围内,色谱峰面积与质量浓度线性关系良好。
应用本试验建立的检测方法,全蛋、蛋黄和蛋清中氟苯尼考和氟苯尼考胺的检出限均为2 μg/kg,定量限均为5 μg/kg。结果表明,该方法灵敏度高,完全能满足氟苯尼考及其代谢物氟苯尼考胺在全蛋、蛋黄和蛋清中残留检测的需要。
2.2 样品回收率和精密度
从表1中可知:氟苯尼考和氟苯尼考胺在添加质量分数为1.0~5.0 μg/kg 时,平均回收率为78.9%~105.0%,日内精密度(日内相对标准偏差)为2.22%~4.22%,日间精密度(日间相对标准偏差)为4.22%~6.54%。准确度和精密度能满足相关标准要求[15]。

表1 氟苯尼考和氟苯尼考胺在全蛋、蛋黄和蛋清中的回收率和精密度Table 1 Recovery and precision of florfenicol(FF)and florfenicol amine(FFA)in egg,egg yolk and egg white
2.3 鸡蛋中氟苯尼考及其代谢物氟苯尼考胺残留量的测定结果
2.3.1 全蛋、蛋黄和蛋清中氟苯尼考残留量
从表2 可以看出:各试验组蛋鸡分别按体质量以15和30 mg/kg的剂量预拌料方式给药,在用药期间(每天给药1次,连续给药5 d),全蛋、蛋黄和蛋清中的氟苯尼考含量总体趋势随用药天数的增加而增大。停药后,15 mg/kg剂量组全蛋和蛋清中FF残留量在停药第1 天达到最大值,分别为341.60 和520.70 μg/kg;蛋黄在停药第2 天达到最大值,为285.96 μg/kg;蛋清中氟苯尼考残留量峰值高于全蛋和蛋黄。停药后,30 mg/kg剂量组全蛋、蛋黄和蛋清中FF 残留量在停药第1 天达到最大值,分别为758.41、442.40 和797.12 μg/kg,蛋清中氟苯尼考残留量峰值高于全蛋和蛋黄。在停药期间,全蛋、蛋黄和蛋清中的氟苯尼考含量整体上随着停药天数的延长不断减少,消除速度与残留量呈正相关。不同剂量组均是蛋清中的氟苯尼考消除速度最快,在停药第10天氟苯尼考含量已低于检出限;蛋黄中消除速度最慢,30 mg/kg剂量组在停药第18天氟苯尼考含量才低于检出限。
2.3.2 全蛋、蛋黄和蛋清中氟苯尼考的代谢物氟苯尼考胺残留量
从表3可以看出:各试验组蛋鸡分别按体质量以15和30 mg/kg的剂量预拌料方式给药,在用药期间(每天给药1次,连续给药5 d),全蛋、蛋黄和蛋清中的氟苯尼考胺含量总体趋势随用药天数的增加而增大。15 mg/kg剂量组蛋黄和蛋清中FFA残留量在停药第1天达到最大值,分别为218.40和87.36 μg/kg;全蛋在停药第3天达到最大值,为78.99 μg/kg;蛋黄中的氟苯尼考胺残留量峰值高于全蛋和蛋清。30 mg/kg剂量组全蛋和蛋清中FFA残留量在停药第1天达到最大值,分别为285.48、36.89 μg/kg;蛋黄在停药第3 天达到最大值,为646.14 μg/kg;蛋黄中的氟苯尼考胺残留量峰值高于全蛋和蛋清。在停药期间,全蛋、蛋黄和蛋清中氟苯尼考胺的消除速度与残留量呈正相关。不同剂量组均是蛋清的氟苯尼考胺消除速度最快,在停药第10天氟苯尼考胺含量已低于检出限;蛋黄中消除速度最慢,在停药第18天氟苯尼考胺残留值才低于检出限。

表2 鸡蛋中氟苯尼考残留量Table 2 Residue of FF in eggs μg/kg
2.3.3 全蛋、蛋黄和蛋清中氟苯尼考及其代谢物氟苯尼考胺总残留量
从表4 可以看出:各试验组蛋鸡分别按体质量以15和30 mg/kg的剂量预拌料方式给药,在用药期间(每天给药1次,连续给药5 d),全蛋、蛋黄和蛋清中的氟苯尼考与氟苯尼考胺总残留量总体趋势随用药天数的增加而增大。15 mg/kg 组全蛋、蛋黄和蛋清中FF与FFA总残留量在停药第1天达到最大值,分别为391.25、500.29 和608.06 μg/kg,蛋清中的总残留量峰值高于全蛋和蛋黄;30 mg/kg组全蛋和蛋清中FF与FFA总残留量在停药第1天达到最大值,分别为1 043.89 和834.01 μg/kg,蛋黄在停药第3 天达到最大值,为1 073.91 μg/kg,蛋黄中总残留量峰值高于全蛋和蛋清。在停药期间,全蛋、蛋黄、蛋清中的氟苯尼考和氟苯尼考胺总残留量整体上随着停药天数的延长不断减少,消除速度与残留量呈正相关。不同剂量组均是蛋清中氟苯尼考与氟苯尼考胺总残留消除速度最快,在停药第10天氟苯尼考和氟苯尼考胺总残留量已低于检出限;蛋黄中氟苯尼考与氟苯尼考胺消除速度最慢,在停药第18天氟苯尼考和氟苯尼考胺总残留量才低于检出限。
3 讨论
3.1 色谱操作条件的影响
试验中比较了不同流动相对分离度、峰形、灵敏度等的影响。结果发现:水相的酸碱度对氟苯尼考和氟苯尼考胺的分离影响不大,对质谱响应值也无明显影响,而有机相用乙腈比用甲醇时氟苯尼考和氟苯尼考胺峰形更好。利用梯度洗脱的方法,分离效果更好,因此,本试验采用水-乙腈作为流动相体系。此外,本试验所使用的Waters XSelectR
CSHTMC18 色谱柱区别于普通C18 色谱柱,其表面带电杂化颗粒,能使极性化合物氟苯尼考胺保留较好,出峰时间稳定。由此可见,该色谱操作条件的选择是较为理想的。
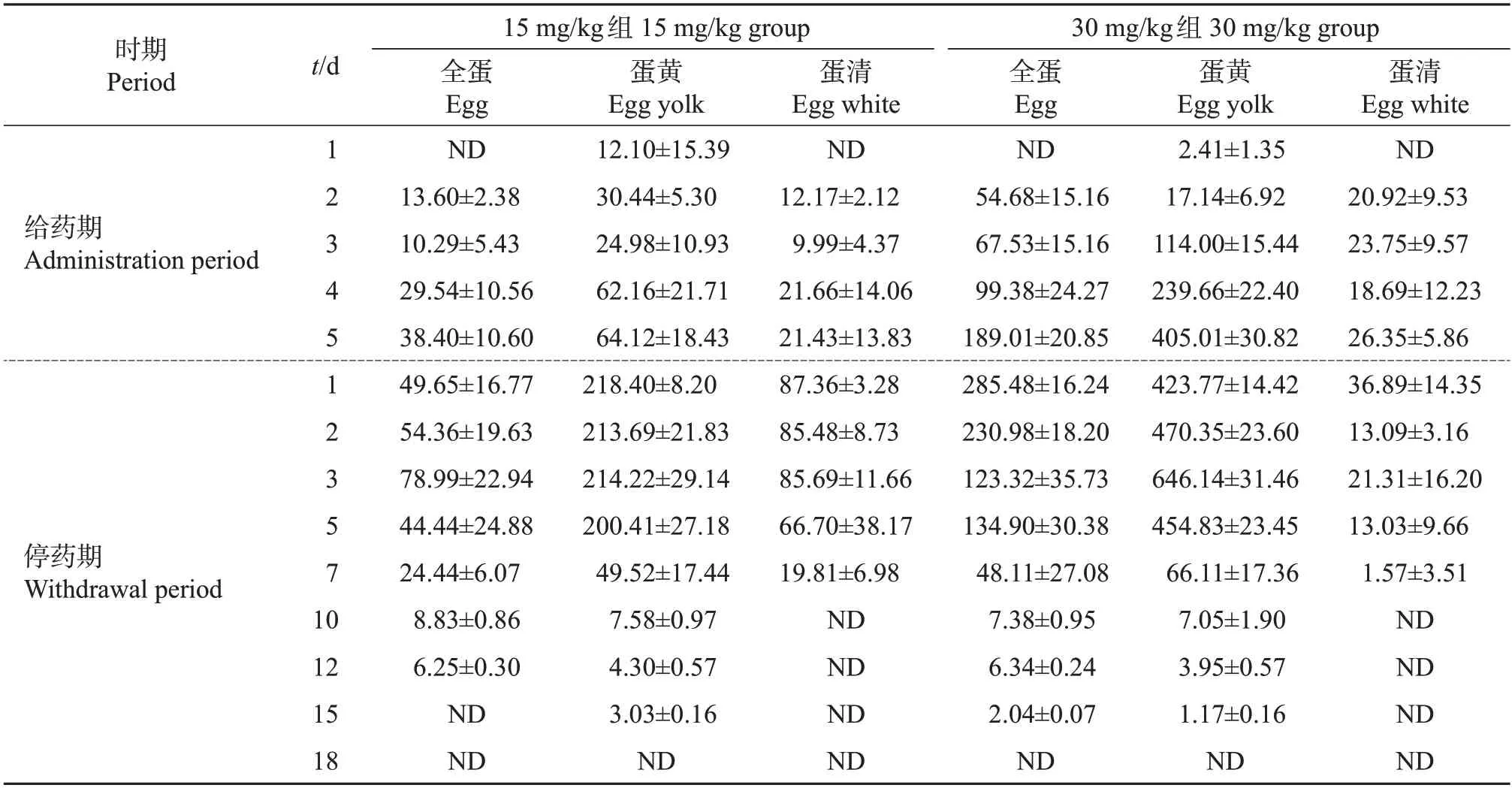
表3 鸡蛋中氟苯尼考胺残留量Table 3 Residue of FFA in eggs μg/kg

表4 鸡蛋中氟苯尼考与氟苯尼考胺的总残留量Table 4 Total residues of FF and FFA in eggs μg/kg
3.2 样品提取与净化的影响
常用的氟苯尼考提取剂主要有碱化的乙酸乙酯、乙腈以及一些混合提取剂。本研究分别采用乙腈和碱化的乙酸乙酯作为提取剂,进行对比试验。结果表明:采用碱化的乙酸乙酯作为提取剂时,会引入油脂等杂质,不利于后续的净化,而且回收率偏低;而采用碱化的乙腈作为提取剂时,提取液较干净,方便快速,且不用制备提取剂,现买现用。
采用固相萃取法进行净化浓缩试验,并比较LC-Si小柱和C18小柱净化效果。结果表明:LC-Si小柱的净化效果更好,回收率更高。同时,也比较了经提取后直接采取正己烷除脂的方法,发现样品不够清澈,有较多油脂,特别是全蛋样品,且对仪器损伤很大。
3.3 氟苯尼考及其代谢物氟苯尼考胺在鸡蛋中的残留消除规律
不同剂量组中氟苯尼考残留的消除规律基本一致,残留量与喂药剂量呈正相关,蛋清中残留的氟苯尼考消除较快,蛋黄中残留的氟苯尼考消除时间较长,这可能与氟苯尼考的亲脂性有很大关系。氟苯尼考胺残留消除规律与氟苯尼考残留消除规律基本一致,即残留量与喂药剂量呈正相关,氟苯尼考胺首先在蛋黄中被检测到,提示氟苯尼考可能首先在蛋黄中残留,其中蛋黄中的含量高于全蛋和蛋清,其在蛋黄中的残留时间最长,这可能与氟苯尼考胺的亲脂结构有关。
同一剂量组中,蛋黄中氟苯尼考和氟苯尼考胺残留量及残留消除速率接近,表明蛋黄中氟苯尼考以原型和代谢物2 种形式残留;而在同一剂量组蛋清中氟苯尼考残留量远高于氟苯尼考胺,提示蛋清中氟苯尼考主要以原型代谢。根据药物残留量及消除速率,建议鸡蛋中以氟苯尼考和氟苯尼考胺总残留量为氟苯尼考残留标志物指示值。
4 结论
氟苯尼考和氟苯尼考胺残留量及其总残留量与喂药剂量呈正相关,氟苯尼考在蛋清中残留消除较快,其残留量高于蛋黄,而氟苯尼考胺主要存在于蛋黄中。蛋黄中氟苯尼考和氟苯尼考胺残留时间长。不同剂量组蛋黄中氟苯尼考残留时间达18 d。

