表面肌电生物反馈结合吞咽训练对脑梗死后吞咽障碍患者吞咽功能康复的影响
邓巍巍
(齐齐哈尔市第一医院神经内科,黑龙江齐齐哈尔 161000)
吞咽障碍是脑梗死后常见的并发症,如不及时治疗,可导致脱水、营养不良等症状,不利于疾病预后[1]。现阶段, 临床针对吞咽障碍尚无特异性的治疗方法,主要通过吞咽训练帮助患者恢复吞咽功能,但吞咽康复过程缓慢,仍会对患者的生活质量造成影响[2]。随着现代康复医学的不断发展,临床不满足于单纯吞咽训练,更加注重行为干预与非行为干预相结合的康复手段。表面肌电生物反馈训练是通过生物反馈技术指导个体进行针对性训练,是一种行为与非行为结合的康复技术,近年来被广泛应用于临床,并取得不错的效果[3]。 基于此,该文选取2019年2月—2020年12月该院收治的94 例脑梗死后吞咽障碍患者为研究对象,通过分组对照,探讨表面肌电生物反馈结合吞咽训练对患者吞咽功能康复的影响。 报道如下。
1 资料与方法
1.1 一般资料
选取该院收治的94 例脑梗死后吞咽障碍患者为研究对象, 按随机数字表法分为对照组与试验组,各47 例。 试验组男26 例,女21 例;年龄57~79 岁,平均年龄(66.92±3.15)岁;病程7~38 d,平均病程(21.13±2.66)d;洼田饮水试验分级:III 级16 例,IV 级25 例,V 级6 例。 对照组男28 例,女19 例;年龄55~78 岁,平均年龄(67.03±3.28)岁;病程9~39 d,平均病程(22.33±2.89)d; 洼田饮水试验分级: III 级18 例,IV级24 例,V 级5 例。 两组一般资料比较,差异无统计学意义(P>0.05)。该研究经该院医学伦理委员会审批通过。
1.2 纳入、排除标准
纳入标准:符合《中国脑梗死中西医结合诊治指南(2017)》[4]脑梗死诊断标准;吞咽造影检查提示不同程度吞咽障碍;存在进食困难、进食期间出现呛咳、哽噎症状;患者签署知情同意书。排除标准:有喉部手术史;入组前伴随营养不良;对表面肌电生物反馈、吞咽训练不耐受。
1.3 方法
两组患者均接受常规治疗, 包括降低颅内压、调脂、营养神经等。
1.3.1 对照组
采用吞咽训练。 (1)基础训练:针对舌、舌骨等部位进行力量训练,医生指导患者伸出舌肌,向不同方向伸展, 配合鼓腮与舌肌咬合进行练习,15 min/次,1次/d。 (2)咽冷刺激训练:医生将冰冻棉棒蘸取适量水后柔和地刺激患者的软腭、舌根、咽后壁等处,引导患者做空吞咽运动,15 min/次,1 次/d。 (3)门德尔松吞咽训练:医生嘱患者吞咽时用舌尖抵住硬腭,屏住呼吸,维持喉部抬起状态,尽可能延长时间,间隔2 min练习1 次,10 次/组,2 组/d。 (4)摄食练习:选择合适摄食体位与食物,医生先用冰棉棒刺激口腔,待患者出现吞咽动作,确定有吞咽功能后,将糊状食物从口腔健侧送入至舌根,控制进食时间为30 min。 以上训练5 d/周,持续训练4周。
1.3.2 试验组
在对照组基础上采用表面肌电生物反馈干预。患者取坐位,放松身体,用酒精擦拭其颈部前侧,将神经和肌肉刺激理疗仪[DJO, LLC,型号:5951,国食药监械(进)字2015 第2263990 号]专用电极对称放置于舌骨上区正中线两侧,再将单个电极放置于颏舌骨肌肌腹部位,调节为AC 模式,设置波宽300 ms、频率30~80 Hz、电流0~20 mA,依据患者耐受程度灵活调节各项参数;患者平静呼吸并放松颌下肌群,自然状态下吞咽唾液,重复5~10 次,中间间隔10 s,记录肌电峰值均值,作为自然吞咽的目标值;嘱咐患者用力吞咽,逐渐提升肌电峰值,直至肌电峰值为自然吞咽目标值的150%,30 min/次,1 次/d,5d/周,持续干预4周。
1.4 观察指标
(1)吞咽功能:干预前后采用标准吞咽功能评价量表(standardized swallowing assessment,SSA)评估患者的吞咽能力,总分17~46分,评分越低提示吞咽能力越好。(2)摄食能力:干预前后采用功能性经口摄食量表(functional oral intake scale,FOIS)评估患者的摄食能力, 总分1~7分,1分为完全不能经口进食,7分为完全经口进食,评分越高提示摄食能力越好。(3)生活质量:干预前后使用吞咽障碍特异性生活质量量表(swallowing quality of life questionnaire,SWAL-QOL)评估患者的生活质量,共44 个条目,每个条目1~5分,评分范围44~220分,分数越高提示生活质量越好。(4)并发症发生率:包括吸入性肺炎、感染、脱水、营养不良。
1.5 统计方法
采用SPSS 20.0 统计学软件进行数据分析,计量资料用(±s)表示,组间比较采用独立样本t 检验,组内比较采用配对样本t 检验;计数资料用[n(%)]表示,采用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者吞咽功能比较
干预前,两组的SSA 评分比较,差异无统计学意义(P>0.05);干预后,两组的SSA 评分低于干预前,且试验组的SSA 评分低于对照组,组间差异有统计学意义(P<0.05)。 见表1。
表1 两组SSA 评分对比[(±s),分]
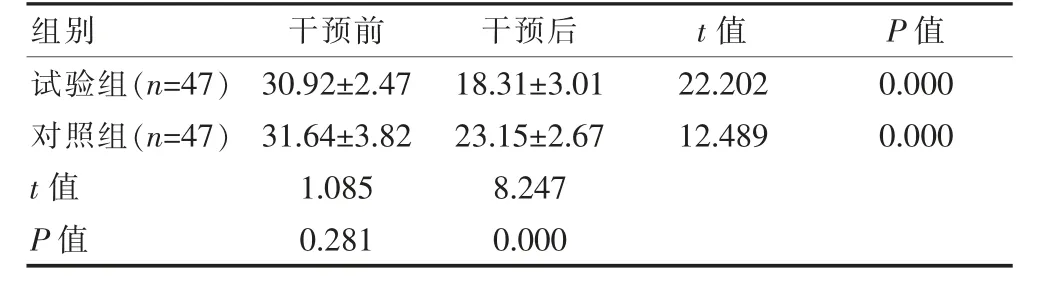
表1 两组SSA 评分对比[(±s),分]
试验组(n=47)对照组(n=47)t 值P 值组别30.92±2.4731.64±3.821.0850.281干预前18.31±3.0123.15±2.678.2470.000干预后22.20212.4890.0000.000 t 值 P 值
2.2 两组患者进食能力、生活质量比较
干预前, 两组的FOIS、SWAL-QOL 评分比较,组间差异无统计学意义 (P>0.05); 干预后, 两组的FOIS、SWAL-QOL 评分均高于干预前, 且试验组的FOIS、SWAL-QOL 评分均高于对照组,组间差异有统计学意义(P<0.05)。 见表2。
表2 两组进食能力、生活质量对比[(±s),分]
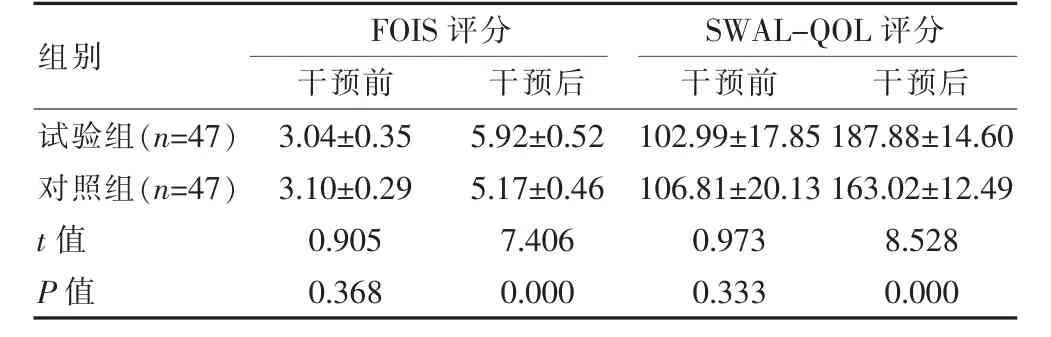
表2 两组进食能力、生活质量对比[(±s),分]
试验组(n=47)对照组(n=47)t 值P 值组别3.04±0.353.10±0.290.9050.3685.92±0.525.17±0.467.4060.000102.99±17.85106.81±20.130.9730.333187.88±14.60163.02±12.498.5280.000 FOIS 评分干预前 干预后SWAL-QOL 评分干预前 干预后
2.3 两组患者并发症发生率比较
试验组的并发症发生率为4.26%,低于对照组的19.15%,差异有统计学意义(P<0.05)。 见表3。

表3 两组并发症发生率比较[n(%)]
3 讨论
吞咽障碍患者摄取食物过程中易发生呛咳、哽噎,还会减少机体营养摄入,导致营养不良、吸入性肺炎、感染等并发症,是引发脑梗死预后不良的重要原因[5-6]。 因此,尽早恢复脑梗死患者的吞咽功能尤为重要。
吞咽是一种神经反射活动,需要颈部、喉部、口腔等多处肌肉共同参与,吞咽训练可通过训练这些部位的肌肉,增强吞咽反射[7]。吞咽基础训练及咽冷刺激训练可提升患者中枢神经系统的吞咽敏感性,强化吞咽反射。直接摄食训练配合门德尔松吞咽训练,能够增强舌肌的力量与灵活性,协调吞咽动作,恢复经口进食能力。但吞咽动作复杂,参与肌肉较多,吞咽训练过程中仅凭患者个人感觉无法准确知晓肌肉的运动状态,康复效果欠佳,还需联合其他康复手段。 该研究中,试验组干预后的SSA 评分低于对照组,FOIS、SWALQOL 评分高于对照组,干预期间的并发症发生率低于对照组(P<0.05),提示表面肌电生物反馈结合吞咽训练能够加快脑梗死后吞咽障碍患者吞咽功能与摄食能力的恢复,促进患者康复。与杜新新等[8]研究结果一致。表面肌电生物反馈是行为与非行为干预结合的神经调控手段,以特定设备将患者吞咽相关肌肉收缩放松状态的肌电信号转化为视听信号,患者能够准确知晓肌肉运动状态,针对性地控制肌肉活动,从而调整吞咽肌肉的时序性与节律性,加快吞咽功能恢复[9-10]。同时电流刺激还能引起咽喉部废用性肌肉主动收缩,纠正肌肉无力状态,增强肌肉力量,进一步增强吞咽反射。中枢神经系统具有可塑性,基于此原理,表面肌电生物反馈训练通过大量重复训练,使得神经侧芽与轴突突触重新联系,恢复吞咽反馈通路。 表面肌电生物反馈与吞咽训练联合,可优势互补,恢复患者进食能力,提升生活质量,减少并发症的发生,提高康复效果。 但该研究观察例数少、时间短,仍有不足之处,今后需进行大量临床试验,探索最佳吞咽康复方案。
综上所述,表面肌电生物反馈结合吞咽训练治疗脑梗死后吞咽障碍可改善患者的吞咽功能与进食能力,减少并发症的发生,提高其生活质量。

