匹莫苯丹关键中间体含量测定方法的建立
赵乐凯 , 郝江南 , 解龙霄 , 崔亮亮 , 王金泉 , 郝智慧
(1. 新疆农业大学动物医学院 , 新疆 乌鲁木齐 830001 ; 2. 中国农业大学动物医学院 , 北京 海淀 100193)
匹莫苯丹又名匹莫苯(Pimobendane),是新一代的钙增敏剂类强心药物[1]。在兽医临床方面,匹莫苯丹已被美国食品药品监督管理局批准用于犬类,治疗继发于慢性瓣膜性心脏病的充血性心力衰竭和扩张型心肌病[2]。匹莫苯丹的作用机制主要是增加肌丝的钙敏感性,并且也有磷酸二酯酶抑制剂的作用和延长动作电位时间的作用[3]。Nautrup等[4]在地高辛和匹莫苯丹临床对比试验中发现,匹莫苯丹较地高辛明显改善患犬心衰评价指标,并且不良反应较少。
目前关于匹莫苯丹合成的文献[5-9]和专利[10-13]已有不少,从这些资料中可以看出,中间体[6-(3,4-二氨基苯基)-4,5-二氢-5-甲基-3(2H)-哒嗪酮(DPDMP)]是合成匹莫苯丹的关键中间体,其结构式见图1。作为匹莫苯丹合成的关键中间体,该化合物的含量将会直接影响后续反应的进料,并最终影响匹莫苯丹的质量和收率,故其合成和含量都十分重要。目前,已有相关文献[8-9]和专利[12-14]涉及此关键中间体的合成,但尚未见该中间体的液相色谱检测方法的报道。本试验建立了DPDMP的高效液相色谱(HPLC)检测方法,并对其进行了验证。
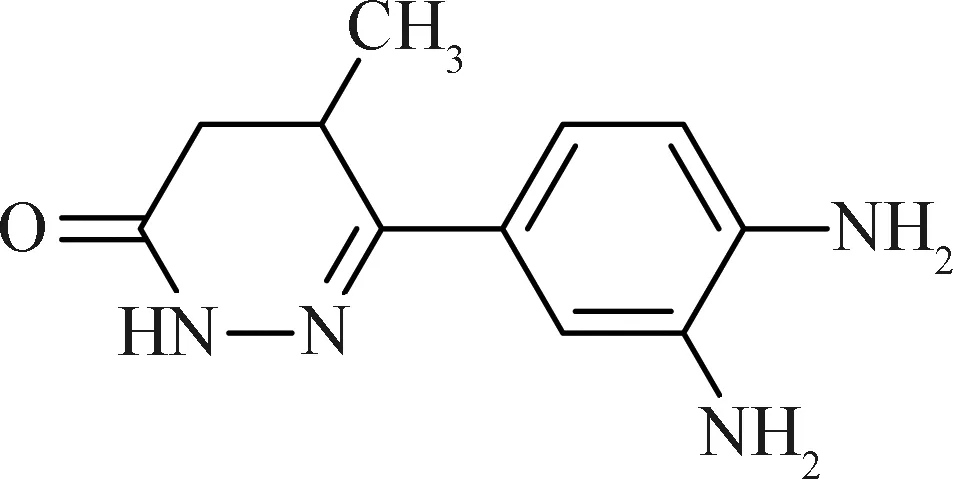
图1 DPDMP结构式Fig. 1 Structural formula of DPDMP
1 仪器与材料
1.1 仪器 安捷伦1260型液相色谱仪(配DAD检测器),购自美国AgiLent公司;电子精密天平(ME203),购自梅特勒-托利多仪器(上海)有限公司。
1.2 试剂与材料 DPDMP对照品,购自香港AOzeal公司,批号:ONL-017-29,含量:99.37%,规格:50 mg;DPDMP供试品,中国农业大学自制,批号:20170810;乙腈、甲醇为色谱纯;水为超纯水。
2 方法与结果
2.1 色谱条件 色谱柱:Inter Sustain C18柱(4.6 mm×250 mm,5 μm),GL Sciences Inc;流动相:20 mmol/L醋酸铵缓冲液(醋酸调至pH 5.5)-甲醇(75∶25,V/V),进样量:10 μL;检测波长:254 nm;流速:1.0 mL/min;柱温:25 ℃。
2.2 溶液制备 DPDMP供试品溶液制备方法:精密称取50 mg DPDMP样品于烧杯中,取少量甲醇溶解,转移至100 mL容量瓶中,在量瓶中加入甲醇稀释至刻度,摇匀,即得。
DPDMP对照品溶液制备方法:供试品溶液准确取1.0 mL,加入至100 mL容量瓶中,加入甲醇,稀释至刻度,摇匀,即得。
DPDMP对照品溶液制备方法:准确称取10 mg DPDMP对照品于烧杯中,取少量甲醇溶解,转移至100 mL容量瓶中,用甲醇稀释至刻度,摇匀,即得。
2.3 系统适用性试验 按照2.2项下制备方法配制6份供试品溶液,按照上述色谱条件进行分析,记录色谱图。结果见表1。结果表明,DPDMP的理论塔板数均在2 000以上,保留时间的RSD小于2%,表明该方法系统适用性良好。

表1 DPDMP含量测定HPLC方法系统适用性试验结果Table 1 System suitability test results for determination of DPDMP content by HPLC method
2.4 方法学考察
2.4.1 线性范围 精密量取DPDMP对照品贮备液适量,加流动相制成DPDMP含量分别为0.67、2.53、25.30、50.60、101.20、253.00 μg/mL和506.00 μg/mL系列浓度的对照品溶液,依照2.1项色谱条件,各个浓度进样2次,进行检测分析,分析后记录色谱图。结果见表2。以峰面积(A)为纵坐标,浓度(C)为横坐标,绘制标准曲线(图2),其线性回归方程:y=24.756 9x+18.651 8,R2=1.000 0。结果表明DPDMP的峰面积与其浓度呈较好的线性关系,可用来进行 DPDMP含量测定。
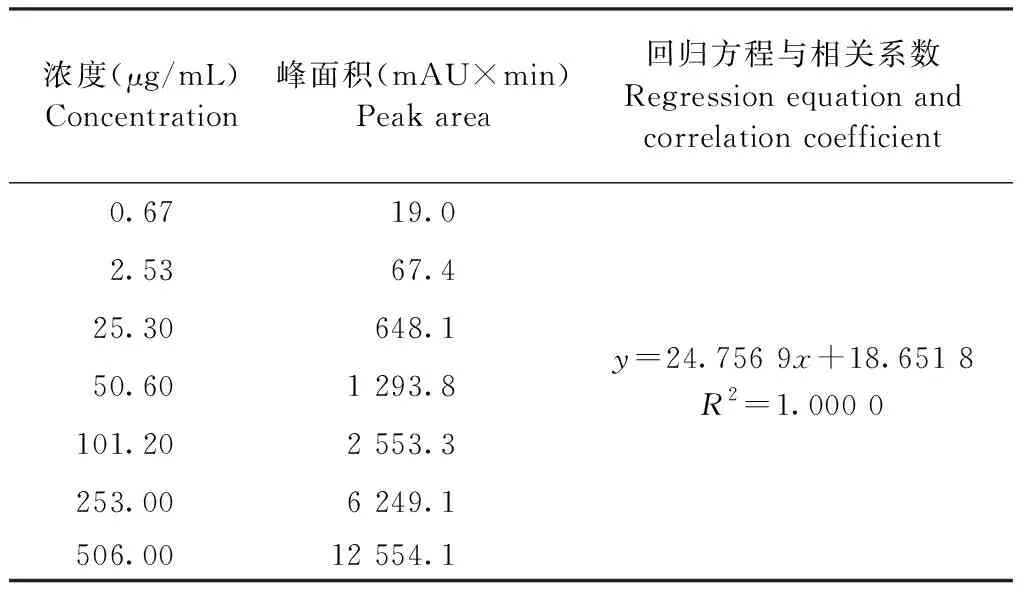
表2 DPDMP线性测定结果Table 2 Linearity determination results of DPDMP

图2 标准曲线Fig.2 Standard curve
2.4.2 专属性试验 以2.1项溶液的配制方法分别配制 DPDMP供试品溶液、对照品溶液。分别量取空白溶剂、供试品溶液及对照品溶液各10 μL,按照2.1项色谱条件进样检测分析,并记录色谱图。结果见图3~5。由色谱图可知,空白溶剂对DPDMP的检测无干扰,该方法的专属性良好。
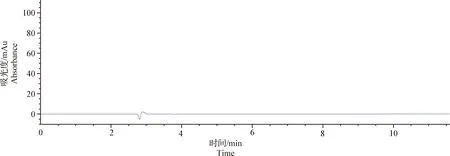
图3 DPDMP空白溶剂色谱图Fig.3 Blank solvent chromatogram of DPDMP
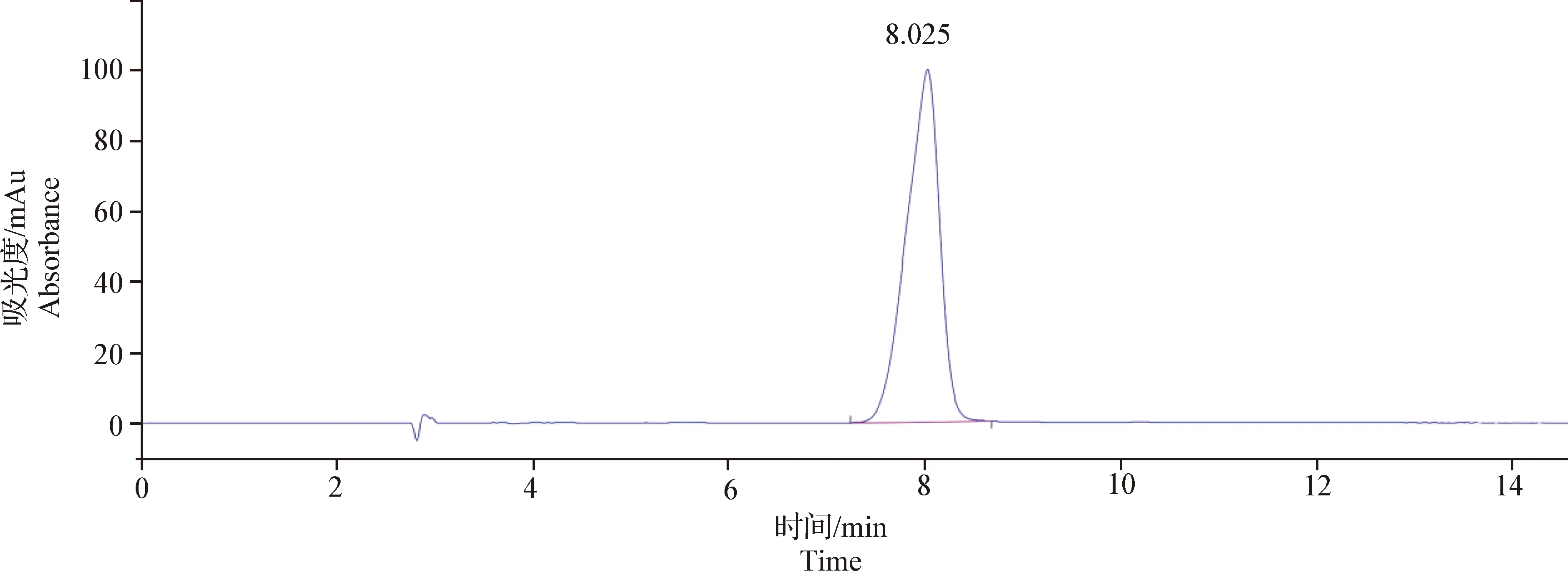
图4 DPDMP对照品溶液色谱图(0.1 mg/mL)Fig.4 Chromatogram of DPDMP reference solution
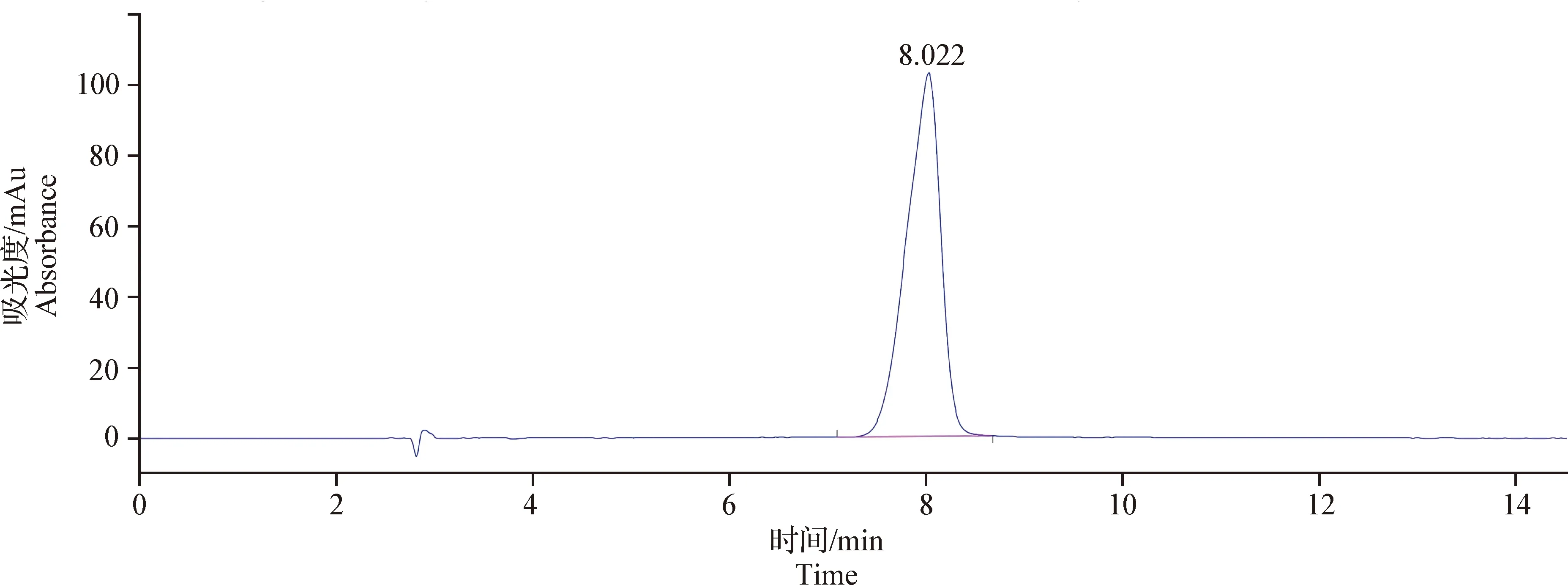
图5 DPDMP供试品溶液色谱图(0.1 mg/mL)Fig.5 Chromatogram of DPDMP test solution
2.4.3 检测限和定量限 用流动相配制系列浓度DPDMP对照品溶液,分别进样;记录色谱图和S/N,进行检测限、定量限的测试。根据《中华人民共和国兽药典》2015年版一部“附录9101兽药质量标准分析方法验证指导原则”,S/N=3对应的浓度为检测限,S/N=10对应的浓度为定量限。结果显示:DPDMP的检测限为0.217 μg/mL,见图6;DPDMP的定量限为0.650 μg/mL,见图7。
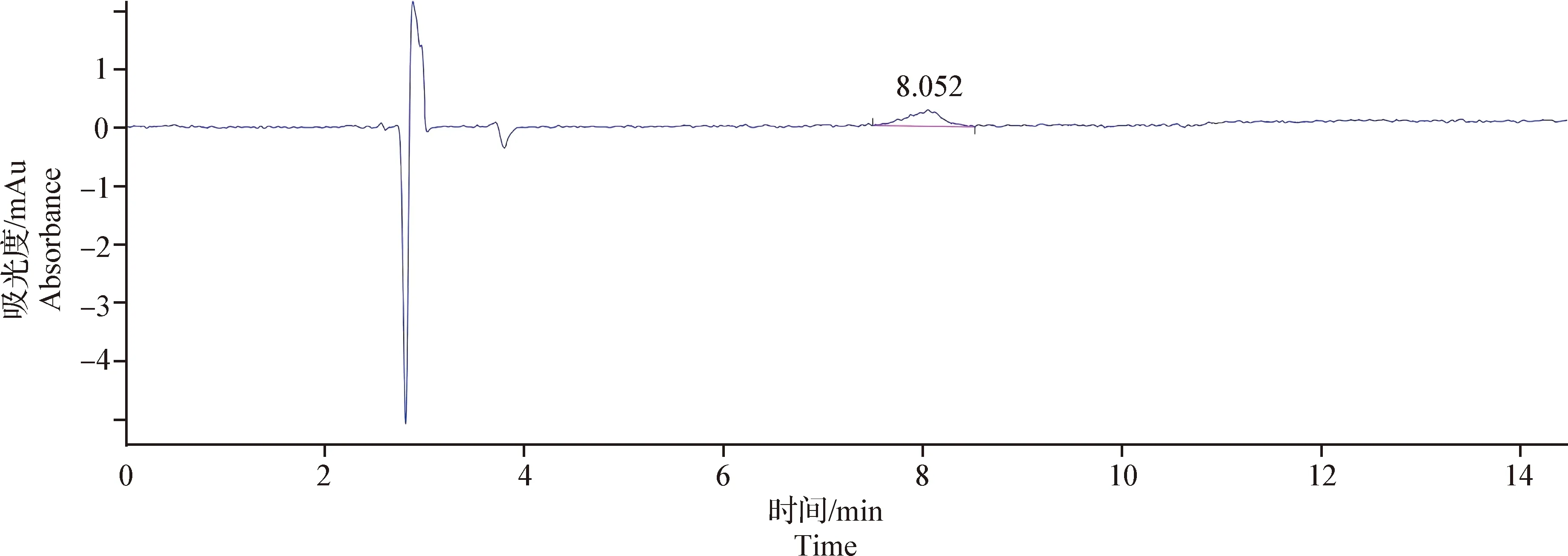
图6 DPDMP检测限色谱图(0.217 μg/mL)Fig.6 Detection limit chromatogram of DPDMP
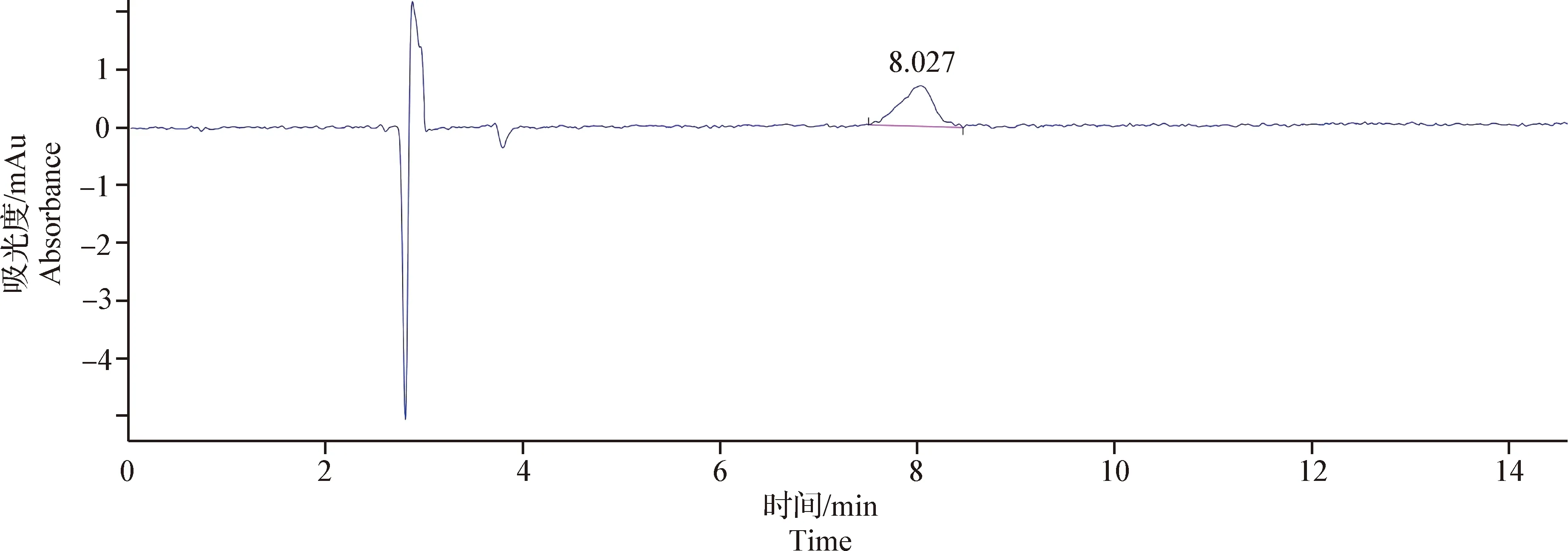
图7 DPDMP定量限色谱图(0.650 μg/mL)Fig.7 Quantitative limit chromatogram of DPDMP
2.4.4 稳定性试验 量取不同时间的供试品溶液,按照2.1项色谱条件进行检测分析,并记录其峰面积。结果如表3所示:DPDMP的峰面积RSD为0.99%,结果表明该溶液稳定性良好。
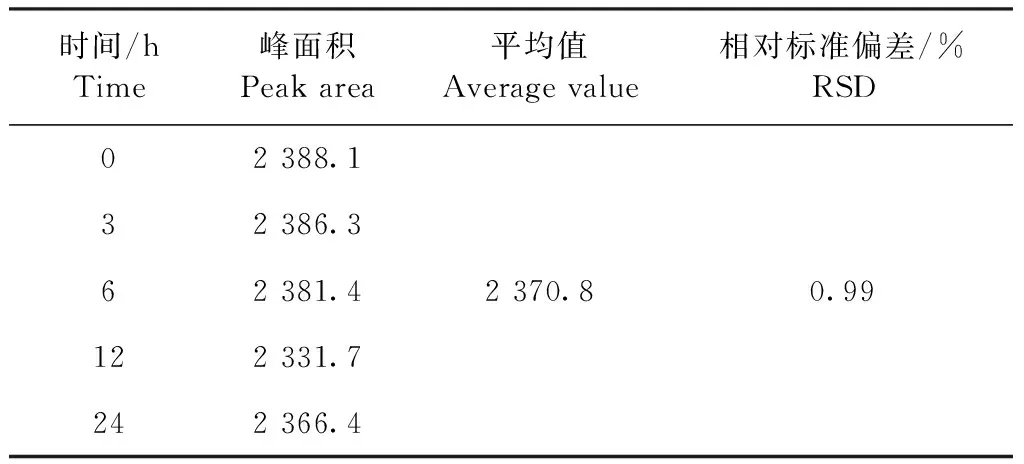
表3 DPDMP含量测定溶液稳定性结果Table 3 Solution stability results for determination of DPDMP content
2.4.5 重复性试验 按照2.2项方法配制6份供试品溶液,以2.1项的色谱条件进行测试分析,记录峰面积。同样,根据对照品溶液的制备方法配制相应的对照品溶液,进行检测分析,并记录峰面积。结果如表4所示:平均峰面积为2 421.4,RSD为1.65%。该试验结果显示,DPDMP峰面积的RSD小于2%,表明本方法重复性良好。
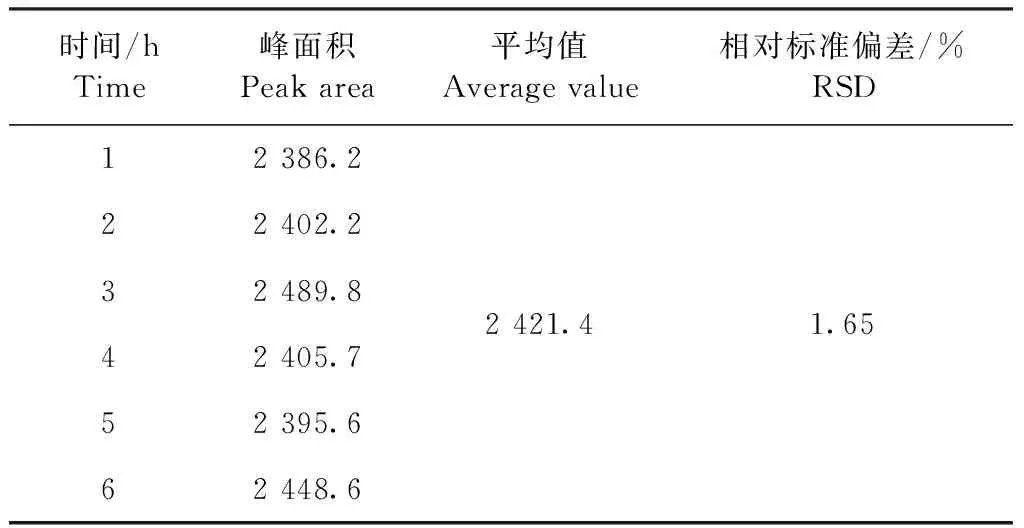
表4 DPDMP含量测定重复性结果Table 4 Repeatability results for determination of DPDMP content
2.4.6 加样回收率试验 取9份已知准确含量的供试品溶液,分别加入匹莫苯丹关键化合物对照品,按照2.2项样品制备方法和2.1项色谱条件进行分析,测定峰面积。结果如表5所示:DPDMP的加样平均回收率为99.52%,RSD为0.86%,符合《中国兽药典》2015年版[15]要求。结果表明本方法准确度好。
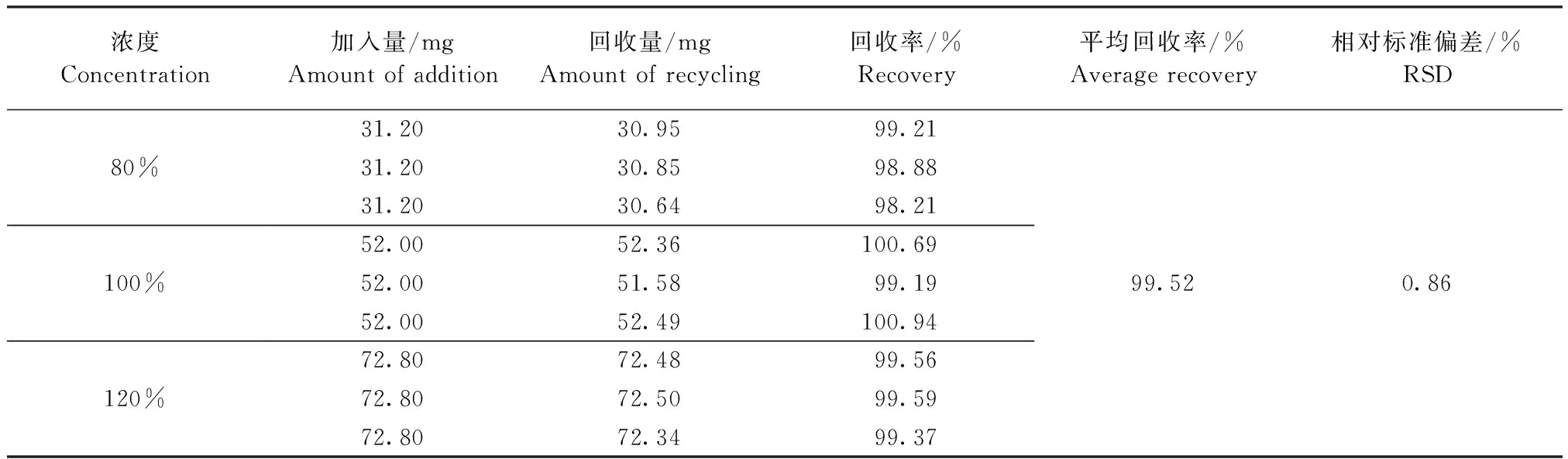
表5 DPDMP回收率试验结果Table 5 Recovery test results of DPDMP (n=9)
2.5 样品测定 取3批自制 DPDMP样品,按照2.2项制备方法配制供试品溶液。并按照2.1项色谱条件进行检测,检测结果见表6。结果表明,采用HPLC法,测定 DPDMP的含量,操作简单,专属性良好。DPDMP三批样品的含量均大于98.0%。

表6 3批 DPDMP样品含量测定结果Table 6 Determination results of DPDMP samples in 3 batches
3 讨论
DPDMP作为哒嗪酮类化合物,是匹莫苯丹合成工艺中的关键中间体,其含量对于制备匹莫苯丹的工艺而言,是十分重要的质量研究内容。本试验根据高效液相色谱法测得的相关数据,建立了一套 DPDMP的高效液相色谱检测方法,用于控制关键中间体的质量,即采用C18柱,以20 mmol/L醋酸铵缓冲液(醋酸调至pH5.5)-甲醇(75∶25,V/V)为流动相;流速为1.0 mL/min;进样量为10 μL;检测波长为254 nm;柱温为25 ℃。经过试验证明该方法可以直接用于检测DPDMP含量。本试验开发的方法通过系统适应性试验和方法学考察,表明该方法具有分析时间短、方法稳定准确、专属性、重复性良好等优点,可用于DPDMP的质量研究。
目前针对DPDMP多为合成工艺的研究,而本试验仅完成了含量测定方法的确定。下一步需要对DPDMP进行更多的质量研究,如性状、鉴别(色谱法和光谱法)、有关物质及稳定性研究等,为匹莫苯丹及其制剂的质量控制提供更多参考依据。

