基底节区高血压性脑出血CT特征与预后的关系
逯慧珍,牛玉军
(锦州医科大学附属第一医院放射科,辽宁 锦州 121000)
脑血管疾病现居我国患病率、死亡率首位,而脑出血高达24%,发病率显著高于发达国家[1],高血压作为其主要危险因素,高血压性脑出血(hypertension cerebral hemorrhage,HICH)发病率也居高不下,且HICH起病急骤、情况凶险,具有高发病率、死亡率、致残率等全球面临的公共卫生问题。CT作为急性脑出血患者的首选检查,能够早期通过客观特征为临床选择治疗方案提供依据,使患者有效接受干预及治疗,改善预后,提高生命质量,对于HICH患者有重要意义。目前,通过CT特征的出血量、中线移位等临床预测的研究较多,但对出血量及中线移位的预测范围值尚无确切定论,同时,通过血肿扩大判断预后的研究较少。
1 资料与方法
1.1 一般资料
收集2018年6月至2019年12月本院非手术治疗的基底节区HICH患者200例,男性113例,女性87例,年龄30~80岁,平均(56.17±11.73)岁;所有患者均符合2019 版《中国脑出血诊治指南》[2]标准,首次发病6 h内行头颅CT检查,24 h内复查。本研究告知患者及家属同意并经本院医学伦理委员会批准。
1.2 方法
应用德国西门子公司128层螺旋CT扫描机,扫描参数:电压120 kV,电流300 mA,层厚3 mm。听眦线为扫描基线,从颅底向颅顶连续扫描,在影像归档和通信系统(picture archiving and communication system,PACS)进行三维重建,再评估出血量、中线移位、破入脑室及复查血肿扩大等情况。由2名放射科高年资医师观测并记录数据,当结果判断不一致时,由第3名医师协助。中线移位测量:以大脑中线为标志,基线为颅脑前额至后枕的连线;出血量测量:用PACS三维重建的横断面、冠状面及矢状面测量出血的最大和最小CT值,选定所要测量血肿范围,自动计算出血量。使用《中国脑血管病影像应用指南2019》[3]定义,血肿扩大:相比首次CT,24 h内复查血肿体积增加33%或血肿容量≥12.5 mL。预后判断:对所有患者进行门诊或电话随访,根据改良Rankin量表(modified rankin scale,mRS)评分对患者发病3个月后的生存质量进行评估,0~2分为预后良好组,3~6分为预后不良组。
1.3 统计学方法
2 结 果
200例患者中,预后良好组85例,预后不良组115例;所有患者出血量≤60 mL,平均(34.35±15.90)mL;中线移位(midline shift,MLS)≤10 mm,平均(4.02±1.12)mm;破入脑室66例;血肿扩大80例。
2.1 基底节区HICH患者预后不良危险因素
预后良好组与预后不良组性别比较,无统计学差异(P>0.05);两组年龄、出血破入脑室、血肿扩大、出血量、中线移位比较,有统计学差异(P<0.05);出血破入脑室、复查血肿扩大者预后较差;出血量≥27.85 mL较<27.85 mL预后较差;中线移位≥3.955 mm预后较差,见表1。
2.2 基底节区HICH患者预后多因素分析
年龄、破入脑室、血肿扩大、出血量和中线移位进入模型,且均为危险因素,见表2。
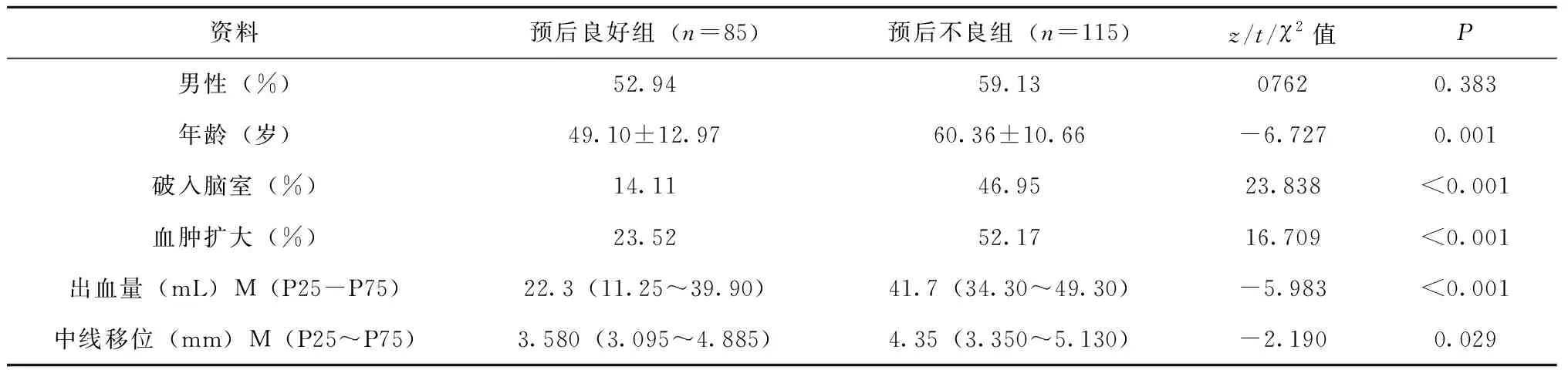
表1 基底节区HICH 3个月预后影响因素单因素分析
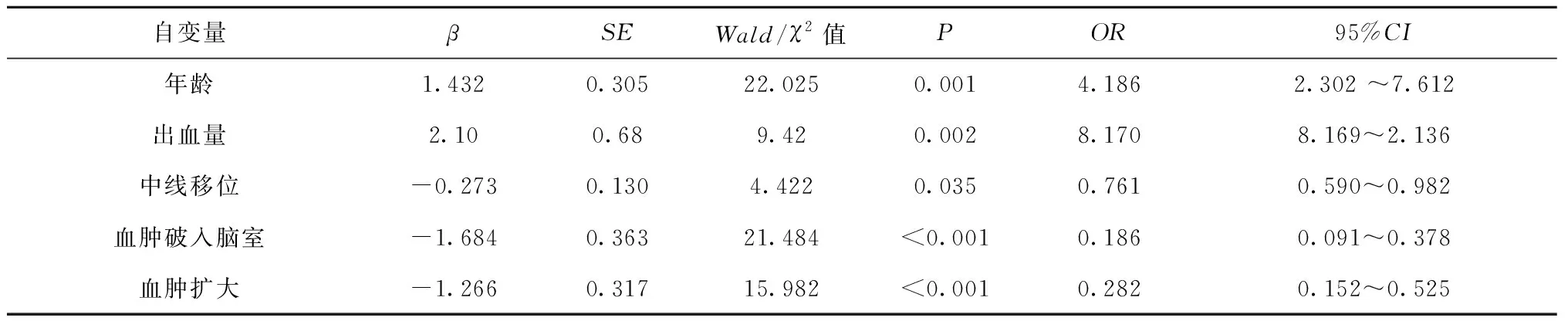
表2 基底节区HICH预后多因素Logistic回归分析
2.3 基底节区HICH患者ROC曲线分析结果
患者出血量曲线下面积为0.748(P<0.05;95%CI:0.673~0.822),预测的最佳分界点为27.85 mL,敏感性为0.887,特异性为0.635;患者中线移位曲线下面积为0.591(P<0.05;95%CI:0.510~0.672),预测的最佳分界点为3.955 mm,敏感性为0.626,特异性为0.647,见图1、图2。

1-特异性 1-特异性
3 讨 论
高血压性脑出血是急性脑血管病中预后最差的一类,全世界30 d内的死亡率达到40%[4]。长期高血压下,脑动脉发生玻璃样变性或纤维素样坏死,同时基底节区的供血小动脉解剖位置特殊,在血压骤升时易破裂出血,因此基底节区是HICH最常见的出血部位。基底节区靠近脑室,出血时易破入脑室,出血量较大的幕上HICH中,优先考虑的治疗方式为外科干预,但基底节区出血选择哪种治疗方式目前没有明确的指导意见[5],因此本组研究选择基底节区HICH为研究目标,此外,基底节区HICH有很多危险因素。
3.1 基底节区HICH与性别的关系
本组研究中,性别与基底节区HICH预后没有统计学差异,与许多学者目前研究结果一致。以往认为男性患者预后比女性差,死亡率比女性高,与男性吸烟、喝酒等行为造成血管硬化和易破裂出血有关,甚至男性患者脑出血后易并发肺部感染、败血症等并发症,而并发症加重了出血后的结果[6],女性患者激素水平、载脂蛋白E可改善神经功能结局[7],女性患者预后较好。随着生活方式改变,女性在生活、工作中占据越来越重要地位,压力越来越大,出血后的预后不良情况也随之增多。因此性别与HICH预后的关系,仍需扩大样本量进一步研究。
3.2 基底节区HICH与年龄的关系
本组研究中,年龄与基底节区HICH预后存在显著性差异,>55岁患者比≤55岁患者预后明显差,因为随着年龄增大,尤其老年人,血管弹性减弱,脆性增加,在情绪激动或紧张时,更易诱发血管破裂而出血,同时老年患者应激能力下降、预防能力减退,其他脏器存在隐匿性疾病,一旦出血并发症较多,导致预后不良。但近期研究表明年龄与预后之间没有相关性,所以目前在各个研究模型中,年龄仍然是HICH预后不良的不确定因素。
3.3 基底节区HICH与血肿破入脑室的关系
本组研究中,血肿破入脑室66例,其中54例预后不良,是预后不良的独立危险因素,可能与血肿破入脑室后引起脑脊液循环不畅,颅内压增高,进一步加重脑组织及神经功能损伤有关。也有文献报道血液进入脑室系统后,会刺激脑室系统的某些细胞(尤其是上皮细胞),产生一定的炎症反应[8],从而造成患者预后不良。但有学者[9]提出血肿破入脑室后,使血肿体积比实际的体积减小,减轻了对脑实质的压迫,从而降低颅内压而改善病情,这与本研究结果并不一致,文献报道也较少。
3.4 基底节区HICH与血肿扩大的关系
30% HICH患者在发病后会出现血肿扩大,一般发生在发病24 h内,尤其在6 h内血肿不稳定时更易发生[10]。本组研究中,无论是单因素还是多因素分析,血肿扩大与预后之间均存在显著差异,血肿扩大是基底节区HICH患者预后不良的独立危险因素,可能因为血肿周围多根血管破裂出血,存在多个出血点,易发生再次出血而造成预后不良。近年有研究[11]发现血肿扩大是目前HICH患者发病后能够进行干预和处理的唯一因素,因此通过早期观察是否有血肿扩大,对于提高HCH患者的生存率有着重要意义。
3.5 基底节区HICH与出血量的关系
出血量>60 mL的死亡率是出血量<30 mL的316倍[12],出血量超过60 mL的患者基本采取外科治疗,预后情况很差,而对于HICH患者来说,提高生存率和生存质量是关键,所以本组只选择出血量≤60 mL进行研究。研究表明脑出血量与预后之间存在显著差异性,出血量越大,预后越差,同时预测了出血量≤60 mL时不良预后的最佳分界值为27.85 mL,该预测值敏感性88.7%,特异性63.5%,具有较高的敏感性,提示基底节区出血量超过27.85 mL时,要早期采取临床干预。出血量的多少直接影响患者生存率和生活质量,是临床选择治疗方式的一个重要指标,因此,准确测量血肿体积对临床至关重要,以往多采取多田氏公式计算,将血肿近似看作椭球体,但在计算血肿量上是存在误差的[13],实际血肿形态多样,且大部分是不规则的,采用PACS系统半自动计算方式计算出血量,人为误差较小,结果更准确,见图4。
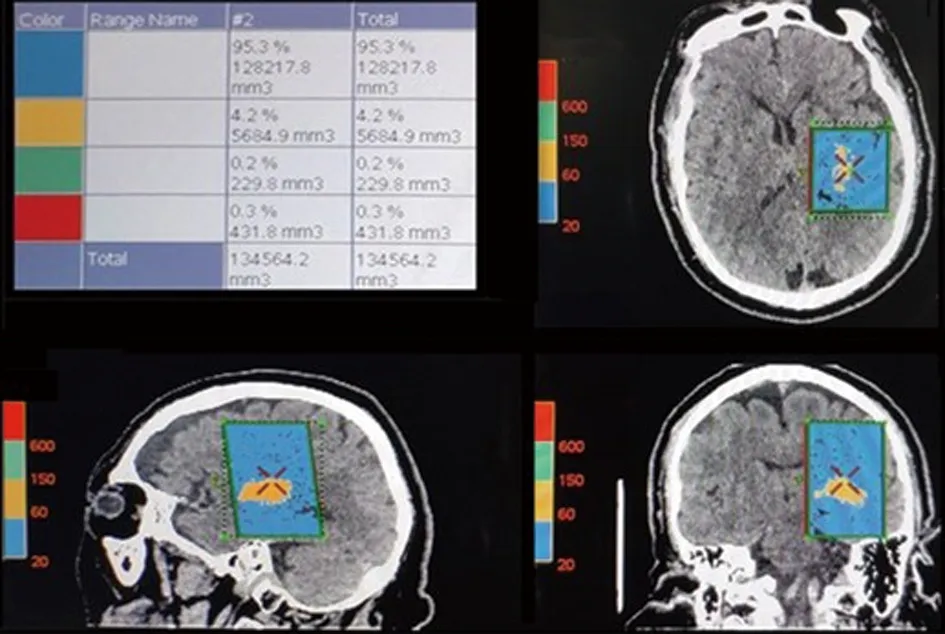
图3 PACS三维方法所测出血量
3.6 基底节区与中线移位的关系
本组研究发现中线移位是基底节区HICH预后不良的独立危险因素,这可能与患者血肿周围水肿造成中线移位有关,而周围水肿体积进一步压迫周围脑组织造成损害;同时中线移位严重的患者发生脑疝的可能性较大,因此中线移位成为预后不良的独立危险因素。本研究发现MLS≥3.955 mm时预测不良预后的敏感度62.6%,特异性64.7%,而徐建星[14]等人发现MLS>3.65 mm时,预测不良预后的价值较高,且敏感度和特异性都较本组研究高,可能与选择出血部位不同有关,本研究均为基底节区出血患者,而后者是选择脑实质内任意部位的出血,因此相比大多数研究[14-15]138-140,本研究对于基底节区的预测价值更高。提示当中线移位超过3.955 mm时,要密切观察患者情况,及时给予治疗,防止病情进一步恶化。但不足之处在于对MLS的测量标准不同,因此对提示预后不良的最佳MLS定量阈值没有取得统一的结果,还需进一步研究探索。
本组研究选取基底节区HICH患者,消除了其它部位与预后之间的相互影响,使其与预后因素之间具有更高的预测价值,同时取得了预测不良预后的最佳出血量和中线移位值;研究采用PACS系统半自动方法计算出血量,比以往误差小。综上所述,对于急性基底节区HICH患者,通过分析患者出血量、中线移位、出血是否破入脑室、血肿是否扩大等CT特征,可以对患者的预后做出较好的判断,对指导临床迅速、准确的选择治疗方式具有重要意义。
——书写要点(三)

