间变性少突胶质细胞瘤术后复发转变为胶质母细胞瘤1例并文献复习
周秋妹,隋爱霞,杨柳艺,马晓丽,雷玉莹,梁岩松
1河北省人民医院肿瘤一科,3病理科,石家庄 050000 2华北理工大学研究生学院,河北 唐山 063210
胶质瘤是中枢神经系统最常见的原发恶性肿瘤。尽管接受了手术、放疗、化疗和靶向治疗等各种治疗,其复发率仍极高。关于低级别胶质瘤复发进展转变为高级别胶质瘤可见相关报道,然而间变性少突胶质细胞瘤复发转变为胶质母细胞瘤的案例较为少见,现报道如下。
1 病历资料
患者女,37岁,2017年4月主因情绪低落、睡眠差2年,加重半年入院。头颅MRI提示:左侧海马区及内侧颞叶异常信号影,大小约41.59 mm×18.71 mm(图1A)。2017年4月19日于全麻下行占位性病变切除术。病理组织学可见细胞呈圆形,核深染,核周有空晕,有明显的细胞异型性和核分裂象增多,可见微血管增生和假栅栏状坏死(图1B)。免疫组化结果:p53(少量细胞弱+)(图1C),少突胶质细胞系转录因子2(oligodendrocyte lineage transcription factor 2,Olig2)(+)(图1D),髓鞘碱性蛋白(myelin basie protein,MBP)(+)(图1E),异柠檬酸脱氢酶1(isocitrate dehydrogenase 1,IDH1)(-)(图 1F),胶质纤维酸性蛋白(glial fibrillary acidic protein,GFAP)(+),CD34(血管+),巢蛋白(Nestin)(+),神经元特异性核蛋白(neuronal nuclei antigen,NeuN)(-),波形蛋白(Vimentin)(-),O6-甲基鸟嘌呤-DNA甲基转移酶(O6-methylguanine-DNA methyltransferase,MGMT)(-),Ki-67 阳性率活跃区约20%。病理学诊断:间变性少突胶质细胞瘤[世界卫生组织(WHO)分级为Ⅲ级]。建议患者行术后辅助治疗,患者及家属未采纳。
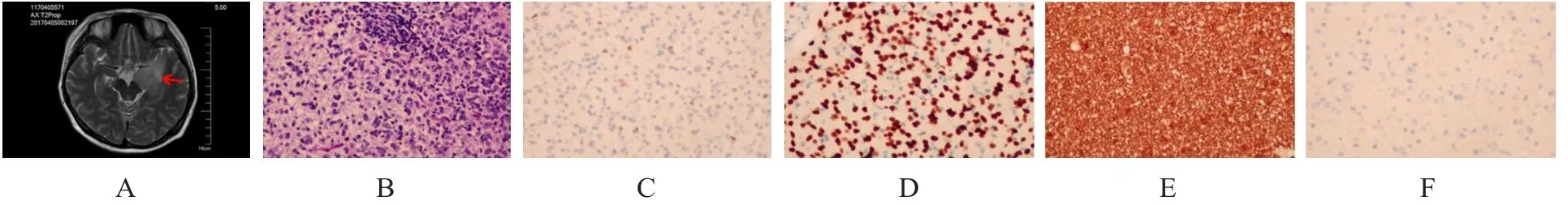
图1 第一次手术术前影像及术后病理图
2017年8月患者复查头颅MRI提示左侧颞叶及海马软化灶伴周围胶质增生。2017年10月复查头颅MRI提示左侧基底节区、海马、颞叶异常强化影。患者无不适症状,未住院治疗。2017年12月患者因突发双眼视物不清伴视野缺损再次就诊。查体:意识清楚,言语不利,左侧颞部可见长约7 cm弧形手术瘢痕,双眼视力减退,视野缺损,右侧较重。头颅MRI提示左侧颞叶、海马、基底节区及丘脑占位,大小约69.15 mm×50.93 mm(图2A),伴出血及周围水肿,考虑为胶质瘤复发。2017年12月8日于全麻下行病灶切除术。病理组织学特点为肿瘤组织内可见明显坏死灶,周围肿瘤细胞呈栅栏状排列,间质内小血管明显增生,肿瘤细胞呈多形性,可见大量异形多核巨细胞(图2B)。免疫组化染色结果:p53(+)(图 2C),Olig2(+)(图 2D),MBP(局灶+)(图 2E),IDH1(-)(图 2F),GFAP(+),Nestin(+),Vimentin(+),CD34(血管+),突触素(Synaptophysin,Syn)(+),NeuN(-),MGMT(-),表皮生长因子受体(epidermal growth factor receptor,EFGR)(-),Ki-67阳性率活跃区约50%。病理学诊断:具有少突胶质细胞瘤成分的胶质母细胞瘤(WHO分级为Ⅳ级)。2017年12月18日患者突发抽搐后呈昏迷状态,双瞳孔散大固定,光反射消失,头颅CT提示左侧大脑半球肿胀明显。当月患者死亡,总生存期8月余。
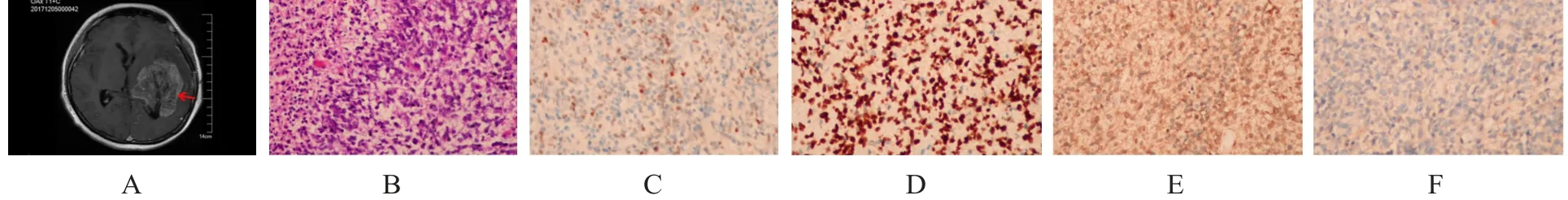
图2 第二次手术术前影像及术后病理图
2 讨论
间变性胶质瘤占恶性胶质瘤的15%~20%,好发年龄为55~64岁,有研究显示中位总生存期为56个月。高级别胶质瘤位于脑实质内,多呈弥漫浸润性生长,很难实现生物学意义上的完全切除,术后复发现象较为多见,但复发后肿瘤类型发生转变的现象较为少见。本文中主要依据苏木精和伊红染色切片的光镜特征、谱系相关蛋白的免疫组化表达和超微结构特征对该患者两次手术病灶做出病理诊断。张俊鹏行相关研究得出高级别胶质瘤复发后病理级别往往高于最初诊断时的病理级别,与本文结果一致。
胶质瘤术后复发恶变的机制较为复杂,可能机制如下:①该患者经过手术等刺激可能发生了肿瘤基因“再突变”,再发了第二肿瘤即胶质母细胞瘤。有报道称分子生物学中IDH
野生型、广泛CD34表达和端粒酶逆转录酶(telomerase reverse transcriptase,TERT)启动子突变等是肿瘤进展迅速的危险因素。本例患者为IDH
野生型、广泛CD34表达,不除外再发恶性肿瘤可能。②参考分析既往文献,继发性胶质母细胞瘤往往由低级别星形细胞瘤或间变性星形细胞瘤发展而来,结合该患者免疫组化结果,患者第一次病理p53少量细胞呈阳性,初发肿瘤内可能局部含有极少量星形细胞成分,手术最大范围地安全切除肿瘤后,残留的极少量星形细胞与免疫微环境相互作用等,增殖恶变转化成胶质母细胞瘤,第二次术后病理p53呈阳性,IDH1呈阴性。目前WHO对Ⅲ级胶质瘤治疗的建议是手术联合放疗,有研究推荐丙卡巴嗪、洛莫司汀和长春新碱(PCV方案)或替莫唑胺辅助化疗,可有效延长间变性少突胶质细胞瘤患者的生存期。患者术后快速复发考虑与拒绝术后辅助治疗有关,这对于高级别胶质瘤患者来说十分必要。此外,肿瘤复发时还应考虑到病理成分或病理类型发生改变的可能性,治疗策略也应随之做出更改。除利用先进的影像学技术,有学者认为可采用立体定向活检技术进行组织诊断,能最大程度地避免功能缺失。还有学者认为应进行开放手术,能最大范围地安全切除肿瘤,并明确病理。
综上所述,对于高级别胶质瘤,在治疗及随访过程中,应考虑到肿瘤病理类型发生改变的可能性。结合影像学表现,通过活检或开放手术获取标本,进行组织和分子病理学检查,对于准确诊断疾病以及制订后续治疗方案尤为重要。

