甲磺酸奥希替尼治疗EGFR基因突变型非小细胞肺癌脑转移的疗效评价
张碧营,何泽来,吴 双,周育夫
根据世界卫生组织2018年的报告,全世界每年大约有1 810万例新的肺癌病例登记,死亡人数甚至高达960万例。2018年中国癌症数据显示,男性中发病率最高的癌症主要是肺癌(占总病例的21.9%),女性中肺癌位列第2(占病例总数的13.3%)。其中非小细胞肺癌(non-smallcell lung cancer,NSCLC)是最常见的肺癌组织类型。相关文献资料报道,新诊断的非小细胞肺癌患者中有16.3%~19.0%发生脑转移,另有30%~50%是在诊治过程中发现。脑转移的出现无疑将在肺癌的治疗中带来更严峻的问题[1]。一方面,是怎么打破血脑屏障-中枢神经系统的天然屏障,其在保护大脑免受有毒物质的侵害,同时限制了药物的可获得性;另一方面,不同的脑转移部位(脑实质转移和脑膜转移)其诊断率、治疗方案选择及预后也不尽相同,治疗过程更加艰难[2-3]。在过去,由于治疗方法局限,以及脑转移的机制和生物学特征尚不清楚,转移性肺癌患者的中位生存时间仅为1~2个月[4]。随着肿瘤治疗水平的提高,目前脑转移的治疗方法主要分为局部和全身治疗2种方向。局部治疗包括手术治疗、全脑放疗和立体定向放疗等;全身治疗包括靶向治疗、全身化疗、免疫治疗和抗血管生成治疗等,越来越多的治疗选择延长了肺癌脑转移患者的生存期。然而,每个治疗手段都存在利弊,如何合理选择最佳治疗方案,仍需更多研究予以指导。如放射治疗在肺癌的治疗中占据非常重要的位置,但随着肺癌脑转移患者的生存时间逐渐延长,也要求更加关注颅脑放疗引起的副作用-神经认知功能损伤。另外神经外科手术治疗容易复发成为攻克的难关[5]。近年来发展最快的莫过于靶向治疗,随着表皮生长因子受体(epidermal growth factor receptor,EGFR)基因的发现,大量研究表明,EGFR基因突变阳性患者的风险高于EGFR基因野生型脑转移患者[6],而EGFR基因突变在亚洲患者中所占的比例远高于欧美患者,因此针对EGFR基因突变的靶向药物在亚洲患者疗效突出。另外大量随机试验和荟萃分析发现,靶向药的治疗优于化疗以及其他细胞毒性药物[7]。2019年一项针对甲磺酸奥希替尼的Ⅲ期临床试验(FLAURA)结果显示,全球29个国家556例EGFR基因突变晚期NSCLC患者一线使用三代EGFR靶向药奥希替尼后,无进展生存期(progression-free survival,PFS)长达18.9个月,总生存期(overall survival,OS)长达38.6个月,成为史上最长PFS与OS;同时在该研究中甲磺酸奥希替尼展现了其强大的入脑能力,进一步改善了颅内病灶的控制[8]。甲磺酸奥希替尼更是荣获全球四大指南均推荐其作为EGFR基因突变阳性NSCLC患者一线用药的殊荣。目前此类研究中,对象大多是国外的患者,单纯国内还是缺乏相关研究数据。另外如何做到精准治疗,制定个性化治疗,使患者从中获得更好效益,需要大量的临床试验来提供依据。为了使NSCLC脑转移患者更好地从靶向治疗中获益,本研究中共收集了60例本院应用甲磺酸奥希替尼治疗后NSCLC脑转移患者的病理资料,回顾性分析了此类患者生存预后,以期为NSCLC脑转移患者进一步更为精准的治疗提供参考依据。
1 资料与方法
1.1 一般资料
收集2017年5月—2019年12月由蚌埠医学院第一附属医院肿瘤放疗科收治的,60例确诊发生脑转移,并接受甲磺酸奥希替尼一线治疗肺腺癌患者的临床资料。其中男性患者31例(51.7%),女性患者29例(48.3%),中位年龄53岁(范围:28~75岁)。脑转移经CT或MRI检查证实,所有患者均经分子病理学检测确定有EGFR基因突变。所用肺癌患者参照TNM分期标准进行临床分期均为Ⅳ期。
1.2 纳入和排除标准
纳入标准:(1)Karnofsky体能状况(karnofsky performance status,KPS)评 分≥45分者;(2)患者年龄≥18岁,且≤80岁;(3)经病理学确诊为肺腺癌;(4)脑转移病灶经脑CT和MRI确诊;(5)应用“下一代”测序(“next-generation”sequencing,NGS)技术分析肺腺癌驱动基因的突变位点,包括EGFR基因常见突变(T790M、19del和L858R)和EGFR基因罕见突变(L861Q、S768I、20-ins和G719X等);(6)均将甲磺酸奥希替尼作为一线靶向治疗的肺腺癌脑转移患者。
排除标准:(1)患者年龄<18岁或>80岁;(2)KPS评分<45分者;(3)患有严重肺纤维化的病例,合并其他系统的恶性肿瘤,多原发癌,活动性感染病者;(4)患有严重不能控制的系统疾病者;(5)脑转移发生前使用甲磺酸奥希替尼的患者。
该研究试验方案经蚌埠医学院第一附属医院医学伦理委员会批准,患者均对该试验知情同意并签署知情同意书。
1.3 治疗方法
60例患者接受甲磺酸奥希替尼治疗(甲磺酸奥希替尼80 mg/d,口服),至肿瘤进展或出现患者不能耐受的不良反应时停药。3个月后评价2组患者的近期疗效,并观察颅内无进展生存期(intracranial progression-free survival,IPFS)和OS。IPFS定义为患者开始治疗至出现颅内疾病进展或末次随访时间。全部患者开始治疗后14~20 d复查脑MRI,随访期间每3个月定期复查。
1.4 疗效及不良反应评价
按照实体肿瘤疗效评价标准(response evaluation criteria in solid tumors,RECIST)1.1版进行评价:完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD),CR+PR计算客观反应率(objective response rate,ORR)。ORR(%)=(CR+PR)/总例数×100%。应用IPFS和OS评价远期疗效。
不良事件根据美国国立癌症研究院通用毒性标准(national cancer institute common terminology criteria for adverse events,NCICTCAE)4.03版进行判定,分为Ⅰ~Ⅴ级。该研究中将Ⅲ~Ⅳ级定义为中重度不良反应,Ⅴ级为死亡。
1.5 随访
所有患者均以电话或面访形式进行随访,随访截止时间为2020年5月,随访率达100%,随访资料完整。本组中位IPFS期为11.0个月,中位OS期为17.0个月。
1.6 统计学方法
应用SPSS 25.0统计学软件对获得的研究数据进行统计学分析;采用Kaplan-Meier法绘制生存曲线并计算生存率,进一步采用logrank检验进行单因素分析;采用COX比例风险模型进行多因素生存分析。该研究所用统计推断均为双侧检验,P<0.05为差异有统计学意义。
2 结果
2.1 临床病理特征
本研究中共纳入的肺腺癌患者60例,初诊断时有36例患者已发生脑转移,在纳入研究时所有患者均已发生脑转移,且均已进展到Ⅳ期。大多数患者的突变位点为EGFR基因常见突变(T790M、19del和L858R),仅有少数患者为EGFR基因罕见突变(L861Q、S768I、20-ins和G719X等),见表1。
2.2 疗效
随访截止时,60例肺腺癌脑转移患者中38例死亡,中位OS期为17.0个月[95%可信区间(confidence interval,CI):13.704~20.296](图1A),中 位IPFS为11.0个 月(95%CI:8.570~13.430)(图1B)。60例入选患者均有可评估疗效,CR者0例(0.0%),PR者26例(43.3%),SD者21例(35.0%),PD者13例(21.7%),ORR为43.3%。
2.3 IPFS和OS影响因素分析结果
Log-rank法进行单因素生存分析结果(表2和图2)显示,KPS评分、脑部有无症状、脑转移病灶数和肝转移是患者接受甲磺酸奥希替尼治疗后的IPFS和OS的影响因素,而年龄、性别、吸烟史、分化程度和脑转移部位等均不是患者接受甲磺酸奥希替尼治疗后OS的影响因素。
2.4 多因素分析结果
将上述相关因素纳入多因素回归模型分析,COX多因素生存分析结果(表3)显示,KPS评分和肝转移是患者接受甲磺酸奥希替尼后IPFS和OS的独立预后因素(P值均<0.001)。另外脑部有无症状也是影响IPFS独立的因素。
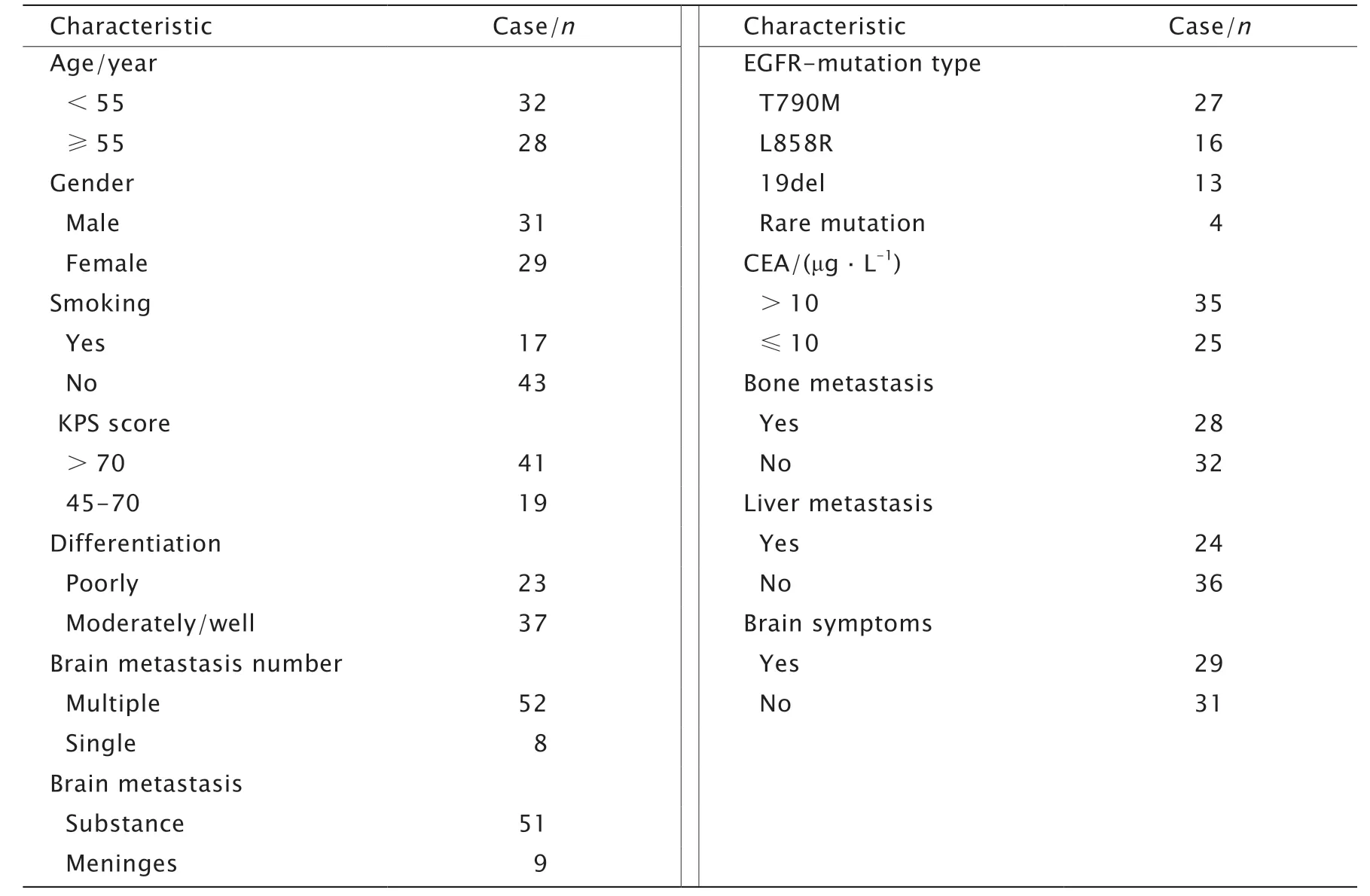
表1 60例接收甲磺酸奥希替尼治疗的EGFR基因突变型晚期NSCLC患者临床病理特征Table 1 Clinicopathologic characteristics of 60 patients with advanced non-small-cell lung cancer(NSCLC) with epidermal growth factor receptor (EGFR)-mutation treated with osimertinib(N=60,n)
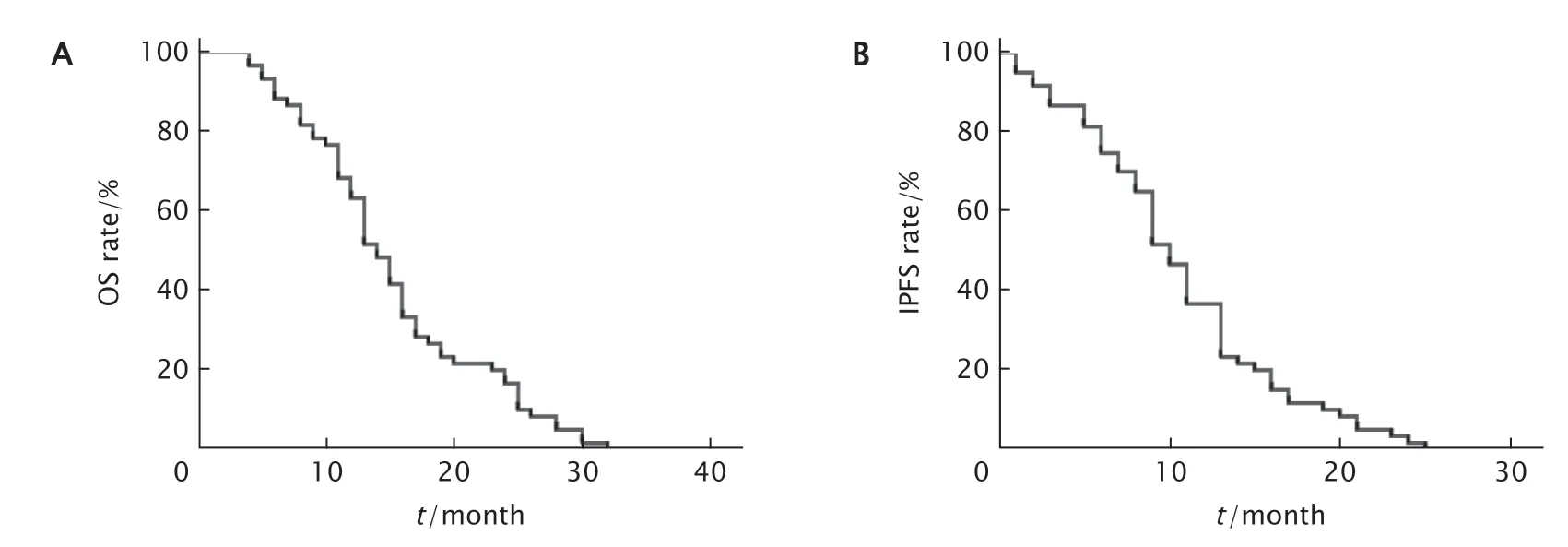
Fig.1 The overall survival (OS) rate (A) and median intracranial progression-free survival (IPFS) rate (B)in 60 patients with advanced non-small-cell lung cancer (NSCLC) with epidermal growth factor receptor(EGFR)-mutation treated with osimertinib were analyzed by Kaplan-Meier method.图1 Kaplan-Meier法份分析60例接收甲磺酸奥希替尼治疗的EGFR基因突变型晚期NSCLC患者的OS率(A)和中位IPFS率(B)
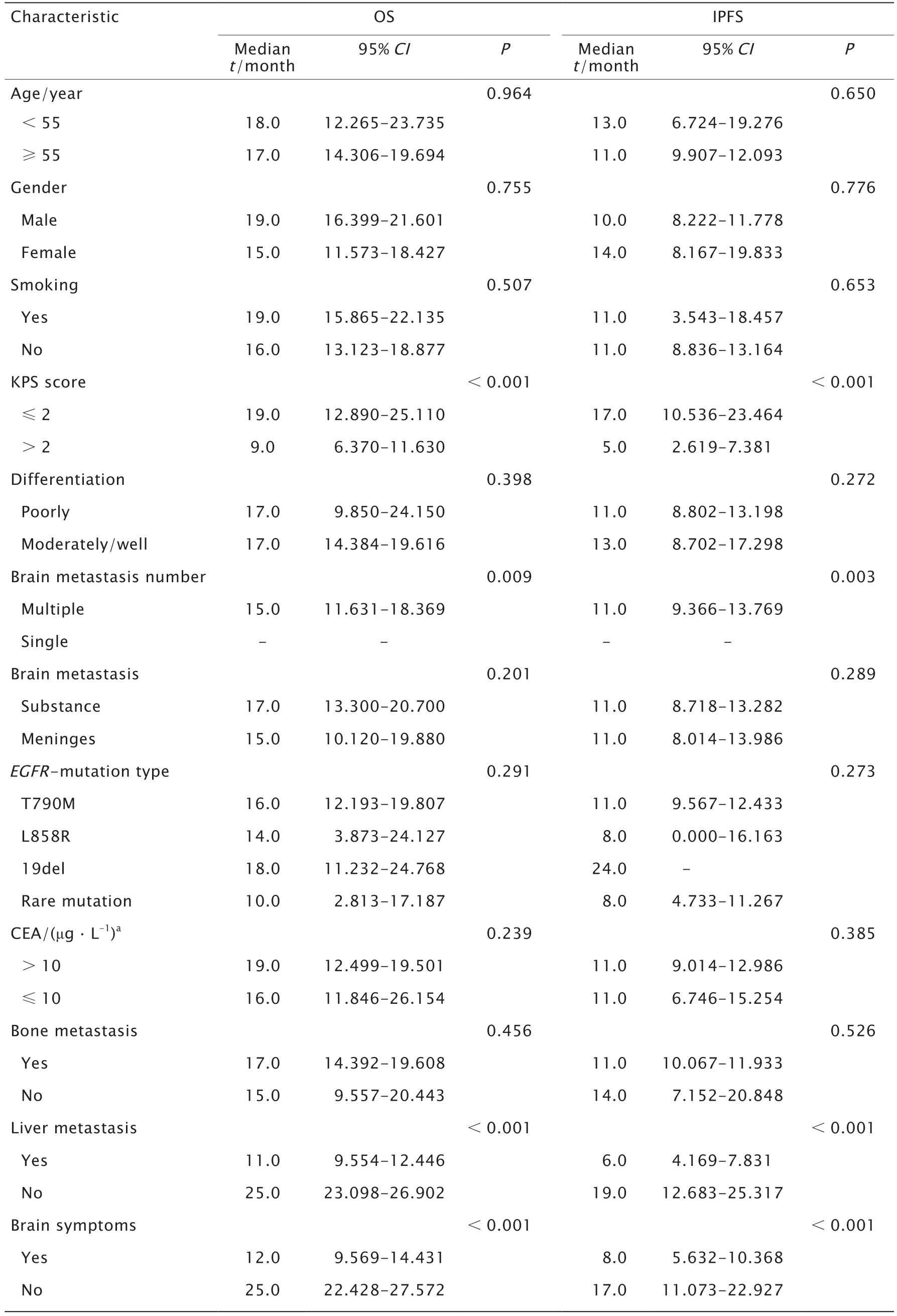
表2 单因素分析NSCLC脑转移患者接受甲磺酸奥希替尼治疗的疗效预后因素Table 2 Univariable survival analysis of prognostic factors in patients with advanced non-small-cell lung cancer (NSCLC) with epidermal growth factor receptor (EGFR)-mutation treated with osimertinib
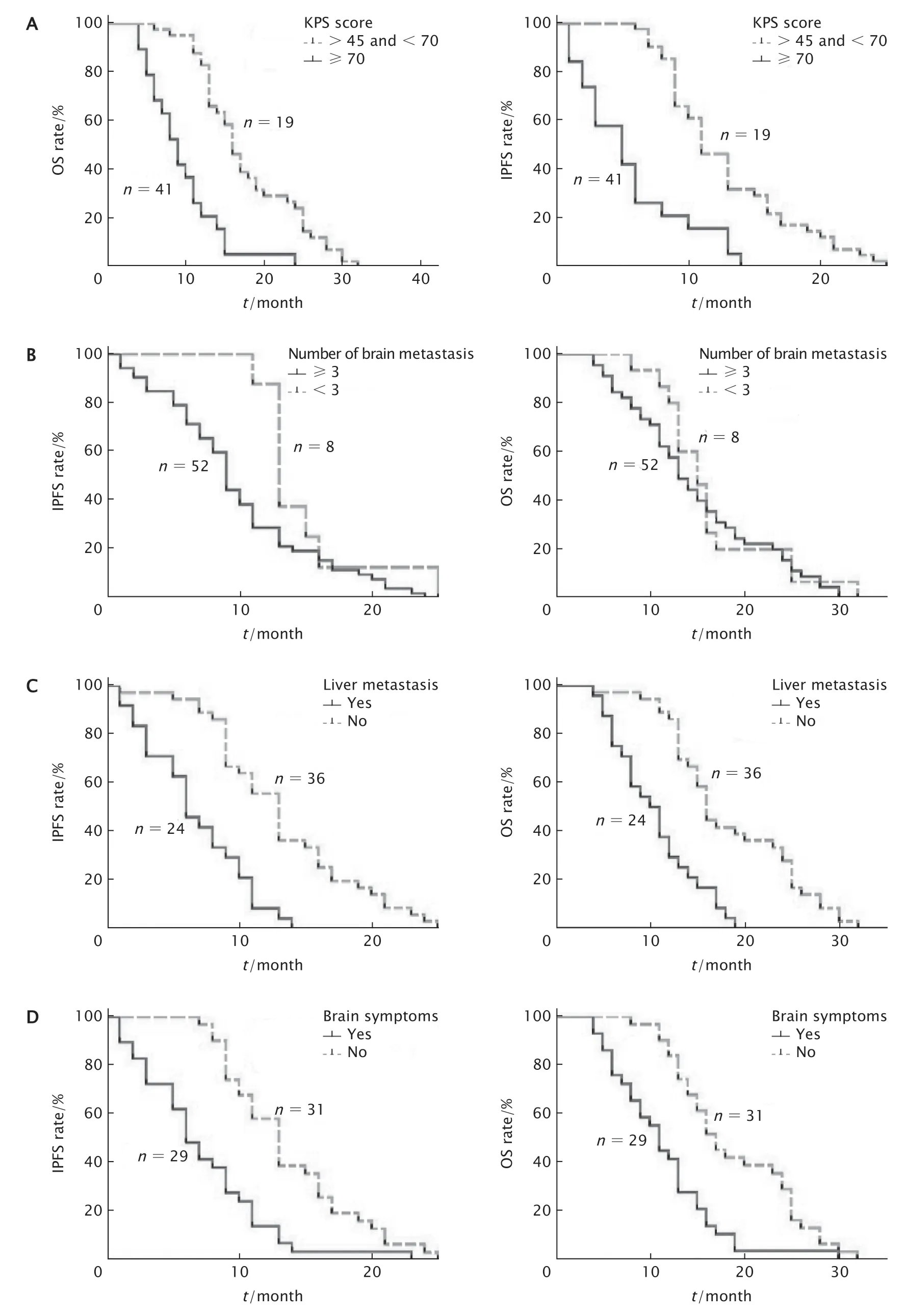
Fig.2 The influence of different karnofsky performance status (KPS) scores (A),number of brain metastases(B),liver metastasis (C),and brain symptoms (D) on the median intracranial progression-free survival (IPFS)and overall survival (OS) of 60 patients with advanced non-small-cell lung cancer (NSCLC) with epidermal growth factor receptor (EGFR)-mutation treated with osimertinib were analyzed by Kaplan-Meier method.图2 Kaplan-Meier法分析不同KPS评分(A)、不同脑转移数目(B)、有无肝转移(C)和有无脑部症状(D)对60例接收甲磺酸奥希替尼治疗的EGFR基因突变型晚期NSCLC患者IPFS和OS率的影响
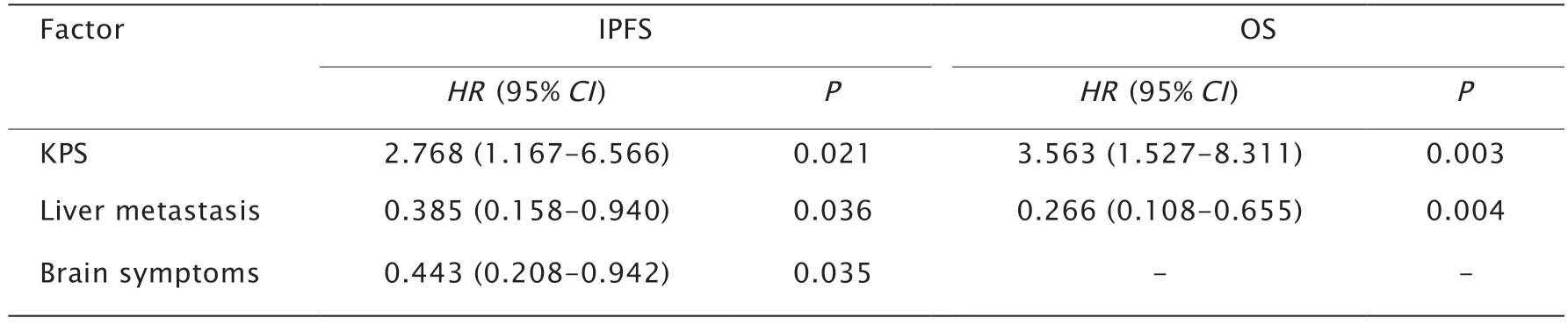
表3 多因素分析接收甲磺酸奥希替尼治疗的EGFR基因突变型晚期NSCLC患者预后的影响因素Table 3 Multivariable survival analysis of prognostic factors in patients with advanced non-small-cell lung cancer (NSCLC) with epidermal growth factor receptor (EGFR)-mutation treated with osimertinib
2.5 不良反应
60例患者均有可评价不良反应,常见不良反应为皮疹14例(23.3%)、皮肤干燥9例(15%)、腹泻5例(8.3%)和指(趾)甲毒性5例(8.3%),其余少见的不良反应为头痛、肺炎以及中性粒细胞减少,各1例(1.7%),这些不良反应均为Ⅰ~Ⅱ级,经对症治疗后均可好转;无1例发生Ⅲ级以上不良反应,总体不良反应可耐受。
3 讨论
目前有多项研究认为,EGFR基因突变是肺癌患者发生脑转移的危险因素,有更高的脑转移发生率[9-11]。为了进一步了解对于这类患者疗效如何,本研究收集并分析60例NSCLC脑转移瘤患者临床资料,发现KPS评分、脑部有无症状和肝转移是对患者生存期有显著影响;而Log-rank法单因素分析结果显示,患者的年龄、性别、吸烟史、分化程度、脑转移部位、EGFR基因状态、初诊癌胚抗原(carcinoma-embryonic antigen,CEA)值以及有无骨转移对于NSCLC脑转移瘤患者OS或IPFS均未见明显差异(P=0.964和P=0.650,P=0.755和P=0.776,P=0.507和P=0.653,P=0.398和P=0.272,P=0.239和P=0.289,P=0.201和P=0.273,P=0.291和P=0.385,P=0.456和P=0.526)。一些研究[12-13]认为,年龄<60岁更容易发生脑转移,本研究中却未得到验证,其原因有待进一步予以探讨。
多因素分析结果显示,KPS评分、脑部有无症状、肝转移和治疗方案是影响NSCLC脑转移瘤患者生存期的独立因素。分析原因可能有以下几点:(1)KPS评分较低的患者体质和机体免疫明显降低,从而影响预后状况;另外,高KPS评分患者身体和心理状态均优于低KPS评分患者,患者能以积极态度配合治疗,为取得良好治疗效果奠定基础;从而利于疾病的恢复[14]。(2)脑部有无症状可能与肿瘤细胞突破血脑屏障侵犯位置和范围有关。虽然甲磺酸奥希替尼能通过血脑屏障,但对于有症状患者可能需要联合放疗来更好地控制病情发展,同时甲磺酸奥希替尼也可提高放疗敏感度[15-16]。另外在使用EGFR-酪氨酸激酶抑制剂(EGFR-tyrosine kinase inhibitors,EGFR-TKIs)的过程中,进一步放疗能够有效防止复发,控制周围浸润细胞和亚临床病灶生长;放疗进一步打破血脑屏障,其通透性增加,提高脑脊液中化疗药物浓度,为其他治疗奠定基础[17]。(3)关于脑转移瘤数目同预后的关系的研究结果存在差异。脑转移瘤以多发常见,可单发患者预后明显较好,是EGFR基因突变型晚期NSCLC脑转移患者的独立预测因素[19]。但本研究中却未发现脑转移瘤数目与IPFS以及OS的相关性,可能与样本量太少,数据具有偏倚性有关。(4)脑膜转移不如脑实质转移常见,在某些患者中,初诊时会出现脑膜转移,而大多在EGFR-TKIs治疗过程中出现。但预后通常并不理想。可能的原因,一方面此类患者由于颅内压升高而常常具有变化的中枢神经系统症状;另一方面可能为药物渗透性可能不足。因此有研究表明,靶向药物治疗联合放疗疗效更显著[19]。本研究中分析了脑膜转移患者的生存情况,结果并未发现2组之间IPFS和OS差异由统计学意义。笔者认为,这可能与本研究中脑膜转移病例患者较少有关,因此需要进行大样本前瞻性研究以进行进一步分析。(5)肝转移在EGFR基因突变的晚期NSCLC患者中可达到约20%[20]。本研究分析了肝转移与IPFS和OS之间的关系,结果表明其是一项独立的预后因素,对既往的研究结果[21-22]进一步予以了验证。目前其中存在的机制尚不清楚,一些研究认为可能存在以下因素:肿瘤细胞激活了肝细胞生长因子(hepatocyte growth factor,HGF),而HGF是间质-上皮转化因子(mesenchymaltoepithelial transition factor,MET)蛋白的配体,它们可以导致MET的激活,而MET基因扩增是导致对EGFR-TKIs产生抗性的机制之一,从而导致抗性的出现[23-24]。此外遗传异质性可以发生在转移中。(6)罕见的突变的NSCLC患者占有大约10%比例[25]。罕见的EGFR基因突变与常见突变不同,其对EGFR-TKIs的敏感性较差[26]。本研究中未发现罕见突变的差异性,可能与患者数量较少,数据具有偏倚性有关,所以具有罕见EGFR基因突变的NSCLC的脑转移患者中对不同TKIs的有效性需要进一步予以探讨。
从本次研究当中可以看出,对于EGFR基因突变的NSCLC的脑转移患者在应用甲磺酸奥希替尼治疗肺癌脑转移患者后生存期明显的改善,对于KPS评分≤2,无肝转移患者的疗效尤为突出。随着精准治疗时代的到来,更需要根据患者不同情况做出更好的选择。有研究者提出,甲磺酸奥希替尼联合放疗未来可期[27],但是介入的时间段具有争议,仍需要大量的实验研究来提供指导。具有EGFR基因突变的NSCLC的脑转移患者一直以来是热门、争议不断的研究课题,给临床治疗带来困惑。笔者认为,应该采取合理的疾病治疗模式,避免当前学科的局限性,促进疾病的发展,使患者受益。
本研究中,甲磺酸奥希替尼治疗肺癌脑转移患者最常见的不良反应有皮疹、皮肤干燥和腹泻等,多为Ⅰ~Ⅱ级,且患者均可耐受;无1例发生Ⅲ级以上不良反应,说明甲磺酸奥希替尼具有较高的安全性,符合中国抗癌协会肺癌专业委员会的EGFR-TKIs不良反应管理专家共识[28]。该研究的不足之处为回顾性研究,资料的收集存在一定局限性,并且随访期可能不够长,可能对于研究结果存在一定系统偏倚。同时由于检测方法所限,对患者EGFR基因突变亚类未能进一步明确及进行分析,其结果有待于大规模前瞻性研究进一步证实。对于存在上述不良因素的患者在临床用药及随访中需要更加关注。
综上所述,甲磺酸奥希替尼治疗NSCLC脑转移患者疗效显著,安全性高。本有研究数据显示,对于KPS评分≤2,无肝转移患者,可以显著改善颅内IPFS和OS,另外无脑部症状也是一项有益的预后因素,可以延长患者OS,但在颅内病灶控制未体现出优势。

