罗替戈汀合成路线综述*
胡 晨,马少玲,彭 璟
(南京大学金陵学院化学与生命科学学院,江苏 南京 210089)
帕金森病(Parkinson’s disease,PD)又称“震颤麻痹”由詹姆斯·帕金森博士在1817年最早发现并描述,是一种常见的老年中枢神经系统退行性疾病。帕金森病(PD)的主要病因是患者大脑黑质部位的神经通路和多巴胺能神经元发生了退行性病变,导致酪氨酸羟化酶(Tyrosine hydroxylase)活性增强或者含量减少,而酪氨酸羟化酶活性增强或者含量减少,致使多巴胺合成受阻,含量下降。患者大脑中多巴胺含量越低,表明病情恶化的越严重[1]。当前国际上主流的有关治疗帕金森病的方法包括采用传统的药物疗法和外科手术治疗,也有在现代分子医学水平上发展起来的基因疗法(Gene therapy)和细胞移植疗法(Cell transplantation therapy)。其中仍旧以传统的药物疗法为主流治疗方法。
罗替戈汀,化学名为(S)-2-(N-丙基-N-(2-(2-噻吩)乙基)氨基)-5-羟基-1,2,3,4-四氢萘,核心成分结构如图1[2]所示。该化合物的构型为S构型,为白色结晶。
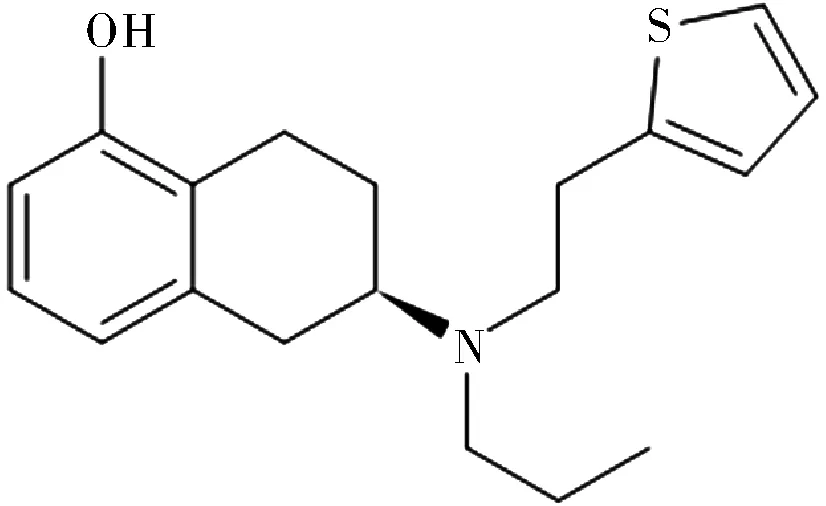
图1 罗替戈汀分子结构Fig.1 Molecular structure of Rotigotine
罗替戈汀(Rotigotine)是非麦角类选择性多巴胺受体激动剂(D1/D2/D3)类药物[3],通过刺激体内的多巴胺受体,模拟多巴胺(神经递质)的功能而起作用,罗替戈汀可激动5-HT1A受体,从而产生抗焦虑作用,通过阻滞肾上腺素α2B受体产生抗运动障碍作用[4]。在早期PD治疗中,罗替戈汀可以用于单药治疗,但随着疾病的发展,通常和左旋多巴联合使用。在这种情况下,罗替戈汀成为左旋多巴的辅助治疗药物,但这也控制了左旋多巴的使用剂量,从而降低了引起的运动并发症的发生率[5]。
由于罗替戈汀口服用药生物利用度差,首过效应极强[6],因此,其经典剂型为透皮贴片,由德国Schwarz公司研制,已在欧洲和美国上市。此外,还有公司将罗替戈汀盐酸盐包埋于生物可降解的乳酸羟基乙酸共聚物制备成缓释微球[7],通过肌内注射给药,使药物在一定周期内持续、稳定释放,形成对多巴胺受体的持续稳定刺激,从而治疗PD。罗替戈汀缓释微球目前正在中国和美国同步开展临床研究,已进入第三期临床研究阶段[8]。
在罗替戈汀的制备过程中,根据引入手性中心的方法不同,其合成路线可分为拆分合成、手性试剂辅助合成和立体选择合成三种。
1 拆分合成
1.1 拆分合成路线1
该方法的合成路线如图2[9]所示。

图2 拆分合成路线1Fig.2 Split synthesis route 1
合成步骤如下:以5-甲氧基-2-四氢萘酮(1)为原料,加入正丙胺和冰醋酸,以氧化铂为催化剂进行加氢还原反应,得到2-(N-正丙基氨基)-5-甲氧基四氢萘(2)。随后以L-二苯甲酞酒石酸为拆分试剂,进行手性拆分得到(S)-2-(N-正丙基氨基)-5-甲氧基四氢萘(3)。(3)与氢溴酸发生去甲基化反应,再溶于氨水和乙醚混合溶液,萃取分离,得到(S)-2-(N-正丙基氨基)-5-羟基四氢萘(4)。(4)与对甲苯磺酸噻吩乙酯和氯化氢进行还原反应,得到罗替戈汀(5)。
此路线生产成本较低,污染较小,但是所用拆分试剂L-二苯甲酞酒石酸不能完全拆分出单一的构型化合物,且(S)-2-(N-正丙基氨基)-5-甲氧基四氢萘(3)的烷基化和去甲基化的反应收率很低,因此合成工艺还需进一步优化。
1.2 拆分合成路线2
合成路线如图3[10]所示。
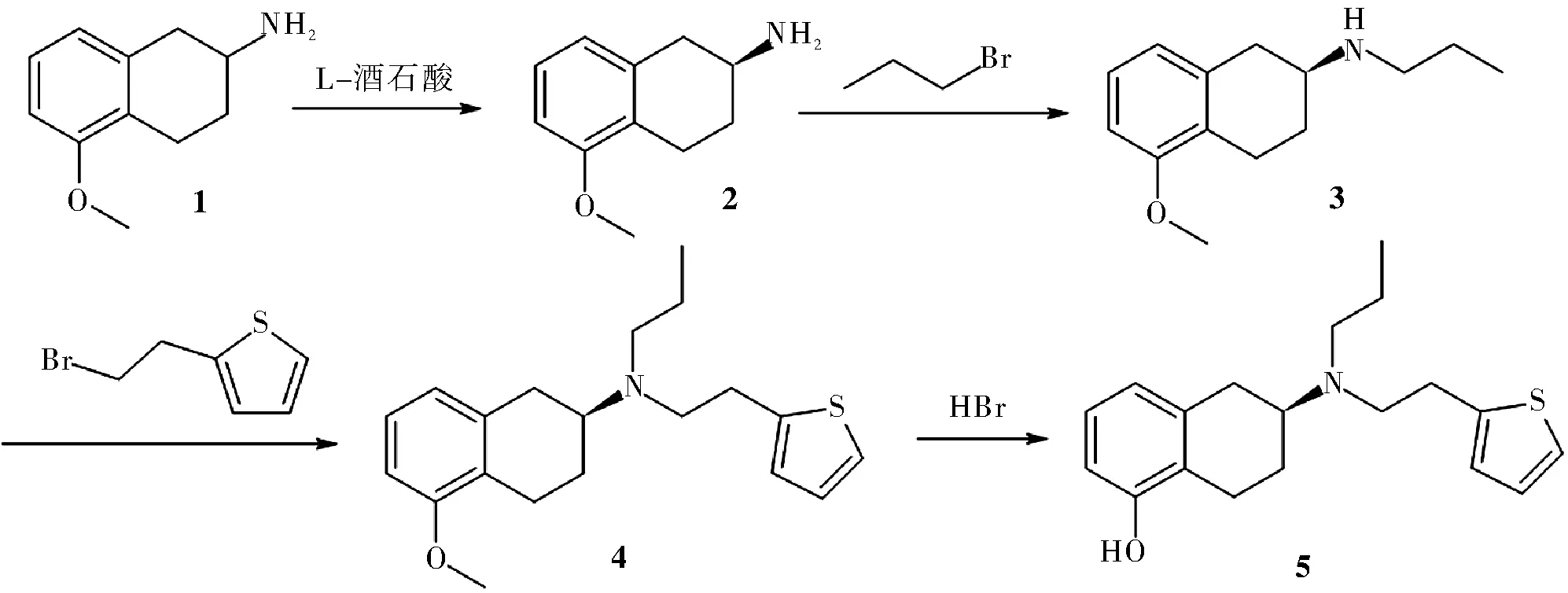
图3 拆分合成路线2Fig.3 Separation and synthesis route 2
合成步骤如下:以2-氨基-5-甲氧基四氢萘(1)为原料,经L-酒石酸拆分得(S)-2-氨基-5-甲氧基四氢萘(2)。(2)与溴丙烷发生烷基化反应得到(S)-2-(N-正丙基氨基)-5-甲氧基四氢萘(3)。(3)和2-(2-溴乙烷)噻吩反应得到(S)-2-(N-正丙基氨基-N-(2-噻吩乙基))-5-甲氧基四氢萘(4)。(4)中加入氢溴酸,加热回流,调节溶液pH值至碱性,萃取,干燥得到罗替戈汀(5)。
此路线得到的目标产物光学纯度高,原料易得,生产成本较低。但跟拆分路线1类似,L-酒石酸手性拆分效果不够理想,两步烷基化反应的选择性问题增加了罗替戈汀纯化的难度,从而降低了收率。
1.3 拆分合成路线3
该方法的合成路线如图4[11]所示。

图4 拆分合成路线3Fig.4 Separation and synthesis route 3
合成步骤如下:将5-取代-N-2’-(噻吩-2-基-)乙基-1,2,3,4-四氢萘-2-胺(1)溶于丙酮和水的混合溶液。加入手性酸进行拆分,得到(S)-5-取代-N-2’-(噻吩-2-基-)乙基-1,2,3,4-四氢萘-2-胺(2)。(2)与溴丙烷进行烷基化反应得到(S)-5-取代-N-丙基-N-(2’-(噻吩-2-基-)乙基)-1,2,3,4-四氢萘-2-胺(3)。(3)与氢溴酸反应脱去保护基R,即可得到罗替戈汀(4)。
该合成路线的原料易得,无需对原料进行进一步修饰,通过一次重结晶即可得到光学纯度96%以上的手性胺(2),且收率较高。该光学纯度的(2)经过后续反应,最终能得到光学纯度不低于99.5%的罗替戈汀,整体工艺生产周期短,合成步骤少,生产成本低,目前已经被应用于工业生产。
2 手性辅助合成
2.1 手性辅助合成路线1
该方法的合成路线如图5[12]所示。

图5 手性辅助合成路线1Fig.5 Chiral aided synthesis route 1
合成步骤如下:以5-甲氧基-2-四氢萘酮(1)为原料,加入叔丁基亚磺酰胺,以钛酸四乙酯为催化剂,进行胺化还原反应得到5-甲氧基-1,2,3,4-四氢萘-2-甲基丙烷-2-亚磺酰胺(2)。在(2)中加入催化剂和溴丙烷进行烷基化反应,过滤,萃取得到5-甲氧基-N-丙基-1,2,3,4-四氢萘-2-甲基丙烷-2-亚磺酰胺(3)。(3)和盐酸、甲醇混合反应,调节溶液的pH为碱性,萃取,干燥浓缩得到5-甲氧基-N-丙基-1,2,3,4-四氢萘-2-胺(4)。将(4)、2-(2-溴乙基)噻吩、碳酸钾和N,N-二甲基甲酰胺混合反应,萃取,干燥浓缩得到(S)-2-(N-正丙基氨基-N-(2-噻吩乙基))-5-甲氧基四氢萘(5)。将(5)、氢溴酸和醋酸混合反应,调节溶液pH为碱性,萃取,干燥浓缩得到罗替戈汀(6)。
此路线中手性基团的引入和烯胺的还原采用了“一锅法”,与其他方法相比,操作简便,收率高,使用溴丙烷代替碘丙烷引入丙基,大大降低了成本,通过分步引入胺上的丙烷和噻吩基,使得反应具有良好的选择性。该合成路线反应的条件温和,绿色环保,制备的罗替戈汀纯度高,具有良好的应用前景。
2.2 手性辅助合成路线2
该方法的合成路线如图6[13]所示。
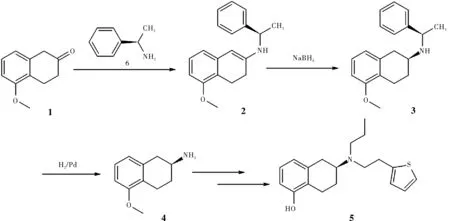
图6 手性辅助合成路线2Fig.6 Chiral aided synthesis route 2
合成步骤如下:5-甲氧基-2-四氢萘酮(1)和R-(+)-A-苯乙胺(6)发生加成-消去反应,得到(R)-5-甲氧基-N-(1-苯基乙基)-3,4-二氢萘-2-胺(2)。(2)与钯碳催化剂进行加氢还原和脱苄反应,得到(S)-2-氨基-5-甲氧基四氢萘(4)。(4)再经后续反应得到罗替戈汀(5)。
该合成路线制备成本低,对环境友好,但实验处理步骤较多,导致收率不高。
2.3 手性辅助合成路线3
该方法的合成路线如图7[14]所示。

图7 手性辅助合成路线3Fig.7 Chiral aided synthesis route 3
合成步骤如下:手性辅剂(R)-α-甲基对甲氧基苄胺(7)与5-甲氧基-2-四氢萘酮(1)缩合得(R)-5-甲氧基-N-[1-(4-甲氧基苯基)乙基]-3,4-二氢萘-2-胺(2)。(2)与硼氢化钠发生还原反应,再与烯丙基溴发生烷基化反应得到(4)。(4)与钯碳催化剂进行加氢还原和脱苄反应,得到(S)-2-氨基-5-甲氧基四氢萘(5)[15]。(5)再经后续反应得到罗替戈汀(6)。
该合成路线采用手性试剂辅助合成,步骤过多,使得目标产品的收率较低。
3 立体选择合成
3.1 立体选择合成路线1
该方法的合成路线如图8[16]所示。

图8 立体选择合成路线1Fig.8 Stereo selection synthesis route 1
合成步骤如下:5-甲氧基-2-四氢萘酮(1)和正丙胺进行胺化反应,得到(2)。将1,4-二氢吡啶和(2)混合,加入手性磷酸催化剂,进行不对称还原反应,反应完全后,使用柱层析进行分离得到(S)-2-(N-正丙基)胺基-5-甲氧基四氢萘(3)。将取代噻吩2-(2-氯乙基)噻吩,(3)和无水碳酸钠,混合加热进行卤代反应,得到(S)-2-(N-丙基-N-(2-(2-噻吩)乙基)氨基)-5-甲氧基四氢萘(4)[17]。将(4)溶于氢嗅酸中加热回流除去甲氧基,得到罗替戈汀(5)。
该合成路线采用了手性催化还原的方式得到手性胺,避免了用手性拆分,缩短了合成步骤,且产物构型单一,但是胺化还原过程所需要使用的试剂种类多,用量大,且最终产物的获得还需要通过柱层析,使得目标产品的收率降低。
3.2 立体选择合成路线2
该方法的合成路线如图9[18-19]所示。

图9 立体选择合成路线2Fig.9 Stereo selection synthesis route 2
合成步骤如下:5-甲氧基-2-四氢萘酮(1)与丙酰胺发生缩合反应,生成5-甲氧基-N-丙酰基-3,4-二氢萘-2-胺(2)。在催化剂二甲基铵二氯三(μ-氯)双[(R)-(+)-2,2′-双(二苯基膦)-1,1′-联萘基]二钌的催化下,经不对称氢化还原反应制得(3)。(3)经还原反应制得(S)-2-(N-正丙基氨基)-5-甲氧基四氢萘(4)。(4)再经后续反应制得到罗替戈汀(5)。
该路线使用了昂贵的手性催化剂和还原剂,导致生产成本大大提高。
4 结 语
本文分别从拆分合成、手性试剂辅助合成和立体选择合成路线三个方面论述了罗替戈汀的合成路线以及各种路线的特点。
其中拆分合成路线3的原料易得,成本低,合成步骤少,能得到纯度99.5%以上的罗替戈汀,收率高,已经被应用于工业生产中。此外,手性辅助合成路线1采用了“一锅法”引入手性基团和还原烯胺,操作简便,反应选择性好,收率高,整个合成路线条件温和,污染小,也具有很好的应用前景。

