基于适配体-金纳米粒子和光热-激光背向散射干涉技术的水中As(Ⅲ)的定量检测
田耀宗, 张校亮, 谭 慷, 李晓春
(1.新型传感器与智能控制教育部与山西省重点实验室,太原理工大学物理与光电工程学院,山西太原 030024;2.太原理工大学生物医学工程学院,山西太原 030024)
砷在自然界中主要以As(Ⅲ)和As(Ⅴ)的形式存在,其中As(Ⅲ)的毒性远高于As(Ⅴ)[1]。含砷工业废水的不合理排放,含砷农药的大量使用均会对水源和土壤造成污染[2-4]。长期饮用、食用被砷污染的水和粮食会造成人体内砷的蓄积,严重危害人体健康[5,6]。世界卫生组织(WHO)要求饮用水中砷含量低于10 μg/L[7];我国要求饮用水中砷含量低于10 μg/L[8],所排放污水中砷含量低于0.5 mg/L[9],土壤中砷含量低于20 mg/kg[10]。因此,对环境中的砷,尤其是As(Ⅲ)的检测,对于环境监测以及保障人民健康具有重要意义。目前对于As(Ⅲ)的检测主要包括:电感耦合等离子体质谱法(ICP-MS)、原子吸收光谱法(AAS)、原子荧光光谱法(AFS)等大型仪器检测法。这些方法具有检测限低、灵敏度高、准确性好等优点[11],但需要大型仪器,成本高、操作复杂,不适合快速筛查。近些年来研究者们一直在探究新的快速检测As(Ⅲ)的方法。
核酸适配体(适配体)是一段能够特异性地与目标分子结合的DNA或RNA片段,与普通的抗体相比适配体具有高特异性、高亲和性、靶范围广、筛选周期短、易修饰等特点[12]。由于As(Ⅲ)的适配体的发现[13],基于适配体检测As(Ⅲ)的方法陆续出现,其中基于As(Ⅲ)适配体-金纳米粒子(Au NPs)结构的光学检测方法引起了众多研究者的关注[14]。2012年,Wu等人利用As(Ⅲ)适配体与阳离子表面活性剂PDDA形成复合结构,当待测样品中存在As(Ⅲ)时,适配体会特异性地与As(Ⅲ)相结合,裸露的PDDA会吸引溶液中的Au NPs相互靠近发生聚集,溶液颜色由酒红色变为蓝色。通过建立溶液在波长650 nm和520 nm的吸光度比值与As(Ⅲ)浓度的关系,实现了水中As(Ⅲ)的定量检测,检出限低至5.3 μg/L[15]。2019年,Matsunaga等人构建了As(Ⅲ)适配体-Au NPs结构,加入高浓度NaCl引起Au NPs聚集,通过溶液吸光度变化实现了地下水中As(Ⅲ)的检测[16],检出限为0.161 mg/L。分光光度法灵敏度高,但该方法对待测样品的体积需求量较大,溶液中未知颗粒发生散射也会对实验结果造成影响[17]。因此,Au NPs 光学信号的新型检测方法一直是人们研究的热点。
Au NPs具有良好的光热效应,在激光照射下,Au NPs强烈地吸收激光能量并将其转化为热量,从而引起周围介质温度的上升及折射率变化,变化的幅度与其浓度和形态有关[18,19]。当Au NPs发生聚集时,溶液由酒红色变为蓝紫色,其固定波长处的光热效应也会发生变化,而光热引起的溶液折射率的变化可以采用激光背向散射干涉等光学方法进行检测,具有灵敏度高、非接触等优点[20]。基于以上研究,我们提出了基于适配体-Au NPs和光热-激光背向散射干涉(Photothermal Laser Backscattering Interference,PT-BSI)原理进行As(Ⅲ)检测的技术。采用波长为532 nm的绿光激光器作为光热效应的激发光源,待测样品中As(Ⅲ)的浓度不同时,Au NPs聚集的程度也不同,光热效应导致溶液的折射率变化幅度就不同,表现为干涉条纹移动量的不同。通过建立干涉条纹移动量与As(Ⅲ)的浓度的关系,实现了水中As(Ⅲ)浓度的检测,检出限为0.127 mg/L,可以用于排放废水、部分地区As(Ⅲ)超标地下水,以及土壤中As(Ⅲ)的检测[9,10,16]。
1 实验部分
1.1 仪器与试剂
MGL-Ⅲ-532全固态激光器(长春新产业光电技术有限公司,100 mW);78 HW-1数显磁力搅拌器(杭州仪表电机有限公司);LC100线阵CCD(THORLABS);HC-2518高速离心机(安徽中科中加科学仪器);TED200C温控器(THORLABS);TKAGenpure UV超纯水系统(美国,赛默飞世尔公司);TEC3-6半导体致冷器(THORLABS);UV-3100紫外-可见光分光光度计(上海美普达仪器有限公司);AD590温度传感器(THORLABS);石英毛细管(佰思特石英)。
As(Ⅲ)适配体5′-TTACAGAACAACCAACGTCGCTCCGGGTACTTCTTCATCG-3′(上海生工生物工程有限公司),NaCl(≥99.5%,分子生物学级,美国Sigma-Aldrich公司),NaAsO2(≥99%,美国Sigma-Aldrich公司),柠檬酸三钠(分析纯,≥99%,美国Sigma-Aldrich公司),NaBH4(98%,美国Sigma-Aldrich公司);HAuCl4(Au:23.5%~23.8% in dilute HCl,上海阿拉丁生化科技股份有限公司)。
1.2 实验装置

图1 实验装置示意图Fig.1 Schematic diagram of the experimental device
如图1所示,激光器发射一束激光(532 nm、光束直径3.16 mm)经过反射镜后,垂直入射到毛细管(内径0.63 mm、外径2 mm)的检测区域。激光在毛细管内外界面产生多次反射、折射,其中一部分反射和折射光经镜面反射至线阵CCD处发生干涉,出现条纹状的干涉图案。通入不同浓度的As(Ⅲ) 溶液后,加入NaCl,Au NPs发生聚集,激光照射检测区域产生光热效应导致检测溶液升温,溶液折射率发生变化,条纹状的干涉图案发生移动,通过检测线阵CCD上干涉条纹的位置变化量,可实现对As(Ⅲ)的定量检测。为了避免环境温度变化的影响,在实验中采用温控器保持检测系统周围环境温度恒定。为了进一步提高检测精度,本文中对条纹信息进行傅里叶变换,从而获取条纹移动时对应的相位移动值[20]。
1.3 Au NPs溶液的制备
分别将0.5 g柠檬酸三钠固体、0.5 g HAuCl4固体溶于两个盛有50 mL去离子水的烧杯中,制得 1%的柠檬酸三钠溶液及1%HAuCl4溶液。用去离子稀释1%的HAuCl4溶液,制得0.01%的HAuCl4溶液。将0.0375 g NaBH4固体溶于盛有50 mL 1%柠檬酸三钠溶液的烧杯中,制得0.075%的NaBH4溶液,室温下在磁力搅拌机上将0.5 mL 1%的柠檬酸三钠溶液加入到50 mL 0.01%的HAuCl4溶液中,搅拌使之充分反应,60 s后向混合溶液中加入1 mL 0.075%的NaBH4溶液,所得Au NPs 溶液为酒红色,其直径约为10 nm[21]。
1.4 As(Ⅲ)的定量检测
分别取250 μL 浓度为2 μmol/L的适配体溶液,分别加入到8个盛有600 μL Au NPs溶液的PE管中,振荡混合均匀得到反应液。然后依次将130 μL 浓度为0、0.5、0.8 、1、2、5、8、10 mg/L的As(Ⅲ)标准溶液,分别加入到反应液中混合均匀,5 min后向上述溶液中分别加入20 μL 浓度为2 mol/L 的NaCl 溶液,最后将混合液通入毛细管的检测区域,调节激光入射功率为20 mW,采集条纹状干涉图案的相位移动值。
2 结果与讨论
2.1 Au NPs聚集原理
稳定的Au NPs溶液为酒红色,加入高浓度的NaCl后,溶液中的阳离子会中和Au NPs表面电荷,使Au NPs发生聚集,溶液变为蓝紫色[16,21]。将适配体加入到Au NPs溶液中,适体链可以包裹在分散的Au NPs上形成保护层,此时加入高浓度的NaCl,由于适配体的保护作用,Au NPs不会发生聚集。如图2所示,将待测溶液加入适配体与Au NPs的混合液中,若待测液中不存在As(Ⅲ),即使溶液中存在阳离子,Au NPs仍处于分散状态并保持稳定;若待测液中存在As(Ⅲ)时,Au NPs表面包裹的适配体会脱落,并与As(Ⅲ)形成更稳定的结构,加入NaCl溶液后,Au NPs发生聚集,溶液颜色发生改变。
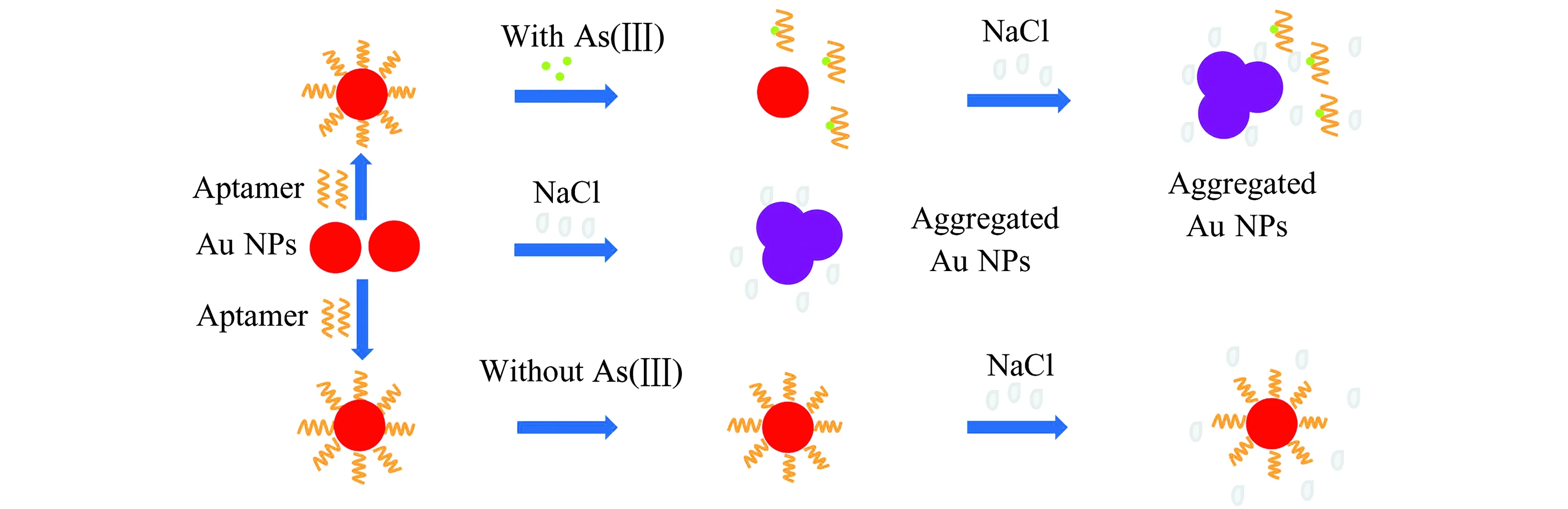
图2 适配体-纳米金检测As(Ⅲ)原理图Fig.2 Schematic illustration of As(Ⅲ) detection using aptamer-Au NPs
2.2 实验条件的优化
2.2.1 NaCl浓度分别取0、4、5、10、15、20、25 μL浓度为 2 mol/L的NaCl溶液与600 μL Au NPs溶液混合均匀,加水使溶液总体积为1 000 μL,NaCl溶液的实际浓度为0、0.008、0.01、0.02、0.03、0.04、0.05 mol/L,利用分光光度计测量溶液的吸收光谱,结果如图3所示。从图中可以看到,NaCl浓度越大,Au NPs逐渐发生聚集,最大吸收峰处的吸光度越低,当加入20 μL NaCl溶液(在混合液中的实际浓度为0.04 mol/L)后,吸收峰的吸光度不再下降,因此,实验中我们选取20 μL浓度为2 mol/L的NaCl溶液。
2.2.2 适配体浓度分别移取0、50、100、150、200、250 μL的浓度为2 μmol/L的As(Ⅲ)适配体溶液与600 μL Au NPs溶液混合均匀,静置5 min后,分别向上述混合液中加入“2.2.1”所述优化的最佳浓度的NaCl溶液,加水使溶液总体积为1 000 μL(混合液中适配体实际浓度为0、0.1、0.2、 0.3、0.4、0.5 μmol/L)混合均匀,测量不同浓度适配体下溶液的吸收光谱,如图4所示。从图可以看到,当适配体浓度为0时,加入NaCl,最大吸收峰处的吸光度最低,长波长处的吸光度增加,表明Au NPs之间发生聚集。当适配体溶液浓度越来越高时,表面形成适配体保护层的Au NPs越来越多,其最大吸收峰值不断增高,当加入250 μL适配体溶液后(对应浓度为0.5 μmol/L),最大吸收峰处吸光度不再增高,说明此时Au NPs被完全包裹,因此实验中我们选取250 μL 浓度为2 μmol/L的适配体溶液(在混合液中实际浓度为0.5 μmol/L)。

图3 加入不同浓度NaCl溶液后Au NPs溶液的吸收光谱Fig.3 Absorption spectra of Au NPs with different concentrations of NaCl

图4 适配体浓度不同时加入NaCl溶液后Au NPs溶液的吸收光谱Fig.4 Absorption spectra of Au NPs in solutions with different aptamer concentrations after NaCl solution added
2.3 基于光热-激光背向散射干涉(PT-BSI)的As(Ⅲ)定量检测
依次取“1.4”所述的As(Ⅲ)、适配体、Au NPs和NaCl组成的混合液20 μL,通入毛细管中,打开激光器,调节激光入射功率为20 mW,使得激光照射毛细管检测区域225 s,观察干涉条纹相对于初始时刻的变化。由于激光器的发射波长为532 nm,接近Au NPs的吸收峰,激光照射检测区域产生光热效应导致检测溶液升温,溶液折射率发生改变,条纹状的干涉图案发生移动。我们将某时刻干涉条纹的相位值相对于初始时刻相位值的差值定义为该时刻的PT-BSI相位变化值信号(rPT-BSI signal),并记录不同时刻的rPT-BSI signal数据。如图5(A)所示,由于光热作用,随着激光照射时间的增加, rPT-BSI signal逐渐增大,最后达到稳定。我们将稳定后的PT-BSI相位变化值作为该溶液的最终有效的PT-BSI相位变化值信号(ePT-BSI signal),并建立As(Ⅲ)浓度与ePT-BSI signal关系(图5(B))
从图4及图5(A)可以看到,随着溶液中As(Ⅲ)浓度的增大,激光波长处的吸光度逐渐降低,光热效应减弱,其ePT-BSI signal逐渐减小。图5(B)给出了0~10 mg/L范围内的不同浓度As(Ⅲ)的相位变化值信号ePT-BSI signal。由图可知,ePT-BSI signal随As(Ⅲ)浓度的增大而减小,两者呈线性关系,线性相关系数R2为0.9939,灵敏度为0.021 rad/(mg·L-1),计算所得检出限(3σ)为0.127 mg/L。

图5 (A)不同浓度 As(Ⅲ)溶液的rPT-BSI signal与时间的关系;(B)ePT-BSI signal与As(Ⅲ) 浓度的关系Fig.5 (A) Relationship between rPT-BSI signal and time for different concentrations of As(Ⅲ);(B) Relationship between ePT-BSI signal and As(Ⅲ) concentration
虽然127 μg/L远高于饮用水中的As(Ⅲ)需低于10 μg/L的限定,但该方法可用于排放废水、部分地区As(Ⅲ)超标地下水,以及土壤中As(Ⅲ)的检测[9,10,16]。此外,若将实验中所用激光器的功率适当增大,还可以进一步提高检测的灵敏度,并降低检出限。
2.4 As(Ⅲ)检测的选择性

图6 As(Ⅲ) 检测方法的选择性Fig.6 The selectivity test for the detection of As(Ⅲ)
为了验证本方法的抗干扰性能,研究了常见的金属离子对As(Ⅲ)的干扰情况。配制2 mg/L的As(Ⅲ)、Ni2+、Na+、Ca2+、Fe(Ⅲ)、Cr(Ⅲ)、Cu2+溶液。分别将250 μL浓度为2 μmol/L的As(Ⅲ)适配体溶液与600 μL Au NPs混合均匀,然后分别加入130 μL浓度为2 mg/L的上述金属离子溶液,振荡后静置5 min使之充分反应,最后加入20 μL的2 mol/L的NaCl溶液。依次取20 μL混合溶液通入毛细管中,打开激光器进行检测。为了便于比较,我们将空白溶液的ePT-BSI signal与每个样品的ePT-BSI signal的差值作为检测信号,即ΔePT-BSI signal,结果如图6所示。由图可以看出,As(Ⅲ) 的信号最强,而以上几种常见离子的信号较弱,对As(Ⅲ)的检测影响较小。说明本方法具有良好的选择性。
2.5 加标水样的检测
为了验证该检测方法的可靠性,对加标自来水水样中As(Ⅲ)进行了检测。配制As(Ⅲ)浓度分别为 0.50、0.80、1.0、5.0 mg/L水样(纯自来水中未检出As(Ⅲ))。实验结果,加标样品检测出As(Ⅲ)浓度分别为0.538、 0.809、 1.05、 4.96 mg/L,回收率分别为107.6%、101.1%、105.0%、99.2%。表明本方法可以用于部分严重超标水的检测。若提前对样品进行一定的预处理,方法还可以用于排放废水以及土壤中As(Ⅲ)的检测。
3 结论
本文研究了一种基于适配体-金纳米粒子结构的探针和光热-激光背向散射干涉技术的As(Ⅲ)定量检测方法。金纳米颗粒和As(Ⅲ)可以与其适配体竞争性结合,导致As(Ⅲ)适配体从金纳米颗粒表面脱落,在高浓度盐作用下发生聚集,造成溶液在激光波长处的光热效应发生变化,通过检测激光背向散射干涉条纹的移动信息,实现了As(Ⅲ)的定量检测。此外,该方法还可用于涉及普通显色反应的目标物检测中。因此,本方法具有快速、微体积、普适性广等优点。

