酪蛋白-羧甲基壳聚糖美拉德产物的制备及表征
魏玉娇,郭晓强,周婷
(成都大学 药学与生物工程学院,成都 610106)
美拉德反应又称褐变反应,是羰基化合物和氨基化合物的组合反应,改变食品的色泽和风味[1], 在食品加工处理过程中很常见[2]。壳聚糖是甲壳素脱乙酰后(D.D)的产物[3],是一种天然的碱性多糖。因其结构中含有大量的COOH和NH2,所以它只能溶于稀的有机酸溶液中,这使它的应用受到一定限制[4]。羧甲基壳聚糖(CAS)是壳聚糖改性后的产物。它有很多活性,如增稠、分散、乳化、保湿等。相比于壳聚糖,改性后的CAS在酸性和碱性溶液中均能溶解[5]。酪蛋白(CN)含有人体需要的多种氨基酸,是一种营养价值很高的完整蛋白质,常被当作食品添加剂,有乳化、增稠等作用。其等电点为4.6,一般溶于碱性溶液,不溶于酸性溶液,限制了它的应用。改变蛋白质性质的方法有很多,MRPs是改变蛋白功能特性的有效方法[6]。这种方法安全、绿色,且能进一步提高原料的功能特性,减少原料用量,降低原料成本,拓展它们的应用领域[7]。
在食品领域中,CN和CAS在美拉德反应反面也有研究,谷风林[8]做了酪蛋白和葡萄糖的结合物,证明了在烟草膨茎中添加MRPs可以显著提高烟草香气的使用价值和扩大茎丝。赵静等[9]确定了美拉德反应的最佳反应条件,并在最佳条件下发现了美拉德反应产物的抗氧化活性和自由基清除率。文献[10]通过美拉德反应,为研发天然的、绿色的抗氧化剂提供了新的方法,制得了一种溶解性和抗氧化能力都更好的产物。文献[11]使用MRPs对天然的防腐剂进行了改良,制备了一种多功能的食品添加剂,拓展了天然防腐剂的使用。
壳聚糖因水溶性较差,将其改性后得到CAS可以扩增它的应用[12]。酪蛋白的营养价值很高,美拉德反应可以提高酪蛋白的特性。它绿色、安全,被认为是一种前景很好的方法,可以明显改善蛋白质的功能和性质。提高蛋白质的抗氧化性,生成有抑制各种菌活性的、抗过敏和抗癌作用的美拉德反应产物[13]。本文用干热法制备美拉德产物,并对其进行表征,对蛋白质的改性研究以及扩展羧甲基壳聚糖的应用都有重要意义。
1 材料与方法
1.1 实验材料
壳聚糖(脱乙酰度95.2%)、酪蛋白氨基酸:食品级,源叶生物化学试剂有限公司;异丙醇、磷酸二氢钾、溴化钾、四硼酸钠:分析纯,麦客林化学试剂有限公司;邻苯二甲醛、十二烷基硫酸钠、β-巯基乙醇:化学纯,麦客林化学试剂有限公司。
1.2 实验设备
IS10傅立叶红外光谱仪 ThermoFisher公司;FW-5压片机 傅天胜达科技发展有限公司;ZNCL-B磁力搅拌器 科泰实验设备有限公司;SCIENTZ-10M冷冻干燥机 新芝生物科技股份有限公司;AR224CN分析天平 奥豪斯仪器有限公司;BG-06D超声波清洗机 邦杰电子产品有限公司;UB-10 pH计 丹佛仪器有限公司;DD5N低速大容量离心机 凯达科学仪器有限公司。
1.3 实验方法
1.3.1 羧甲基壳聚糖的制备
准确称取4 g CAS,加入40 mL 40%浓度的预配制NaOH溶液,碱性环境中超声30 min,使其充分溶解。再加入100 mL异丙醇,于30 ℃在磁力搅拌器上搅拌1 h。称取16 g氯乙酸并溶于40 mL异丙醇溶液中。反应完成后,加入200 mL的95%乙醇溶液停止反应。滴加乙酸将反应体系的pH调至中性,用体积分数为95%的乙醇溶液和无水乙醇清洗羧甲基壳聚糖滤饼,抽滤,收集沉淀。50 ℃干燥直至恒重,干燥后将其研磨成粉末状,即得到羧甲基壳聚糖样品。
1.3.2 酪蛋白-羧甲基壳聚糖反应产物的制备
反应产物的制备参考雷涛等[14]的方法并稍作改动。将酪蛋白和羧甲基壳聚糖加入pH 7.4的磷酸盐缓冲液,在室温下磁力搅拌1 h使其完全溶解并制备成均匀浓度的溶液。按一定比例(蛋白和多糖比为5∶1、5∶2、5∶3、5∶4、1∶1、4∶5、3∶5)制成含酪蛋白10%的混合溶液,于室温下超声搅拌1 h,使糖和蛋白充分混合均匀。预冻24 h后再冷冻干燥48 h,研磨成粉末。过筛,放入含有饱和溴化钾的密封容器中(相对湿度为79%)并将反应温度控制在50,55,60,65,70 ℃, pH为7.4,反应时间控制在24,36,48,60,72,84 h中让其反应, 达到反应时间后冷却终止反应。取适当的去离子水溶解样品,离心15 min,取上清液,冻干,研磨即得到样品。
1.4 美拉德产物的性能测定
1.4.1 褐变指数的测定
分别称取不同条件下的反应产物0.5 g于试管中,加入15 mL去离子水将其充分溶解。使用分光光度计,在420 nm波长下测量其吸光度。
1.4.2 接枝度的测定
为了测定游离氨基含量并计算接枝程度,使用OPA法。
OPA(邻苯二甲醛)试剂的配制:使用分析天平准确称取40.0 mg OPA到100 mL烧杯中。吸取管中的1.0 mL甲醇。20%(W/W)的十二烷基硫酸钠(SDS)溶液的配制:称取2 g十二烷基硫酸钠,溶解于10 mL去离子水中。0.1 mol/L的硼砂溶液的配制:准确称取3.814 g硼砂,加入100 mL去离子水,超声直至其完全溶解。分别取5 mL SDS溶液和25 mL硼砂溶液(0.1 mol/L)加入到装有OPA试剂的烧杯中,再加入100 μL的β-巯基乙醇,然后将烧杯中的液体转移到50 mL容量瓶中,并用超纯水调节体积。
取4.0 mL OPA试剂于试管中,加入200 μL不同比例、不同时间、不同温度反应前后的样品溶液,摇匀,35 °C,水浴2 min。倒入石英比色皿中,置于分光光度计中测量。以200 μL去离子水作为空白对照,按下式计算接枝度:
GD(%)=(A0-A1)/A0×100。
式中:A0为反应前溶液的吸光度值;A1为反应后溶液的吸光度值。
1.4.3 自由氨基含量的测定
准确称量0.1 g的样品,向其中加入10 mL的去离子水,使用磁力搅拌机,使样品溶解形成分布均匀的溶液。取事先配制好的OPA溶液4 mL和已经溶解均匀的样品溶液200 μL加入试管中,摇晃混匀,35 ℃水浴2 min。使用分光光度计在340 nm处测量其吸光值,所得到的结果称为A样。在同样的环境和条件下,以未经过处理的酪蛋白为A标,去离子水为空白对照。按照下式对所配制的样品中游离氨基含量进行测定:
式中:A样为OPA试剂加入样品在 340 nm处的吸光度值;A空为OPA试剂加入水在340 nm处的吸光度值;A标为OPA试剂中加入酪蛋白在340 nm处的吸光度值。
1.4.4 傅立叶红外光谱
取事先烘干的不含有任何水分的样品约1 mg放入干净的玛瑙研钵中, 在红外灯下研磨成细粉。估量加入150 mg干燥的且已经在红外灯下事先研磨好的 KBr一起研磨到它们完全、均匀的、充分地混合,让它们的粒度为2 μm以下(样品与 KBr的比例为1∶100~1∶200),将适量的混合样品放入干净的模具中,轻轻摇动模具使样品均匀,然后用手压机将其压成透明片材。在电脑上设置范围,之后将薄片放到光路中测定红外光谱,一般先采集KBr背景的红外光谱测定,然后再采集样品,范围为4000~400 cm。
1.5 数据分析
对所测样品数据均检测3次,用SPSS 17.0软件对实验数据采用Duncan多重比较进行分析。
2 结果与分析
2.1 蛋白和多糖比例对反应的影响
控制反应条件pH一定,湿度一定,温度为60 ℃,反应时间为72 h。CAS/CN对反应的影响见表1。
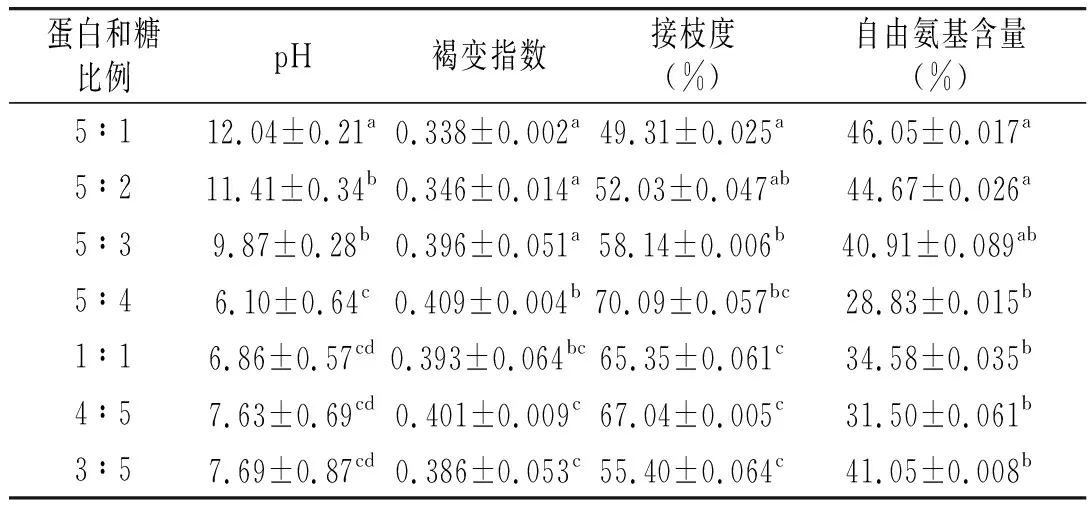
表1 蛋白和糖比例对反应的影响Table 1 The effects of protein and sugar ratio on the reaction
统计结果表明,不同浓度的酪蛋白和糖对美拉德反应的接枝率和游离氨基含量有显著影响(P<0.05)。对褐变指数也有显著影响(P<0.05)。反应底物的用量变化可以影响反应速度。适当的反应比例避免了副反应的发生并且可以提高反应速率。当蛋白和糖浓度不断增大时,它们之间碰撞的机会会增大很多,这样有利于反应的进行。然而,蛋白质分子和多糖分子受到空间阻碍,当浓度增加到一定程度时,它们之间的碰撞概率会降低,这对反应是非常不利的。由表1可知,随着酪蛋白和多糖比例的增加,接枝度先增大后减小,当底物比为5∶4时,褐变指数在0.4左右,褐变程度最大,接枝程度最大,游离氨基含量最低。说明蛋白中的氨基减少,发生了反应。pH值也先不断下降后趋于平稳,因此蛋白和糖的比例在5∶4左右最适宜。
2.2 温度对反应的影响
控制反应条件,蛋白和糖的比例为5∶4,pH值一定,湿度不变,不同温度对反应的影响见表2。

表2 温度对反应的影响Table 2 The effect of temperature on the reaction
统计结果表明,美拉德反应中温度起着很重要的作用。当温度低于60 ℃时,温度对褐变指数(P<0.05)有显著影响。褐变指数随着温度的升高而增加,但在60 ℃后,褐变指数缓慢下降。 当温度小于时60 ℃,温度对接枝度与自由氨基含量有显著的影响(P<0.05),接枝度随着温度的增大而增大,自由氨基含量随着温度的增大而减小。 当温度大于60 ℃时,接枝度的增长趋于平缓,再升高温度对接枝度和自由氨基含量影响不显著(P>0.05)。pH值逐渐减小,是因为氨基酸在碱性介质中表现为阴离子,反应性较强,容易发生反应。发生反应之后,氨基也被消耗,所以自由氨基含量下降,接枝度增加,pH值不断下降。因此,选择60 ℃为最佳培养温度。
2.3 时间对反应的影响
控制反应条件,温度60 ℃,pH恒定,湿度恒定,蛋白质和糖的比例为5∶4,不同反应时间对反应的影响见表3。
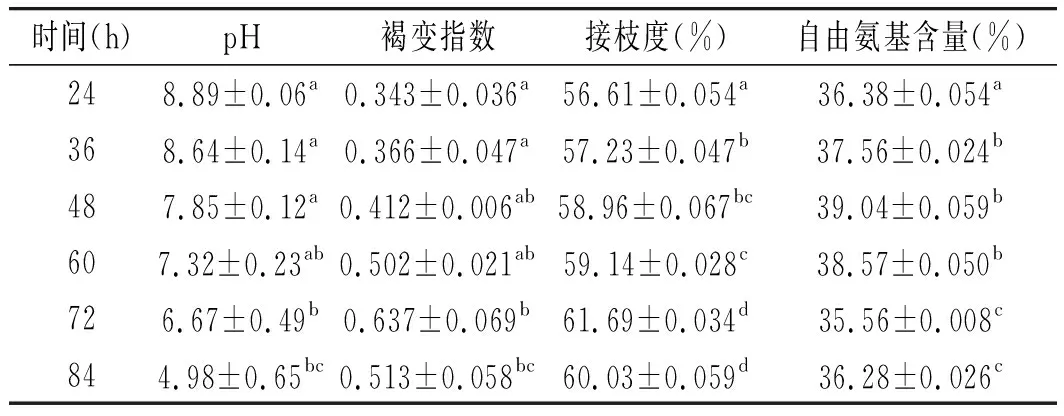
表3 时间对反应的影响Table 3 The effect of time on the reaction
统计结果表明,当反应时间小于72 h时,pH值缓慢下降,时间对接枝度和游离氨基含量有显著影响(P<0.05)。时间达到72 h后,接枝度增长趋势渐缓,再升高温度对接枝度影响不显著(P>0.05),随着时间的延长,褐变指数逐渐增加,效果显著(P<0.05)。
在蛋白质和多糖之间的反应中,可能发生还原性醛基和氨基之间的反应。因此,反应开始后,随着不断地加热,蛋白中的氨基随着结构的展开慢慢暴露在分子的表面,加热后糖和蛋白质连续结合,并且接枝程度逐渐增加。但是过度加热后会使蛋白质分子中的氨基酸结构被破坏,而且会增加蛋白质之间的相互作用,导致凝聚和沉淀,对反应产生不利影响。因此,在72 h时接枝度最大,游离氨基含量最小,褐变指数为0.6左右,褐变程度较大。
2.4 美拉德产物的红外光谱分析
本实验的目的是为了进一步确定蛋白质和多糖是否发生反应以及反应过程的变化。而红外光谱可以通过不同的吸收峰来表明反应。图中A代表混合物,B代表美拉德产物,C代表酪蛋白。
当蛋白和糖分子结合后,最明显的变化就是蛋白质分子中的羟基增多。具体表现在红外光谱图上是,在1700~1000 cm-1时出现吸收峰,在3700~3200 cm-1时出现一个宽峰。由图1可知,B在3700~3200 cm-1和1700~1000 cm-1的吸收对比酪蛋白都有所增加,它们分别是-OH和-CO键的吸收峰。由图1可知,在1650 cm-1处,B的吸收减弱,说明蛋白中的氨基参与了反应,数量明显减少。
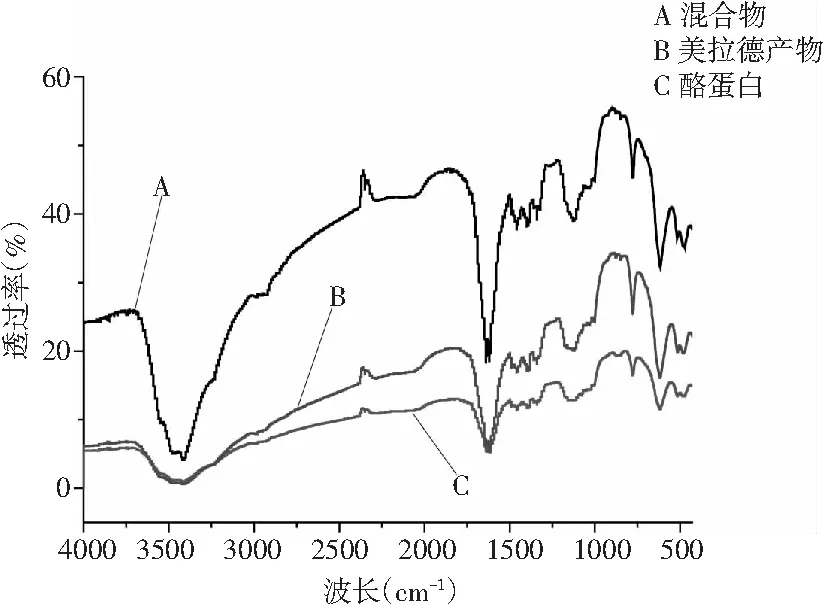
图1 红外光谱图Fig.1 The infrared spectrogram

3 结果与讨论
国内外研究蛋白质的改性主要有物理改性、化学改性和酶改性等方面。其中化学改性中的美拉德改性受到越来越多的关注,美拉德改性与其他化学改性相比简单、安全,而且还能改善蛋白质的多种功能性质。本文运用干热法使酪蛋白与羧甲基壳聚糖发生美拉德反应,进一步深入研究美拉德反应的条件,从而延伸和拓宽酪蛋白和羧甲基壳聚糖的应用领域。
本研究制备了酪蛋白和羧甲基壳聚糖的美拉德产物,并对产物的一系列特性进行了表征,测定了不同蛋白和多糖的比例、不同温度、不同反应时间对反应的影响。通过测定产物的pH值、褐变指数、自由氨基含量、接技度来确定最佳反应条件。最终结果表明最适宜反应条件是在60 ℃,相对湿度为79%,CN/CAS比例为5∶4,最终蛋白质浓度为10%的美拉德反应产物反应72 h具有最高的反应程度。 测得其褐变指数为0.697,接枝度为70.09%,自由氨基含量为28.83%。CN、CN/CAS和MRPs的红外光谱表明,酪蛋白与羧甲基壳聚糖发生美拉德反应。

