孟鲁斯特钠抑制半胱氨酸白三烯表达治疗阻塞性睡眠呼吸暂停低通气综合征远期疗效分析:前瞻性单中心单臂临床研究
倪俊杰
天津市武清区第二人民医院,天津 301700
流行病学研究显示[1],儿童阻塞性睡眠呼吸暂停低通气综合征(OSAHS)的发病率目前在3%左右,其发病机制主要是上气道的狭窄和阻塞[2-3]。临床表现为打鼾、张口呼吸、呼吸暂停等,严重影响患儿的睡眠质量。正常的睡眠是儿童正常分泌生长激素的重要条件,不良的睡眠可能导致生长激素分泌不足,从而影响生长发育。同时,长时间地张口呼吸对儿童的口腔颌面部发育会产生严重的影响,造成发育畸形。对于症状较为严重的OSAHS 患儿应予以手术治疗,但手术有一定创伤且在全麻下进行,因而部分患儿家属难以接受。最近国外有研究报道白三烯拮抗剂孟鲁斯特钠可以通过缩小肥大的咽扁桃体来缓解OSAHS 患儿临床症状,有望使病情缓解[4]。但国内鲜有此方面的报道。因此本研究探讨孟鲁斯特钠治疗OSAHS 临床疗效及对血清半胱氨酸白三烯(CysLTs)表达的影响。
1 材料和方法
1.1 研究设计
单臂开放前后对照前瞻性临床研究。
1.2 临床资料
2018 年3 月年至2020 年6 月天津市武清区第二人民医院经多导睡眠仪确诊为OSAHS 患儿62例为研究对象。纳入标准:年龄<16 周岁;符合OSAHS 诊断标准;PSG 监测夜间睡眠过程中阻塞性呼吸暂停指数>1 次/h,或阻塞性呼吸暂停指数>5次/夜;近亲属签署知情同意书。排除标准:高血压、糖尿病患儿;近期服用过白三烯拮抗剂(孟鲁司特钠);正在应用激素患儿;已摘除腺样体患儿。
1.3 药物仪器与设备
多导睡眠监测仪,购自澳大利亚Compumedics公司;全自动生化分析仪,购自美国贝克曼公司;人半胱氨酸白三烯酶联免疫吸附试剂盒,购自上海春晓生物技术有限公司。
1.4 治疗方法
多导睡眠监测:两组受试患儿经过夜间连续检查至少7 h 睡眠监测。同步记录胸腹呼吸运动、口鼻气流等。同时测量患儿身高、体质量、颈围,计算体质量指数(BMI)。标本采集:多导睡眠监测检查当天清晨空腹静脉采血3 mL,置于管中,以3 000 r/min 离心10 min,分离血清后,取上层血清置-80 ℃冰箱保存备检测。血清CysLTs 检测采用竞争性酶联免疫吸附法,根据试剂盒操作说明进行。
1.5 观察指标及疗效评价
观察记录患儿治疗前1周及治疗结束后1周响鼾、不安宁地睡眠或频繁觉醒、鼻塞张口呼吸、频繁上呼吸道感染及流涕评分情况及治疗前后血清CysLTs 变化情况。评分标准:未观察记录到上述症状1 分;几乎没有(极少)记录到2 分;很少记录到3 分;偶尔记录到4 分;常有5 分;大部分时间6 分;每时每刻7分。分值越高表示患儿症状越严重[5]。
1.6 统计学方法
2 结果
2.1 入组患儿一般情况
入组患儿年龄为(7.8±3.6)岁,男37 例,女25 例,具体情况见表1。
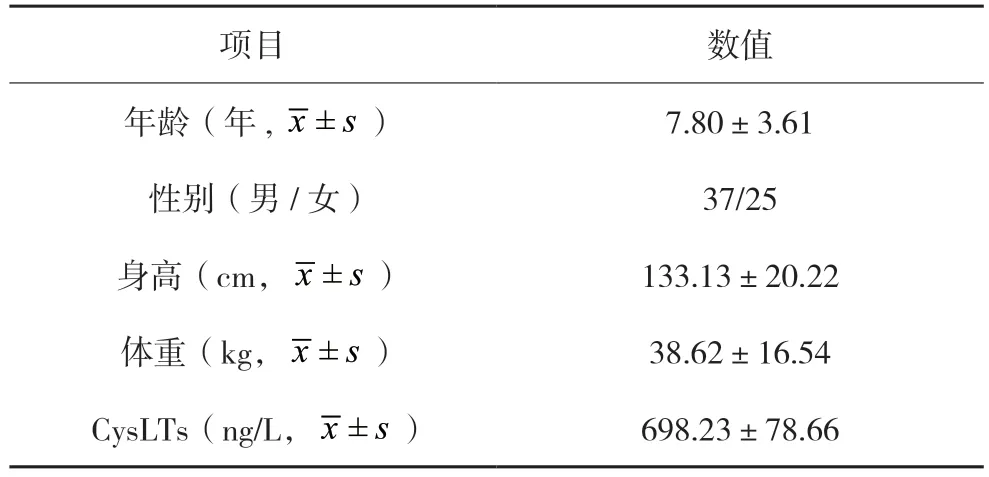
表1 临床一般情况比较
2.2 治疗前后症状评分
治疗12周后患儿响鼾、不安宁睡眠或频繁醒觉、鼻阻塞而张口呼吸等症状评分显著低于治疗前且差异有统计学意义(P<0.05),见表2。
表2 治疗前后患儿症状评分比较(分,)
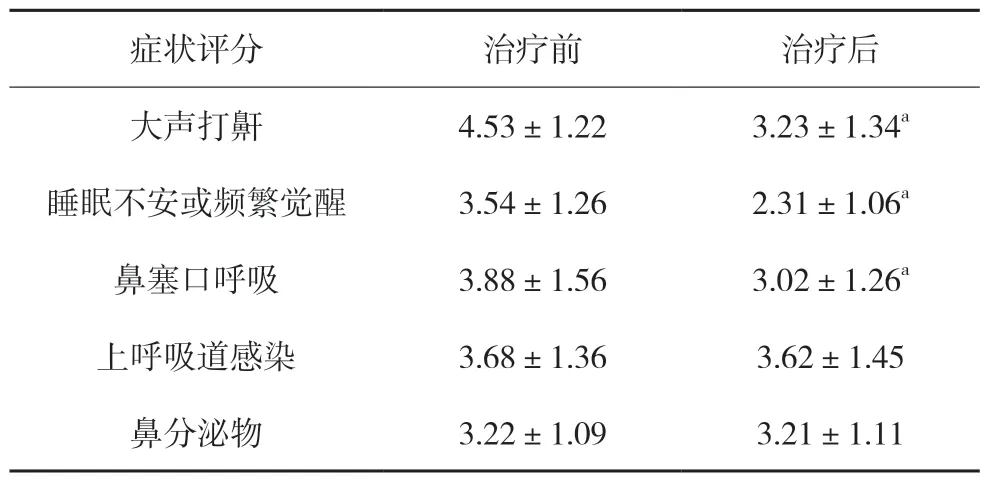
表2 治疗前后患儿症状评分比较(分,)
注:与治疗前比较,aP<0.05。
2.3 血清CysLTs 水平比较
治疗前血清CysLTs 为(698.23±78.66)ng/L,治疗12 周后为(456.88±60.12)ng/L,治疗后显著降低(P<0.05),图1。
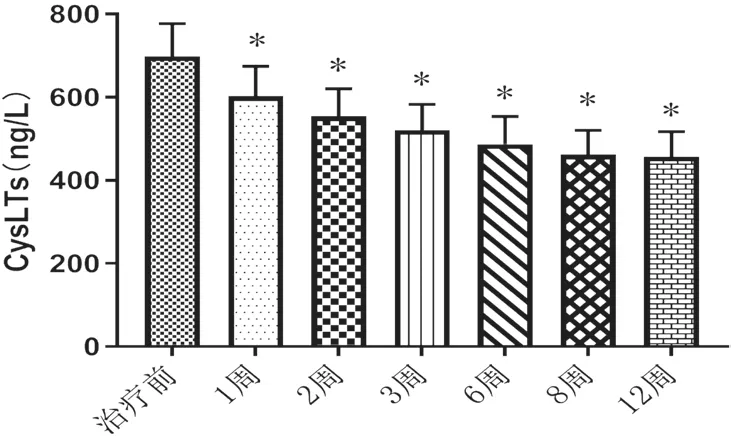
图1 患儿治疗前后血清CysLTs水平比较
2.4 远期随访
对患者治疗后进行为期12 个月的随访,其中症状复发者(症状评分>治疗12 周时1.5 倍)18 例,无复发者44 例。复发组治疗12 周时CysLTs 水平显著高于对照组[(478.3±54.2)vs(431.2±65.9),P<0.05],图2。以治疗12周时CysLTs水平为参考预测患儿复发的敏感性为72.73%(95%CI:57.21%~85.04%),特异性为66.67%(95%CI:40.99%~86.66%),ROC 曲线下面积为0.75(95%CI:0.625 8~0.870 5),图3。

图2 复发和无复发组患儿血清CysLTs分布图
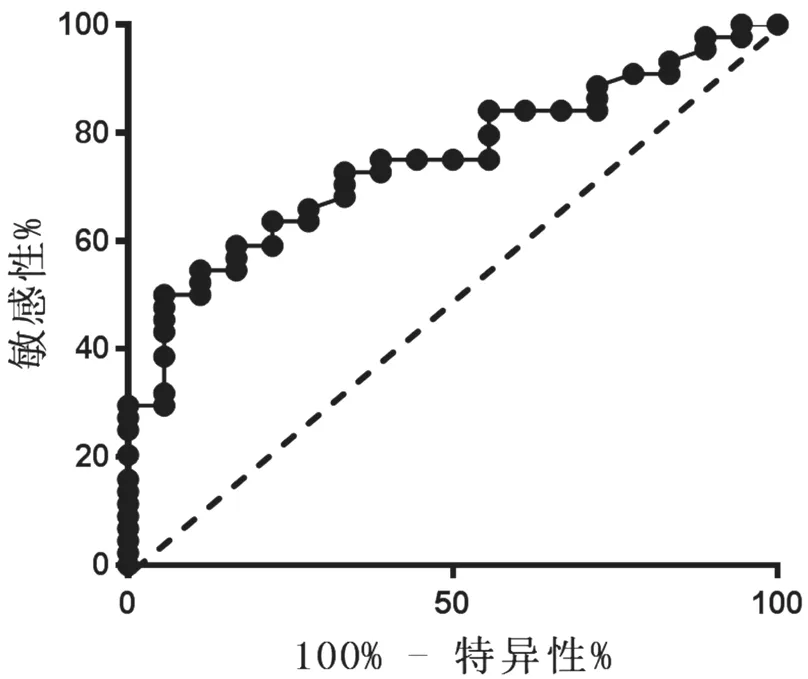
图3 复发和无复发组患儿治疗12周时血清CysLTs水平预测复发的ROC曲线
2.5 CysLTs 水平与患者症状复发的关系
根据治疗12 周后CysLTs 水平中位数(445.10 ng/L)分为CysLTs 高表达(n=30)和低表达(n=32)组,高表达组治疗后12 个月复发12 例,低表达组复发6 例,高表达组复发风险(HR=0.38,95%CI:0.15~0.97)显著高于低表达组(P<0.05),见图4。

图4 CysLTs高低表达组患儿12个月随访复发风险比较
2.6 不良反应
服药期间发生患儿头痛1 例,恶心呕吐1 例,不良反应发生率为3.23%。
3 讨论
孟鲁司特为CysLTs 受体拮抗剂,能特异性抑制气道中的CysLTs 受体,通常被认为在运动和阿司匹林诱导的哮喘的治疗中具有明显作用[6-7]。它也被用作哮喘患者的附加治疗,这些患者的哮喘通过吸入性皮质类固醇单一疗法或长效β2-激动剂和吸入性皮质类固醇的联合疗法控制不佳。然而,最近有报道称孟鲁司特具有次级抗炎特性。这些活性使孟鲁司特能够靶向嗜酸性粒细胞、单核细胞,尤其是皮质类固醇不敏感的中性粒细胞,这表明该药物可能具有更广泛的抗炎活性[8]。因此,孟鲁司特在间歇性哮喘、慢性阻塞性肺疾病、OSAHS的治疗中可能具有一定疗效[9]。
目前研究已证实孟鲁司特钠可以缓解哮喘患儿的临床症状,减少哮喘的发作次数。同时近年来的研究发现,儿童OSAHS的病因和发病机制,除了与上气道梗阻有关外还与体内的炎症因子有关[3]。患儿夜间低氧可诱发体内细胞因子增多,进而激活相关炎症因子,导致患儿OSAHS 进一步发生发展。研究报道CysLTs 为体内重要的炎症因子,参与体内多种炎症反应过程。CysLTs 相关的炎症过程可能影响患儿呼吸道黏膜,造成黏膜水肿及卡他症状,进而导致咽喉部塌陷,从而加重OSAHS 症状[10]。已有国外研究报道[11],孟鲁司特钠口服可缓解OSAHS 患儿临床症状,部分患儿通过长期口服孟鲁斯特咽扁桃体明显缩小。国内梁振江等[12]报道了一项关于孟鲁司特钠治理儿童OSAHS的前瞻性临床随机对照研究,研究认为与空白对照组比较孟鲁司特钠组患儿有一定的临床疗效,可缓解部分患儿响鼾、不安宁睡眠或频繁醒觉症状。对于服药后症状无明显缓解者可再考选择手术治疗。
在本研究中,我们采用开放性前后对照研究,探讨孟鲁司特钠对儿童OSAHS 临床疗效,结果认为鲁斯特钠可显著缓解OSAHS 患儿临床症状,其作用机制可能是通过降低血清CysLTs 水平来实现的。研究同时还发现,患者的症状缓解程度和复发水平与治疗后CysLTs 水平有关,治疗12 周后CysLTs 水平越高,其随后1 年内复发风险越高。因此提示,CysLTs 治疗后水平可作为OSAHS 疗效和复发风险的预测指标,且具有较高的敏感性和特异性。同时,部分患儿效果并不理想,对于症状较重,服药后无缓解的患儿建议手术治疗。
但研究也存在一定的局限性,首先纳入的患儿数较少,随访时间较短,因而统计学效能不高;其次,研究未设置对照组,其与其他药物或标准治疗无直接比较。因此,后续应加大样本量进行长期随访并设置对照组,提高结论的可靠性。

