电解水在小龙虾壳脱矿物质和蛋白质中的应用
张建旭,王旭旭,孙一丹,龚建刚,桑亚新,孙纪录*
(1 河北农业大学食品科技学院 河北保定071001 2 承德市水产技术推广站 河北承德067000)
几丁质是仅次于纤维素的第二大天然多糖,是2-氨基-2-脱氧-D-葡聚糖和2-乙酰氨基-2-脱氧-D-葡聚糖由β-1,4-糖苷键连接而成,广泛存在于甲壳类动物壳中[1]。几丁质可以作为许多生物基材料的成分[2]。它在许多领域作为具有高潜力的新功能生物材料而受到极大关注[3]。
从甲壳类动物壳中提取几丁质的传统方法是分别使用盐酸和氢氧化钠去除壳中的矿物质(主要为CaCO3)和蛋白质,之后脱色。该方法虽然效率高,但是产生大量的酸碱废液,造成环境问题,增加生产成本[4]。电解水(Electrolyzed water,EW)是在特殊的装置中电解稀氯化钠溶液而得到的酸性电解水(Acidic electrolyzed water,AEW)和碱性电解水(Basic electrolyzed water,BEW)的总称[5]。近年来,EW 在食品工业领域广泛用于抗菌和保鲜[6-7]。利用EW 提取甲壳类动物壳中的几丁质,迄今鲜有报道。
我国小龙虾产量大,其可食部分少,虾壳等废弃物多,而虾壳中富含几丁质。本实验室曾使用BEW 脱除蟹壳中的蛋白质[8]。本研究拟在前期试验的基础上,分别使用AEW 和BEW 对小龙虾壳进行脱矿物质和脱蛋白质研究,并分析几丁质的理化性质和结构,旨在为从虾壳中提取几丁质开发一种新型环保的生产工艺。
1 材料与方法
1.1 主要材料
虾壳,保定市场售小龙虾;其它试剂均为分析纯级。
1.2 主要仪器设备
电解水发生器,河北农业大学食品科技学院食品微生物学实验室自制;752N 紫外可见分光光度计,上海佑科仪器仪表有限公司;XL-100 型马弗炉,河南市鹤壁亿欣仪器仪表有限公司;WSC-2B 便携式精密色差仪,上海仪电物理光学仪器有限公司;SU8010 型扫描电子显微镜,日本Hitachi公司;TG/DTAA6200 热重分析仪,精工电子纳米科技有限公司;Spectrum65 傅立叶红外变换光谱仪,铂金埃尔默仪器有限公司;XD6 多晶X 射线衍射仪,北京普析通用。
1.3 试验方法
1.3.1 虾壳粉制备 清洗虾壳,放入60 ℃电热鼓风干燥器中,干燥至恒重。将烘干的虾壳粉碎,过120 目筛,制得虾壳粉,密封,干燥贮存备用。
1.3.2 EW 处理虾壳粉
1) AEW 处理虾壳粉 向电解水发生器的酸性、碱性电解槽中分别加入1 L 的NaCl 溶液,称取20 g 虾壳粉放入酸性电解槽中。接通电源进行处理,电压设为20 V。每隔0.5 h 测溶液pH 值及钙离子含量,直至钙离子含量趋向稳定,停止电解,记录处理时间。将处理液5 000 r/min 离心10 min,沉淀洗涤至中性,60 ℃干燥至恒重,即得脱去矿物质的虾壳粉。
2) BEW 处理虾壳粉 操作过程与1.3.2(1)基本相同。其区别在于将虾壳粉放入碱性电解槽中,处理期间测定处理液的pH 值及蛋白质含量,所得为脱蛋白质的虾壳粉。
3) AEW 和BEW 联合处理虾壳粉 对虾壳粉进行AEW(2%NaCl 制备)处理脱矿物质,操作过程与1.3.2(1)基本相同,将脱去矿物质的虾壳粉进行BEW(2%NaCl 制备)处理脱蛋白质,操作过程与1.3.2(2)基本相同,所得为几丁质。
1.3.3 传统无机酸碱法制备几丁质 参考王娟娟[9]的方法。
1.3.4 钙离子含量测定 参照国标GB 7476-1987《水质钙的测定EDTA 滴定法》[10]方法测定。
1.3.5 BEW 处理液中蛋白质含量测定 采用紫外吸收法中的直接法[11]测定。
1.3.6 灰分测定 参照国标GB 5009.4-2016《食品安全国家标准食品中灰分的测定》[12]方法测定。
1.3.7 固体样品中蛋白质含量测定和蛋白质脱除率的计算 参考韩晓梅等[8]的方法。
1.3.8 颜色测定 取不同EW 处理的粉末状样品约2 g,平铺于称量纸上,压平,随机选取3 个点用色差仪测量其L*、a*、b*值,以AEW 和BEW 联合处理的样品为对照,测定其它样品的ΔL*、Δa*、Δb*及ΔE 值并进行比较[13]。
1.3.9 水分含量测定 参照GB 5009.3-2016《食品安全国家标准食品中水分的测定》[14]方法测定。
1.3.10 特性黏度及黏均分子量的测定 黏均分子量测定参照Hong 等[15]和Poirier 等[16]的方法。选择5%LiCl/DMAc 作为几丁质的溶剂,采用参数是α=0.95 和K=7.6×10-5dl/g。特性黏度测定参照蒋挺大[17]的方法,采用外推法计算特性黏度。
1.3.11 脱乙酰度测定 采用行业标准《甲壳素与壳聚糖》中附录A 的方法[18]。
1.3.12 扫描电镜观察 将干燥样品均匀地固定在贴胶的电镜进样台上,真空条件下离子溅射喷金,采用扫描电子显微镜拍照观察样品结构。
1.3.13 热重分析 参照《中华人民共和国药典》第4 部0661 热分析法中的热重分析方法,设定升温范围30~600 ℃,升温速率10 ℃/min[19]。
1.3.14 傅立叶变换红外光谱分析 采用压片法制备样品,在Spectrum 65 傅立叶红外变换光谱仪上扫描,扫描范围4000~400 cm-1,扫描次数4次。
1.3.15 X 射线衍射分析 使用XD6 多晶X 射线衍射仪,扫描范围为3°~60°,扫描速度8°/min。根据公式(1)计算结晶指数(CrI,%)。
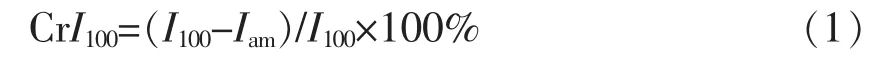
式中,I100——2θ≌19°处的最大强度;Iam——2θ≌14°处的非晶衍射强度[15]。
1.4 数据处理
用SPSS Statistics 22 进行误差分析和显著性分析。
2 结果与分析
2.1 AEW 对小龙虾壳的脱矿物质作用
在本研究的预试验中,考察了用0.1%和1%的NaCl 分别制备AEW,对虾壳粉进行处理。结果表明,用0.1%NaCl 制备的AEW 产酸量小而且缓慢,脱矿物质作用很差;而采用1%NaCl 制备的AEW 产酸量提高,速度快,有明显的脱矿物质作用。因此,在本研究中,考察了1%和2%的NaCl 制备的AEW。
由图1可知,2%NaCl 制备的AEW 处理液的pH 值从9.99 下降到1.98,然后趋于稳定;1%NaCl制备的AEW 处理液的pH 值从9.99 下降到2.37后又上升到4.76,然后趋于稳定,其原因可能与Cl-的耗尽有关。随着电解时间的延长,Cl-不断转化为Cl2,其中一部分散发于空气中,一部分溶于水中,造成低pH 值;同时,虾壳里的碳酸钙会消耗H+,使pH 值上升。在本研究中,也曾尝试进一步提高NaCl 浓度,然而,在更高浓度下制备的AEW 对电解槽的离子交换膜损害很大,处理过程中经常引起交换膜的穿孔渗漏。因此,本研究没有使用更高浓度的NaCl。
由图2可知,1%和2%NaCl 制备的AEW 处理液中的Ca2+浓度从起始的244 mg/L 分别增加到2 015 mg/L 和3 100 mg/L,并分别在330 min 和270 min 趋于稳定,表明AEW 可有效脱除虾壳粉中的CaCO3,制备AEW 的NaCl 浓度对CaCO3的脱除具有明显影响。
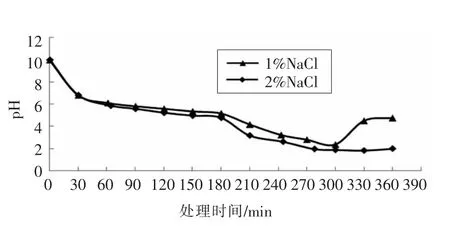
图1 AEW 处理期间pH 值的变化Fig.1 The pH value change during AEW treatment
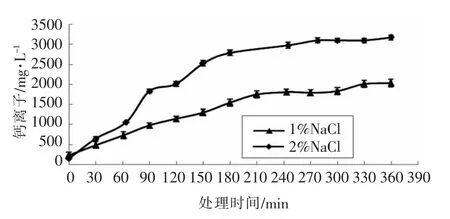
图2 AEW 处理期间Ca2+含量变化Fig.2 The change of calcium ion content during AEW treatment
由表1可知,经1%NaCl 与2%NaCl 制备的AEW 处理的虾壳粉,灰分分别从起始的53.10%下降到13.70%和0.77%,矿物质脱除率分别达到86.08%和99.59%,表明AEW 对虾壳粉具有强大的脱矿物质作用,2%NaCl 比1%NaCl 制备的AEW 更为有效,这也验证了图2的结果。
2.2 BEW 对小龙虾壳的脱蛋白质作用
由图3可知,在BEW 处理虾壳粉的过程中,1%与2%NaCl 制备的BEW 处理液的pH 值由10.07 分别上升至13.11 和13.70 左右,后者的pH值略高一些,这将更有利于蛋白质的脱除。
由图4可知,随着电解时间的延长,1%与2%NaCl 制备的BEW 处理液中的蛋白质含量增加,表明发生了脱蛋白。1%NaCl 制备的BEW 处理液中蛋白质浓度从90 min 开始增加,在300 min 达到0.31 mg/mL,然后处于平稳状态;而2%NaCl 制备的BEW 处理液中蛋白质浓度从0 min 就开始增加,至240 min 时增加速度趋于恒定,表明更高的碱性环境(图3) 更适于对虾壳粉蛋白质的脱除。
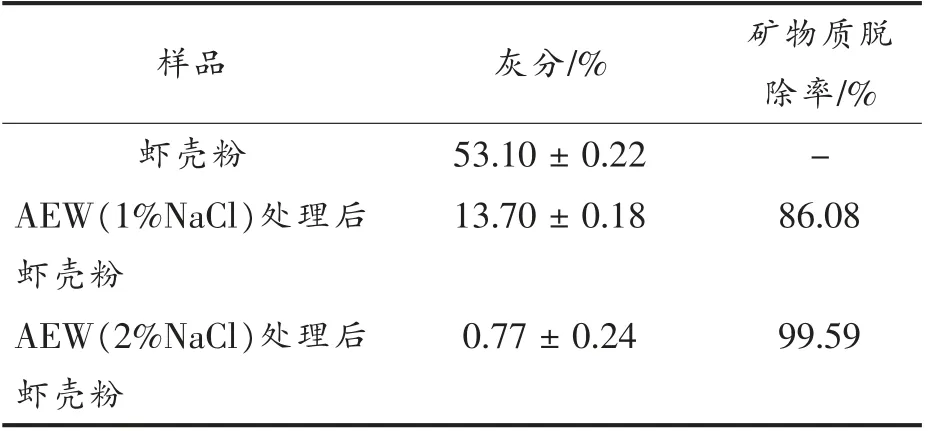
表1 AEW 处理后虾壳中的灰分及矿物质脱除率Table 1 Ash content and mineral removal rate of crawfish shell after AEW treatment
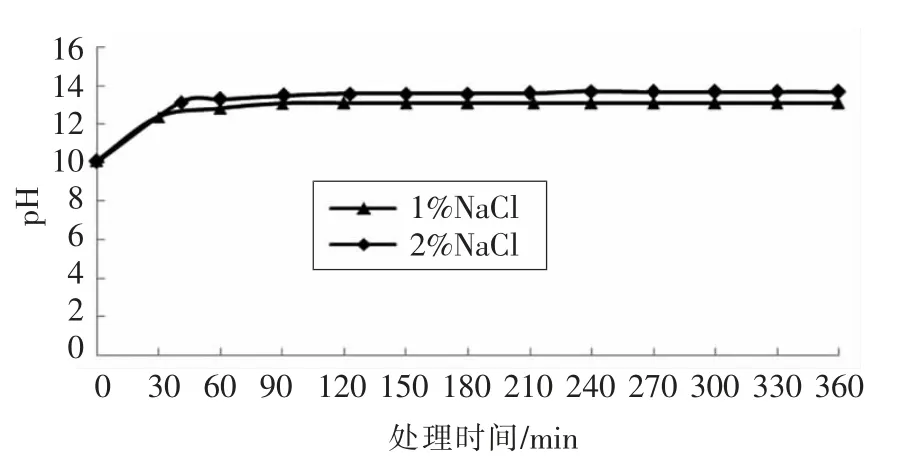
图3 BEW 处理期间pH 值的变化Fig.3 The change of pH value during BEW treatment
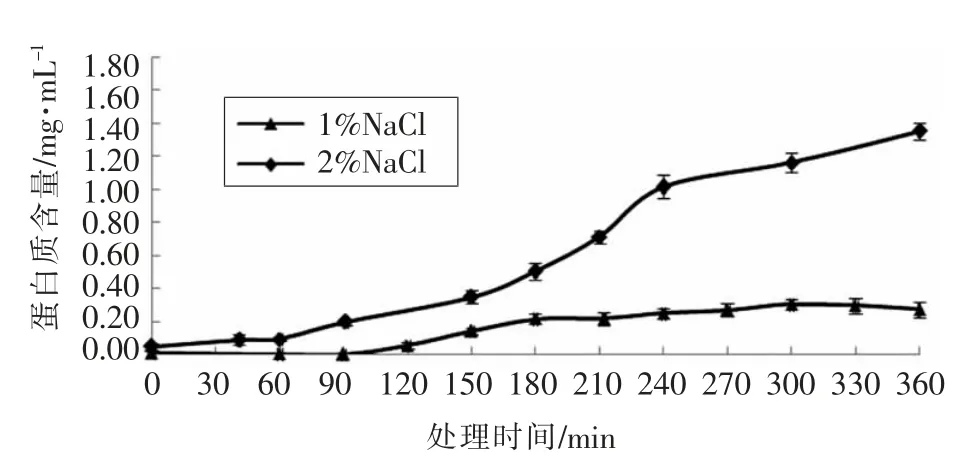
图4 BEW 处理期间蛋白质含量的变化Fig.4 The change of protein content during BEW treatment
由表2可知,1%和2%NaCl 制备的BEW 处理后的虾壳粉中蛋白质含量分别由处理前的16.97%降至7.93%和2.16%,蛋白质脱除率分别为65.53%和91.31%,表明BEW 能有效脱除虾壳中的蛋白质,后者的脱蛋白效果更好,这与图4的结果基本一致。
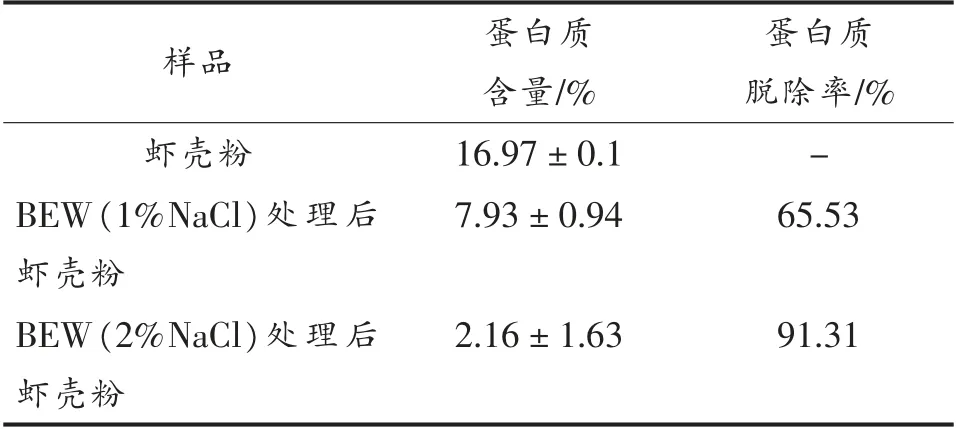
表2 BEW 处理后小龙虾壳中的蛋白质及其脱除率Table 2 Protein content and its removal rate of crawfish shell after BEW treatment
2.3 AEW 和BEW 联合处理小龙虾壳制备几丁质
由图5可知,2%NaCl 制备的BEW 处理液中蛋白质的浓度在270 min 后不再上升,达到3.06 mg/mL,这是因为经过AEW 处理后的虾壳中的蛋白质没有了矿物质的束缚,再经BEW 处理时就较容易就被脱下。
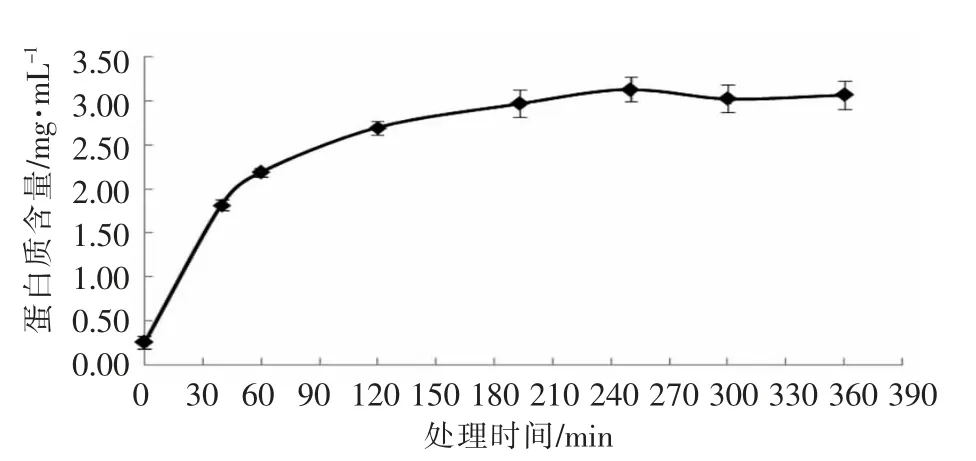
图5 联合处理工艺中BEW 处理阶段的蛋白质含量的变化Fig.5 The change of protein content during BEW treatment of combination process
由表3可知,由2%NaCl 制备的AEW 和BEW 联合处理后的虾壳粉,矿物质脱除率和蛋白质脱除率分别达到99.65%和98.31%;灰分和蛋白质含量分别为0.86%和1.31%,已经符合几丁质生产标准;与传统工艺相比,其脱除效率非常接近。因此,利用2%NaCl 制备的AEW 和BEW 联合处理虾壳粉,从中提取几丁质,可作为一种新的生产方法。其总处理时间确定为9 h,其中AEW 处理时间为270 min(图2),BEW 处理时间也为270 min(图5)。
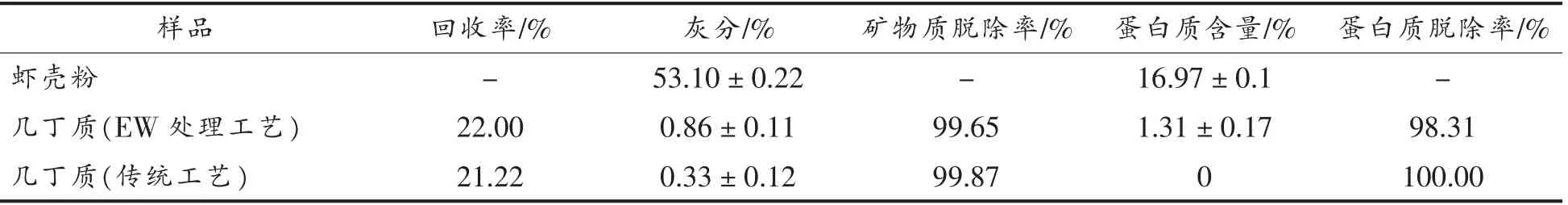
表3 电解水处理工艺和传统工艺的效率比较Table 3 Comparison of efficacy of EW treatment process and traditional process
2.4 EW 处理对小龙虾壳的脱色作用
在本研究中,观察到EW 处理除了能够脱除虾壳粉中的矿物质和蛋白质,还有很好的脱色作用。
由图6可知,AEW 处理虾壳粉后,颜色变化明显,表明脱色主要发生在AEW 处理过程中。这可能是因为制备AEW 时生成的Cl2和ClO-具有漂白作用。这将省去传统方法中的脱色过程。
从表4可知,在总色差方面,虾壳粉较大,其次是传统法处理的虾壳粉,然后是BEW 处理的虾壳粉,AEW 处理的样品较小,而2%NaCl 制备的AEW 处理后的样品色差值最小,进一步证明脱色主要发生在AEW 处理中。
2.5 几丁质的理化性质和结构表征
2.5.1 一般理化性质 脱乙酰度是区分几丁质与壳聚糖的主要参数,也是影响其物化性质的主要原因[20]。分子质量则直接决定了几丁质及其衍生物的黏度[17],对几丁质的利用至关重要。
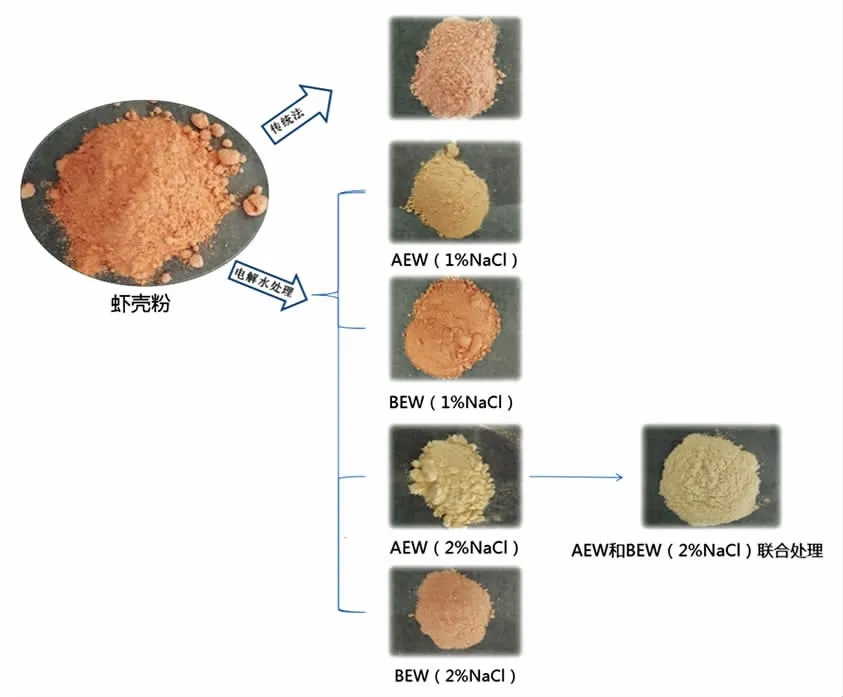
图6 小龙虾壳粉在不同处理后的颜色变化Fig.6 Changes in color of crawfish shell powder after different treatments
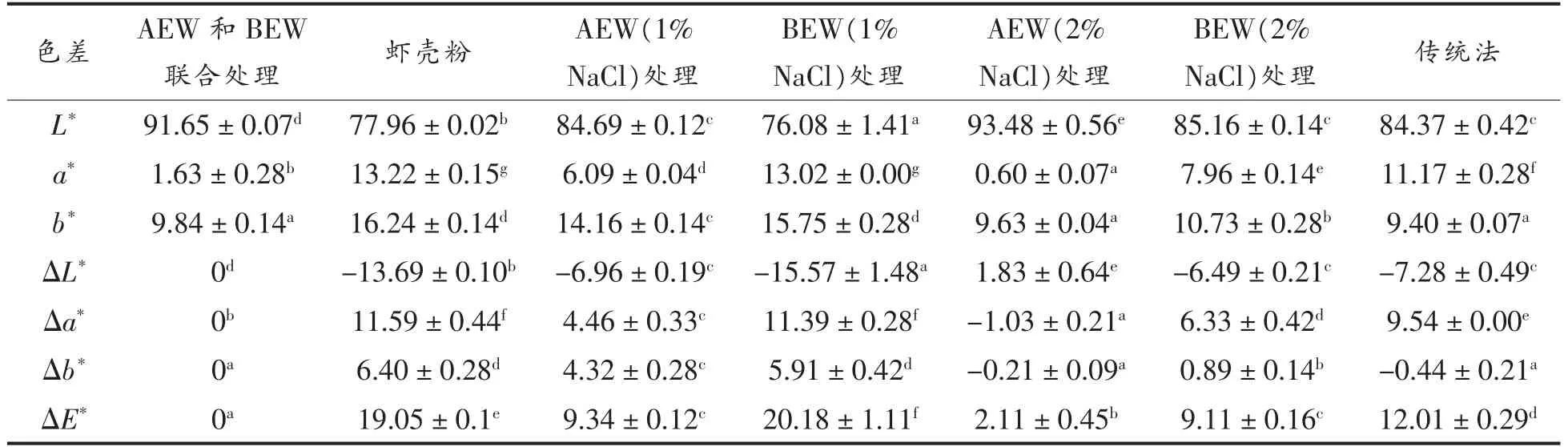
表4 不同处理后小龙虾壳粉的色差值Table 4 Chromaticity values of crayfish shell powders after different treatments
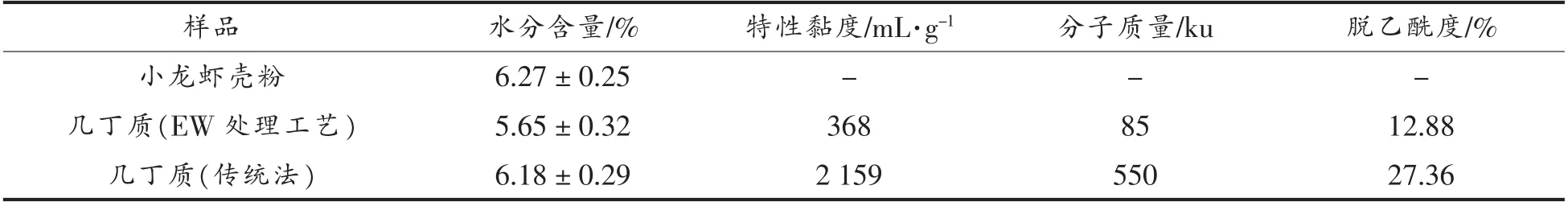
表5 EW 处理工艺和传统法制备的几丁质的一般理化性质Table 5 Physicochemical properties of chitin prepared by EW treatment process and traditional method
由表5可知,传统法和EW 处理工艺制备的几丁质的分子质量和脱乙酰度分别为550,85 ku和27.36%,12.88%,后者具有较低的分子质量和脱乙酰度。这可能是因为AEW 中持续产生H+和ClO-,造成糖苷键的酸水解和氧化降解,从而产生低分子质量的几丁质;传统法中的高浓度NaOH溶液处理是发生脱乙酰化的主要原因。因此,EW处理工艺生产的几丁质是一种新型的几丁质,有助于其应用领域的拓展。
2.5.2 热重分析和差热分析 由图7可知,3 种样品的热重分析(Thermogravimetric analysis,TGA)曲线变化趋势大致相同。不同的是,EW 法制备的几丁质(图7a) 和传统法制备的几丁质(图7b)的质量随温度的变化曲线有较明显梯度变化,质量损失均为80%~90%,而小龙虾壳粉(图8c)的变化曲线较为平缓,质量损失为35%~40%。这是因为虾壳粉经过脱矿物质和蛋白质处理后剩下的几丁质组分单一,从而表现出晶体性质;而虾壳粉成分复杂,使得热分解过程变化缓慢。3 种样品的差热分析(Differential thermal analysis,DTA)曲线的变化均随其TGA 曲线的变化呈规律性,图7a和7b 中均出现了凹点,这是短时间吸热所致,对应温度是几丁质降解温度,分别为382 ℃和389℃,表明EW 法制备的几丁质比传统法制备的几丁质更易分解,这可能与前者的较低分子质量有关。图7c 中未明显出现这样的凹点。因此,EW 法与传统法制备的几丁质有相似的结构和热稳定性。
2.5.3 扫描电镜观察 EW 法制备的几丁质纤维并排排列,略有散乱(图8a);传统法制备的几丁质呈平滑多孔结构(图8b);虾壳粉呈现层状堆积结构,虽然也有一些细孔状结构,但更像是由纤维镶嵌粘连杂质组成的实体(图8c)。无论是EW 法还是传统法,从小龙虾壳中提取的几丁质均呈网状多孔结构,这在吸附染料和金属离子等方面具有潜在应用价值[21-22]。
2.5.4 傅里叶变换-红外光谱 图9A 和9B 都出现几丁质的特征吸收峰,一系列窄吸收峰带表现出典型的结晶多糖谱带。1 660 cm-1和1 626 cm-1两个吸收峰是α-几丁质在酰胺Ⅰ谱带(C=O)的特征吸收峰,表明2 种方法提取的几丁质均为α-几丁质;1 558 cm-1处的吸收峰属于酰胺Ⅱ谱带(NH);1 313 cm-1处的吸收峰属于酰胺Ⅲ谱带(CN)。对比图9A、9B 和9C,EW 法与传统法制备的几丁质结构基本相似,而虾壳粉在3 种酰胺带上均未出现明显吸收峰,这是因为虾壳粉中的杂质影响了几丁质的特定吸收峰。
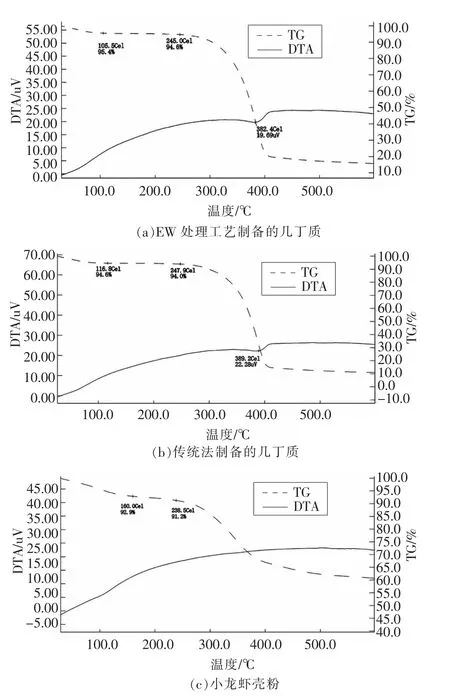
图7 热重分析和差热分析曲线Fig.7 TGA/DTA curves
2.5.5 X-射线衍射 图10A 和10B 反映出几丁质显著的结晶信号,纯度再次得到验证。图10C 有CaCO3的衍射峰,图10A 和10B 都无CaCO3的峰,同样表明2 种方法都脱除了CaCO3。EW 法和传统法制备的几丁质的结晶度指数分别为82.48%和78.82%,都远高于虾壳粉的45.78%。另外,EW 法制备的几丁质的结晶度指数略高于传统法,这与两者分子质量差异导致分子间和分子内氢键不同以及无定形态几丁质生成有关[23]。

图8 扫描电镜图(×5 000)Fig.8 SEM(×5 000)
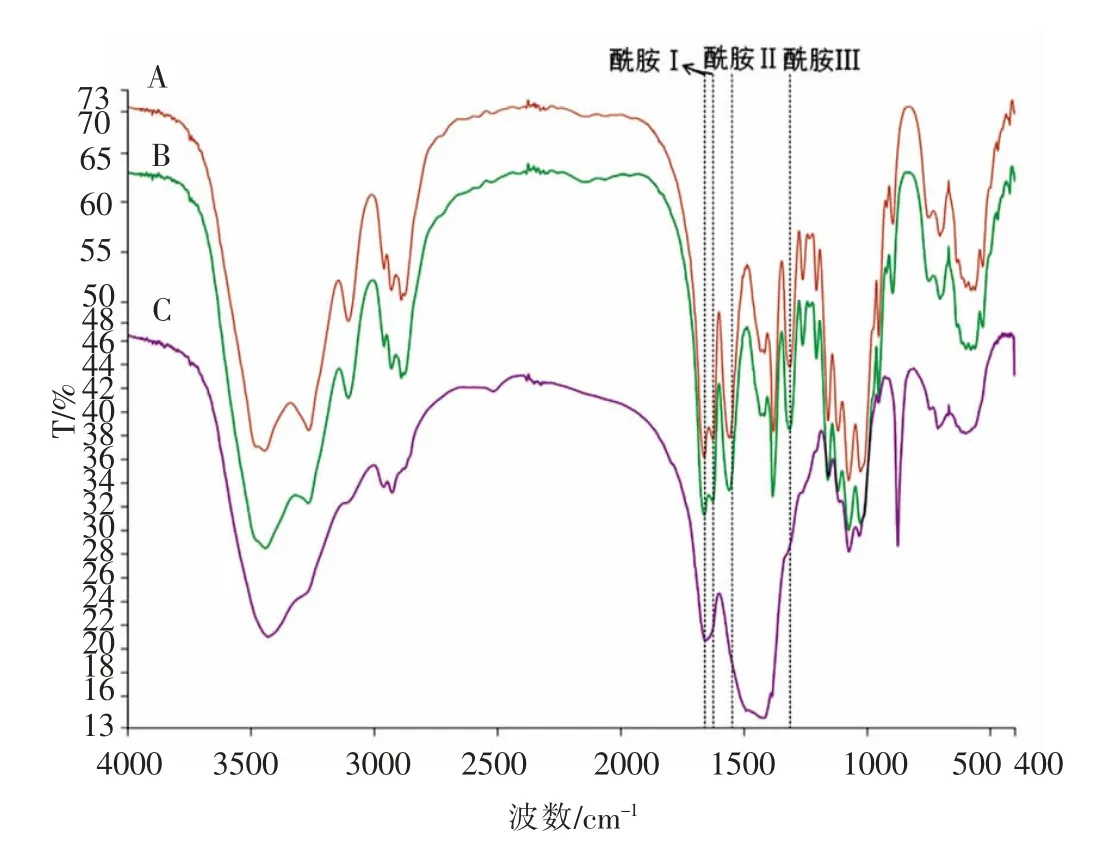
图9 傅里叶变换-红外光谱Fig.9 FT-IR spectra

图10 X-射线衍射图谱Fig.10 XRD patterns
3 结论
本文试验结果表明,AEW 能够有效脱除小龙虾壳中的矿物质,并具有良好脱色作用。BEW 能够有效脱除小龙虾壳中的蛋白质。脱除效果与用于制备EW 的NaCl 浓度有关。以2%NaCl 制备的AEW 和BEW 先后对小龙虾壳连续处理各270 min,制得符合标准要求的几丁质。与传统酸碱法相比,EW 处理工艺制备的几丁质具有较低的特性黏度、分子质量和脱乙酰度。TGA、TDA、SEM、FT-IR 和XRD 的结果表明,2 种方法制备的几丁质理化性质和结构具有很高的相似性,也直观证实了矿物质和蛋白质的脱除。因此,EW 处理工艺是一种用小龙虾壳制备几丁质的新方法。

