XELOX联合贝伐珠单克隆抗体方案转化治疗同时性结肠癌并发肝转移患者初步研究
张 华,孙宝峰,刘世祺
结肠癌是我国最常见的恶性肿瘤之一。近年来,随着中国人群饮食结构的改变,结肠癌发病呈现明显的上升趋势。肝脏是结肠癌最常见的远处转移器官,约15%~35%结肠癌患者在初次就诊时就已存在肝脏转移[1-3]。随着对结肠癌并发肝转移病理生理学和临床研究的深入,发现结肠癌肝脏转移具有特殊的生物学特征。对于无肝外转移的患者,进行原发病灶和转移病灶的根治性治疗亦能取得良好的治疗效果[4-7]。然而,超过50%结肠癌并发肝转移患者在初次就诊时就因肿瘤侵犯大血管和肝内多发转移灶等因素而不能实施根治性手术。有学者提出了转化治疗的概念,即通过化疗、放疗、免疫治疗、分子靶向治疗和介入治疗等手段治疗后使该类患者临床肿瘤降期,再次获得手术的机会,从而改善患者的远期预后。本研究采用奥沙利铂联合卡培他滨(XELOX)方案化疗联合贝伐珠单克隆抗体对初始不可切除的同时性结肠癌并发肝转移患者进行转化治疗,使部分患者获得了转化手术的机会,转化治疗的疗效满意,现报道如下。
1 对象与方法
1.1 研究对象 本研究纳入2015年6月~2017年7月我院收治的结肠癌并发肝转移患者。经肠镜检查取材病理学检查诊断为结肠腺癌,同时经CT或PET-CT检查发现存在初始不可切除的肝脏转移灶,肝肾功能基本正常,能够耐受化疗和分子靶向治疗。排除标准:1)存在肝外转移灶;2)并发其他未治愈的恶性肿瘤;3)预计生存期不超过3个月;4)存在奥沙利铂、卡培他滨、贝伐珠单克隆抗体等相关药物过敏史;5)年龄小于18周岁。研究退出标准:1)经过8个周期的转化治疗后,病情仍然进展,经研究者判断继续治疗无法获益;2)在转化治疗过程中无法耐受相关化疗药物和分子靶向治疗药物的毒副反应。本研究经本院医学伦理委员会批准通过,所有患者在入组前均充分告知治疗相关风险及可能收到的治疗获益,本组患者均同意入组并签署知情同意书。
1.2 多学科团队(MDT)评估与转化治疗 本组患者在诊断结肠癌并发初始不可切除的肝脏转移后进行主要脏器功能和影像学评估,均常规进行PET-CT检查排除肝外转移。在完成相关检查后,由一个包括外科、消化内科、肿瘤科、影像科和药学科组成的MDT进行会诊。对适宜进行转化治疗的患者,与其充分沟通,在获得同意并签署知情同意书后纳入本研究。转化治疗方案采用XELOX联合贝伐珠单克隆抗体,具体实施方法为:贝伐珠单克隆抗体15 mg.kg-1静脉滴注,D1/q3w,奥沙利铂85 mg/m-2静脉滴注,D1/q3w ,卡培他滨85 mg/m-2口服,D1/q3w。
1.3 疗效评估 本组患者均在转化治疗4个疗程后,再次进行影像学检查并由MDT评估疗效。1)完全缓解(complete response,CR):所有病灶消失,无新病灶出现,且肿瘤标志物正常;2)部分缓解(partial response,PR):肝脏转移灶最大径之和减少≥30%;3)疾病稳定( stable disease,SD):肝脏转移灶最大径之和缩小未达PR,或增大未达PD;4)疾病进展( progressive disease,PD):肝脏转移灶最大径之和至少增加≥20%,或出现新病灶。
1.4 转化手术 经过转化治疗和MDT评估,认为为可切除肿瘤,则根据患者病情采用同期或分期手术,切除原发病灶(联合D3淋巴结清扫)和肝脏转移灶。本研究转化手术治疗均由MDT中的同一外科团队完成。肝转移灶的根治性外科治疗方法包括半肝或肝叶切除术、肝段切除术、不规则局部切除。采用射频消融或微波消融治疗残留病灶。对于手术范围较大、预计不能耐受同期手术的患者,则采取分期手术,一期处理原发病灶,二期手术处理肝脏转移灶。二期手术在一期手术后4周内进行。术后,继续予以XELOX方案化疗4个疗程。在转化治疗4个疗程后再次进行影像学评估,发现仍无根治性手术机会则继续给予姑息化疗联合靶向治疗,直至患者不能耐受或死亡。
1.5 随访和不良事件记录 采用门诊和电话随访,不良事件(adverse event, AE)定义为:受试者在接受药物或治疗方案后出现任何不利的医学事件,但不一定与治疗有因果关系。本研究中随访事件起点为患者完成4个疗程转化治疗后的第一天(D1),终点定义为患者死亡或失访。随访期间主要观察总生存期(overall survival,OS),次要观察指标为AE和转化手术相关并发症。

2 结果
2.1 一般情况 本研究共纳入41例患者,男性27例,女性14例;年龄 31~72 岁,中位年龄为50岁;其中左半结肠癌3 例,右半结肠癌33例,乙状结肠癌5例;所有患者均合并初始不可切除的肝脏转移。初始肝脏转移灶不能切除的原因有:21例为肝脏转移灶较大且压迫肝中静脉或肝静脉,9例肝脏转移灶为不局限于同一半肝内的多发转移灶且不能一并手术,7例为肝脏储备功能较差,预计行转移灶手术后可能发生肝衰竭的可能性大,4例为转移灶侵犯门静脉主干而无法实施根治性手术。
2.2 转化治疗短期疗效 41例患者均接受了不少于4个疗程的转化治疗。在转化治疗4个疗程后,再次经MDT评估认为:31例为PR,6例为SD,4例为PD;其中14例在转化治疗4个疗程后获得转化治疗的手术时机,1例在转化治疗8个疗程后获得转化治疗的手术时机,其中1例拒绝手术治疗,14例接受了根治性手术,其中右半结肠癌根治术联合肝部分切除术7例,右半结肠癌根治术联合射频消融治疗肝癌5例,乙状结肠癌根治术联合射频消融治疗肝癌2例;在14例转化手术患者中,1例出现术后肝功能不全,1例出现术后胆瘘,经护肝、营养支持、持续腹腔引流等保守治疗后,康复出院。14例接受了转化手术患者1 a生存率显著高于27例未接受转化手术患者(P<0.05,表1)。
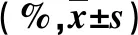
表1 两组临床资料比较
2.3 转化治疗过程中的不良事件 在41例患者中,12例(29.3%)在转化治疗过程中出现AE。部分患者发生超过一种AE,其中发生中性粒细胞减少10例,胃肠道反应4例,肝功能受损2例,外周神经炎1例。
2.4 远期随访 本组41例患者在转化治疗后随访13~26个月(中位随访时间为18个月)。经Log-rank 检验发现转化手术组1 a生存率显著高于未手术组(P=0.019,图1)。
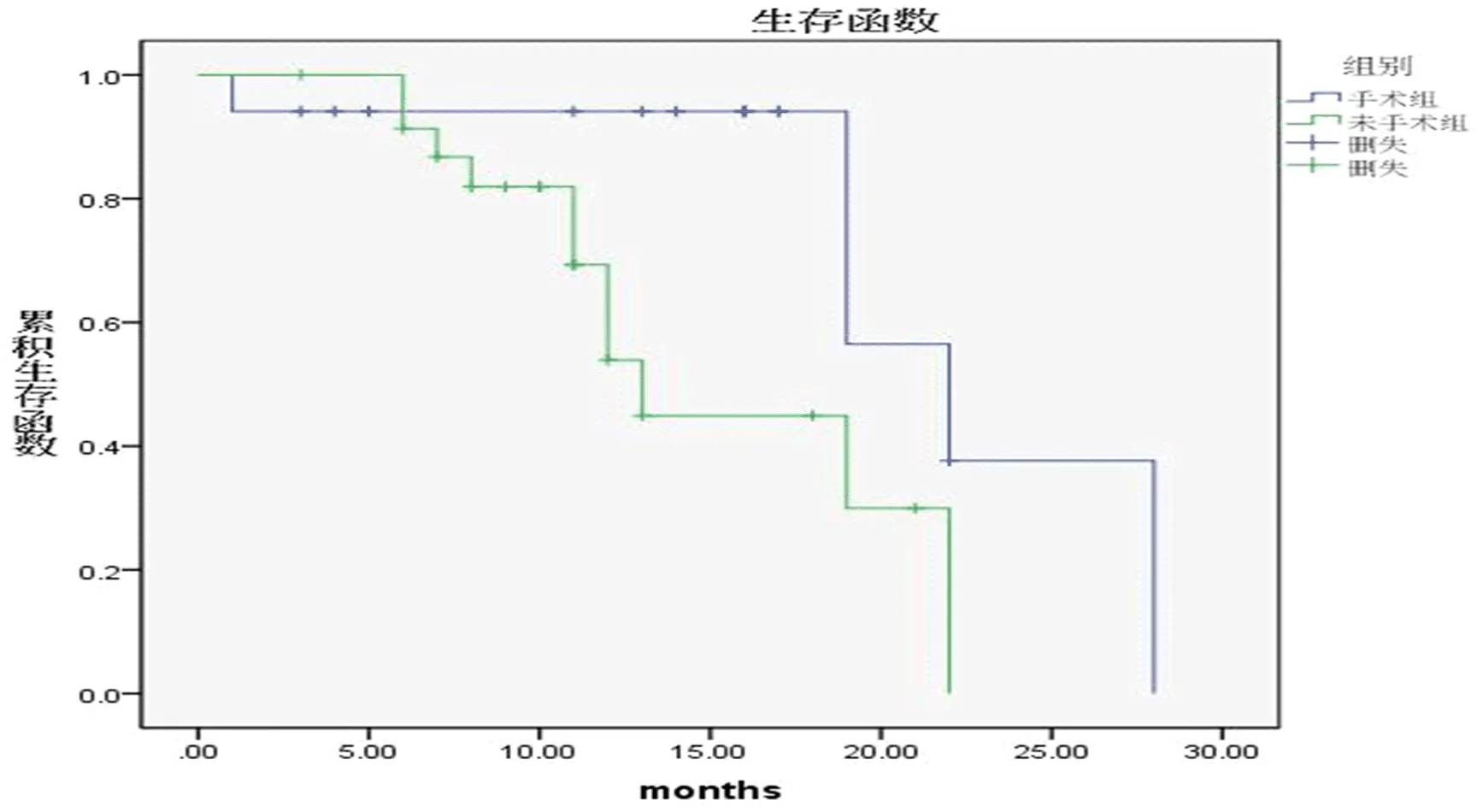
图1 41例患者远期生存情况
3 讨论
结肠癌并发肝转移主要由结肠癌细胞由门静脉回流至肝脏时发生的血运转移,结肠癌并发肝转移是结肠癌一种特殊的转移类型。现有的研究证实,对于不并发肝外转移的患者,根治性切除原发病灶及肝内转移灶往往能收到较好的治疗效果[8-10]。然而,约50%~80%结肠癌并发肝转移患者在初次就诊时肝脏内即为多发转移。当肿瘤体积较大、侵犯大血管、肝内转移灶较多、预计肝脏残余量不足时,往往难以实施原发病灶和转移灶的同期切除[11-13]。因此,对于该类结肠癌并发肝转移患者,在前期通过以全身化疗为主的综合治疗,可提高肿瘤根治性切除的比例,提高该类患者近、远期疗效,亦称之为转化治疗。
奥沙利铂联合卡培他滨(xelox方案)是目前结肠癌辅助化疗的一线方案,广泛应用于结肠癌术后的辅助治疗,近年也被尝试应用于初始不可切除结肠癌患者的转化治疗[14-16]。贝伐珠单克隆抗体(bevacizumab,商品名为Avastin)是一种单克隆抗体,可通过特异性结合血管内皮生长因子受体进而抑制肿瘤细胞的增殖[17]。近年来的研究发现,联合应用贝伐珠单克隆抗体和全身化疗可以提高初始不可切除结肠癌患者的转化治疗应答率[18, 19]。在一项前瞻性研究中,对结直肠癌并发肝转移癌患者实施了6周的FOLFIRI联合贝伐珠单克隆抗体治疗,结果患者应答率高达66.7%[20]。
本研究41例患者中有14例患者在转化治疗4个疗程后获得了手术时机,1例患者在转化治疗8个疗程后获得转化治疗手术时机,其中14例患者接受根治性转化手术,转化手术率为34.1%。在本研究41例患者中有12例患者在转化治疗过程中出现AE,总发生率为29.3%。所有的转化治疗不良反应均为I~II度,均通过保守治疗后缓解。因此,我们认为应用XELOX方案联合贝伐单克隆抗体对同时性结肠癌并发肝转移患者的转化治疗是安全有效的。
本研究41例患者在转化治疗后随访13~26个月(中位随访时间为18个月)。转化手术组与未手术组1 a总生存率分别为94.1%和69.3%,术后的生存分析发现转化手术组患者总生存期明显长于未手术组患者(P= 0.019),提示对于不可切除的患者通过转化治疗再实施转化手术,有望延长患者的生存时间。因此,对于不并发肝外转移的结肠癌并发肝转移患者,我们建议在经过MDT讨论后,对于有转化潜能的患者应积极实施相关的转化治疗,谋求转化治疗手术时机。对于转化治疗成功获得再次转化手术时机的患者,应积极实施手术治疗以获得更好的手术后预后[21,22]。
综上所述,应用贝伐珠单克隆抗体联合xelox方案治疗结肠癌并发肝转移患者是安全的,部分初始不可切除患者可以通过转化治疗再次获得手术机会,且一旦实施转化手术,有望延长患者的生存时间。

