稀有人参皂苷Rg5的高效制备方法
张仔豪,叶安琪,成乐琴
吉林化工学院化学与制药工程学院(吉林 132022)
人参为五加科多年生草本植物,在我国有数千年的药用历史,具有抗肿瘤、抗衰老、抗心律失常、抑制细胞凋亡、降糖降脂、改善学习记忆、增强性功能和免疫功能等方面的作用[1-4],广泛用于医药领域、保健食品和功能食品[5-9]。人参含有人参皂苷、人参多糖、挥发油(萜类、醇类、脂肪酸类等)和氨基酸等化学成分[10],其中人参皂苷被视为人参最重要的标志性成分[11]。人参皂苷是一种固醇类糖苷化合物,一定条件下通过糖苷键的修饰可以转化成为次级稀有人参皂苷。大量研究表明,次级人参皂苷比未经修饰的人参皂苷显示出更好的吸收和药理活性。例如人参皂苷Rg3显示出抑制肺癌细胞增值作用[12]、Rh2显示出抑制前列腺癌细胞PC3增殖作用[13]、C-K显示出抑制乳腺癌MCF-7细胞迁移和侵袭作用[14]等。
人参皂苷Rg5是比人参皂苷Rg3少1分子水的次级稀有人参皂苷,现代药理研究表明人参皂苷Rg5对抑制慢性皮炎[15]、改善肺部炎症[16]、抗乳腺癌[17]、促进血管生成和血管舒张[18]等方面具有良好的作用。从人参皂苷Rg3和Rg5的对比研究可见,人参皂苷Rg5在改善记忆[19]、抗癌作用(宫颈癌、胃癌、结肠癌、肺癌、肝癌)、益智作用[20-22]和抗氧化方面的作用[23]均优于人参皂苷Rg3,并且具有与后者类似的免疫提高作用[24]。相比人参皂苷Rg3已经成功开发成为一类抗癌药物“参一胶囊”相比,人参皂苷Rg5的研究还非常滞后,因此有必要对人参皂苷Rg5的高效制备进行深入研究。
原人参二醇组皂苷(简称PPD型人参皂苷)经不同糖苷键的结构修饰,可以得到众多结构不相同的次级人参皂苷(见图1)。Rg5是PPD型人参皂苷的众多结构修饰产物中的一种,显然,如何通过提高人参皂苷Rg5的选择性和稳定性来提高人参皂苷Rg5收率是非常值得探究的问题。目前PPD皂苷经结构修饰制备人参皂苷Rg5往往采用水溶剂和有机弱酸[25-26],不仅原料处理量少、而且生成大量的人参皂苷Rg3导致收率普遍较低。以PPD型皂苷为原料,以无机强酸盐酸为催化剂,95%乙醇为溶剂,以原料转化率和人参皂苷Rg5的收率为考察指标,研究人参皂苷Rg5的制备方法,并通过单因素和正交试验优化制备条件,探索一条高效方便地制备人参皂苷Rg5的工艺条件。
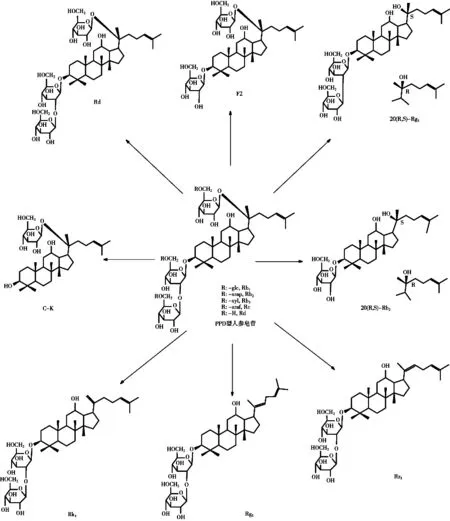
图1 PPD型人参皂苷的结构修饰次级皂苷结构式
1 试验部分
1.1 仪器与试剂
DK-98-Ⅱ型恒温水浴锅,天津市泰斯特仪器有限公司;RE-52C型旋转蒸发仪,巩义市予华仪器有限责任公司RE-52C;P2303型高效液相色谱仪,大连依利特分析仪器有限公司;反向色谱柱PinnacleⅡ C18(250 mm×4.60 mm,5 μm),Restek U.S。
P P D 皂苷,自制;人参皂苷标准品R b1(纯度≥98%)、Rb2(纯度≥98%)、Rb3(纯度≥ 98%)、Rc(纯度≥98%)、Rd(纯度≥98%)、Rg5(纯度≥98%),成都曼斯特公司;乙腈(色谱纯),瑞典欧森巴克化学公司;甲醇(色谱纯),天津市永大化学试剂有限公司;盐酸(分析纯)、乙醇(分析纯)等,天津市永大化学试剂有限公司。
1.2 试验方法
1.2.1 原人参二醇组皂苷的分离
向处理好的D101C大孔吸附树脂中加入15 mg/mL的人参根总皂苷溶液,于60 ℃静态吸附12 h。再将已吸附有人参皂苷的D101C大孔吸附树脂用蒸馏水反复洗涤,依次使用35%和80%乙醇水溶液于25 ℃下静态解吸12 h,将80%乙醇解析液用旋转蒸发仪蒸干,所得残留物用适量的70%乙醇溶解,磁力搅拌下缓慢加入丙酮,经过滤、干燥得PPD皂苷原料。
1.2.2 单因素试验优化
取5个编号为1~5的小玻璃瓶,分别加入100 μL质量浓度为20 mg/mL的PPD皂苷的95%乙醇溶液,并加入一定浓度的95%乙醇盐酸溶液,水浴加热数小时。反应结束,加入适量的饱和碳酸钠溶液至pH 6.0左右,在45 ℃下用旋转蒸发仪蒸干,残留物中加入6 mL色谱纯甲醇溶解,用0.45 μm滤膜过滤,进行HPLC分析,分别计算原料中各单体皂苷的转化率和人参皂苷Rg5的收率。
1.2.3 正交试验
在单因素试验基础上,选取反应温度(A)、反应时间(B)、酸量(C)为考察因素,根据L9(34)正交表设计试验。因素水平表如表1。
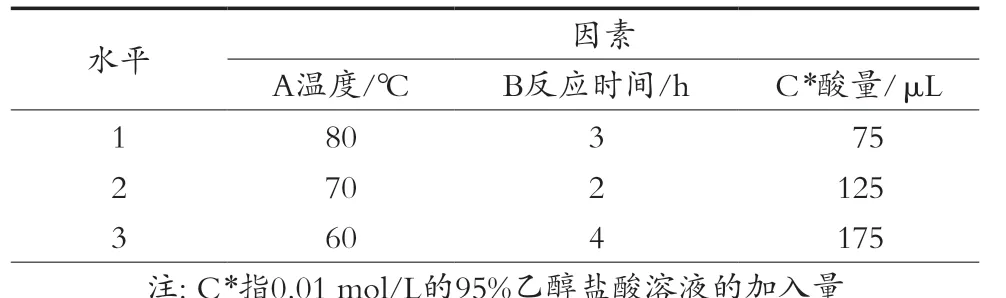
表1 因素水平表
1.2.4 HPLC分析方法
试验中采用的色谱条件为:色谱柱PinnacleⅡC18(250 mm×4.60 mm,5 μm);流速,1.0 mL/min;检测波长,203 nm;柱温,35 ℃;进样量,20 μL;流动相A,乙腈;流动相B,纯净水(超声除气处理)。梯度洗脱程序:0.00~10.00 min,A 22%;10.00~20.00 min,A 22%~27%;20.00~25.00 min,A 27%~31%;25.00~45.00 min,A 31%~38%;45.00~60.00 min,A 38%~52%;60.00~65.00 min,A 52%;65.00~75.00 min,A 52%~55%;75.00~77.00 min,A 55%~60%;77.00~77.10 min,A 60%~90%;77.10~97.00 min,A 90%;97.00~97.10 min,A 90%~22%;97.10~110.00 min,A 22%。
2 试验结果与讨论
2.1 PPD皂苷的制备
人参根总皂苷通过D101C大孔吸附树脂静态吸附与静态解吸,并结合丙酮沉淀法沉淀,分离得到PPD原料,经HPLC定量分析结果表明,PPD皂苷含量为92.33%,其中单体人参皂苷Rb1、Rc、Rb2、Rb3和Rd的含量分别为46.55%,13.43%,17.42%,4.26%和10.66%。HPLC分析见图2。
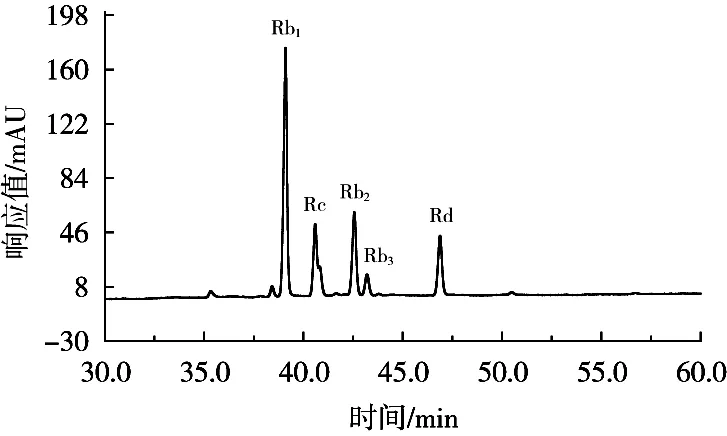
图2 原人参二醇组皂苷PPD液相色谱图
2.2 单因素试验优化人参皂苷Rg5的制备方法
2.2.1 盐酸浓度对制备人参皂苷Rg5的影响
在质量浓度为20 mg/mL的PPD型人参皂苷溶液(溶剂为95%的乙醇)中,依次加入等体积的用95%乙醇配制的0.01~0.05 mol/L浓度的盐酸溶液,在70 ℃反应3 h。反应产物的HPLC定量分析结果见图3。
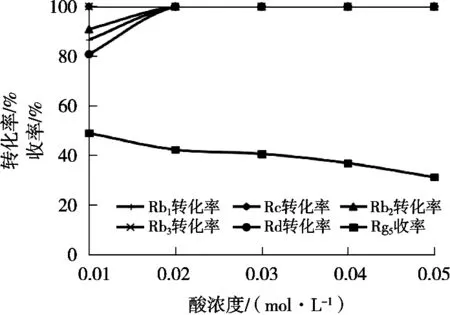
图3 酸浓度对原料的转化率和人参皂苷Rg5收率的影响
从原料中各种单体人参皂苷的转化率来看,当酸浓度为0.01 mol/L时,除了人参皂苷Rc和Rb3全部参与反应以外,人参皂苷Rb1、Rb2、Rd均有剩余。HPLC定量分析结果表明,在该反应条件下人参皂苷Rb1的转化率为86.61%,而Rb2和Rd的转化率分别为90.81%和80.71%,表明这3种皂苷还有约10~20%没有参加反应;酸浓度进一步增加到0.02 mol/L或以上时,原料中所有单体皂苷的转化率全部可以达到100%。从酸浓度对人参皂苷Rg5的收率影响来看,酸浓度为0.01 mol/L时Rg5的收率最高可达到48.91%,而随着酸浓度的进一步增加,Rg5的收率逐渐下降,说明酸浓度的提高一方面可以提高原料的转化率,另一方面还会促进人参皂苷Rg5的进一步分解。因此结合人参皂苷Rg5的收率和原料的转化率,选择0.01 mol/L的盐酸溶液进行了进一步的工艺条件优化。
2.2.2 盐酸用量对制备人参皂苷Rg5的影响
在100 μL质量浓度为20 mg/mL的PPD型人参皂苷溶液(溶剂为95%的乙醇)中,依次加入50~150 μL的用95%乙醇配制的0.01 mol/L浓度的盐酸溶液,在70 ℃反应3 h。反应产物的HPLC定量分析结果见图4。
由图4可见,酸量对反应的影响非常显著。当酸量为50 μL时,原料中所有的皂苷都有大量的剩余,但随着酸量的增加,人参皂苷Rc,Rb3,Rb2,Rd和Rb1的转化率依次达到100%,而且当酸量为150 μL时,原料中所有皂苷的转化率均可达到100%。而酸量对人参皂苷Rg5收率的影响显示,酸量在50~125 μL范围内,人参皂苷Rg5的收率随酸量的增加而升高,而进一步增加酸量时,Rg5的收率有所下降,即显示出先增后降趋势。
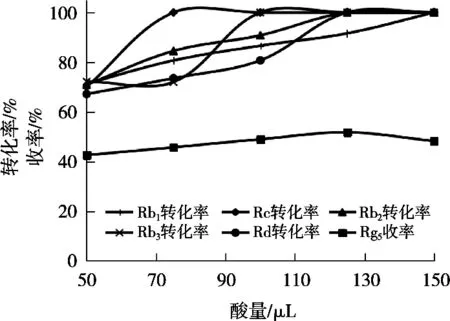
图4 酸量对原料的转化率和人参皂苷Rg5收率的影响
2.2.3 反应温度对制备人参皂苷Rg5的影响
在100 μL质量浓度为20 mg/mL的PPD型人参皂苷溶液(溶剂为95%的乙醇)中,依次加入125 μL的用95%乙醇配制的0.01 mol/L浓度的盐酸溶液,分别在60~80 ℃反应3 h。反应产物的HPLC定量分析结果见图5。
由图5可知,当反应温度为60 ℃时,只有含量极低的Rb3的转化率为100%以外,其它单体皂苷的转化率基本在65%~80%之间,但随着反应温度的升高,转化率逐渐提高,而且人参皂苷Rc,Rb2,Rd和Rb1的顺序依次达到100%的转化率,并在75 ℃反应温度下所有皂苷的转化率均达到100%。反应温度对人参皂苷Rg5的收率影响方面,刚开始,随反应温度的升高而升高,而且温度到70 ℃时收率达到最高值51.68%。如果反应温度继续升高,虽然可以加快原料的转化速度,但是因人参皂苷Rg5的分解加快,导致收率反而快速下降,因此选择70 ℃进行了进一步的条件优化。
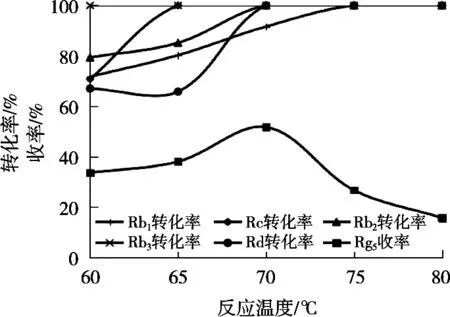
图5 反应温度对原料的转化率和人参皂苷Rg5收率的影响
2.2.4 反应时间对制备人参皂苷Rg5的影响
在100 μL质量浓度为20 mg/mL的PPD型人参皂苷溶液(溶剂为95%的乙醇)中,依次加入125 μL的用95%乙醇配制的0.01 mol/L浓度的盐酸溶液,在70 ℃反应2.5~4.5 h。反应产物的HPLC定量分析结果见图6。
图6表明,原料中人参皂苷Rc、Rb2、Rb3和Rd在反应2.5 h时就可以达到100%的转化率(Rb1为89.34%),而含量最高的人参皂苷Rb1在反应3.5 h时达到100%的转化率。反应时间对人参皂苷Rg5的影响如同反应温度,也是先增后降。在反应2.5~3 h内,Rg5的收率增加,而进一步延长反应时间时,原料转化生成Rg5的反应变少,而更多的是次级皂苷Rg5的进一步降解反应,即Rg5的分解量大于Rg5的生成量,因此Rg5的收率逐渐下降。

图6 反应时间对原料的转化率和人参皂苷Rg5收率的影响
2.3 正交试验对制备人参皂苷Rg5的优化
在单因素试验基础上,以反应温度(A)、反应时间(B)和酸量(C)为考察因素,根据L9(34)正交表进一步优化了人参皂苷Rg5的制备工艺条件。正交试验结果及分析结果见表2。
由表2的极差分析可知,影响Rg5收率的因素主次顺序为A>C>B,即反应温度的影响大于酸量、大于反应时间;最优方案为A2B1C2,即反应温度为70 ℃,反应时间为3 h,酸量为125 μL,此时对产物的HPLC定量分析(见图7)结果表明,人参皂苷Rg5的收率可以达到52.32%,远远高于通过人参皂苷制备人参皂苷Rg5的已报道的文献水平[25-26]。

表2 正交试验结果分析

图7 最优方案液相色谱谱图
3 结论与讨论
综上分析可知,以盐酸为催化剂,95%的乙醇为溶剂,制备人参皂苷Rg5的优化条件为PPD皂苷质量浓度为20 mg/mL、盐酸浓度0.01 mol/L、酸量为125 μL、反应温度为70 ℃、反应时间3 h,此时PPD皂苷中Rb1的转化率为88.84%,Rc转化率为100%,Rb2转化率为100%,Rb3转化率为100%,Rd转化率为100%,Rg5的收率为52.32%。
人参皂苷Rg5的收率主要取决于原料的转化率、人参皂苷中糖苷键的修饰位置即选择性(见图1)以及人参皂苷Rg5的分解情况。一般来说,原料转化率和对糖苷键修饰选择性越高、Rg5的分解越少,Rg5的收率就越高。研究选择无机强酸作催化剂,提高了原料的处理量和转化率;采用乙醇作溶剂,提高了人参皂苷发生消除反应生成Rg5的选择性;通过优化制备条件,减少了人参皂苷Rg5的分解,从而有效提高了人参皂苷Rg5的收率。方法与Huang等[27]所报道的酒石酸催化制备人参皂苷Rg3、Rg5相比,一方面,原料PPD皂苷质量浓度由1 mg/mL提高到了20 mg/mL,即原料处理量提高到了20倍,而酸浓度由有机酸的0.8~ 1.5 mol/L降低到了0.01 mol/L,显著提高了制备效率,而且降低了成本;另一方面,孙成鹏[25]和杨凌[26]研究相比,提高了反应选择性,使人参皂苷Rg5的收率由30.77%和14.7%提高到52%以上。由此可见,方法操作简单,收率和制备效率高,适合实验室或工业上大规模生产,这对于研究人参皂苷Rg5的制备及其药理活性具有重要参考价值。

