3-芳基-1H-5-取代吡唑酰腙类化合物的合成与生物活性初探
林立文,谢 权,朱明辉,杨 琳,李思凡,邓先清
(井冈山大学 医学部,江西 吉安 343009)
0 引言
癫痫是多种原因引起脑部神经元群阵发性异常放电所致的反复性的、突发性的脑功能短暂异常的疾病。临床表现有大发作、小发作、失神发作、局限性和混合性发作等类型。据世界卫生组织统计,现今全球大概有5000万的癫痫患者,而我国有近1000万的癫痫患者,每年新增癫痫患者约50万人[1]。现有药物可以控制70%左右患者的癫痫发作,但仅仅是抑制发作,并不能治愈,需要长期服药(半年以上甚至终身),因而带来了严重的耐药性和毒副作用的问题[2]。开发新的具有广谱、强效、毒副作用小的新型抗癫痫药物(AEDs)仍然是癫痫治疗的重要方向。
吡唑是一种含氮五元杂环化合物,它的芳香性和富电子性质使其易于与各种不同的酶和受体结合,从而赋予其广泛的生物活性。如抗炎[3],抗菌[4],及抗癫痫活性[5,6]。课题组在前期工作中设计了一系列芳基吡唑缩氨基脲类化合物并对其抗癫痫活性进行了初步探索,结果表明该类化合物大多数都具有良好的抗癫痫活性,尤其是对戊四唑诱导的癫痫小鼠,显示出较好的保护作用[7]。酰腙是一类酰肼与羰基化合物缩合而成的结构片段,其结构中含有酰胺和席夫碱,后两者在抗癫痫药物设计中被广泛应用[8-9]。为了获得新的抗癫痫活性结构,本实验基于前期研究中发现的芳基吡唑缩氨基脲类化合物,将酰腙替代上述化合物中的氨基脲片段,设计合成了一系列3-芳基-1H-5-取代吡唑酰腙类化合物并对其进行了抗癫痫活性和神经毒性的初步评价。
近年来,研究发现炎症因子能够直接影响神经元以及胶质细胞的电活动,调节中枢神经兴奋性,在颞叶内侧癫痫患者手术切除的脑组织标本上可以观察到TNF-α表达上调[10,11]。此外,癫痫发作也会引起神经炎症反应,进一步加重中枢神经系统的损伤,形成难治性癫痫的病理基础[12]。自靶向COX-2的塞来昔布被上市用于炎症治疗以来,大量吡唑类抗炎药物和抗炎活性分子被发现和报道[13,14],而酰腙结构在抗炎药物中同样被广泛报道[15]。因此,基于我们的目标化合物中也含有吡唑和酰腙结构,以及炎症与癫痫发病的相关性,我们也对目标化合物的抗炎活性进行了评价。
1 实验部分
1.1 仪器与试剂
核磁共振分析采用BURKER AV-300 型核磁共振仪(Bruker,Switzerland),四甲基硅(TMS)为内标,溶剂使用CDCl3或DMSO-d6;高分辨质谱采用UltrafleXtreme MALDI-TOF/TOF 质谱仪(Bruker Daltonik GmbH,Leipzig,Germany)测定;熔点采用毛细管法测定(温度计未经校正)。实验所用试剂包括苯乙酮(99%,阿拉丁试剂公司)、苯甲醛(99%,阿拉丁试剂公司)、草酸二乙酯(99%,天津博迪化工股份有限公司)、水合肼(80%,上海化学试剂厂),和其他常规溶剂(分析纯,麦克林试剂有限公司)。
1.2 化合物合成
1.2.1 化合物3a-3f的合成。以化合物3a为例[16]:在 100 mL 圆底烧瓶中加入40 mL新配制的乙醇钠溶液(1 mol/L),冰浴下滴加苯乙酮(4.8 g,40 mmol)和草酸二乙酯(5.85 g,40 mmol),滴毕,于30 ℃反应2.5 h(TLC跟踪,展开剂V石油醚/V乙酸乙酯=6:1)。反应液凝固成固体时,反应完成,得中间体2a。 中间体2a不经过后处理,直接滴加冰醋酸0.6 mL,调节至pH 6-7(固体全部溶解),室温搅拌0.5 h后再滴加80%水合肼3.0 mL(48 mmol),90 ℃下加热回流2 h(TLC跟踪,展开剂V石油醚/V乙酸乙酯=6:1)。冷却,浓缩一半溶剂,残留物在搅拌下倒入到冰水中,析出固体,抽滤,乙醇重结晶得到黄色固体3a。采用相同方法,用其他取代苯乙酮为原料制备得到化合物3b-3f。
1.2.2 化合物4b-4f的合成。以化合物4a为例:在 100 mL 圆底烧瓶中依次加入化合物3a(2.16 g,10 mmol) 和80% 水合肼(10 ml,160 mmol)。混合物于120 ℃下回流反应2 h(TLC跟踪,展开剂V石油醚/V乙酸乙酯=1∶2)。冷却至室温,抽滤,乙醇重结晶得白色固体4a。采用相同方法制备得到化合物4b-4f。
1.2.3 化合物5a-5o的合成。以化合物5a为例[17]:在 100 mL 圆底烧瓶中依次加入20 ml无水乙醇,化合物4a(4.04 g, 20 mmol)和苯甲醛(2.12 g,20 mmol)。加毕,于90 ℃下回流反应2 h(TLC跟踪,展开剂 V石油醚∶V乙酸乙酯=1∶4)。冷却至室温,抽滤,乙醇重结晶得白色固体5a。相同方法下,化合物4a和其他取代的苯甲醛及呋喃甲醛反应得到化合物5b-5h,化合物4a分别与苯乙酮及4-氯苯乙酮反应得到化合物5i和5j;化合物4b-4f分别与苯甲醛反应得到化合物5k-5o。化合物5a-5o的理化数据如下:
N'-苯亚甲基-3-苯基-1H-吡唑-5-甲酰肼(5a):熔点 236-239 ℃,产率 75 %.1H-NMR(DMSO-d6,300 MHz):δ7.25(s,1H,Pz-H),7.40-7.86(m,10H,Ph-H),8.56(s,1H,N=CH),11.73(s,1H,CONH),13.82(s,1H,Pz-NH).13C-NMR(DMSO-d6,75MHz):δ158.64,155.88,148.07,147.21,144.21,135.00,130.44,129.52,129.31,129.07,127.53,125.88,103.97.ESI-HRMS calcd for C17H15N4O+([M+H]+):291.1240; found:291.1238.
N'-(2-氟苯亚甲基)-3-苯基-1H-吡唑-5-甲酰肼(5b):熔点 218-220 ℃,产率 70 %.1H-NMR(DMSO-d6,400 MHz):δ7.25(s,1H,Pz-H),7.28-7.99(m,9H,Ph-H),8.81(s,1H,N=CH),11.94(s,1H,CONH),13.83(s,1H,Pz-NH).13C-NMR(DMSO-d6,100MHz):δ161.26(d,1Jc-f=247.7 Hz),158.71,147.09,144.23,140.74,132.28(d,3Jc-f=7.5 Hz),129.55,129.34,129.08,126.85,125.92,125.60,125.39,116.46(d,2Jc-f=20.3 Hz),104.05.ESI-HRMS calcd for C17H14FN4O+([M+H]+):309.1146; found:309.1143.
N'-(3-氟苯亚甲基)-3-苯基-1H-吡唑-5-甲酰肼(5c):熔点 216-218 ℃,产率 73 %.1H-NMR(DMSO-d6,400 MHz):δ7.24(s,1H,Pz-H),7.28-7.86(m,9H,Ph-H),8.55(s,1H,N=CH),11.84(s,1H,CONH),13.82(s,1H,Pz-NH).13C-NMR(DMSO-d6,100MHz):δ162.90(d,1Jc-f=242.4 Hz),158.71,147.09,146.62,144.23,137.56,131.42(d,3Jc-f=8.3 Hz),129.56,129.10,125.91,125.63,123.95,117.15(d,2Jc-f=21.4 Hz),113.29(d,3Jc-f=21.2 Hz),104.06.C17H14FN4O+([M+H]+):309.1146; found:309.1144.
N'-(4-氟苯亚甲基)-3-苯基-1H-吡唑-5-甲酰肼(5d):熔点 230-233 ℃,产率 75 %.1H-NMR(DMSO-d6,400 MHz):δ7.26(s,1H,Pz-H),7.29-7.86(m,9H,Ph-H),8.53(s,1H,N=CH),11.75(s,1H,CONH),13.82(s,1H,Pz-NH).13C-NMR(DMSO-d6,100MHz):δ163.56(d,1Jc-f=247.2 Hz),158.66,147.36,146.99,144.17,131.52,129.70(d,3Jc-f=7.6 Hz),129.50,129.00,125.83,116.38(d,3Jc-f=21.8 Hz),103.85,103.18.ESI-HRMS calcd for C17H14FN4O+([M+H]+):309.1146; found:309.1151.
N'-(4-氯苯亚甲基)-3-苯基-1H-吡唑-5-甲酰肼(5e):熔点 278-280 ℃,产率 79 %.1H-NMR(DMSO-d6,400 MHz):δ7.24(s,1H,Pz-H),7.50-7.75(m,7H,Ph-H),7.85(d,2H,J=7.2 Hz,Ph-H),8.55(s,1H,N=CH),11.80(s,1H,CONH),13.82(s,1H,Pz-NH).13C-NMR(DMSO-d6,100MHz):δ158.67,147.16,146.68,144.22,134.82,133.96,129.53,129.41,129.29,129.11,125.92,125.66,104.02.ESI-HRMS calcd for C17H14ClN4O+([M+H]+):325.0851; found:325.0846.
N'-(4-溴苯亚甲基)-3-苯基-1H-吡唑-5-甲酰肼(5f):熔点 290-292 ℃,产率 79 %1H-NMR(DMSO-d6,400 MHz):δ7.25(s,1H,Pz-H),7.40-7.73(m,7H,Ph-H),7.85(d,2H,J=7.4 Hz,Ph-H),8.53(s,1H,N=CH),11.81(s,1H,CONH),13.82(s,1H,Pz-NH).13C-NMR(DMSO-d6,100MHz):δ158.64,147.14,146.77,144.24,134.29,132.32,129.51,129.38,129.07,129.03,125.89,123.60,104.00.ESI-HRMS calcd for C17H14BrN4O+([M+H]+):369.0346; found:369.0344.
N'-(4-甲基苯亚甲基)-3-苯基-1H-吡唑-5-甲酰肼(5g):熔点 295-297 ℃,产率 91 %.1H-NMR(DMSO-d6,400 MHz):δ2.35(s,3H,Ph-CH3),7.24(s,1H,Pz-H),7.28(d,2H,J=7.4 Hz,Ph-H),7.39-7.63(m,5H,Ph-H),7.85(d,2H,J=7.4 Hz,Ph-H),8.51(s,1H,N=CH),11.66(s,1H,CONH),13.80(s,1H,Pz-NH).13C-NMR(DMSO-d6,100MHz):δ158.53,148.10,147.30,144.16,140.22,132.25,129.92,129.50,129.03,127.52,125.87,125.67,103.91,21.50.ESI-HRMS calcd for C18H17N4O+([M+H]+):305.1397; found:305.1399.
N'-(呋喃-2-基亚甲基)-3-苯基-1H-吡唑-5-甲酰肼(5h):熔点 223-225 ℃,产率 67 %.1H-NMR(DMSO-d6,400 MHz):δ6.53-6.55(m,1H,Fur-H),6.91(d,1H,J=3.6 Hz,Fur-H),7.23(s,1H,Pz-H),7.40-7.86(m,6H,Ph-H,Fur-H),8.44(s,1H,N=CH),11.75(s,1H,CONH),13.80(s,1H,Pz-NH).13C-NMR(DMSO-d6,100MHz):δ158.55,150.17,147.18,145.48,144.19,137.77,129.56,129.09,129.05,125.92,113.44,112.66,104.02.ESI-HRMS calcd for C15H13N4O2+([M+H]+):281.1033; found:281.1030.
3-苯基-N'-(1-苯亚乙基)-1H-吡唑-5-甲酰肼(5i):熔点 266-268 ℃,产率 70 %.1H-NMR(DMSO-d6,400 MHz):δ2.39(s,3H,CH3),7.27(s,1H,Pz-H),7.38-7.86(m,10H,Ph-H),10.40(s,1H,CONH),13.86(s,1H,Pz-NH).13C-NMR(DMSO-d6,100MHz):δ158.38,147.20,144.31,138.48,133.66,129.92,129.53,129.06,128.87,126.88,125.86,125.73,103.74,14.06.ESI-HRMS calcd for C18H17N4O+([M+H]+):305.1397; found:305.1396.
N'-(1-(4-氯苯基) 亚乙基)-3-苯基-1H-吡唑-5-甲酰肼(5j):熔点 251-253 ℃,产率 81 %.1H-NMR(DMSO-d6,400 MHz):δ2.38(s,3H,CH3),7.29(s,1H,Pz-H),7.39-7.90(m,9H,Ph-H),10.43(s,1H,CONH),13.85(s,1H,Pz-NH).13C-NMR(DMSO-d6,100MHz):δ158.39,152.29,147.19,144.44,137.30,134.62,129.49,129.07,128.91,128.64,126.12,125.82,103.80,14.07.ESI-HRMS calcd for C18H16ClN4O+([M+H]+):339.1007; found:339.1010.
N'-苯亚乙基-3-(4-氟苯基)-1H-吡唑-5-甲酰肼(5k):熔点 268-270 ℃,产率 47 %.1H-NMR(DMSO-d6,400 MHz):δ7.24(s,1H,Pz-H),7.30-7.91(m,9H,Ph-H),8.56(s,1H,N=CH),11.73(s,1H,CONH),13.80(s,1H,Pz-NH).13C-NMR(DMSO-d6,100MHz):δ162.58(d,1Jc-f=243.3 Hz),158.60,148.06,147.27,143.30,135.00,130.40,129.31,128.15(d,3Jc-f=7.8 Hz),127.50,125.75(d,4Jc-f=3.0 Hz),116.52(d,2Jc-f=21.4 Hz),104.06.ESI-HRMS calcd for C17H14FN4O+([M+H]+):309.1146; found:309.1144.
N'-苯亚乙基-3-(4-氯苯基)-1H-吡唑-5-甲酰肼(5l):熔点 267-269 ℃,产率 67 %1H-NMR(DMSO-d6,400 MHz):δ7.32(s,1H,Pz-H),7.43-7.49(m,3H,Ph-H),7.56(d,2H,J=8.0 Hz,Ph-H),7.72-7.74(m,2H,Ph-H),7.87(d,2H,J=8.0 Hz,Ph-H),8.53(s,1H,N=CH),11.78(s,1H,CONH),13.89(s,1H,Pz-NH).13C-NMR(DMSO-d6,100MHz):δ158.52,156.47,148.35,148.26,134.86,133.49,132.44,130.53,129.53,129.31,127.57,107.01,104.27.C17H14ClN4O+([M+H]+):325.0851; found:325.0846.
N'-苯亚乙基-3-(4-溴苯基)-1H-吡唑-5-甲酰肼(5m):熔点 258-260 ℃,产率 76 %.1H-NMR(DMSO-d6,400 MHz):δ7.32(s,1H,Pz-H),7.46-7.87(m,9H,Ph-H),8.52(s,1H,N=CH),11.79(s,1H,CONH),13.90(s,1H,Pz-NH).13C-NMR(DMSO-d6,100MHz):δ157.47,148.27,137.40,134.85,132.44,131.89,130.54,129.32,129.04,127.79,127.57,123.90,104.28.ESI-HRMS calcd for C17H14BrN4O+([M+H]+):369.0346; found:369.0345.
N'-苯亚乙基-3-(4-甲苯基)-1H-吡唑-5-甲酰肼(5n):熔点 248-249 ℃,产率 71 %.1H-NMR(DMSO-d6,400 MHz):δ2.35(s,3H,Ph-CH3),7.21(s,1H,Pz-H),7.30(d,2H,J=8.0 Hz,Ph-H),7.44-7.74(m,7H,Ph-H),8.53(s,1H,N=CH),11.73(s,1H,CONH),13.73(s,1H,Pz-NH).13C-NMR(DMSO-d6,100MHz):δ158.48,148.10,148.07,138.39,138.30,134.93,130.46,130.04,129.46,129.31,127.53,125.76,103.36,21.30.ESI-HRMS calcd for C18H17N4O+([M+H]+):305.1397; found:305.1394.
N'-苯亚乙基-3-(4-甲氧基苯基)-1H-吡唑-5-甲酰肼(5o):熔点 239-241 ℃,产率 73 %.1H-NMR(DMSO-d6,400 MHz):δ3.81(s,3H,Ph-OCH3),7.05(d,2H,J=8.4 Hz,Ph-H),7.12(s,1H,Pz-H),7.44-7.73(m,5H,Ph-H),7.77(d,2H,J=8.4 Hz,Ph-H),8.53(s,1H,N=CH),11.68(s,1H,CONH),13.64(s,1H,Pz-NH).13C-NMR(DMSO-d6,100MHz):δ161.05,159.95,147.98,135.01,131.10,130.41,129.31,128.47,127.51,127.35,114.91,114.23,103.01,55.72.ESI-HRMS calcd for C18H17N4O2+([M+H]+):321.1346; found:321.1340.
1.3 化合物抗惊厥活性及神经毒性评价
按照美国NIH的抗癫痫药物开发方案,采用最大电惊厥模型和皮下戊四唑模型评价目标化合物的抗癫痫活性,旋转棒法评价目标化合物的神经毒性[18,19]。实验动物采用昆明种小鼠(湖南斯莱克景达实验动物有限公司提供,许可证号:SCXK(湘) 2016-0003),体重18-22 g,雌雄均可。实验前3 d饲养于23-27 ℃、相对湿度45%-65% 的实验室中,实验时间以外可以自由采食和饮水。测试化合物均用DMSO溶解,以0.05 mL/20 g容积腹腔注射,评价化合物在30、100、300 mg/kg三个剂量下的抗癫痫活性和神经毒性。活性观测时间为给药后0.5 h。
最大电休克发作实验(MES):使用110 V,60 Hz的交流电,小鼠耳电极通电0.3 s,出现后肢强直的视为惊厥。正式实验前一天预筛小鼠,出现惊厥的小鼠用于正式实验。腹腔给药0.5 h后对小鼠进行电刺激,观察药物的抗电诱导惊厥活性,不出现后肢强直,视为化合物在该剂量下有效。
皮下戊四唑实验(sc-PTZ):小鼠给药0.5 h后皮下给予85 mg/kg的戊四唑(该剂量可以使97%以上的小鼠产生连续5 s的阵挛性惊厥),小鼠单独放置在鼠笼中观察30 min,以没有出现连续5 s以上的阵挛性惊厥为有效,认为该化合物可以对抗由戊四唑诱导的惊厥。
神经毒性实验:神经毒性实验采用旋转棒法,腹腔给药 0.5 h后将小鼠置于直径 1 英寸、转速为 6 r/min的木棒上,在连续三次的测试中小鼠均不能在木棒保持1 min而掉下视为有神经毒性,反之则无神经毒性。
1.4 细胞培养与ELISA实验(TNF-α浓度测定)
小鼠 RAW264.7 巨噬细胞(北京协和细胞库,北京)用添加了10% FBS(BI生物有限公司, 批号:1552680)、100 U/mL青霉素和100 μg/mL链霉素混合液(索莱宝科技有限公司,批号:20160909)的RPMI 1640 完全高糖培养基(杭州四季青生物工程有限公司,批号:170504)于37 ℃ 5% CO2恒温培养箱中培养。每 24 h更换培养基,细胞生长至 90% 传代。待细胞传至 3 代,状态稳定后,用于实验。将细胞接种到24孔板中,培养24 h后,药物组加入20 μg/mL的化合物或阳性药地塞米松(DXMS)预处理4 h,然后加入LPS(Sigma Chemical Co.,St.Louis,MO,USA)(1 μg/ml)培养24 h。收集培养液,1000 rpm离心10 min后取上清液,使用小鼠TNF-α ELISA试剂盒(San diego,CA,USA)检测TNF-α浓度水平[20]。
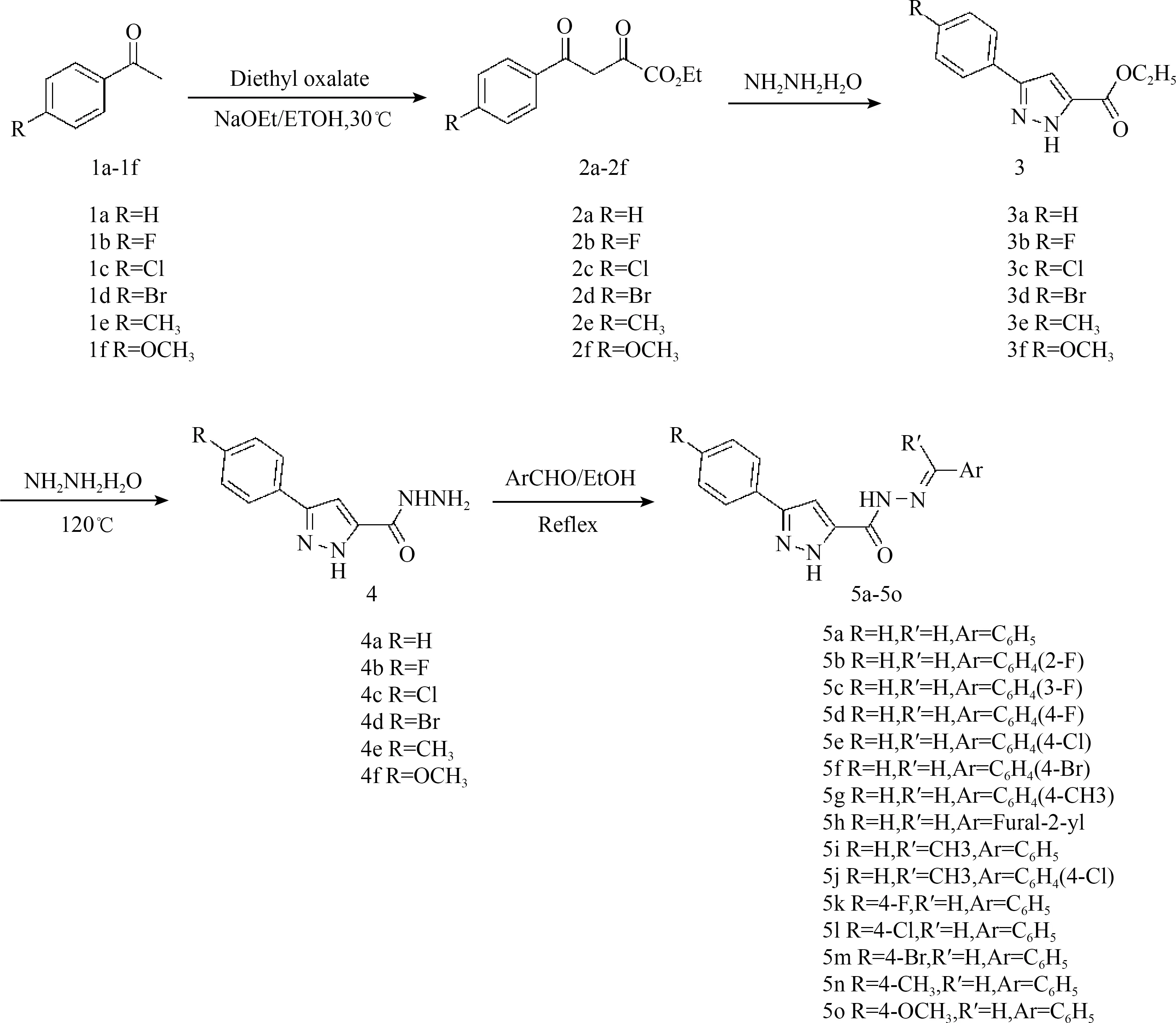
图1 目标化合物5a-5o的合成路线
2 结果与讨论
2.1合成部分
本实验以以苯乙酮(或取代苯乙酮)为起始原料,先后与草酸二乙酯发生缩合反应,与水合肼进行环化、缩合,最后与芳香醛(酮)缩合得到目标化合物5a-5o(见图1)。化合物2的制备过程中,使用新制备的乙醇钠并保证反应体系无水比较关键,反应体系中水的存在会降低乙醇钠的活性从而阻止反应的进行。该反应结束后反应体系会凝固成固体,这是因为化合物2在碱性条件下以盐的形式存在,在乙醇中溶解度变低导致的。加入醋酸调整pH到7可以使其转换成分子形态,溶解度增加,从而溶解到乙醇溶液中。再加入水合肼在90 ℃下回流,可以得到环合后的吡唑甲酰乙酯3。化合物3直接与水合肼发生肼解得到酰肼化合物4。该反应中我们尝试了不同溶剂,发现反应至少需要110 ℃的反应温度,才能确保反应进行。如甲苯作溶剂同样得到预计产物,但比较发现水合肼直接充当溶剂,可以加快反应速度,并且易于后处理。最后,在醋酸催化下,化合物4与各种羰基化合物缩合得到目标化合物5a-5o。
化合物5a-5o的结构通过核磁共振氢谱、碳谱和质谱得到了确证。结构解析以化合物5a为例:在1H-NMR 中,δ7.25处的单峰为吡唑环上C-H的吸收峰,δ7.40-7.86范围的多重峰为两个苯环上10个质子的吸收峰,δ8.56处的单峰为席夫碱上的质子信号,δ11.73和13.82位置的两个单峰则分别为酰胺氮和吡唑氮上的两个质子的吸收峰。13C NMR谱也准确的给出了该化合物结构的各种信息,恰好是13种不同化学环境的碳。高分辨质谱分析中,化合物5a([M+H]+)理论分子质量为291.1240,实测值为291.1238,结合氢谱和碳谱可以确证其分子结构。

表1 化合物5a-5o的抗癫痫活性及神经毒性
2.2 药理实验部分
2.2.1 抗癫痫活性。本实验采用MES和sc-PTZ模型来评价目标化合物5a-5o的抗癫痫活性。虽然这两个模型在对难治性癫痫的药物筛选方面有所欠缺,但目前依然是抗癫痫药物筛选的首要选择,被美国NIH列举为主要的抗癫痫药物筛选模型[21]。其中MES模型用于筛选能对抗全身强直阵挛性发作的候选药[22],而sc-PTZ 模型则用来筛选失神发作的候选药物[23]。本实验对目标化合物进行了30,100 和300 mg/kg 三个剂量的活性和神经毒性的初步评价,其结果见表1。化合物5d和5e在100 mg/kg剂量下表现出抗电刺激所致惊厥活性,化合物5g,5k和5o在300 mg/kg剂量下表现出对抗电刺激所致惊厥活性。其他化合物在最大剂量300 mg/kg 下未见抗电惊厥活性。
scPTZ实验中,绝大多数化合物在100 mg/kg剂量下表现出抗戊四唑所致惊厥活性,说明该系列化合物对戊四唑所致癫痫更为敏感,其中化合物5f在30 mg/kg剂量下仍表现出抗癫痫活性。旋转棒实验模型中,所有化合物在300 mg/kg剂量下均未表现出神经毒性。
2.2.2 抗炎活性。脂多糖(LPS),革兰氏阴性细菌细胞壁外壁的组成成分,被认为是通过刺激炎性细胞因子(如肿瘤坏死因子(TNF-α)的释放而启动炎症过程的主要危险因素[24]。LPS诱导TNF-α 释放模型被认为是一种有效的用于筛选抗炎活性的体内外模型[25,26]。在本研究中,我们通过建立LPS诱导RAW 264.7细胞炎症模型来筛选化合物5a-5o的体外抗炎活性。如图2所示,被LPS刺激的RAW 264.7细胞TNF-α浓度显著升高,阳性药DXMS可以显著抑制LPS诱导的TNF-α浓度的升高,在20 μg/mL剂量下抑制率达到62%。化合物中5a-5f,5h和5k-5m在20 μg/mL剂量下可以显著抑制LPS诱导的TNF-α浓度的升高。简单的构效关系分析可以发现,氟取代化合物5b,5k和呋喃化合物5h具有最好的抗炎活性,抑制率分别为64%,61%和55%,与阳性药地塞米松相当。而给电子基团甲基或者甲氧基取代的5g,5n和5o则抗炎活性偏弱,对LPS诱导TNF-α表达的抑制率分别为23%,21%和11%,统计时与模型组相比没有显著性差异。不同氟取代化合物中,邻位氟取代的化合物抑制活性更好(5b>5c,5d),卤素取代的化合物中,氟取代化合物抑制活性优于氯溴取代化合物(5d>5e,5f;5k>5l,5m)。
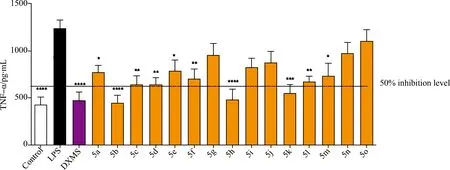
图2 化合物5a-5o(20 μg/mL)在LPS诱导RAW 264.7细胞炎症模型中的抗炎活性(与LPS组比较,*p<0.05,**p<0.01,***p<0.001,****p<0.0001,未标注组p>0.05,没有显著性差异,统计分析采用ANOVA followed by Dunnett’s test)
3 结论
本文合成了一系列3-芳基-1H-5-取代吡唑酰腙类化合物,其结构均经过光谱学方法确证。体内抗癫痫活性评价表明:该系列化合物大部分表现出不同程度的抗癫痫活性,尤其是对sc-PTZ 模型更为有效,且化合物未见明显神经毒性。此外,该系列化合物在LPS诱导的RAW 264.7细胞炎症模型中可以显著抑制TNF-α的释放,说明其具有良好的抗炎作用。该研究为研究失神发作类癫痫和炎症的治疗药物提供了一定基础。

