MR 动态增强联合DWI 对于卵巢肿瘤诊断的应用价值
王雨充 姚铭
卵巢癌是临床常见的女性生殖系统肿瘤类型之一,位于女性恶性肿瘤的第二位,也是妇科肿瘤手术的首要指征[1]。由于卵巢癌早期无特异性表现,且五年生存率较低,故早期诊断及准确治疗关系到患者预后质量。超声是评价盆腔疾病的一线方法,操作方便、敏感性高,无放射性损伤,但受医师操作经验、肥胖、肠管气体等因素影响,特异性极低[2];CT 检查速度快,可用于全身检查,但组织分辨率低、放射性损伤等,应用较为局限[3]。磁共振检查软组织分辨率高、可多平面成像等优势,应用广泛,随着磁共振成像技术的进展,MR 动态增强(DCE-MRI)、扩散加权成像(DWI)技术已逐渐用于各类型肿瘤,能够反映肿瘤的微血管、细胞水平等病理生理学特征[4-5]。因此,本研究拟回顾卵巢肿瘤患者两种联合技术的影像学诊断结果,报道如下。
1 资料与方法
1.1 临床资料
回顾一汽总医院在2018 年1 月—2020 年6 月收取的60 例卵巢肿瘤患者的临床资料,所有患者均经手术病理检查,年龄30 ~68 岁,平均(45.81±6.18)岁。纳入标准:(1)纳入受试者无激素水平异常;(2)患者因下腹疼痛、体质量下降、腹胀不适等症状就诊;(3)患者及其家属对研究知情,签署同意书;(4)临床资料完整。排除标准:(1)精神障碍性疾病、意识不清者;(2)伴其他原发恶性肿瘤、免疫性疾病以及脏器器质性疾病等;(3)妊娠期或哺乳期女性;(4)过敏体质或无法实施MR 检查者。
1.2 方法
GE SIGNA Creator1.5 T 超导型磁共振扫描仪。受试者检查前禁食、禁水6 h,训练其准确呼吸。仰卧位,头先进,线圈位于中下腹部,子宫作为中心。MR 平扫:矢状位脂肪抑制FSE-T2WI 参数:TR3 600 ms,TE90 ms。横轴位FSE-T1WI 参数:TR 669 ms,TE 11 ms;横轴位FSE-T2WI 参数:TR 3 217 ms,TE 85 ms。冠状位参数:TR 2 848 ms,TE 85 ms。扫描层厚4 mm,FOV 220×100 mm。DWI 扫描:采用单次激发平面回波成像技术(SE-EPI),TR/TE 为5 000/77 ms,FOV 为306×306 mm 层厚为4 mm,扩散敏感系数(b)值为1 000 s/mm2;扫描后获得的图像传至工作站,获取表观扩散系数(ADC)图像,标记感兴趣区(ROI),记录ADC 值。每例患者测量3 次ADC 值,取最低值作为结果。DCEMRI 扫描:使用高压注射器注射对比剂钆喷酸葡胺15 mL,速率:4 mL/s,注射结束后以氯化钠溶液20 mL 冲洗,进行增强扫描:15、30、45 s 作为横断位扫描;60 s 进行冠状位、90 s 进行矢状位扫描。扫描参数:TR 为0.8 ms,TE 为1.77 ms,FOV 为260×260 mm,层厚为3.5 mm。图像采集共35 期,并传入至工作站,运动校正、图像匹配,标记ROI,确定时间-信号曲线(time-intensity curve,TIC),记录其类型:渐进上升型、平台型及流出型曲线。由医院影像科高年资、经验丰富、专业性强的两名影像科医师观察图像并进行阅片。
1.3 观察指标
(1)以手术病理检查作为金标准,统计DCE-MRI、DWI 技术对卵巢肿瘤恶性检出率,计算其敏感性、特异性、阳性及阴性预测值;(2)比较良恶性肿瘤(实性、囊性)ADC 值;(3)比较良恶性肿瘤TIC 类型。
1.4 统计学方法
2 结果
2.1 分析DCE-MRI、DWI 技术诊断效能
60 例卵巢肿瘤患者经手术病理检查良性肿瘤42 例,其中成熟性囊性畸胎瘤18 例,浆液性囊腺瘤5 例,黏液性囊性瘤5 例,子宫内膜异位囊肿8 例,纤维卵泡膜细胞瘤6 例;恶性肿瘤18 例,其中浆液性囊腺癌6 例,子宫内膜样腺癌4 例,黏液性囊腺癌3例,透明细胞癌3 例,移行细胞癌2 例。良性组T1WI 图像呈等或稍低信号,T2WI 呈高信号;DWI 图像为等信号,DCE-MRI 大部分呈渐进性强化特点。恶性肿瘤T1WI 为等-低信号,T2WI 为混杂信号;DWI 图像为混杂高信号;DCE-MRI 部分病灶呈快进快出型强化,部分病灶呈快进慢出型强化。DCE-MRI 联合DWI技术对恶性病变检出率94.44%(17/18),DWI 恶性病变检出率55.56%(10/18),DCE-MRI 恶性病变检出率61.11%(11/18),DCE-MRI 联合DWI 技术分别与DWI 和DCE-MRI 比较差异均具有统计学意义(P<0.05);联合技术诊断阳性预测值为88.24%、阴性预测值93.02%、敏感性83.33%、特异性95.24%均高于DCEMRI(63.64%、77.55%、38.89%、90.48%)、DWI 技 术(60.0%、76.0%、33.33%、90.48%),其中阴性预测值、敏感性差异具有统计学意义(P<0.05);见表1 ~表3,图1 ~3。
良 性 组: 实 性ADC 值(1 524.38±184.36)mm2/s, 囊性ADC 值(2 804.35±196.89)mm2/s; 恶 性 组: 实 性ADC 值(842.13±95.65)mm2/s,囊性ADC 值(1 984.53±135.78)mm2/s;差异具有统计学意义(t=14.819,16.066;P<0.05)。
2.2 比较良恶性肿瘤TIC 类型
良性组:渐进上升型曲线占90.48%(38/42),平台型曲线占9.52%(4/42);恶性组:平台型曲线占16.67%(3/18);流出型曲线占83.33%(15/18);差异具有统计学意义(χ2=28.403,P<0.05)。
3 讨论
卵巢肿瘤病理分型复杂,根据组织学分类可将其分为上皮-间质肿瘤、性索-间质肿瘤、生殖细胞类肿瘤等;根据肿瘤性质又分为良性、交界性及恶性。因此,探索一种敏感性、特异性高的诊断技术,早期鉴别肿瘤性质起到积极意义。由于超声、CT 检查有各自不容忽视的缺陷,自MR 技术的广泛应用,使肿瘤性质检出准确性增加。常规MRI 检查组织分辨率高,卵巢肿瘤定性效果较好,但无法评价肿瘤组织功能特征。DCE-MRI 是将快速成像作为特点,跟踪观察注射对比剂通过血管的过程,利用药代动力学评估肿瘤血管结构以及功能特性,并得到肿瘤病灶ROI 区的功能数据[6]。DWI 技术则通过对组织内水分子运动观察,分辨组织含水量生理学变化,同样可为病变鉴别提供参考[7]。
本组研究中,联合技术诊断阳性预测值为88.24%、阴性预测值93.02%、敏感性83.33%、特异性95.24%。均高于DCE-MRI(63.64%、77.55%、38.89%、90.48%)、DWI 技术(60.0%、76.0%、33.33%、90.48%),其中阴性预测值、敏感性差异具有统计学意义(P<0.05)。结果提示,DCE-MRI 联合DWI 技术对卵巢肿瘤性质鉴别效能高于单一技术。DCE-MRI 技术能评估肿瘤组织的血流动力学状态;DWI 技术无需使用对比剂,操作性强、耗时短,能提高卵巢肿瘤检出率。与石良瑜等[8]研究相一致,表明DCE-MRI+DWI 诊断的灵敏度高于单独检测方法(P<0.05)。

表1 DCE-MRI 技术诊断效能(例)

表2 DWI 技术诊断效能(例)

表3 联合技术诊断效能(例)
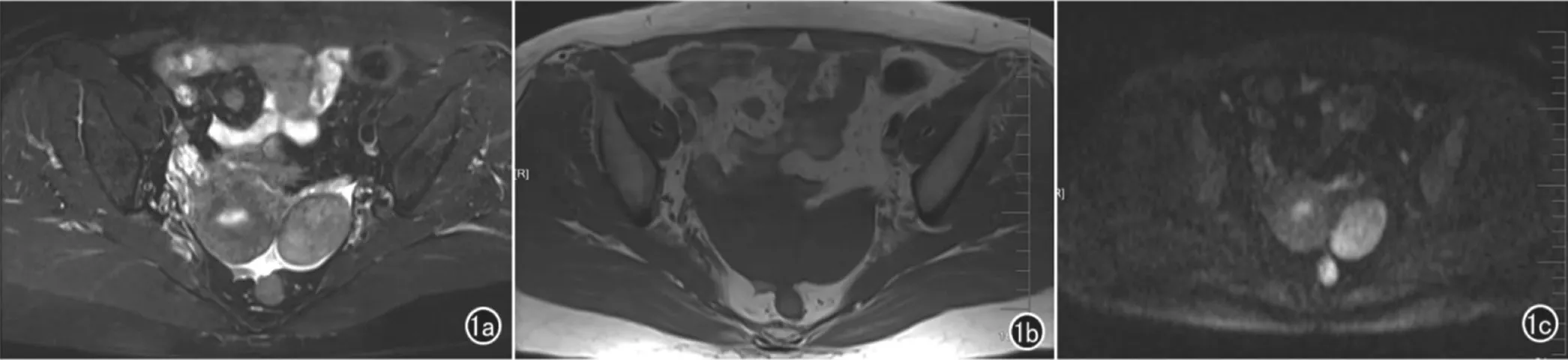
图1 卵泡膜细胞瘤 MRI 检查图像
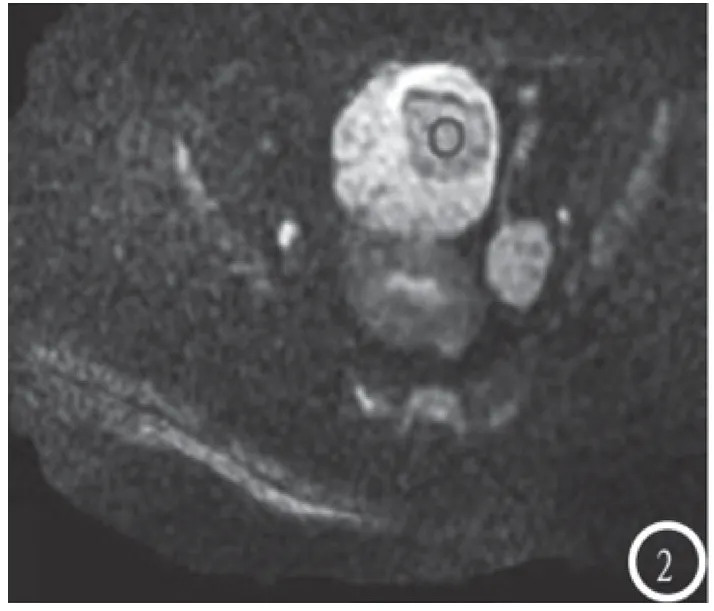
图2 DWI 检测图像为肿瘤实性部位

图3 测出实性区域ADC 值
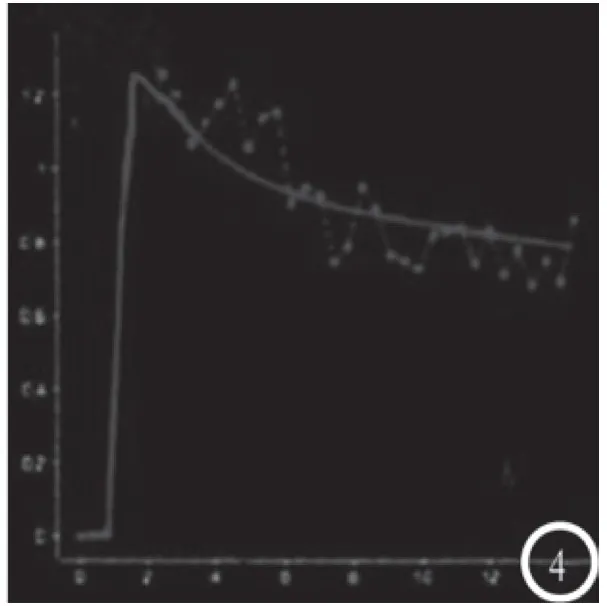
图4 TCI 为Ⅲ型曲线
本组研究中,良性组(实性、囊性)ADC 值高于恶性组,TIC 类型良性组以渐进上升型曲线为主,恶性组以流出型曲线为主(P<0.05)。DWI 技术检查是利用ADC 值反映组织水分子扩散运动情况,明确肿瘤组织的微观结构。因卵巢恶性肿瘤细胞增殖、分化迅速、细胞密度增加,使组织内水分子弥散运动受限,故会降低病灶组织内ADC 值,DWI 图像显示高信号[9-10]。而通过DCE-MRI 技术也可帮助评估肿瘤性质,在注射对比剂后,可连续、准确描述肿瘤组织的血流变化特点,一般渐进上升型曲线无强化峰值,病灶组织多提示良性可能;平台型曲线提示肿瘤组织为交界性可能;流出型曲线以恶性病变为主。此外若病灶区强化峰值超过子宫肌层,提示病变属于恶性[11-12]。
综上所述,MR 动态增强联合扩散加权成像技术能高效鉴别卵巢肿瘤良恶性,为患者的治疗方案的选择提供更多依据,有较为广阔的应用前景。

