短链二烷基多硫的热裂解
吴明清, 吴晓颖, 潘罗奇, 曾光乐, 李 涛
(1.中国石化 石油化工科学研究院,北京 100083;2.中国石化 大连石油化工研究院,辽宁 大连 116045;3.中国石化 巴陵分公司,湖南 岳阳 414014)
轻烃中常存在烃基二硫或多硫化合物,例如:稳定汽油、含硫醇凝析油中的硫醇常以C2~C4烷基硫醇为主,经Merox工艺处理后,硫醇转化为烷基二硫或多硫[1];炼油厂精制液化石油气(LPG)中残余硫化物常以C1~C2烷基二硫或三硫为主[2-3]。在进一步的热处理过程中这些硫化物的形态会继续发生变化,大部分转移到下游产品中[4],从而影响产品质量或下游加工。烃基二硫或多硫的热稳定性一般低于多数烃类化合物[5],硫化物的热裂解会产生腐蚀性更强的小分子硫化物[6-7]。
对烃基二硫及多硫热裂解的研究发现,烃基多硫的热裂解反应主要受温度影响。Faragher等[8]研究了C2及C2以上的有机多硫(包括二烷基二硫(Dialkyl disulfide, DADS))在496 ℃下的热裂解产物,其中二烷基二硫的热裂解产物主要是H2S、S0、RSH、RSR和噻吩(THP)。Coope[9]和Patrick[10]研究了二甲基二硫(Dimethyl disulfide, DMDS)及二乙基二硫(Diethyl disulfide,DEDS)在气相状态下的热裂解行为,提出了一级反应的自由基机理。Moldavskii等[11]研究了在MoS作催化剂及临氢条件下,溶解在煤油中的二乙基二硫的热裂解行为,发现在230 ℃时反应2 h就有超过75%的二硫醚发生热裂解反应,产物以H2S和乙硫醇为主。Clark等[12]研究了烃基多硫的热稳定性,发现二甲基多硫(CH3SnCH3,n≥3)在50 ℃时就可发生热裂解反应,产生甲硫醇及硫化氢等小分子硫化物,且n值越大,热裂解反应越易进行;而二芳基多硫(Diaryl disulfide, DArPS)的热稳定要高得多,其他条件相同时在200 ℃也未发现其明显热裂解反应。徐海升等[13]用热重及差示扫描量热方法研究了二乙基多硫(CH3CH2SnCH2CH3,n为2~4)在常压下的热分解行为,发现在50 ℃开始就有热裂解反应发生,至235 ℃时可裂解完全。
二烷基多硫(Dialkyl polysulfide, DAPS)用途广泛,如作为润滑剂[14]、催化剂预硫化剂、硫磺捕集剂[12]等;热稳定性是其在制备及使用中的重要指标。
在含硫轻烃的热加工过程中,烃基多硫的热裂解会改变下游物料中硫的形态分布,影响最终产品或中间产品的质量。因此,有必要详细研究溶解在轻烃中的短链二烷基多硫的热裂解行为,为石油加工过程中涉及烃基多硫热裂解的工艺控制提供依据。笔者以轻烃中比较常见的几种短链二烷基二硫及三硫(为方便起见,以下将二烷基二硫及二硫以上的硫化物统称为二烷基多硫)为代表,为避免实验温度下芳烃及烯烃与硫醇可能的反应[15],选择化学稳定性及热稳定性较好的饱和烃(90~120 ℃石油醚)作为溶剂,并以高纯氮为平衡气,探讨反应温度及压力对轻烃溶剂中二烷基多硫的热裂解产物分布的影响。
1 实验部分
1.1 原料和试剂
H2S(100 mg/m3,N2平衡气)、甲硫醇(50 mg/m3,N2平衡气),北京华元标准气体公司产品;石油醚(90~120 ℃)、乙硫醇、二甲基硫醚(Dimethyl sulfide, DMS)、叔丁硫醇、二甲基二硫、二甲基三硫(Dimethyl trisulfide, DMTS)、二乙基二硫、乙醇胺、硫磺(升华硫),均为分析纯,Adamas试剂有限公司产品;二乙基三硫(Diethyl trisulfide, DETS),工业纯,石家庄利达化学品有限公司产品;二叔丁基二硫(di-tert-Butyl disulfide, DTBDS),由实验室合成[16]。
1.2 二烷基多硫热裂解实验方法
将二甲基二硫、二乙基二硫、二叔丁基二硫、二甲基三硫、二乙基三硫分别溶解在90~120 ℃石油醚中,配成硫质量分数为0.10%的溶液,作为不同二烷基多硫热裂解反应的测试溶液。将高压反应釜(KTFD05-20,有效体积500 mL,哈氏合金材质,烟台科立化工设备有限公司产品)作为二烷基多硫热裂解实验的反应器。
分别将不同二烷基多硫的裂解测试液置于反应釜内,以高纯N2置换釜内空气,预置一定量的N2(预置初压),进行以下3类实验:
(1)将反应釜直接快速升温至80 ℃,然后以升温速率0.5 ℃/min缓慢升温,温度每升高5 ℃时,测定反应釜内压力,采样测定气相中硫化物,直至气相中可检测到硫醇生成。
(2)将反应釜直接加热至80~320 ℃,稳定 120 min 后快速冷却至常温,对气相及液相分别采样,以GC-SCD方法测定硫化物形态及其含量。
(3)常温下对不同测试液继续补充N2至0.1~1.0 MPa,然后升温至200~290 ℃,再补充适量N2至压力为0.9~6.0 MPa,稳定120 min后,快速冷却至常温,分别从气相及液相采样,以 GC-SCD 方法测定硫化物形态及其含量。
1.3 硫化物测试
采用美国Agilent公司的GC 7890A气相色谱仪分析硫化物。PONA色谱柱起始温度35 ℃,以升温速率2 ℃/min升温至180 ℃后,保持5 min;高纯N2为载气,流速0.60 mL/min;进样器温度280 ℃,液体进样体积2.0 μL,气体进样体积1.0 mL,分流比50/1;净化H2流速40 mL/min,净化空气流速6 mL/min;燃烧器温度800 ℃;SCD设置在355 nm波长处检测SO2信号。
以标准硫化物标定大部分相关硫化物的色谱保留时间。采用文献[12]中方法制备二烷基四硫,并在相同色谱条件下进行GC-MS分析,得到相应二甲基四硫(Dimethyl tetrasulfide, DMTTS)及二乙基四硫(Diethyl tetrasulfide, DETTS)的保留时间。
以二甲基二硫为标样、石油醚为溶剂,配制硫质量分数为0.002%~0.02%及0.02%~0.10%的两个浓度系列的硫标准溶液,分别测定各标样的GC-SCD色谱图,根据SCD色谱峰响应与硫原子物质的量成正比[17]的原理,制备定硫标准曲线。热裂解实验中,对反应釜内的液相样品与气相样品分别采样,以 GC-SCD 测定硫形态及其含量(硫质量分数),根据反应釜内液相和气相体积,将液相和气相中相同硫形态的硫含量合并,折算到液相物料中,并计算各种形态硫在总硫中所占比率(本研究中定义为硫形态比率,ΦS)。由于未反应的二烷基多硫也存在于反应后物料中,为便于比较,也将其作为反应产物列出以进行对比。第i种硫化物在总硫中的硫形态比率(ΦS,%)的计算如式(1):
(1)
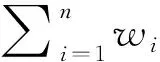
反应前测试溶液中二烷基多硫的ΦS为100%,其他硫化物的硫形态比率为0;反应后部分二烷基多硫裂解为其他形态的硫化物,反应前与反应后物料中二烷基多硫的ΦS之差即为二烷基多硫热裂解率(ξ,%),如式(2)计算。
(2)
2 结果与讨论
2.1 短链二烷基多硫的热裂解起始温度
在对二甲基二硫及二乙基二硫进行热裂解实验时发现,加热过程中最先可检测到的热裂解产物是硫醇,与文献[8]中结论相一致。因此将可检测到硫醇的最低温度视为热裂解反应发生的起始温度。
测定了不同预置起始压力下,二甲基二硫、二乙基二硫、二叔丁基二硫、二甲基三硫、二乙基三硫开始热裂解产生硫醇的温度及其对应的压力(关联压力),结果如表1所示。由表1可知:(1)热裂解反应发生时的对应压力都高于 25 ℃ 时的预置起始压力,说明升温过程中伴随着压力的升高;(2)随着样品预置起始压力的增大,二烷基多硫热裂解反应发生的起始温度及其关联压力也随之升高。
升温过程中压力的上升可能归因于3方面:(1)二烷基多硫发生热裂解,产生小分子硫化物;(2)升温引起釜内N2压力的升高;(3)石油醚的气化及热裂解。二烷基多硫是微量组分,即使全部汽化或裂解也不至对压力的增加产生明显影响;N2作为平衡气,升温时压力会增加,依据气态方程,当温度由25 ℃升至120~340 ℃时,计算反应器内N2压可升至其初压的1.3~2.1倍;石油醚全部为饱和烃,明显裂解的温度一般在400 ℃以上[18],实验中对裂解产物的GC-FID(烃类色谱峰)分析也显示烃类组成几乎不变,说明石油醚分子裂解很少;所用石油醚的实际馏程为92~111 ℃(IBP~98%馏出温度),表1中二烷基多硫的热裂解起始温度都高于石油醚的初馏点温度,因此石油醚将产生大于 0.10 MPa 的蒸汽压。以沸点位于石油醚馏程范围的正庚烷(常压沸点 98.5 ℃)为模型化合物,采用Antoine方程计算正庚烷的蒸汽压随温度的变化,如表2所示。根据表2可推测升温过程中作为溶剂的石油醚会产生与正庚烷相近的蒸汽压,如对于 表1 中预置起始压力为0.10 MPa的二乙基二硫实验液,当温度由25 ℃升至200 ℃时,测定反应器内的压力由0.10 MPa升至1.10 MPa;计算200 ℃时N2压力为0.17 MPa,按表2估计石油醚蒸汽压约为0.95 MPa,二者之和约为1.12 MPa,与实测压力1.10 MPa相近。可见在升温过程中反应釜内压力的增加主要源于石油醚蒸汽压力及预置N2压力的升高,因此升温过程中产生了对应的关联压力的升高。

表1 二烷基多硫在不同预置起始压力(pp)下的热裂解起始温度(Tip) 及对应Tip的关联压力(pt)Table 1 Initial pyrolysis temperature (Tip) and related pressure (pt) for dialkyl polysulfides at different preset pressures (pp)

表2 正庚烷蒸汽压(pv)随温度(T)的变化Table 2 Heptane vapor pressure (pv) changewith temperature (T)
表1显示,对同一烷基多硫醚,增加预置起始压力可使热裂解反应的起始温度提高。表1中不同烷基多硫的热裂解起始温度及其关联压力都不相同,难以比较不同烷基多硫在相同压力下的热裂解起始温度,为此将表1中不同二烷基多硫的热裂解起始温度Tip与其对应的关联压力pt采用多项式进行关联,得到如式(3)~(7)所示的不同二烷基多硫的热裂解起始温度Tip与其关联压力pt的关系。
DMDS:
Tip=4.6851pt2-6.6042pt+231.50
(3)
DEDS:
Tip=-20.504pt2+91.007pt+125.17
(4)
DMTS:
Tip=-17.056pt2+53.095pt+125.17
(5)
DTBDS:
Tip=-14.416pt2+46.026pt+111.49
(6)
DETS:
Tip=12.255pt2+9.1799pt+117.77
(7)
以式(3)~(7)分别估算二甲基二硫、二乙基二硫、二叔丁基二硫、二甲基三硫、二乙基三硫在一定压力(pt)下发生热裂解反应的起始温度Tip,结果如表3所示。
由表3可见:(1)在相同压力下, 5种二烷基多硫的热裂解起始温度从高到低的顺序为:DMDS、DEDS、DMTS、DTBDS、DETS,基本反映出5种二烷基多硫的热稳定性顺序;(2)相同烷基时,硫原子数越多,二烷基多硫的热裂解起始温度越低;(3)硫原子数相同时,烷基较大或支链较多的二烷基多硫的热裂解起始温度较低;(4)压力越高,二烷基多硫的热裂解起始温度越高。
此外,对二甲基二硫、二乙基二硫、二乙基三硫热裂解的物料平衡测定结果显示,实验过程中总硫及物料的质量回收率均在95%以上。

表3 基于表1计算的二烷基多硫在不同关联压力(pt)下的热裂解起始温度(Tip,cal) Table 3 Calculated initial pyrolysis temperature (Tip,cal) of dialkyl polysulfides underdifferent related pressures (pt) based on Table 1
2.2 反应温度对二烷基多硫热裂解产物硫分布的影响
2.2.1 反应温度对二烷基二硫热裂解产物硫分布的影响
采用GC-SCD方法分别测定石油醚中的二甲基二硫、二乙基二硫、二叔丁基二硫在不同反应温度下热裂解产物的硫化物分布,计算产物中各形态硫在总硫中所占的硫形态比率(ΦS)。所得二烷基二硫在不同反应温度及其关联压力下的热裂解产物分布如图1所示。
由图1可知,二烷基二硫的热裂解反应具有以下特点:(1)裂解产物均以相应的烷基硫醇为主,H2S为辅,二甲基二硫裂解产物中还含有少量DMS;(2)随着反应温度升高,二烷基二硫的ΦS逐渐降低,裂解产物的ΦS逐渐升高;(3)升温过程中每种烷基二硫的ΦS均存在一“拐点温度”,低于此温度时,其ΦS随温度升高而缓慢降低,高于此温度后,其ΦS快速降低。裂解产物中硫醇的ΦS急剧增大,但H2S及二甲基硫醚的ΦS增速较低。二甲基二硫、二乙基二硫、二叔丁基二硫的ΦS变化“拐点温度”分别为270 ℃、250 ℃和140 ℃,高于此温度点后二烷基二硫的ΦS随温度升高近于直线降低。(4)从图1(a)和(b)可看出,反应温度从210 ℃(关联压力1.2 MPa)升至310 ℃(关联压力5.2 MPa)时,二甲基二硫和二乙基二硫的ΦS分别从100%和98%降至24%和22%,意味着裂解率ξ从0和2%分别升至76%和78%;330 ℃时(关联压力6.5 MPa)剩余二甲基二硫的ΦS在5%以下,尽管ξ已大于95%,但完全裂解尚需更高温度。从图1(c)可以看出,在反应温度为200 ℃时,剩余二叔丁基二硫的ΦS约为25%;在反应温度为230 ℃(关联压力1.6 MPa)时二叔丁基二硫可完全裂解。这说明二甲基二硫与二乙基二硫的热裂解条件相当,但二叔丁基二硫的热裂解反应要容易得多。
从图1还可以看出,随着反应温度的升高,与温度关联的压力(pt)也在增加。因此,图1中反映的是反应温度及其关联压力对二烷基二硫热裂解产物硫形态分布的共同影响。
2.2.2 反应温度对二烷基三硫(DATS)热裂解产物硫分布的影响
反应温度对二甲基三硫、二乙基三硫裂解产物中各硫化物ΦS的影响如图2所示。由图2可知,2种二烷基三硫的热裂解反应具有以下特征:
(1)随着温度的升高,烷基三硫的ΦS下降,裂解产物的ΦS增加,当反应温度从120 ℃(关联压力0.2 MPa)升至310 ℃(关联压力5.2 MPa)时,二甲基三硫及二乙基三硫裂解产物ΦS总和分别由0及3%升至95%及97%。(2)二烷基三硫在较低温度下(二甲基三硫160 ℃以下,二乙基三硫120 ℃以下)的分解产物以二烷基二硫及二烷基四硫为主,表明在较低温度下主要发生二烷基三硫转化为二烷基二硫及二烷基四硫的歧化反应,进一步的裂解反应不明显;二甲基三硫在120 ℃时的裂解率小于1%。(3)热裂解反应发生后的产物以硫醇为主,H2S为辅,并含单硫醚(仅二甲基三硫产生)。(4)二甲基三硫的裂解产物中甲硫醇及H2S的ΦS与二甲基二硫(见图1(a))裂解反应中相差不大,但二乙基三硫的裂解产物中乙硫醇的ΦS明显低于二乙基二硫(见图1(b))的热解反应,而H2S的ΦS则高于二甲基二硫及二甲基三硫的裂解产物。(5)二烷基三硫加热后均有相应二烷基二硫及二烷基四硫生成,且随着温度的升高,二烷基二硫的ΦS增大到峰值后逐渐降低,二甲基二硫及二乙基二硫的ΦS达到最大值的温度分别约为235 ℃和215 ℃;而二烷基四硫的ΦS随温度升高持续降低,在190 ℃时的反应产物中已检不出二甲基四硫,在210 ℃时反应的产物中检测不出二乙基四硫。(6)二烷基三硫加速热裂解的“温度拐点”不如二烷基二硫明显。
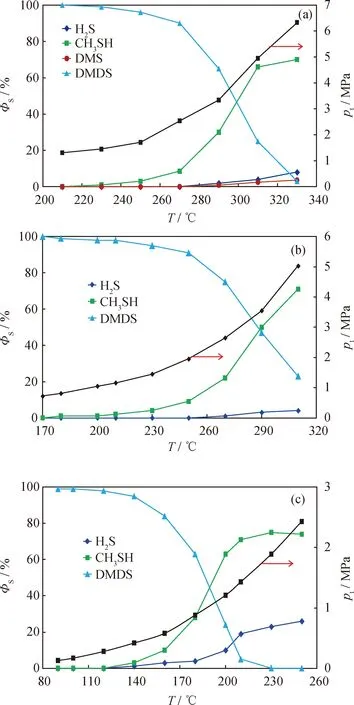
图1 反应温度(T)及其关联压力(pt)对二烷基二硫热裂解产物硫分布的影响Fig.1 Effect of reaction temperature (T) and relatedpressure (pt) on ratio of sulfur types fordialkyl disulfide pyrolysis products(a) DMDS, t=120 min; (b) DEDS, t=120 min;(c) DTBDS, t=120 min;ΦS—Ratio of sulfur type in total sulfur;pt—Pressure change due to rising of temperature;DMS—Dimethyl sulfide; DMDS—Dimethyl disulfide;DEDS—Diethyl disulfide; DTBDS—Di-tert-butyl disulfide
压力为1.9 MPa时,二甲基二硫的热裂解起始温度为235 ℃左右(表3),即在压力为1.9 MPa以上、温度为235 ℃以下时,二甲基二硫不发生裂解。从图2(a)可知,由二甲基三硫歧化生成二甲基二硫的ΦS达到最大值的温度在230 ℃(关联压力为1.8 MPa)左右,此时二甲基二硫接近热裂解起始反应条件,其ΦS约为28%;剩余二甲基三硫的ΦS约为17%;如歧化生成的二甲基四硫不裂解,则计算其ΦS应为此时二甲基二硫的ΦS的2倍(即56%),三者之和应接近100%。但从图2(a)可见,此时产物中并不存在二甲基四硫,表明其在生成的同时就已裂解,此时的硫醇、H2S等小分子硫化物应是由二甲基三硫经歧化生成的二甲基四硫裂解反应所生成。由此可知,在230 ℃以下时,生成的小分子硫化物主要来自于歧化产物二甲基四硫的裂解反应;而在230 ℃以上时,歧化生成的二烷基二硫与二烷基四硫都会发生裂解反应,生成小分子硫化物。从图2(a)还可看出,当温度升至290 ℃时(关联压力3.7 MPa),剩余二甲基三硫的ΦS为已接近0,但歧化生成的二甲基二硫尚未完全裂解,其ΦS为10%左右;进一步升温至310 ℃(关联压力5.3 MPa)反应后,其ΦS仍有5%左右,此时二甲基三硫的热解率ξ为95%左右,其完全裂解还需更高温度,应与二甲基二硫相当。
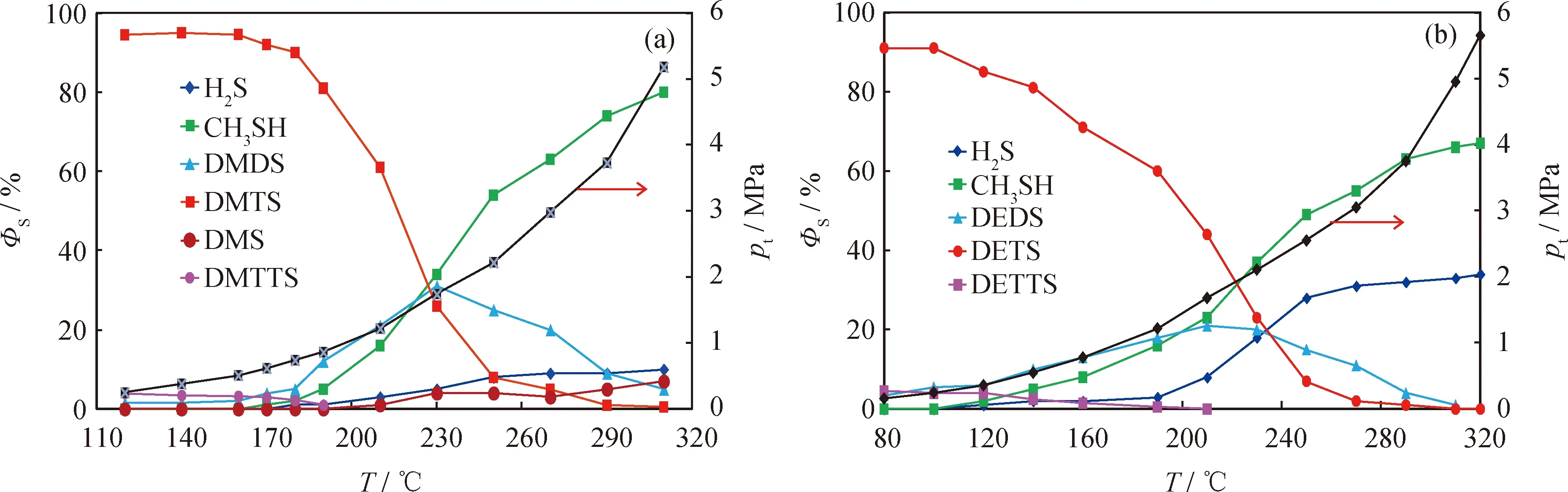
图2 反应温度(T)及关联压力(pt)对二烷基三硫热裂解产物硫分布的影响Fig.2 Effect of reaction temperature (T) and related pressure (pt) on ratio of sulfur types for dialkyl trisulfide pyrolysis products(a) DMTS, t=120 min; (b) DETS, t=120 minΦS—Ratio of sulfur type in total sulfur; pt—Pressure change due to rising of temperature; DMS—Dimethyl sulfide;DMDS— Dimethyl disulfide; DMTS—Dimethyl trisulfide; DMTTS—Dimethyl tetrasulfide; DEDS—Diethyl disulfide;DETS—Diethyl trisulfide; DETTS—Diethyl tetrasulfide
从图2(b)可知,二乙基三硫的热裂解反应同样是先歧化为二乙基二硫和二乙基四硫,前者的ΦS先升高后降低,后者则是迅速裂解。
可见二烷基三硫并不直接发生热裂解,而是经历先歧化、歧化产物再继续裂解的过程。歧化反应的温度低于热裂解实验的起始温度,其中二烷基四硫的热稳定性较差,裂解速率大于生成速率,以至在一定温度以上时(二甲基三硫为 190 ℃,二甲基二硫为210 ℃),裂解产物中检不出二烷基四硫;歧化生成的二烷基二硫会按图1所示的趋势继续裂解。
另外,由于甲基或乙基二硫的裂解温度却要比二叔丁基二硫高得多。因此,尽管二甲基三硫(或二乙基三硫)与二叔丁基二硫的热裂解起始温度相差不大,但完全裂解的温度却要高很多。
2.3 反应压力对二烷基多硫热裂解产物硫分布的影响
2.3.1 反应压力对二烷基二硫热裂解产物硫分布的影响
图3为一定温度下反应压力对二烷基二硫热裂解产物分布的影响。由图3可知,随着压力的增加,产物中剩余二甲基二硫或二乙基二硫的ΦS都在升高,表明二烷基二硫的热裂解程度都随反应压力的增大而降低。相应裂解产物中的硫醇、H2S及DMS的ΦS均随压力的增大而减小。
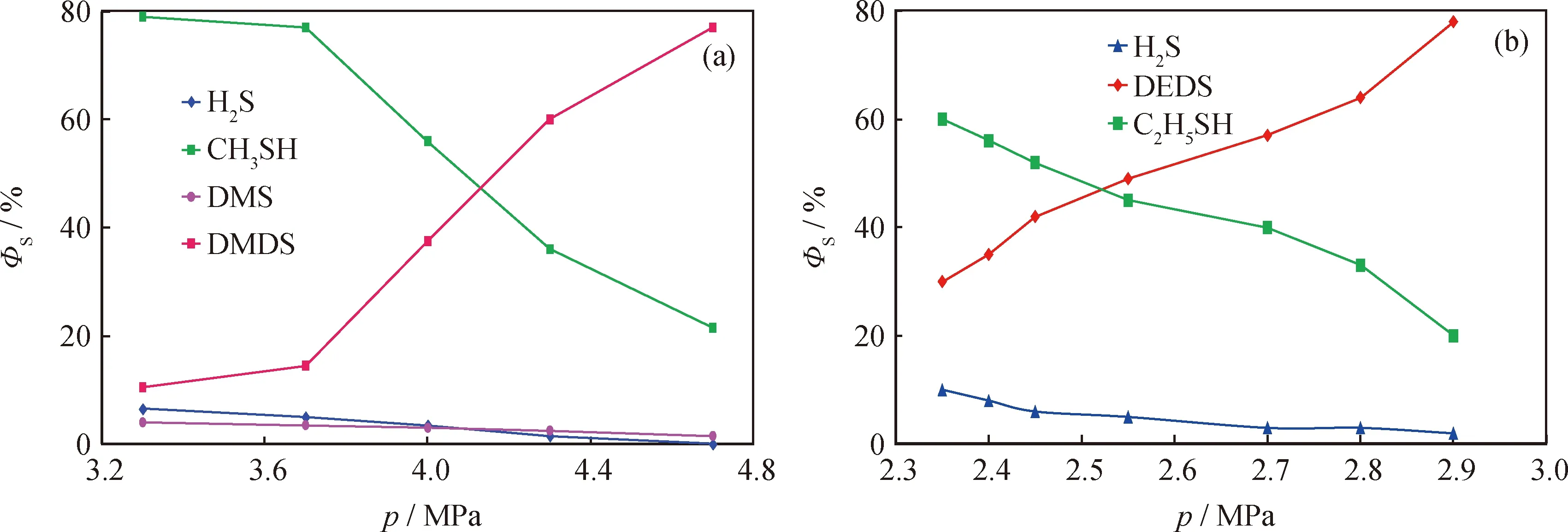
图3 反应压力(p)对二烷基二硫热裂解产物硫分布的影响Fig.3 Effect of reaction pressure (p) on ratio of sulfur types for dialkyl disulfide pyrolysis products(a) DMDS, T=290 ℃, t=120 min; (b) DEDS, T=270 ℃, t=120 minΦS—Ratio of sulfur type in total sulfur; DMS—Dimethyl sulfide; DMDS—Dimethyl disulfide; DEDS—Diethyl disulfide
2.3.2 反应压力对二烷基三硫热裂解产物中硫分布的影响
图4为一定温度下反应压力对二烷三硫热裂解产物中硫形态分布的影响。从图4(a)可以看出,在210 ℃、1.20 MPa下反应120 min后,硫化物的热裂解产物中,硫化氢、甲硫醇及甲硫醚的ΦS分别约为8%、3%及25%,合计为36%;未反应二甲基三硫的ΦS约为26%,歧化反应产生的二甲基二硫及二甲基四硫的ΦS分别约为38%及0,三者合计为64%。此时二甲基三硫的热裂解率ξ为36%。在210 ℃、2.4 MPa下反应120 min后,产物中几乎没有硫化氢、甲硫醇及甲硫醚,此时物料中的硫化物几乎全部是二甲基三硫及歧化生成的二甲基二硫和二甲基四硫。可见,当反应压力由1.2 MPa增加至2.4 MPa时,二甲基三硫的热裂解率由36%降至0。从图4(a)还可知,歧化产物二甲基二硫及二甲基四硫的ΦS变化表现出相反趋势:二甲基二硫的ΦS随着压力的增大而下降,而二甲基四硫的ΦS则随着压力的增大而上升。由图4(b)可见,在反应温度200 ℃下,反应压力对二乙基三硫热裂解产物中硫形态分布的影响也呈现类似的规律。
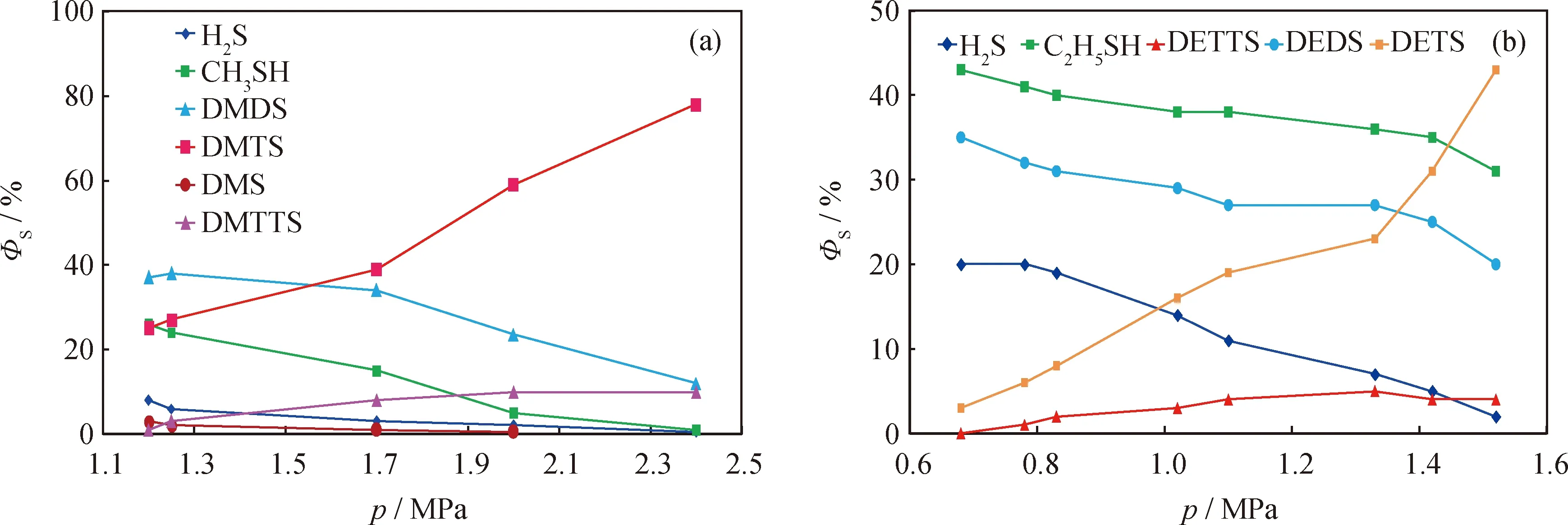
图4 反应压力(p)对二烷基三硫热裂解产物硫形态分布的影响Fig.4 Effect of reaction pressure (p) on ratio of sulfur types for dialkyl trisulfide pyrolysis products(a) DMTS, T=210 ℃, t=120 min; (b) DETS, T=200 ℃, t=120 min;ΦS—Ratio of sulfur type in total sulfur; DMS—Dimethyl sulfide; DMDS—Dimethyl disulfide; DMTS—Dimethyl trisulfide;DMTTS—Dimethyl tetrasulfide; DEDS—Diethyl disulfide; DETS—Diethyl trisulfide; DETTS—Diethyl tetrasulfide
从表3可知,当压力从0.9 MPa升至2.1 MPa后,二甲基二硫发生热裂解反应的起始温度Tip从210 ℃升至239 ℃;如果设定反应温度为210 ℃,压力在0.9~1.9 MPa,二甲基二硫应基本不会裂解。从图3(a)可知,二甲基二硫的ΦS随压力升高增加,则歧化反应生成的二甲基二硫的ΦS也应随着压力升高而增大,但图4(a)显示二甲基二硫的ΦS随压力升高而降低,说明压力增加抑制了二甲基三硫的歧化反应,使二甲基二硫的生成速率低于裂解速率。但另一方面,二甲基四硫的ΦS却随压力升高而增大,说明压力增加尽管抑制了二甲基三硫的歧化,使其ΦS降低;但同时也抑制了二甲基四硫的热裂解反应,使二甲基四硫的生成速率大于裂解速率。
可见,升高压力不仅会提高二烷基多硫的热裂解起始温度,还会抑制二烷基多硫的热裂解反应。因此,反应温度和压力都是影响二烷基多硫热裂解反应程度及其产物硫形态分布的重要因素。不同烷基、不同硫原子数烷基多硫的热裂解反应产物中都含相应烷基的硫醇及H2S,但不同多硫的热裂解反应条件很不相同。因此,在热处理含有机多硫的轻烃时,可根据生产要求,结合原料中硫化物的形态,适当调整温度和压力,控制产物中的硫分布。
2.4 其他反应条件对热裂解产物的影响
以往对二烷基(及芳基等)多硫热裂解的研究多在常压[8,12]或负压下[9-10]进行,研究对象是无溶剂的“纯”二烃基多硫,个别研究[11]虽涉及烃类溶剂,但热裂解反应涉及加氢催化剂及H2的参与。本研究中以轻质烷烃为溶剂,研究温度及压力对其中微量二烷基多硫热裂解产物分布的影响。表4为二烷基多硫热裂解实验中所使用的硫化物、主要反应条件及裂解产物对比。
由表4可以看出,不同实验条件下二烷基多硫热裂解产物的共同特点是热裂解产物均以硫醇和H2S为主。不同点在于:(1)无烃类溶剂时,C1烷基多硫的热裂解产物中含CS2,但C2及C2以上二烷基多硫的热裂解产物中未发现CS2,二烷基多硫热裂解产物的种类较多,可检测到S0、CH2=S,甚至极微量的H2S2及CH3SCH2SSCH3等;(2)以烃类为溶剂时,热裂解产物中可检测到的硫化物种类较少,即使二甲基多硫的裂解产物中也未发现CS2。

表4 不同反应条件下短链二烷基多硫热裂解产物硫分布Table 4 Sulfur distribution of short-chain dialkyl polysulfides pyrolysis products under various reaction conditions
本研究中,二乙基二硫在温度270 ℃、压力3.0 MPa下反应120 min,热裂解率小于30%;在310 ℃、5.3 MPa下反应120 min,热裂解率仅80%;裂解产物均以乙硫醇为主,H2S为辅。Moldavskii等[11]在MoS(一种加氢催化剂)及H2存在下,将溶解在煤油中的二乙基二硫(0.8 mol/L)在230 ℃、3.0 MPa下反应120 min,测得其热裂解率超过75%,且产物以H2S为主、乙硫醇为辅;而Coope[9]对无溶剂的二乙基二硫,在318 ℃、0.01 MPa时反应20 min后,发现二乙基二硫完全裂解。这说明:催化剂可促进二乙基二硫的热裂解;H2能将生成的部分CH3CH2SH还原为H2S,改变裂解产物中的硫分布;降低压力可促进有机多硫的热裂解。
可见,短链二烷基多硫的热裂解率及产物分布不仅与硫化物本身的化学结构有关,还与温度、压力、溶剂、催化剂、H2等多种因素相关。
2.5 轻烃中二烷基多硫热裂解反应机理
如烃类[19-21]及某些含杂原子的有机过氧化物[22]、硫醇[15]的热裂解等多属于自由基反应。一般认为,二烷基多硫的热裂解反应也遵循自由基机理[8]。
热裂解反应伴随化学键的断裂及重组,反应时化学键断裂所需的活化能实际上就是离解能,在短链烷基多硫中,存在的化学键包括C—H、C—C、C—S、S—S及S—H键等,离解能不仅取决于毗邻元素的性质,而且与所处化学环境相关。相关化学键的典型离解能如表5所示。
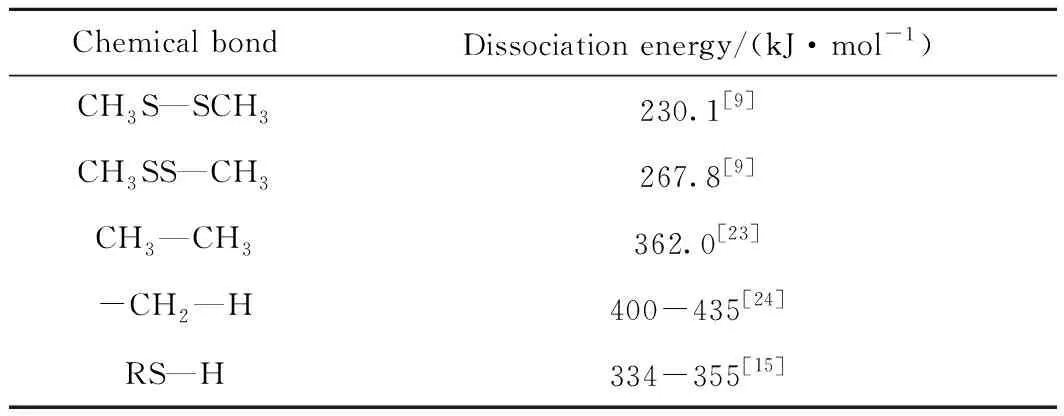
表5 相关化学键的离解能Table 5 Dissociation energy of related chemical bonds
升温过程中离解能低的化学键会优先断裂,形成自由基或进一步热裂解,然后重组形成新的分子。依据相关化学键的离解能数据,S—S键优先断裂,其次是S—C键,然后是C—C键,最后才是C—H键。C—C键及C—H键的离解能大于S—S键及S—C键,因此,热裂解过程中首选断裂的主要是S—S键,断键后形成自由基,自由基进一步与其他分子或自由基结合,形成新分子。有关热裂解反应的机理可能部分与文献[9]类似,但Sehon等[15]以甲苯为溶剂研究硫醇的热裂解反应时,发现裂解产物中含有CH4、H2S及1,2-二苯基乙烷,于是提出甲硫醇可能发生如式(8)~(11)的包括热裂解在内的系列反应,产生H2S及CH4等。显然作为溶剂的甲苯参与了反应,但因CH3SH为微量,甲苯的参与量也是微量。故作为本实验溶剂的烃类可能参与反应。
CH3SH+C6H5CH3→C6H5CH2·+CH3·+H2S
(8)
CH3·+CH3SH→CH3S·+CH4
(9)
CH3S·+C6H5CH3→C6H5CH2·+CH3SH
(10)
2C6H5CH2·→C6H5CH2CH2C6H5
(11)
本研究中以烷烃为主要成分的石油醚作为二烷基多硫的溶剂,当温度升高后,二烷基多硫分子首先发生S—S键断裂,形成烃基硫自由基,该自由基再从烷烃分子中夺取氢原子生成硫醇,烷烃分子则生成新的自由基,这些自由基相互间结合生成大分子的烷烃,如式(12)~(14)所示。
CH3SSCH3→2CH3S·
(12)
CH3S·+RCH3→CH3SH+RCH2·
(13)
2RCH2·→RCH2CH2R
(14)
生成的硫醇可进一步裂解,生成H2S、硫醚及烃类,如式(15)~(20)所示。实验中烷基多硫的热裂解先产生硫醇,再产生H2S或DMS等。
CH3SH→CH3·+SH·
(15)
SH·+CH3·→CH4+S
(16)
S+CH3SH→CH3SSCH3+H2S
(17)
CH3S·+CH3·→CH3SCH3
(18)
CH3CH2SH→CH3CH2·+SH·
(19)
SH·+CH3CH2·→CH=CH2·+H2S
(20)
CH3SH的C—S键能为284 kJ/mol,CH3CH2SH的C—S键能为263 kJ/mol[15],因而后者热裂解相对更容易。由图1和图2可知,相同温度下,二乙基二硫比二甲基二硫、二乙基三硫比二甲基三硫产生更多的H2S;二甲基二硫及二甲基三硫在热裂解过程中都产生了DMS,但二乙基二硫在热裂解过程中均未产生相应二乙基硫醚(DES),这可能是二乙基二硫按类似于式(12)裂解反应产生的CH3CH2·优先与式(19)产生的SH·按照式(20)反应迅速生成H2S的缘故。其他如二乙基三硫及二叔丁基二硫可能基于相同原因,裂解反应未产生相应硫醚。
本研究中二烷基多硫的热裂解产物中未发现CS2,可能与反应环境有关。Clark等[12]认为,二甲基多硫产生CS2,需经过生成·SCH2S·双自由基阶段,而该自由基需经由单自由基CH3S·形成,但因实验中烃类大量存在,使CH3S·依据式(13)反应迅速生成CH3SH,因而得不到CS2。由此可见,大量烃类的存在可能改变了二烷基多硫的热裂解产物硫形态分布。
二烷基多硫分子中S—S键的离解能最小,在热裂解过程中首先断裂形成自由基,与其他原子或原子团结合[25],形成新的含硫化合物;二烷基三硫则经历了歧化为二烷基二硫及二烷基四硫的反应,如式(21)所示。
RSSSR→RSSR+RSSSSR
(21)
生成的RSSSSR及RSSR同时也在发生热裂解反应,但RSSSSR裂解温度更低,而RSSR按照式(12)~(20)的裂解方式进行反应。以CH3SSSSCH3为例,热裂解可描述如式(22)~(26)所示。生成的CH3S·等自由基按照式(12)~(20)继续进行反应,生成小分子硫化物。
CH3SSSSCH3→CH3S·+CH3S3·
(22)
CH3S·+RCH3→CH3SH+RCH2·
(23)
CH3S3·→CH3S·+S2
(24)
S2+2CH3SH→CH3SSCH3+2H2S
(25)
2RCH2·→RCH2CH2R
(26)
二烷基多硫分子中的硫原子数越多,S—S键越弱,越易断裂形成自由基;烷基越大或异构化程度越高,断裂形成的自由基越稳定[26]。由此推测,相同烷基多硫的分子中硫原子越多,或相同硫原子数的多硫中的烷基越大,或烷基的异构化程度越高,烷基多硫的热稳定性越差。实验中短链二烷基多硫热裂解的难易程度及热裂解的产物分布基本符合这种规律。
3 结 论
(1)本实验考察的二甲基多硫热裂解产物主要为烷基硫醇、H2S,也含有二甲基硫醚。
(2)相同硫原子数的二烷基多硫,烷基越大,热稳定性越差;相同烷基的多硫,分子中硫原子数越多,越易发生热裂解。二甲基二硫、二乙基二硫、二甲基三硫、二乙基三硫及二叔丁基二硫在 1.0 MPa 下发生热裂解反应的起始温度分别为213、196、161、139及143 ℃。
(3)反应温度和反应压力是影响烷基多硫热裂解反应的主要因素,升高温度可促进热裂解反应,增大压力则抑制热裂解反应。
(4)二烷基三硫的热裂解过程中先歧化生成二烷基二硫和二烷基四硫,歧化产物继续热裂解。这使得低碳数烷基多硫的热裂解反应初始温度低,但完全裂解需较高温度。烷基多硫的热裂解反应遵循自由基机理;烃类溶剂会减少烷基多硫的热裂解产物中硫的类型;H2及加氢催化剂的存在可提高二烷基多硫的热裂解率。

