坎地沙坦分散片的处方工艺优化
宋梦文,郑林霞,谢子晴,张磊
坎地沙坦为新一代二苯并咪唑类血管紧张素Ⅱ受体拮抗剂,其通过阻断AT1受体[1],从而起到降压的作用,尤其对原发性中度高血压的治疗效果显著[2]。坎地沙坦可有效预防和改善心肌肥厚,对肾脏也具有一定保护作用[3]。因此,坎地沙坦在临床应用具有高效、作用时间长、选择性高、不良反应较少等特点。但因坎地沙坦在水中的溶解度较小,所以在实际应用方面存在一定局限性,为解决坎地沙坦难溶的问题,本实验首先采用固体分散体技术将其制成固体分散体,增大其溶解度,其次采用正交实验设计筛选出制备坎地沙坦分散片的最优处方,使其能够迅速崩解[4-5],从而产生快速降压的作用,同时也利于吞咽困难的高血压患者使用[6],丰富坎地沙坦分散片制备工艺的研究。
1 仪器与试剂
TDP-1.5单冲式压片机(长沙市长宏制药机械设备厂);U-1901紫外可见分光光度仪(北京普析通用仪器有限责任公司);ZRS型智能溶出度实验仪(上海黄海药检仪器有限公司);MA110电子天平(上海鸿都电子科技有限公司);SYU-22-600DT超声波清洗机(郑州生元仪器有限公司);BJ-Ⅲ型崩解时限测定仪(天津市旭阳仪器设备有限公司)。坎地沙坦原料药(福州腾远生物科技有限公司);α-乳糖(LAC)(邯郸市林峰精细化工有限公司);微晶纤维素(MCC)(国药集团化学试剂有限公司);滑石粉(浙江亚太药业股份有限公司);甲醇(上海方野化工有限公司);无水乙醇(邯郸市林峰精细化工有限公司);聚维酮(PVP)(上海麦克林生化科技有限公司);交联聚维酮(PVPP)[攻碧克新材料科技(上海)有限公司];十二烷基硫酸钠(SDS)(天津市科密欧化学试剂有限公司);聚乙二醇6000(佛山市德中化工科技有限公司)。
2 方法与结果
2.1 坎地沙坦固体分散体的制备
2.1.1 溶剂法制备固体分散体:称取坎地沙坦原料药1 g,加入无水乙醇50 ml,超声至完全溶解,加入聚乙二醇[7]4 g(坎地沙坦∶聚乙二醇=1∶4)搅拌溶解,将溶液倒入旋转蒸发仪中除去大部分乙醇,并置于干燥箱中过夜干燥得白色结晶,将上述结晶研磨过80目筛即得固体分散体。
2.1.2 研磨法制备固体分散体:称取坎地沙坦原料药1 g,聚乙二醇4 g,用研钵共研磨,并将研磨过的粉末过80目尼龙筛得坎地沙坦固体分散体[8]。
2.1.3 溶出度比较:分别取上述方法(溶剂法、研磨法)制备的固体分散体各40 mg,以0.4%SDS溶液作溶出介质,采用转篮法,取500 ml溶出介质加入到溶出仪中,温度为37 ℃,转速为75 r/min,开动搅拌后开始计时,并在各时刻取样,取续滤液于紫外分光光度计下254 nm[9](0.4%SDS校正空白)处测得吸收度并计算其溶出度。溶剂法制备的固体分散体在t=60 min时溶出度为89.9%,即溶出较好,故本课题固体分散体的制备选用溶剂法进行。
2.2 正交实验设计 确定坎地沙坦固体分散体的制备方法后,通过预实验对分散片中的崩解剂、填充剂、粘合剂进行筛选,最终确定以LAC+MCC(1∶1)为填充剂,PVPP为崩解剂,PVP为粘合剂。并且三者的用量对分散片的制备尤为重要,因此将LAC+MCC、PVPP的比例、PVP乙醇浓度作为变量,以崩解时限为指标,得正交实验设计表(表1)。对正交实验结果进行极差分析(表2)可得,影响坎地沙坦分散片崩解时间的综合因素依次为A>B>C,可知填充剂(A)为主影响因素,崩解剂是次要因素,最终确定最佳工艺为A3B3C1,即填充剂(A)LAC+MCC的量为30%,崩解剂(B)PVPP的量为7%,粘合剂(C)选用1%PVP乙醇溶液时,按此处方比例制备的分散片崩解时限最优,压缩成型性较好。
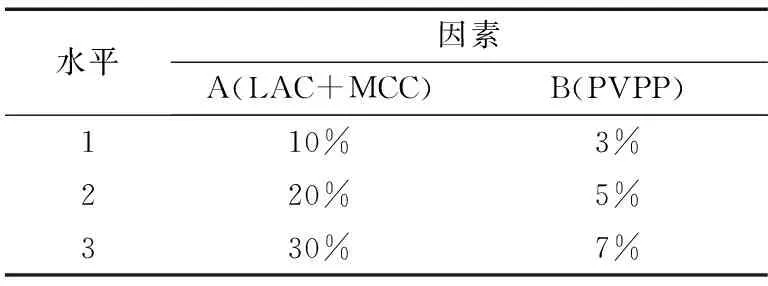
表1 正交实验设计表

表2 正交实验结果及分析表
2.3 分散片的制备 按处方量称取坎地沙坦固体分散体,并与处方中的各辅料混合均匀,加入1%PVP制软材,过16目筛,55 ℃干燥30 min,过筛整粒,并外加崩解剂和滑石粉,混匀,压片即得。
2.4 线性关系考察 取坎地沙坦原料药粉末25 mg于容量瓶(50 ml)中,加甲醇溶解稀释,最终配制为3、6、9、12、15、18 μg/ml浓度的溶液。在254 nm波长处分别测定吸光度,并以吸收值对相应的浓度作图,得线性回归方程A=0.0401C+0.1051,R2=0.9977。
2.5 精密度实验 称取坎地沙坦原料药粉末约20 mg,倒入50 ml容量瓶中,加入甲醇溶液反复稀释,得16 μg/ml的坎地沙坦溶液,并于不同时刻在254 nm波长处测定吸光度,通过计算同一溶液在不同时刻吸光度的相对标准误差RSD=4.09%<5%,可得实验所用的仪器精密度良好。
2.6 回收率实验 称定6.4 mg(80%)、8.0 mg(100%)和9.6 mg(120%)的坎地沙坦原料药于3个50 ml容量瓶中,并按药物与各辅料对应的处方比例,称定辅料的量加入对应比例的容量瓶中,加甲醇溶解稀释。最终得到浓度分别为12.8、16、19.2 μg/ml的溶液,另称取8 mg原料药在不加辅料情况下制备浓度为16 μg/ml的坎地沙坦溶液作为对照品溶液,按照“2.4”项下方法进行测定,结果得:当药物的量分别占标示量的80%、100%、120%时,平均回收率分别为98.74%、100.30%、100.90%。表明该处方中辅料对药物含量影响较小,准确度较高。
2.7 体外溶出度实验 取最优处方制得的坎地沙坦分散片6片(规格:8 mg),分别放入溶出介质为0.4%SDS(500 ml)溶液中。设置溶出仪温度37 ℃,转速75 r/min,并在不同时刻抽取样品溶液5 ml。另配制坎地沙坦溶液(16 μg/ml)作为对照品溶液,将处理过的7组供试品溶液按照UV法于254 nm处测定吸光度值,计算每片的溶出量并绘制溶出曲线。见图1。该优化处方制得的坎地沙坦分散片平均溶出度>80%,即溶出合格,且在前10 min时溶出速度较快,表明该制备方法可极大改善其溶出度和崩解速度。

图1 坎地沙坦分散片平均累计溶出曲线
3 讨 论
利用溶剂法制备坎地沙坦固体分散体的过程中,由于PEG6000对机体刺激性较小,稳定性较好,并且可使药物分散度和比表面积增加,故选其作为最佳载体材料。在坎地沙坦分散片的处方研究过程中,选用LAC+MCC、PVPP、PVP分别作为填充剂、崩解剂、粘合剂的原因如下:首先,LAC+MCC与坎地沙坦合用时可掩盖坎地沙坦的不良气味,并且压制的片剂表面较为光洁,因此将其作为填充剂;其次选用PVPP作为崩解剂,主要由于PVPP遇水后具有高度的毛细管作用,溶液中的水进入药物内部,使药片快速崩解为小颗粒;再次用外加法加入PVPP进行压片时,所得的片剂硬度较大,且不影响主药的含量与疗效。
本实验通过溶出度考察发现,采用溶剂法制备的坎地沙坦固体分散体溶出较为理想,根据正交实验结果分析得出,LAC+MCC(1∶1)比例为30%,PVPP在处方中的含量为7%、PVP乙醇溶液浓度为1%时制得的坎地沙坦分散片崩解时间较短,可在3 min内迅速崩解,并且溶出度大于80%,符合药典标准。

