卢帕他定联合转移因子口服液治疗慢性荨麻疹的临床观察
郭亚茜
(锦州医科大学,辽宁 锦州 121000)
荨麻疹是一种常见的肥大细胞驱动性疾病,伴有风疹或血管性水肿或两者兼有[1]。荨麻疹影响各个年龄段的人,并且很普遍。大约五分之一的人一生中都会经历荨麻疹发作,估计每年患慢性荨麻疹的患病率约为人口的1%[2]。CSU的风疹和血管性水肿涉及皮肤肥大细胞的脱颗粒,肥大细胞释放组胺、蛋白酶和细胞因子,同时产生血小板活化因子和其他花生四烯酸代谢物。这些介质诱导血管扩张,增加血管通透性,刺激感觉神经末梢,导致肿胀、发红和瘙痒。病变部位或风团的特征是水肿、肥大细胞脱颗粒和血管周围细胞浸润[3]。最近的研究发现,在病变皮肤真皮中检测到支持Th2的上皮源性细胞因子,包括IL-33、IL-25和TSLP以及血管活性剂VEGF和CGRP,但这些因子在未感染皮肤中未被观察到[4-5]。
目前,非镇静抗组胺药和抗免疫球蛋白E抗体奥马珠单抗被推荐用于慢性荨麻疹的治疗,因为它们均具有良好的疗效和安全性[1]88-101。血小板活化因子(platelet-activating factor,PAF)作为一种有效的介质参与了过敏性变态反应,这一作用得到了越来越多的重视。卢帕他定对组胺H1受体和PAF受体具有双重亲和力[6]。富马酸卢帕他定是第二代抗组胺药,可以有效、持久平衡体内的双重血小板活化因子和组胺拮抗剂活性,并且在高水平下将两种活性独特地结合在一起[7]。转移因子作为细胞的免疫调节剂已经被应用到荨麻疹的治疗当中[8]。
本研究中使用第二代抗组胺药卢帕他定以及联合转移因子口服液对两组慢性荨麻疹患者进行治疗,通过对IL-33、IL-35的水平含量变化测定,以及两组患者的总体治愈率,不良反应进行统计观察,为更好合理使用卢帕他定联合转移因子提供理论依据。
1 材料和方法
1.1 一般资料
收集本市2018年3月至2019年3月间皮肤科门诊就诊的70例慢性荨麻疹患者,按照随机数字表法分为两组,各35例,其中女38例,男32例,年龄(17~35)岁,平均年龄(22.35±2.48)岁病程(2~12)个月,平均病程(5.35±0.94)个月。观察组和对照组的临床资料经分析,差异无统计学意义(P>0.05),具有可比性。
纳入标准:(1)入选患者均符合慢性荨麻疹诊断标准[9],临床上以瘙痒、风团为主;(2)病程≥6 w,每周发病2次以上;(3)经检查无其他皮肤病,患者自愿参加科学研究并签署知情同意书;(4)近2 w内未使用过组胺类药物,对组胺类药物不过敏。排除标准:(1)伴有自身免疫性疾病的患者;(2)正在妊娠或哺乳的女性患者;(3)有重大心脑血管、血液及肝肾病的患者;(4)有精神疾病,不能配合医生进行治疗的患者。
1.2 主要试剂
对照组患者使用卢帕他定片治疗(扬子江药业集团,国药准字H20130047),患者每日1次,饭后服药,10 毫克/次 。观察组患者给予卢帕他定联合转移因子口服液(万通,H22025247),每日1次,每次10 mL。患者持续用药治疗6 w,治疗期间禁止使用其他药物。IL-33、IL-35 ELISA检测试剂盒购自(上海酶联生物)。
1.3 采集标本
两组患者分别在用药前后采集静脉血5 mL,待血液冷却凝固后,3000 rpm离心15 min,取上层血清于新的EP管中,-80 ℃保存待用。
1.4 观察指标及评分标准
分别于治疗前、治疗后按照四级评分法(0~3)进行积分,使用瘙痒程度、风团数量、风团直径、瘙痒持续时间四项指标的评分总和对CSU疾病程度进行评价,见表1。两组患者的临床疗效根据症状积分下降指数(symptom score reduce index,SSRI)进行评价,SSRI=(治疗前总积分-治疗后总积分)/治疗前总积分×100%。临床疗效根据症状积分下降指数进行评判:SSRI≥90%为有效,60% 表1 受试者症状积分标准 两组患者治疗前IL-33、IL-35水平含量比较,差异无统计学意义(P>0.05),具有可比性。治疗后,对照组和观察组的IL-33含量均有下降,差异有统计学意义(P<0.05),并且观察组与对照组相比,IL-33水平进一步下降,差异有统计学意义(P<0.05)。治疗后,两组患者的IL-35含量均较治疗前有所提高,差异有统计学意义(P<0.05),并且观察组与对照组相比,IL-35水平进一步提高,差异有统计学意义(P<0.05),见表2。 表2 IL-33、IL-35治疗前后表达差异 治疗前,对照组的症状积分为(5.03±0.34),观察组的症状积分为(5.08±0.38),两组患者的症状积分经比较差异无统计学意义(P>0.05),具有可比性。治疗后,对照组和观察组的症状积分分别为(4.83±0.23)和(4.71±0.19),两组的症状积分均有所下降,差异有统计学意义(P<0.05),且观察组的症状积分较对照组进一步下降,差异有统计学意义(P<0.05),见表3。 表3 两组患者治疗前后的症状积分比较 对照组治疗后有效例数26例,有效率74.29%,观察组治疗后有效例数32例,有效率91.43%,两组有效率比较,差异有统计学意义(P<0.05),见表4。 观察组和对照组发生不良反应的例数分别为3例和5例,不良反应的发生率分别为8.57%和14.29%,观察组和对照组患者的不良反应发生率差异无统计学意义(P>0.05),见表5。 表4 两组患者治愈有效率比较 表5 两组患者不良反应的比较 已有研究表明,IL-33参与了荨麻疹的发病机制,并且,与健康人比较,荨麻疹患者的皮肤活检IL-33的水平明显更高[10]。在体外,IL-33诱导Th2细胞释放IL-5和IL-13等Th2细胞因子,并在体内升高血浆IgE和血嗜酸性粒细胞[11]。IL-33还可引起肥大细胞[12]的活化、成熟和Th2细胞因子的产生,并诱导嗜酸性粒细胞依赖性皮肤纤维增生[4,13]1294-1302。在本研究中,对照组和观察组治疗后的IL-33水平明显降低,且观察组的IL-33较对照组进一步降低,说明卢帕他定联合转移因子能够进一步降低慢性荨麻疹引起的IL-33升高。 IL-35通过将T细胞的周期终止在G1期,同时促进Treg细胞增生,被认为具有强大的免疫功能。已有研究证实[14]荨麻疹患者中的IL-35表达水平明显低于健康人。在本研究中,治疗后的对照组和观察组IL-35水平均有所提高,且观察组较对照的IL-35含量进一步提高,证明卢帕他定联合转移因子能够进一步提高荨麻疹患者的IL-35。但是,IL-35是如何参与了荨麻疹的发病机制尚不清楚,我们推断可能是荨麻疹患者的自身免疫系统紊乱,导致了IL-35的减少,而抗组胺药物卢帕他定联合细胞的免疫调节剂转移因子能够较好改善IL-35的表达。 富马酸卢帕他定作为第二代抗组胺药物,不表现出第一代H1抗组胺药的副作用,例如嗜睡,疲劳,头痛,记忆力和学习障碍,镇静,食欲增加,口干,眼睛干涩,视力障碍,便秘和勃起功能障碍[7]1807-1813。卢帕他定是具有有效,持久且平衡体内的双重血小板活化因子和组胺拮抗剂活性,并且在高水平下将两种活性独特地结合在一起[7]1807-1813。本研究中,使用卢帕他定后明显改善了荨麻疹患者的症状积分,有效缓解瘙痒、风团,在此基础上联合转移因子口服液提高了荨麻疹患者的有效治愈率。观察组的不良反应较对照组略低,但是差异不显著。 综上所述,卢帕他定联合转移因子能够有效改善IL-33、IL-35的表达水平,降低CSU患者的症状积分,提高治愈有效率,且不良反应少,具有较好的临床应用价值。1.5 统计学分析
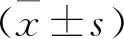

2 结 果
2.1 IL-33、IL-35治疗前后表达差异

2.2 两组患者治疗前后的症状积分比较

2.3 两组患者治愈疗效的比较
2.4 两组患者不良反应的比较


3 讨 论

