EGFR-TKI靶向联合尿激酶精准治疗非小细胞肺癌伴MPE 1例并文献复习
邸金娜,刘敬禹,张莉,冯邵强,李季洋
(锦州医科大学附属第三医院呼吸内科,辽宁 锦州 121000)
根据2018年全球癌症发病率和死亡率(GLOBOCAN 2018)统计数据,每年肺癌新发约209万例(约占11.6%),死亡176 万例(约占18.4%)[1]。肺癌是全世界首位肿瘤杀手。目前中国男性肺癌发病及死亡居第一位,女性肺癌发病居第二位,死亡居首位[2]。85%为NSCLC,其中腺癌是最常见的组织学分型,肺癌晚期可转移至壁层胸膜形成恶性胸腔积液[3],Sahak[4]和Chen[5]等研究结果显示,大约46%~67%的大量MPE 由肺腺癌产生。随着医学科学的飞速发展,晚期肺癌的治疗进入个体化精准时代,即从传统的化疗到基因靶向、抗血管生成治疗及顶端的免疫治疗时代。据报道,在伴有MPE的肺腺癌患者中EGFR突变率高达68.4%[6]。表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor tyrosine kinase inhibitor,EGFR-TKI)靶向药物治疗使EGFR突变人群获益。临床上对肺癌晚期恶性胸腔积液的处理方式包括:全身化疗、胸膜腔内化疗、埋置胸腔导管(PleurX导管)引流、化学性胸膜固定术、反复胸腔穿刺抽液、胸膜切除术等[7]。其中有部分肺癌出现恶性包裹性胸腔积液,单靠胸腔穿刺抽液困难较大。Viedma EC等[8]通过临床研究得出结论,将尿激酶注入胸腔内治疗包裹性胸腔积液比胸腔引流抽液更为有效,且发生胸膜肥厚等并发症较少。目前对于包裹性恶性胸腔积液的处理方式未达成共识。因此,我们在临床工作中口服吉非替尼靶向药物联合胸腔内注射尿激酶治疗非小细胞肺癌恶性包裹性胸腔积液的成功案例,不断总结临床经验,现对此临床病例进行回顾性分析如下:
1 临床资料
患者男,60岁,于2018年3月12日住院。因“渐进性呼吸困难半个月”入院。患者于半个月前无诱因出现气短,逐渐出现呼吸困难,上3楼费力,夜间可平卧,偶有咳嗽,可少量白痰,无咯血,无胸痛,未口服药物,至外院行胸部CT提示左侧大量胸腔积液。为进一步诊治以“左侧胸腔积液”收入呼吸科。既往慢性支气管病史约10年。左侧手尺侧部手术术后6年。否认结核病史。乙型病毒性肝炎病史多年,已系统诊治,现为乙肝病毒携带者。否认过敏史。吸烟40余年,20~30支/日。职业:文学作家。入院查体:生命体征平稳,口唇无发绀,左侧胸廓饱满,左侧肋间隙略增宽,左侧呼吸动度减弱,左侧触觉语颤减弱,无胸膜摩擦感,左侧肩胛下角线第8肋间以下叩诊浊音,呼吸音消失,右侧呼吸音粗,可闻及少许湿性啰音,余查体无阳性体征,无杵状指(趾)。辅助检查:3月12日胸部CT:左肺下叶实变,左肺见磨玻璃密度影,左侧胸腔见大量积液,纵膈淋巴结未见肿大。心电图未见异常。左侧胸水超声定位:左侧胸膜腔内间大片状液性暗区,暗区内回声不清晰,见大量光点悬浮,皮肤距离液性暗区为1.1 cm,4.5 cm达液性暗区处,液性暗区最大深度为11.2 cm。生化检查:PCT、C-反应蛋白、D-二聚体、凝血功能、肝功能(转氨酶)、肾功能、心肌酶、心钠素、血常规未见明显异常。痰培养为肺炎克雷伯杆菌感染。痰脱落细胞学提示可见少许核异质细胞,见图1。
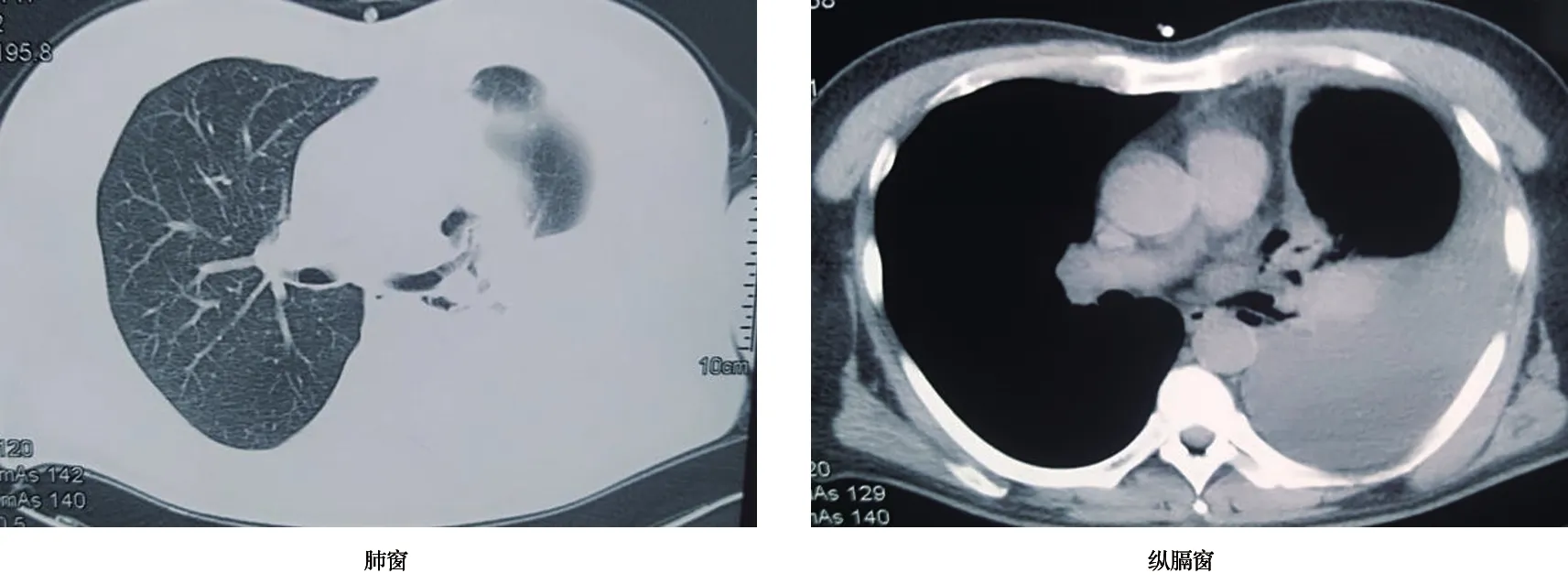
图1 胸部CT(2018.03.12)
2 结 果
入院后初步诊断:左侧大量胸腔积液,慢性支气管炎,阻塞性肺气肿,乙型病毒性肝炎携带者。诊治意见:抗感染、平喘、祛痰、引流胸腔积液及对症等治疗。诊治过程:充分与患者及家属沟通,取得患者及家属同意,2018年3月13日以超声定位点(左侧腋后线第9肋间)为穿刺点,于2%利多卡因局部麻醉下,成功完成胸腔闭式引流术,抽取暗红色胸腔积液550 mL,检验结果提示胸水生化:胸水ADA 1.2 U/L,胸水蛋白39.5 g/L,胸水淀粉酶 369 U/L,胸水葡萄糖 3.74 mmol/L,胸水LDH 1016 IU/L,根据胸腔积液的Light标准结果提示为渗出液(胸水LDH/血LDH=1016/153=6.64)。3次胸水病理脱落细胞学见:瘤细胞,瘤细胞卵圆形,大小不一,核大染色深,核仁明显,散在或成团排列。细胞形态符合腺癌。确定诊断为左侧恶性胸腔积液。为减轻患者呼吸困难症状,充分引流胸腔积液500 mL 2次/日,4 d后(2018年3月17日)共计引流暗红色胸腔积液量约3800 mL。引流后复查胸部CT:左肺下叶背段可见一22 mm×27 mm不规则软组织肿块影,密度不均,边缘可见毛刺,临近胸膜可见胸膜凹陷征,小叶中央型肺气肿,左肺可见条索影,左侧可见少量积液。患者出现左侧胸痛,以左肋下深吸气后胸痛加重,胸痛原因考虑与少量胸腔积液时脏层胸膜与壁层胸膜间摩擦粘连所致。补充诊断:左侧恶性胸腔积液,左肺下叶腺癌,胸膜转移,Ⅳ期,慢性支气管炎,阻塞性肺气肿,乙型病毒性肝炎携带者。患者家属表示告知患者本人肺腺癌实情,患者及家属表示积极治疗,外送胸水EGFR基因检测,基因检测结果EGFR外显子21(L858R)基因突变,于2018年3月22日,予吉非替尼片(易瑞沙,AstraZeneca UK Limitied,批号:09122411),口服250 mg,1次/日。于3月26日办理出院手续。出院后继续口服吉非替尼片及保肝药物,见图1、图2、表1。

图2 胸部CT(2018.03.17)

表1 孙某 EGFR基因突变检测(标本:胸腔积液)
出院1 w后电话随访,患者自诉无不适症状。继续口服药物(同上)。出院半个月后电话随访发现,患者自诉出现咳嗽,偶有痰中带血丝,无整口咯血,再次出现胸闷、气短、呼吸困难、胸痛,活动后费力,未在意,出院1个月后复查(2018年4月21日):胸部CT提示:左侧可见大量包裹性积液。为进一步诊治,于当日收入我科诊治。
面临第二次左侧大量包裹性胸腔积液处理过程如下:(1)胸水超声提示左侧胸膜腔内见大片状液性暗区,最大深度8.5 cm,暗区内回声不清晰,见大量光点悬浮,较多纤维光带漂浮。在2%利多卡因局部麻醉下行胸腔穿刺术,抽取暗红色胸腔积液量约80 mL,送检病理及培养。因左侧胸腔内被大量纤维光带分割,继续引流失败;(2)为减轻患者呼吸困难及胸痛等临床症状,重点解决引流胸腔积液的问题,经科室主任及医生商讨后,于胸腔引流管内第一次注射尿激酶10万单位加0.9% NaCl 20 mL,并嘱患者适度摇晃身体,让尿激酶充分溶解24 h,次日引流出暗红色胸腔积液量约600 mL。此后500 mL每日1次引流,4 d(4月27日)后共引流暗红色胸腔积液量约2100 mL,复查胸水超声提示左侧胸膜腔内见片状液性暗区,最大深度为4.9 cm,见大量光点及纤维光带,呈分隔状。引流速度减慢,引流时间较前延长,每次量约20~50 mL,为防止胸膜腔粘连;(3)经商讨后第二次注射尿激酶5万单位加用0.9% NaCl 20 mL,4月28日引流暗红色胸腔积液量约500 mL,胸膜腔内溶解纤维光带成功。接下来两日引流暗红色胸腔积液量共约2500 mL。5月3日第三次行胸水超声检查提示左侧胸膜腔内未见液性暗区。患者因血性恶性包裹性胸腔积液两次胸膜腔内注射尿激酶,成功引流血性胸腔积液量共约4600 mL,全程患者均无发热等不适症状,呼吸困难及胸痛症状明显减轻;(4)该患者于5月7日拔出胸腔引流管,穿刺点处无化脓及红肿,拔出引流管顺利,局部消毒、包扎、固定。复查胸部CT提示左肺下叶病灶未见明显变化(左肺下叶背段可见一21 mm×26 mm不规则软组织肿块影),左侧肺部复张良好,左侧胸膜略增厚,左侧胸腔未见液性暗区。
整个胸腔积液处理过程中患者一直规律服用吉非替尼片,5月8日办理出院手续。出院后1、2、3、6、12个月随访中,最后一次随访时间为2019年8月,患者身体状态良好,复查胸部CT:左肺下叶背段可见一18 mm×22 mm不规则软组织肿块影,密度不均,边缘可见毛刺,左侧未见胸腔积液,左肺下病灶较前略缩小,见图3。

图3 胸腔闭式引流的日引流量(mL)
3 讨 论
肺癌最常见的类型是非小细胞肺癌(NSCLC)。NSCLC的平均确诊年龄为 70 岁,5年总生存率为17%[9]。多数患者发现时已经处于中晚期,肿瘤细胞已经发生浸润转移,从而造成治疗的失败。晚期NSCLC虽然失去了手术机会,但是基因靶向治疗、抗血管治疗、免疫治疗等个体化治疗方案带给患者了福音。表皮生长因子受体(epidermal growth factor receptor,EGFR)是当前非小细胞肺癌靶点突变率较高的,应用最广泛的靶点之一。EGFR是一种跨膜受体,传递胞外信号到胞内的重要蛋白,磷酸化的配体通过激活PI3K/AKT/mTOR、RAS/RAF/MAPK和JAK/STAT信号传导途径起作用,这可能导致肿瘤增殖、迁移、转移和抑制细胞凋亡[10]。EGFR突变主要包括4种类型:18、19、20、21外显子点突变。最常见的EGFR突变为19外显子缺失和21外显子L858R突变[11]。表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)在 NSCLC个体化分子靶向治疗的发展历程中具有里程碑式的意义。代表药物主要包括一代吉非替尼和厄洛替尼,二代阿法替尼和达克替尼,三代奥西替尼。奥西替尼可透过血脑屏障,是中枢神经系统(CNS)活性药物,可有效地抑制EGFR-TKIs T790m阳性突变,可作为晚期NSCLC疾病进展或脑转移患者的可靠选择方案[12]。本例患者为中老年男性,吸烟40余年,诊断肺腺癌晚期IV期,胸腔积液检测结果为EGFR 21(L858R)基因突变,第一时间采取一线靶向药物吉非替尼治疗,治疗约17个月。刘玉涛等人[13]研究分析了255名单纯化疗的晚期肺腺癌患者和255名吉非替尼治疗的晚期肺腺癌患者的生存率,结果显示中位生存时间(MST)为22.8个月(95%CI,20.7~24.9)月,接受吉非替尼治疗患者的MST明显长于单纯化疗患者的MST(33.5个月vs 14.1个月,P<0.001)。
Froudarakis研究提示 EGFR 基因突变多发生在恶性胸水脱落肿瘤细胞中,而 KRAS 突变更常发生在原发肿瘤细胞中[14-15]。肺腺癌晚期也可产生大量包裹性MPE,其原因是癌细胞转移至壁层胸膜,且渗出速度快,纤维蛋白含量高,沉积于胸膜腔,在胸膜脏层与壁层间形成网格状粘连,形成“纤维苔素”,多成囊状分割,并且粘稠不易抽出,有时大量渗出的纤维蛋白牵拉胸膜、胸壁,导致胸廓塌陷。因此,在肺癌晚期包裹性MPE的引流成为临床诊治的难点。非小细胞肺癌产生MPE的具体机制尚未完全明确可能与肿瘤生成血管内皮生长因子(VEGF)有关。贝伐株单抗联合卡铂和紫杉醇治疗NSCLC,可以明显的延长患者的生存期。尿激酶属于纤维蛋白溶解剂,可以有效催化并裂解纤溶酶,纤溶酶在一定程度上可有效溶解胸腔积液中大量纤维蛋白,起到充分引流的作用。一般剂量为10~20万单位,胸膜腔内给药,无出血倾向,无发热。尿激酶用于结核性包裹性胸腔积液治疗报道较用于恶性胸腔积液的报道多。对于晚期肺癌包裹性胸腔积液,杨芳伟[16]等利用尿激酶联合博来霉素进行胸腔内给药安全有效,副作用小。该患者因包裹性胸腔积液,严重影响患者的生活质量,先后应用2次应用尿激酶10万单位和5万单位,胸腔积液引流良好,有效溶解纤维蛋白,充分引流胸腔积液,无出血等倾向。
综上所述,该患者做到了肺癌诊断新模式即:“影像诊断+病理诊断+分子诊断”。患者住院后医生第一时间获得了病理学资料,明确诊断肺腺癌,经胸水分子靶向检测明确为EGFR外显子21(L858R)基因突变,予吉非替尼EGFR-TKI一线靶向治疗,同时予尿激酶局部胸腔内给药,有效解除粘连包裹性胸腔积液,随访时间约17个月,患者体力状态(performance status,PS)评分为0~1分,状态良好,定期随访中,T790检测结果为阴性,头CT未见转移病灶,国家已免费发放,减轻家庭的经济负担,并且避免了应用全身化疗药物导致的不良反应,提高了患者的依从性及生活质量。

