血管内超声在左主干病变介入治疗中的临床应用
王 博,袁 驰,汪和贵,柯永胜
(1.铜陵市人民医院心内科,安徽 铜陵 244000;2.皖南医学院第一附属医院心内科,安徽 芜湖 241000)
球囊和裸金属支架(Bare metal stent,BMS)时代,冠状动脉旁路移植术一直作为左主干病变患者的首选治疗方式,指南上作为Ⅰa类推荐[1]。随着PCI技术的完善和器械的不断升级,有越来越多研究证实左主干病变患者行PCI治疗的安全性和有效性得到了明显提升[2]。2018年的欧洲指南将PCI作为SYNTAX评分为低危(≤22分)的左主干病变患者的Ⅰ类推荐[3]。与冠脉造影(Coronary argiography,CAG)相比,IVUS检查能实时提供冠脉的管腔和管壁的横截面图像,能更有效帮助评估靶血管的病变特点,优化策略,评估支架的贴壁情况。通过虚拟组织学超声(VH-IVUS)还能识别易损板块,对判断冠心病患者的预后以及指导和优化治疗方案有着重要的意义[4]。因此近年来许多学者建议在PCI术中使用IVUS指导,尤其推荐在左主干病变PCI术中使用IVUS指导[5-7]。本研究旨在进一步明确IVUS指导对左主干病变PCI的临床决策、术后即刻效果及临床预后的影响。通过虚拟组织学超声识别“易损斑块”,评估IVUS对含有“易损斑块”的左主干病变PCI术后的影响。
1 资料与方法
1.1 一般资料回顾性分析于2012年1月1日至2016年1月1日间皖南医学院第一附属医院收住的冠状动脉左主干病变并接受PCI治疗的患者共76例。所有患者经冠脉造影和(或)IVUS检查均符合美国指南推荐的冠脉左主干病变介入治疗指证[1]。入选标准:(1)IVUS检查,左主干最小管腔面积(Minimum lumen area,MLA)<6.0 mm2;(2)最小管腔直径(Minimum lumen diameter,MLD)<2.8 mm;(3)定量冠状动脉造影(Quantitative coronary angiography,QCA)提示:管腔直径狭窄率>50%。排除标准:(1)SYNTAX评分≥33分;(2)左室射血分数<50%;(3)由导管造成的左主干损伤需要紧急植入支架。分组方法:依据患者术中是否行IVUS检查将入选患者分成两组,IVUS组(n=29):患者术中行IVUS检查;造影组(n=47):患者术中未行IVUS检查,而是使用常规造影指导。IVUS组患者依据左主干病变是否含有易损斑块再分成两个亚组。易损斑块定义为:病变血管斑块负荷>40%,坏死核心占整体斑块面积10%以上而且靠近管腔,并至少在3个连续的横断面出现。易损斑块组(n=12):VH-IVUS识别的左主干病变含有易损斑块的患者;非易损斑块组(n=17):VH-IVUS检查左主干病变不含易损斑块的患者。术中植入支架均为DES。所有患者均在术前服用阿司匹林(负荷量300 mg)和氯吡格雷(负荷量300 mg)。术后联合使用阿司匹林(100 mg/d)和氯吡格雷(75 mg/d)抗血小板治疗至少1年。所有患者术前均签署知情同意书,本研究通过本院伦理委员会批准。
1.2 手术策略所有患者的造影影像均由至少两名有冠脉介入资质的医生使用QCA软件对病变血管相关参数进行测量和分析。检测指标包括:PCI术前靶病变长度、MLD、管腔直径狭窄率、MLA。支架植入后MSD、MSA。由术者根据病变血管进行评估后自行决定是否进行IVUS检查。IVUS检查使用Volcano Corp公司生产的血管内超声成像系统,采用40 MHz血管内超声导管。检查时采用5 mm/s的速度回撤超声导管并实时记录影像数据。IVUS检测指标包括:术前MLD、MLA,术后MSD、MSA,外弹力膜(Extermal elastic membrane,EEM)直径和面积。计算斑块横截面积(EEM横截面积-管腔横截面积)、斑块负荷(斑块横截面积/EEM横截面积)、膨胀指数(最小支架横截面积/正常参考段管腔横截面积)、对称指数(最小支架直径/最大支架直径)和重构指数(病变段EEM横截面积/正常参考段EEM横截面积)。正性重构定义为重构指数>1.05,负性重构定义为重构指数<0.95。当发现存在严重的残余狭窄、支架膨胀不全和贴壁不良时,应进一步处理直到获得满意效果为止。发现支架边缘血管夹层或支架未能完全覆盖病变时,应植入额外的支架使病变或夹层完全覆盖为止。植入支架后发现支架边缘血管夹层或斑块脱垂,应植入额外的支架使夹层完全覆盖和(或)术后增加抗栓强度,如:增加抗血小板药物用量,使用低分子肝素或Ⅱb/Ⅲa受体拮抗剂。
1.3 研究终点和定义研究的主要终点为1年内主要心血管不良事件发生率,包括:心源性死亡、心肌梗死(Myocardial infarction,MI)和靶血管血运重建(Target vessel revascularization,TVR)。除尸检或临床证实是非心源性死亡外,所有的死亡类型均被认为是心源性死亡。MI定义为典型心肌梗死临床表现且肌酸激酶同工酶(Creatine kinase MB,CK-MB)大于3倍的正常值上限,伴或不伴心电图改变。TVR定义为左主干、前降支、回旋支任何部位的再次血运重建。
1.4 统计学方法使用SPSS 18.0软件进行统计。计量资料呈正态分布的采用“均数±标准差”表示,组间比较行t检验;计量资料呈非正态分布的采用中位数(四分位间距)表示,组间的比较采用秩和检验(Mann-Whitney U检验)。计数资料采用率或百分比表示,组间采用卡方检验或Fisher确切概率法进行比较。术后随访的各终点事件采用Kaplan-Meier生存曲线分析和log-rank检验比较组间差异。所有检验均以P<0.05为差异有统计学意义。
2 结果
2.1 临床基线特征IVUS组在男性比例和吸烟史比例方面大于冠脉造影组,其余临床基线特征方面,两组相比无统计学差异。见表1。

表1 IVUS组和冠脉造影组患者的基线特征
2.2 冠脉造影的特点IVUS组和冠脉造影组患者病变血管特点无统计学差异(P>0.05)。见表2。

表2 IVUS组和冠脉造影组患者的病变特点
2.3 IVUS组和冠脉造影组的手术策略IVUS组患者术后即刻MSD和MSA大于冠脉造影组[(3.9±0.3)mm vs (3.7±0.3)mm,P=0.004;(12.2±2.1)mm2vs(10.9±1.6)mm2,P=0.003],其余两组患者在Ⅱb/Ⅲa受体拮抗剂、预扩张、左主干支架数目、支架长度、左主干末端双支架术等策略方面差异,均无统计学意义。见表3。

表3 IVUS组和冠脉造影组患者的手术策略
2.4 易损斑块组和非易损斑块组的IVUS特点易损斑块组的斑块负荷大于非易损斑块组[(79.0%±7.3%) vs (72.2%±6.0%),P=0.010],易损斑块组中正性重构较非易损斑块组多见(66.7% vs 33.3%,P=0.029),其余观察指标方面无统计学差异。见表4。
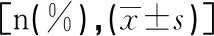
表4 易损斑块组和非易损斑块组患者的IVUS特点
2.5 随访结果
2.5.1 IVUS组和冠脉造影组 所有患者随访1年。IVUS组和冠脉造影组患者的随访结果见表5。患者在术后1年的随访中IVUS组患者MACE事件发生率低于冠脉造影组的趋势,但结果无统计学差异(6.9% vs 19.1%,log-rankP=0.072)。两组患者1年的无MACE事件生存率Kaplan-Meier曲线见图1。IVUS组患者死亡率低于冠脉造影组的趋势,但结果也无统计学差异(0.0% vs 8.5%,log-rankP=0.080)。两组患者在术后1年的心肌梗死、靶血管血运重建发生率方面无明显的统计学差异(0.0% vs 2.1%,log-rankP=0.335;6.9% versus 10.6%,log-rankP=0.349)。Cox回归分析未发现性别、年龄、吸烟史、糖尿病、高血压和高脂血症是患者终点事件的危险因素。
2.5.2 易损斑块组和非易损斑块组 易损斑块组合非易损斑块组患者的随访结果见表5。1年的随访中两组患者的MACE事件发生率相似,无统计学差异(8.3% vs 5.9%,log-rankP=0.702)。
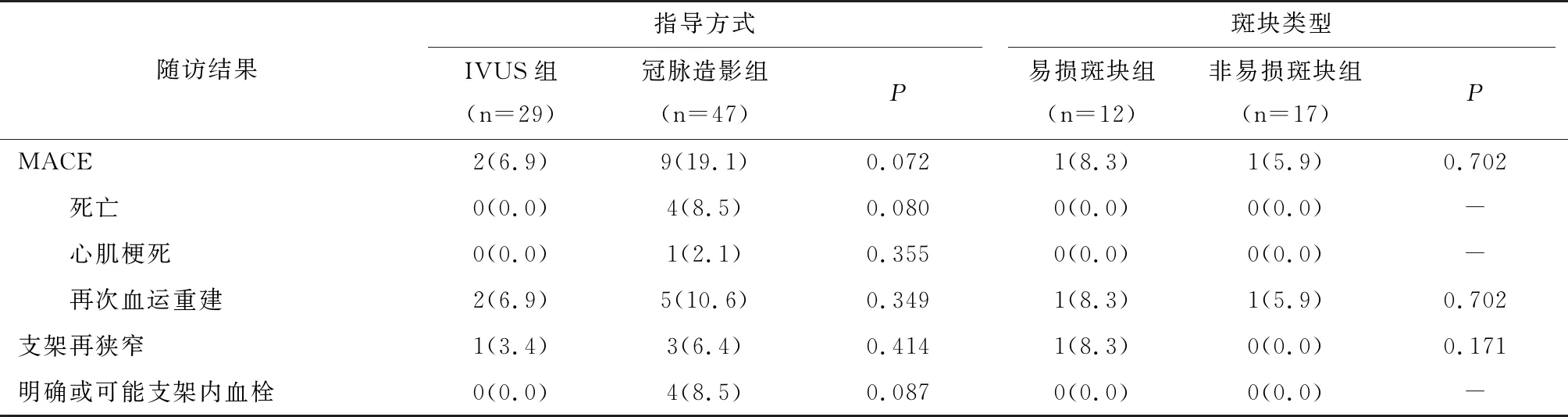
表5 各组患者的随访结果[n(%)]

图1 IVUS组和冠脉造影组患者PCI术后1年无MACE事件生存率曲线(Kaplan-Meier曲线)
3 讨论
目前,IVUS是否能提高左主干病变PCI的临床预后仍不明确[1,8]。早期的研究显示IVUS指导不会降低左主干病变PCI术后6个月内支架内再狭窄的发生率[9]。近年的一项Meta分析显示,IVUS指导与冠脉造影指导相比能减少患者MACE事件和支架内血栓的发生[10]。另一项研究发现IVUS指导的左主干患者围手术期心肌坏死标志物升高比冠脉造影指导更明显,这显示IVUS指导会增加术中侵入性的操作[11]。还有研究认为IVUS指导能仅减少左主干病变患者PCI术后3年的死亡率但不会降低患者术后心肌梗死和靶血管血运重建的发生率[5]。以上研究均不能充分证实IVUS能优化左主干患者术后的预后。既往研究表明左主干患者PCI术后术后即刻MLA是手术远期预后的最重要的独立预测因素。术后即刻MLA越大,远期再狭窄率越小[12]。本研究中IVUS组患者术后即刻MLA大于冠脉造影组[(12.2±2.1)mm2vs(10.9±1.6)mm2,P=0.003]可能与IVUS组MACE事件发生率趋势更低有相关性(6.9% vs 19.1%,log-rankP=0.072)。
大多数急性冠脉综合症(Acute coronary syndrome,ACS)患者发病的病理基础是易损斑块破裂出血导致血栓形成。既往研究报道左主干病变的ACS患者PCI术后MACE事件风险较非ACS患者明显增加。ACS是左主干患者PCI术后MACE事件的独立预测因子[HR:1.84,95%CI(1.30,2.60),P=0.0006][7]。本研究中易损斑块组和非易损斑块组的MACE事件发生率均较低且无明显的统计学差异(8.3% vs 5.9%,log-rankP=0.702)。因此,IVUS指导不增加含有易损斑块的左主干病变PCI患者的MACE事件的发生风险,但具体机制还不甚明了。既往非左主干血管的IVUS研究发现易损斑块在植入支架时更易导致组织脱垂,而严重的组织脱垂与支架再狭窄和早期支架血栓形成密切相关[13]。另外当支架边缘存在易损斑块时,释放支架后易引起斑块破裂导致支架边缘血管夹层,而目前的研究认为,支架边缘血管夹层是早期支架内血栓和支架再狭窄的预测因子[14]。因此,一方面IVUS可能通过准确的支架定位并选取合适长度的支架完全覆盖斑块,而减少支架边缘血管夹层的发生,另一方面IVUS可能通过及时识别出已出现的支架边缘血管夹层,而采取植入额外的支架等措施对夹层进一步处理来优化即刻效果。本研究中易损斑块组患者未发现支架边缘血管夹层和组织脱垂,可能是IVUS指导不增加易损斑块组患者PCI术后MACE事件风险的原因之一。
综上所述,IVUS指导与冠脉造影指导相比有减少左主干病变患者PCI术后1年的MACE事件发生率的趋势,值得临床推广。与非易损斑块组相比,IVUS指导未增加易损斑块组患者PCI术后1年MACE事件的发生风险。本研究可能由于样本量小,IVUS组和冠脉造影组随访的主要终点事件相比较,结果无明显统计学差异,研究结论有待后续通过大样本随机对照研究的进一步支持。

