高中化学教学中微型实验的开发与研究
◇ 甘肃 交巴才旦
化学教学中最重要的是实验,因为实验能将枯燥的教材知识生动地表现出来,可激发学生学习的主动性.但是教材中有些化学实验比较烦琐,且有一定危险性,需要改进.基于此,教师要多进行微型实验开发与运用的教研,令实验过程更加环保、简单、安全,弥补当前教学中的不足.
1 微型实验的开发原则
1.1 科学性原则
科学性是设计高中化学实验的第一步,也是确定微型实验是否成功的主要依据.实验设计主要依靠实验现象与记录结果,最终得出科学的结论.例如,检验苯酚的微型实验设计中,可以用苯酚钠与人们呼出的二氧化碳反应进行测试.实验过程为:往苯酚钠溶液中吹气,实验现象为溶液可能变浑浊.虽然此实验也能观察到实验现象,但是因为课堂教学时间有限,有些教师将实验进行了改进:吹气前用吹气玻璃管接触苯酚钠溶液,再蘸少量稀盐酸,然后再吹气,发现苯酚钠溶液立刻变浑浊,此过程虽然效果明显,但是此实验没有遵循科学性原则,即稀盐酸溶液影响实验结果,且改进后的实验只能说明苯酚是弱酸,不能说明其酸性比碳酸弱.
1.2 安全性原则
化学微型实验的设计,需以安全为前提,要保障师生的安全、实验环境的安全.教师设置实验的时候,要多考虑实验过程是否存在危险,并采取措施尽量避免这些危险.另外,还要禁止一些可能发生危险的操作.例如,稀释浓硫酸的时候,要严格按照实验要求操作,要将浓硫酸缓缓倾倒入水中,严禁顺序发生变化,否则会出现危险,令实验者受伤.再如实验过程中需检测气体纯度,不能不检验纯度就直接点燃气体,否则会有爆炸的危险.
2 微型实验的开发案例
2.1 离子检测的微型实验设计
高中教材中关于二价与三价铁离子的描述较多,涉及各自的性质、转换和除杂等内容也较多.关于此知识点考查的题型有很多,如涉及化学方程式、离子方程式、实验过程与现象等.有文字方面的描述,也有实验操作方面的内容.且这一知识点在高考中频频出现,不但是因为铁元素在化学领域中占有重要的位置,还因为铁在生活生产中有举足轻重的作用.所以教师可以设计关于Fe2+和Fe3+的微型实验.
图1为检验Fe2+和Fe3+的常规实验,通过沉淀法进行检测,Fe2+和OH-反应,产生Fe(OH)2沉淀,因为Fe2+还原性很强,且容易被氧化,因此产生的白色沉淀在空气中很快就会变成红褐色.此为传统实验的缺陷,很多教师为了解决这一问题,在课堂教学中对实验做了简单的改进,例如,在反应前,在氢氧化钠溶液中加入苯,因为苯不溶于水且密度小于水的特点,在实验中起阻隔空气的作用.但是本次实验关于Fe2+的性质检验比较单一,如果要继续讨论Fe2+和Fe3+的检测与鉴别,还要使用其他药品和实验仪器.为了保障学生实验的安全性,保证实验科学性,教师可让学生自主合作,完成微型实验的设计与改进,进而更好地激发学生的学习兴趣,让学生在化学实验过程中,感受化学的魅力.本次改进实验需要的药品有稀H2SO4溶液、FeSO4溶液、NaOH 溶液、氨水、铁粉、煤油及KSCN 溶液.实验仪器有试管、导管、胶头滴管等,实验装置如图2 所示.实验步骤:第1 步,组装仪器,在A 试管中加入FeSO4溶液,同时加入少量的铁粉防止二价铁离子被氧化,接着使用三孔胶塞塞好.在B试管中装入煤油与KSCN 溶液.第2步,在A 试管中滴入稀硫酸排出试管中的空气,然后滴入NaOH 溶液观察实验现象,此过程产生白色沉淀,然后观察试管B的颜色变化.实验结束后再向试管B 中滴入氯水,观察颜色变化.

图1 常规实验装置

图2 微型实验改进装置
在实验过程中有很多细节值得学生深思,经常引导学生对实验进行改进,是对其化学学习能力的培养,可以顺利将新知识运用于实际解决问题的过程中,加强对知识的运用与理解.该实验中值得深思的细节有:1)为什么在A 试管中加入铁粉? (为了避免二价铁离子被氧化.)2)该实验中的Fe2+和Fe3+的转化,为什么先加入KSCN 溶液的目的是确定B 试管中是否有三价铁离子,然后加入氯水(为了观察二价铁离子是否被氧化).3)B 试管中为什么要放入煤油? (是为了使实验更科学、严谨,避免空气进入影响实验效果.)改进后的实验,不但能检测铁离子,还能实现二价与三价铁离子之间的转换,提升学生思考的整体性.另外多种药品的使用便于学生思考多种物质间的反应,还能节省药品,让学生在实验中养成节约的意识,发挥微型实验设计的环保性.若站在知识的传输方面,此类实验的设计,也便于学生更好地学习Fe2+和Fe3+的性质与转化.
2.2 性质检测的微型实验设计
以“氯气的制取与性质”为例,教学目标为:学生通过实验与学习,了解氯气的性质;在实验中提升学生的探究兴趣,提升学生的学习能力,养成正确的学习方法,并为后期学习元素周期表提供基础.氯元素对学生来说很熟悉,在生活中经常遇到,如食用盐中主要元素就是氯,所以在学习前,学生会对此部分内容产生亲切感,能有效降低探究难度.另外高中生已经有自己一套独特的学习方法与思路,且具备一定实验能力,对于教师教学很有帮助.氯气在人们生活中有重要的利用价值,但是氯气自身有毒,所以为了保证师生安全,教学过程中关于此部分的实验都是通过播放实验视频或者教师单方面的演示完成的,这样使学生学习积极性降低.所以开发设置相关微型实验很有必要.图3是制取与探究氯气性质的常规装置,可以训练学生基础仪器与药品的使用.但是从整体实验装置上分析,装置过于烦琐,药品用量大,产生尾气过多,在实验过程中还会有危险性.

图3 制取氯气与性质探究常规实验装置
教师往往将本次实验课设置为演示课,虽然在课堂教学中教师反复强调基本操作步骤,但是学生不能很好地提升操作技能.因此设计微型实验,弥补了这一缺点,且通过操作简单、直观、安全等优势,锻炼学生的动手能力.微型实验中需要的药品为:浓盐酸、红纸条、高锰酸钾、淀粉KI试纸、溴化钠试纸、石蕊试纸、氢氧化钙颗粒等,实验装置如图4所示.
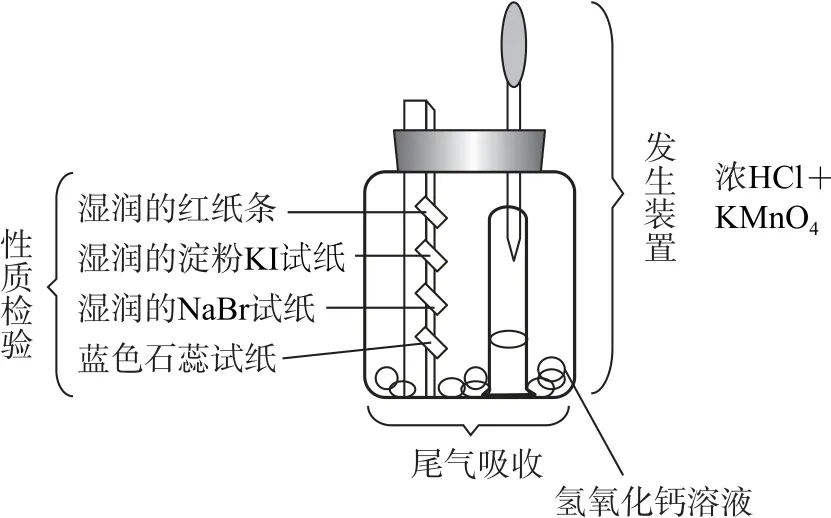
图4
实验步骤为:首先,教师带领学生组装实验装置,并加入药品.找1个250mL的空饮料瓶,清洗干净并干燥后,在瓶盖处打2 个小孔,先装入50 mL Ca(OH)2溶液,并挑选长度适合的玻璃棒,一侧穿入小孔中,玻璃棒固定后,从上往下以此粘贴试纸(湿润红纸条、淀粉KI试纸、溴化钠试纸与石蕊试纸.瓶盖的另一个小孔放置装有浓盐酸的胶头滴管.另取一只试管,装入5g高锰酸钾,并固定在空饮料瓶中,将瓶盖拧紧.其次,学生捏胶头滴管,令其中的浓盐酸滴出,发生化学反应,产生黄绿色的气体,随着气体量的增多,逐渐逸出试管,进入饮料瓶,此时观察玻璃棒中多个试纸的颜色变化.最后,将试纸的变化记录下来,实验后产生过量的氯气,通过瓶中的氢氧化钙吸收,完成尾气的处理.
高中化学课堂教学中,经常出现这样一种情况,就是教师传递的知识与学生可以接受的内容失衡,进而使得本来就“死气沉沉”的化学课更加雪上加霜.借此,在课堂中运用实验,并让学生动手操作,可以优化教学方法,活跃课堂氛围.本次微型实验设计的优点有:1)学生可以参与到传统实验装置的改进中,在形成新的实验装置图时,培养了学生的创新与动手能力.2)微型实验课令学生更直观观察实验现象,进而深刻记忆氯气的化学性质,便于运用.3)随着实现现象明显地呈现出来,便于学生以小组的形式分析并讨论,以此加强对氧化还原反应的理解.4)经过本次微型实验的优化,保证氯气不会外漏,更加安全环保.
微型实验的设计与运用,需要每名学生都参与其中,进而令化学课堂不再“死气沉沉”,而是“其乐融融”,在生生之间、师生之间有更好的交流与沟通.以此锻炼学生的化学思维,做到真正的教学相长.

