完全腹腔镜经食管裂孔修补联合空肠营养造口术治疗自发性食管破裂1例报告
廖健南 区小卫 谢 宏 程 飞 吴显博
(广州中医药大学附属佛山临床学院 佛山市禅城区中心医院普通外科,佛山 528000)
自发性食管破裂(spontaneous esophageal rupture, SER)是少见的外科急重症之一,病死率高,手术是首选的治疗方法,但没有标准的手术入路和手术方式。传统手术方式为经左胸入路行食管破口修补、左胸及纵隔清创引流术,但经胸入路手术对这种危重病人创伤和术后心肺功能影响大,不利于患者术后快速康复。随着腹腔镜经食管裂孔入路(transesophageal hiatus approach,THA)在食管胃结合部手术的成功应用,该手术入路为SER的手术治疗开拓了新的思路。2020年3月我科采用完全腹腔镜THA修补联合空肠营养造口术成功治疗1例SER,现报道如下。
1 临床资料
男,67岁,因上腹痛2 d,加重3 h于2020年3月6日急诊入院。患者2 d前出现上腹部隐痛,阵发性加剧,伴有恶心、呕吐(呕吐白色胃内容物)。入院3 h前患者剧烈呕吐后突发胸前剧烈疼痛并呼吸困难。入院后查体:体温38.1 ℃,呼吸35次/min,脉博140次/min,血压105/62 mm Hg。神清,呼吸急促,双肺呼吸音减弱,上腹部膨隆,可见胃型,上腹部腹肌紧张,上腹部压痛、反跳痛,未触及包块,肝脾肋下未触及肿大,肝肾区无叩痛,移动性浊音阴性,肠鸣音减弱。急诊查血常规:白细胞8.0×109/L,中性粒细胞百分比57.9%,中性粒细胞绝对数4.6×109/L。由于患者胸痛剧烈,术前未行上消化道造影检查,上腹部增强CT示:纵隔-小网膜囊大量包裹性积液、积气,纵隔气肿,考虑食管下段破裂,双下肺炎症、双侧胸腔积液(图1)。既往有胃病史,间断口服药物治疗,无手术史。
根据术前上腹部增强CT表现(纵隔-小网膜囊大量包裹性积液、积气),高度怀疑食管下段破裂,有手术探查指征。积极完善术前准备后,入院6 h急诊在全麻下腹腔镜探查。取平卧人字形体位,脐上10 mm trocar作为观察孔,左右上腹肋缘下锁骨中线处分别置入12、5 mm trocar作为主操作孔,剑突下及左肋缘下腋中线处分别置入5 mm trocar作为辅助操作孔。小网膜囊内见咖啡色样积液,超声刀切开小网膜囊及纵隔腹膜,显露食管裂孔,见纵隔内大量食物残渣及咖啡色积液(图2)。吸净积液,显露食管下段,见食管下段右侧壁贲门上约2 cm处有纵行裂口长约3 cm,食管壁稍水肿,未见肿物,见咖啡样胃内容物不断从食管破口处溢出(图3)。术中诊断:①SER;②纵隔积液合并感染。THA修补食管破裂口,纵隔清创引流,空肠营养造口术。先用大量生理盐水冲洗纵隔和上腹部,清除食物残渣及炎症坏死组织,直视下把胃管置入裂口远端,然后用3-0倒刺线全层连续缝合修补食管破口(图4)。再用3-0倒刺线行空肠营养造口,于左侧腋前线trocar引出体外固定(图5)。纵隔处食管两侧分别放置1根双套管及负压球引流。手术时间143 min,术中出血量30 ml。术后入ICU给予呼吸机机械通气、亚胺培南抗感染及纵隔双套管冲洗负压引流,早期肠内营养支持治疗。术后第3天脱离呼吸机并顺利拔除气管插管。复查胸部CT示双侧大量胸腔积液伴双侧肺压迫性肺不张,给予双侧胸腔穿刺置细管引流。术后第5天转普通病房。术后第6天口服碘海醇上消化道造影示:食管下段缝合口通畅,未见造影剂渗漏。术后第7天恢复流质饮食,进食后第3天见纵隔引流管引出泡沫样引流液,口服美蓝引流管引出蓝色液体,证实食管缝合口漏,病人无明显腹痛、气促及发热等不适,体查无腹膜炎,生命体征平稳,考虑漏口小且局限,引流通畅,决定保守治疗,继续禁食、保持纵隔引流通畅及肠内营养支持治疗。术后第26天复查上消化道造影及口服美蓝,证实食管漏口已闭合,逐渐恢复半流饮食后患者无不适,拔除纵隔引流管及空肠造口管,术后34 d出院(图6)。术后3个月复查上消化道造影未见食管下段狭窄及造影剂渗漏,无食道裂孔疝表现(图7)。随访至2020年8月10日(术后5个月),无胸痛、腹痛、腹胀,无吞咽困难、恶心、呕吐及返酸等不适。
2 讨论
SER是指非外伤引起的食管壁全层破裂,又称Boerhaave综合征,为少见的外科急重症之一,起病急,病情重,易误诊,处理棘手,预后差,病死率高达39%[1]。食管破裂部位常发生在食管下段左侧,近胃食管连接处2~3 cm的胸段食管。典型临床症状为胸痛、呕吐和皮下气肿“三联征”,胸部增强CT具有重要的诊断价值,上消化道造影可确诊。目前,SER的治疗方法有手术、内镜下治疗及内科保守治疗,手术仍是目前首选及主要治疗方式,有多种手术入路和方式。
目前,报道较多的手术方式为经左胸入路(开胸或经胸腔镜辅助下完成)、食管破口修补、左胸及纵隔清创引流术。对于发病时间超过12 h,纵隔和胸腔污染重,食管破裂处炎症水肿重不宜行一期修补的患者可行胸段食管切除,食管胃颈部吻合术或胸段食管旷置术[2,3]。但经胸手术对这种危重患者创伤大,即使是胸腔镜辅助小切口手术,也对病人术后心肺功能影响较大,不利于患者渡过危险期,且不便于早期建立肠内营养通路(空肠营养造口)。随着内镜技术的进步,有报道在胃镜下行自膨式带膜金属食管内支架置入术和经皮内镜空肠造瘘术[4,5],再辅予左侧胸腔闭式引流治疗SER,但内镜下治疗虽能暂时堵住食管破口,但无法彻底清除纵隔及胸腹腔内污染物,不利于炎症的控制,且食管支架有扩大食管破口之嫌,不利于食管破口的自然愈合[6]。近年来,国外文献[7~10]报道腹腔镜THA行食管破裂修补术,手术更加微创,术后心肺功能影响更小,病人恢复更快,是一种理想的手术入路。
近年来,我科开展腹腔镜食道裂孔疝修补术、腹腔镜胃上部癌根治术及腹腔镜食管胃结合部腺癌(Serwert Ⅱ型)根治术等,对食管胃结合部区域手术积累一定的手术操作经验。腹腔镜THA行食管破裂修补术国内未见报道,国外文献虽有此手术方式的病例报道,但所报道的病例均未行一期空肠营养造口术建立早期肠内营养通路[7~10]。鉴于本例术前增强CT提示病灶位于食管下段,且炎症坏死组织波及下纵隔及小网膜囊,THA更有利于病变部位的显露及炎症坏死组织的清除引流。因此,我们利用腹腔镜在深部狭小空间视野良好的优势,THA显露纵隔及食管下段,清除纵隔食物残渣、炎症坏死组织,3-0倒刺线行食管破裂口一期缝合,纵隔大量生理盐水冲洗直至干净,术后于纵隔放置双套管引流,术后持续冲洗引流,同期用3-0倒刺线行空肠营养造瘘术建立早期肠内营养通路,术后早期实施肠内营养治疗,减少肠道细菌移位。由于SER手术后禁食时间长,且因食管壁水肿,局部污染严重,术后缝合口漏的概率高,因此,我们特别强调空肠营养造口以建立术后早期肠内营养通路的重要性,即使术后出现食管漏也能经保守治疗治愈。
完全腹腔镜THA修补食管破裂口联合空肠营养造口术的优点包括:①腹腔镜能良好显露破裂的食管下段和下纵隔,既能做到彻底清除纵隔污染物,又能直视下确切修补食管破裂口。②经腹腔镜手术便于一期行空肠营养造口术,建立早期肠内营养通路,利于早期肠内营养实施,加促患者康复。③腹腔镜THA对术后患者肺功能影响小、微创、术后疼痛轻及恢复快。因此,我们认为完全腹腔镜THA修补食管破裂联合空肠营养造口术是治疗SER较理想的手术方式,可供临床治疗选择,特别适用于食管下段破裂且炎症波及下纵隔及小网膜囊的病例。由于本手术入路难予显露中段食管及中纵隔,不适用于中段食管破裂手术,宜选用经胸入路。
腹腔镜THA手术需切开食管裂孔进入纵隔进行操作,势必会破坏食管裂孔的解剖结构,理论上会增高术后食管裂孔疝的发生率。术中可通过重建食管裂孔预防疝的发生,且SER局部炎症重,术后食管裂孔周围形成致密粘连,使食管裂孔疝不易形成。本例术后3个月行上消化道造影未见食管裂孔疝,文献[7,9,10]也未有该手术入路导致食管裂孔疝发生的报道,但需要更多的病例积累及长期的随访资料证实。
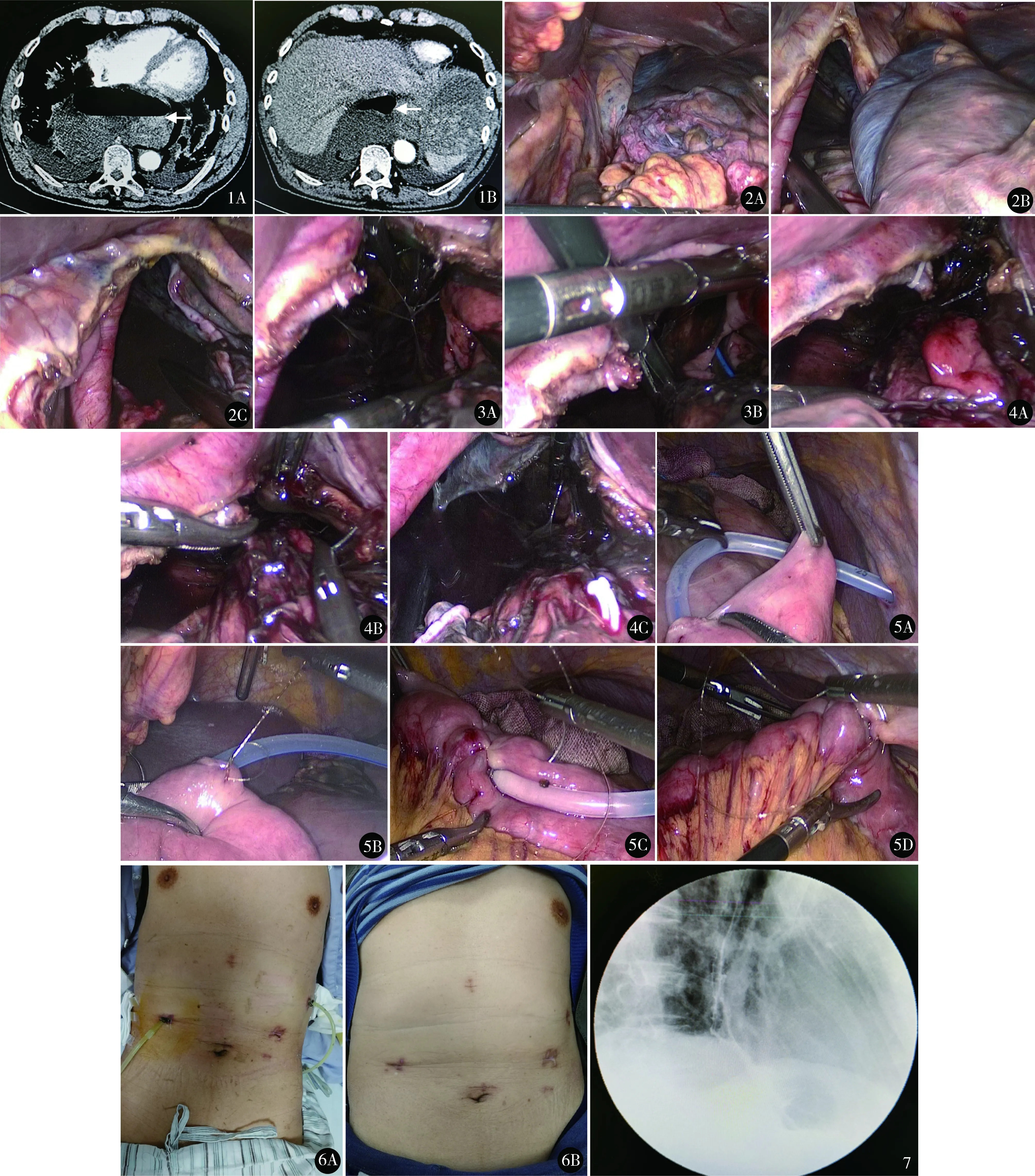
图1 术前胸腹部CT A.纵隔扩张明显,食管下段周围积液积气; B.小网膜囊包裹性积液积气 图2 术中探查小网膜囊及食管裂孔 A.小网膜囊及下纵隔咖啡色样积液积气;B.切开小网膜,见小网膜囊内积液;C.切开食管裂孔腹膜,见下纵隔咖啡色样积液、积气和食物残渣 图3 术中探查见食管下段破裂 A.食管右侧壁全层裂开约3 cm,黏膜外翻;B.直视下把胃管置入破口远端 图4 术中经食管裂孔修补食管破口 A,B.用3-0倒刺线全层连续缝合修补破口;C.食管破口缝合修补后情况 图5 倒刺线1针法空肠营养造口 A.上段空肠切开置入营养管;B.用3-0倒刺线围绕营养管做荷包缝合;C.营养管浆肌层包埋;D.营养管腹壁固定 图6 A.术后引流管及营养管留置情况;B.腹壁切口 图7 术后3个月复查上消化道造影未见食管下段狭窄及造影剂渗漏

