原子荧光光谱仪测定粮食中汞含量的不确定性
怀闪闪,汤有宏,徐小伟,程 伟,郭乾玲,朱娜娜,孙 猛,张 燕
(安徽古井贡酒股份有限公司,安徽亳州 236820)
一切测量结果都不可避免地具有不确定度[1]。不确定度是反映被测量值的分散性,与测量结果相联系的参数[2]。它可以根据测定数据和已有信息来评定,具有可操作性。一个实验分析测试过程需要经历多个分析步骤,经受多种因素的影响,每种因素引入的误差都要传递和反映到最终的测定值上。因此,最后的结果不可避免的具有不确定度,而且这种不确定度是测试过程中所有不确定度的综合。
依据JJF 1059.1—2012《测量不确定度评定与表示》和GB/T 27411—2012《检测实验室中常用不确定度评定方法与表示》两个不确定度相关标准对GB 5009.17—2014《食品安全国家标准食品中总汞及有机汞的测定》(原子荧光光谱分析法)中汞的测量过程进行不确定度分析,找出影响测量过程的不确定度分量来源并进行评定。
1 材料与方法[3]
1.1 材料、试剂及仪器
材料:小麦(国产)。
仪器设备:PL2002 电子分析天平;原子荧光光谱仪(北京瑞利AF-640A);微波消解仪;0.5 mL 移液管;1 mL 移液管;25 mL/50 mL/100 mL 容量瓶;控温电热板。
试剂:硝酸(HNO3),优级纯;盐酸(HCl),优级纯;硼氢化钾,分析纯;氢氧化钾,分析纯。
1.2 检验方法
1.2.1 样品制备
称取固体试样小麦0.5 g(精确到0.001 g)于消解罐中,加入5 mL 硝酸,加盖放置过夜,旋紧罐盖,按照微波消解仪的标准操作步骤进行消解,冷却后取出,缓慢打开罐盖排气,用少量水冲洗内盖,将消解罐放在控温电热板上,于80 ℃加热,赶去棕色气体,取出消解液转移至25 mL 塑料容量瓶中,用少量水分3 次洗涤内罐,洗涤液合并于容量瓶中并定容至标线,混匀,待测。同法制备空白试样。
1.2.2 方法原理
试样经酸加热消解后,在酸性介质中,试样中汞被硼氢化钾还原成原子态汞,由载气(氩气)带入原子化器中,在汞空心阴极灯照射下,基态汞原子被激发至高能态,再由高能态回到基态时,发射出特征波长的荧光,其荧光强度与汞含量成正比,与标准系列溶液比较定量。
1.2.3 配制标准曲线
1.2.3.1 试剂配制
盐酸溶液(2%):量取20 mL 硝酸,缓慢加入到980 mL水中,混匀。
硼氢化钾溶液0.05 %(w/v)溶液:(a)称取2 g氢氧化钾溶于约50 mL 去离子水,加入1 g 硼氢化钾并使其溶解,用去离子水稀释至100 mL,摇匀。此溶液为1 % KBH4。(现用现配);(b)称取2 g 氢氧化钾溶于200 mL 去离子水,加入1%KBH4溶液50 mL,用去离子水稀释至1000 mL,摇匀。此溶液为0.05%KBH4。(现用现配)。
硝酸溶液(1+9):量取硝酸50 mL 缓缓加入到450 mL水中。
1.2.3.2 标准溶液配制
汞标准储备液(10 μg/mL)。
汞标准中间液(100 μg/L):准确吸取汞标准储备液(10 μg/mL)1.00 mL 于100 mL 容量瓶中,用含有0.5 %重铬酸钾的5 %的硝酸溶液定容至刻度,混匀。
汞标准系列溶液:分别吸取汞标准中间液(100 μg/L)0.00 mL、0.10 mL、0.25 mL、0.50 mL、0.75 mL、1.00 mL 于50 mL 容量瓶中,用硝酸溶液(1+9)稀释至刻度,混匀。此汞标准系列溶液的质量浓度分别为0.00 μg/L、0.20 μg/L、0.50 μg/L、1.00 μg/L、1.50 μg/L和2.00 μg/L。
1.2.4 数学模型
试样中汞的含量按式(1)计算:
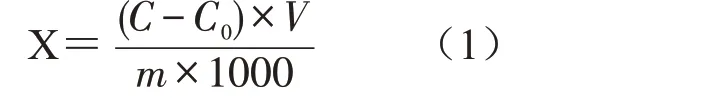
式中:X——试样中汞的含量,mg/kg;
C——供试品溶液中汞的含量,μg/L;
C0——试剂空白溶液中汞的含量,μg/L;
V——样品定容体积,mL;
m——样品质量,g。
2 不确定来源分析
根据数学模型分析及方法简述,可知小麦中汞的测定不确定度来源于以下几个分量。
(1)汞标准溶液引入的相对标准不确定度ur(C);
(2)试样处理引入的相对标准不确定度ur(V);
(3)试样重复性检测引入的相对标准不确定度ur(S);
(4)原子吸收光谱仪引入的相对标准不确定度ur(A);
则有:

3 不确定度分量的评定
3.1 标准溶液引入的相对标准不确定度ur(C)
3.1.1 标准溶液配制
汞标准储备液(10 μg/mL)。
汞标准中间液(100 μg/L):准确吸取汞标准储备液(10 μg/mL)1.00 mL 于100 mL 容量瓶中,用含有0.5 %重铬酸钾的5 %的硝酸溶液定容至刻度,混匀。
汞标准系列溶液:分别吸取汞标准中间液(100 μg/L)0.00 mL、0.10 mL、0.25 mL、0.50 mL、0.75 mL、1.00 mL 于50 mL 容量瓶中,分别加入硝酸溶液(1+9)稀释定容至标线,混匀。此汞标准系列溶液的质量浓度分别为0.00 μg/L、0.20 μg/L、0.50 μg/L、1.00 μg/L、1.50 μg/L 和2.00 μg/L。
3.1.2 标准溶液配制引入的不确定度ur(C)
汞标准溶液引入的相对标准不确定度ur(C)主要来源于标准溶液本身及配制过程引入的相对标准不确定度,结合标准溶液配制方法可知,标准溶液引入的相对标准不确定度来自于3个分量:
(1)汞标准储备液(10 μg/mL)引入的相对标准不确定度ur(C0);
(2)汞标准中间液(100 μg/L)引入的相对标准不确定度ur(C1);
(3)汞标准系列溶液引入的相对标准不确定度ur(C2)。
3.1.3 汞标准储备液(10 μg/mL)引入的相对标准不确定度ur(C0)
国家标准样品编号8500-6940-Hg,质量浓度10 μg/mL,有效期为2020 年11 月30 日,其证书上给出相对扩展不确定度为0.7%,K=2。则有:
ur(C0)=0.007/2=0.0035
3.1.4 汞标准中间液(100 μg/L)引入的相对标准不确定度ur(C1)
来自于3 个分量:汞标准储备液(10 μg/mL)引入的相对标准不确定度ur(C0)、1.00 mL 移液管引入的相对标准不确定度ur(V1)和100 mL 容量瓶引入的相对标准不确定度ur(V2)。
(1)汞标准储备液(10 μg/mL)引入的相对标准不确定度ur(C0)=0.0035
(2)1 mL移液管引入的相对标准不确定度ur(V1):
1 mL 移液管引入的相对标准不确定度ur(V1)来自两个分量:
(a)移液管的容量引入的标准不确定度u(V11)
1 mL A级移液管的容量允许偏差为±0.007 mL,按均匀分布有:

(b)移液管温度变化引入的标准不确定度u(V12)
设温度变化为±5 ℃,20 ℃时水的膨胀系数α=2.1×10-4/℃,按均匀分布,则有:
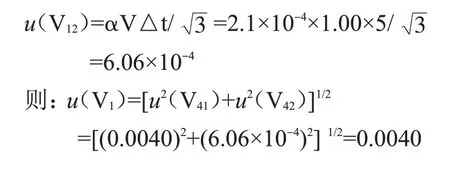
1 mL 移液管引入的相对标准不确定度为:
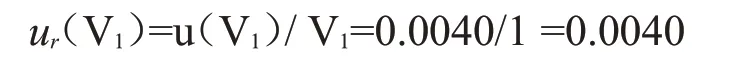
(3)100 mL 容量瓶引入的相对标准不确定度ur(V2)来自两个分量:
(a)容量瓶的容量引入的不确定度u(V21)
100 mL 容量瓶的容量允许偏差为±0.10 mL,按均匀分布有:

(b)容量瓶温度变化引入的不确定度u(V22)
设温度变化为±5 ℃,20 ℃时水的膨胀系数α=2.1×10-4/℃,按均匀分布,则有:
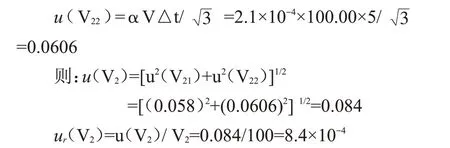
所以汞标准中间液(100 μg/L)引入的相对标准不确定度ur(C1)为:

3.1.5 汞标准系列溶液引入的相对标准不确定度ur(C2)
来自于3 个分量:汞标准中间液(100 μg/L)引入的相对标准不确定度ur(C1),1.00 mL 移液管引入的相对标准不确定度ur(V1)和50 mL 容量瓶引入的相对标准不确定度ur(V3)。
(1)汞标准中间液(100 μg/L)引入的相对标准不确定度ur(C1)=5.38×10-3;
(2)1.0 mL 移液管引入的相对标准不确定度ur(V1)=0.0040;
(3)50 mL 容量瓶引入的相对标准不确定度ur(V3)来自两个分量:
(a)容量瓶的容量引入的不确定度u(V31)
50 mL 容量瓶的容量允许偏差为±0.05 mL,按均匀分布有:
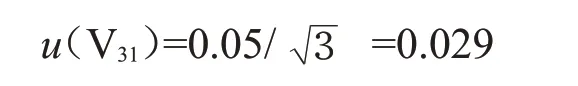
(b)容量瓶温度变化引入的不确定度u(V32)
设温度变化为±5 ℃,20 ℃时水的膨胀系数α=2.1×10-4/℃,按均匀分布,则有:

表1 样品测定结果
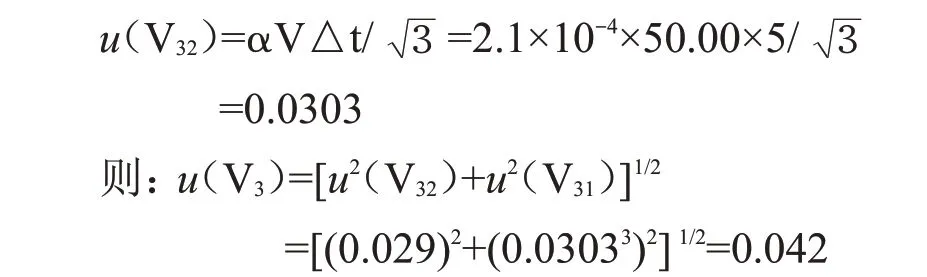
故50 mL容量瓶引入的相对标准不确定度ur(V3):
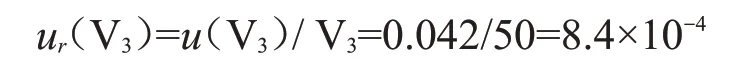
所以汞标准系列液引入的相对标准不确定度ur(C2)为:
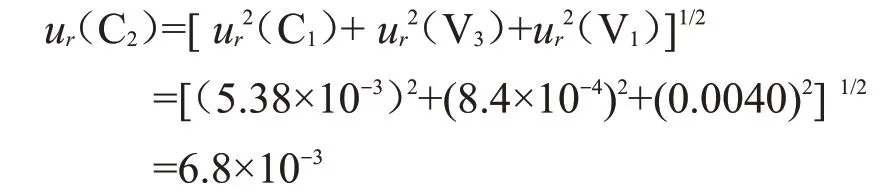
3.1.6 综上可知标准溶液配制引入的相对标准不确定度ur(C)为:

3.2 试样处理引入的相对标准不确定度ur(V)
由实验方法可知,试样处理定容体积引入的相对标准不确定度ur(V)分为25 mL A 级容量瓶的容量引入的相对标准不确定度ur(V3)和试样称量引入的相对标准不确定度ur(m)。
3.2.1 25 mL容量瓶引入的相对标准不确定度ur(V3)来自两个分量
(a)容量瓶的容量引入的不确定度u(V31)
25 mL 容量瓶的容量允许偏差为±0.03 mL,按均匀分布有:

(b)容量瓶温度变化引入的不确定度u(V32)
设温度变化为±5 ℃,20 ℃时水的膨胀系数α=2.1×10-4/℃,按均匀分布,则有:
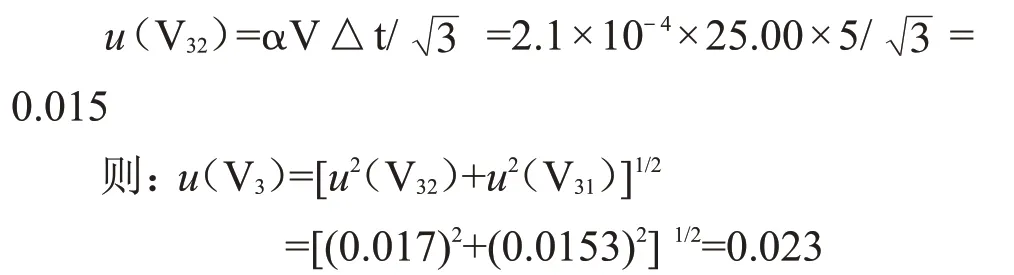
故25 mL容量瓶引入的相对标准不确定度ur(V3):
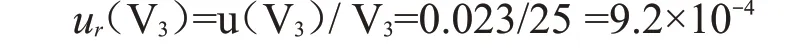
3.2.2 试样量取引入的相对标准不确定度ur(m)
由实验方法可知,试样称量引入的相对标准不确定度ur(m)即为称量样品质量引入的不确定度,由检定证书可知所用分析天平在0~50 g范围内,示值误差检定结果为0.1 e,实际分度值为0.0001 g,按均匀分布有:
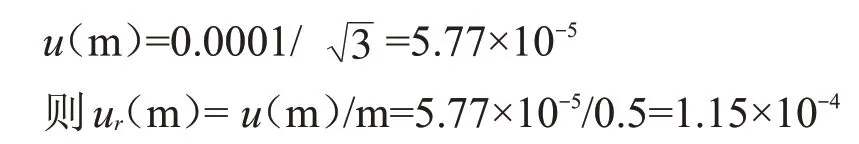
故试样处理引入的相对标准不确定度为:

3.3 试样重复性检测引入的相对标准不确定度ur(S)
采用《食品安全国家标准食品中总汞及有机汞的测定》GB 5009.17—2014 中汞的标准系列分析技术条件检测小麦种汞含量重复进行试验6 次(n=6),分析同一样品中汞的含量,测定结果见表1。
试样重复性检测引入的相对标准不确定度ur(S)为:
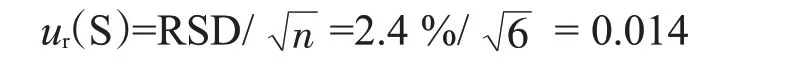
3.4 原子荧光光谱仪引入的相对标准不确定度ur(A)
仪器经检定知原子吸收光谱仪引入的不确定度为:
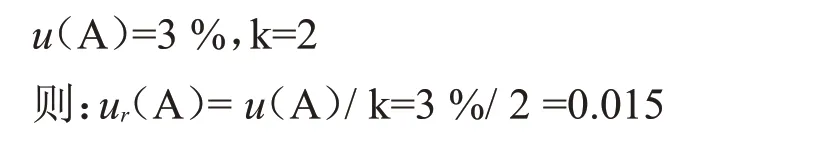
4 合成标准不确定度
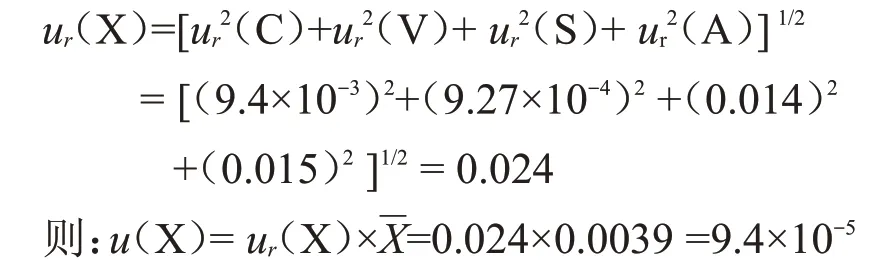
5 结论
扩展不确定度:取包含因子k=2,则扩展不确定度U=k×u(X)=9.4×10-5×2=0.0002 μg/L。
测量结果不确定度报告:由上面分析计算,最终得出水中汞的含量为0.0039±0.0002(μg/L)[k=2]。
本次不确定度评定依据JJF 1059.1—2012《测量不确定度评定与表示》和GB/T 27411—2012《检测实验室中常用不确定度评定方法与表示》两个不确定度相关标准中的有关规定,对GB 5009.17—2014《食品安全国家标准食品中总汞及有机汞的测定》(原子荧光光谱分析法)中汞含量的方法进行不确定评定,其检测过程中的不确定度来源主要有汞标准溶液引入的相对标准不确定度,试样处理引入的相对标准不确定度,试样重复性检测引入的相对标准不确定度,原子荧光光谱仪引入的相对标准不确定度,对此4 个分量进行不确定度评定,最终得出扩展不确定度为包含因子k=2 时扩展不确定度U=0.0002 μg/L,粮食中汞的含量为0.0039±0.0002(μg/L)[k=2]。

