E 成像联合睾丸体积在无精子症鉴别诊断中的初步应用*
许 丽 张时君 王鸿祥 杜 晶 李红丽 卢慕峻 李凤华
上海交通大学医学院附属仁济医院超声医学科(上海 200127)
无精子症占男性不育的15%[1],常根据输精管道是否通畅分为梗阻性无精症(obstructive azoospermia,OA)和非梗阻性无精症(non-obstructive azoospermia,NOA),两者的鉴别诊断对临床后续治疗具有重大意义。 利用生物组织的弹性(或硬度)改变与病灶的生物学特性紧密相关的原理, 超声弹性技术已广泛用于乳腺、甲状腺、肝脏等疾病的诊断[2-5],但睾丸无精子症方面的研究较少报道,尚处于探索阶段。 本研究以男科显微手术获得组织病理学为“金标准”,旨在探讨实时剪切波弹性成像(shear wave elastography,SWE,也称E 成像) 定量分析结合睾丸体积在无精子症鉴别诊断中的应用价值,为无精子症患者建立无创评估体系提供新方法。
资料与方法
一、临床资料
回顾分析2017 年8 月24 日至2018 年8 月21 日就诊于我院男科的男性不育患者, 根据WHO 男性不育诊断标准诊断为无精子症。 所有患者均通过病史采集、临床触诊、精液分析、精浆生化检查、血清性激素测定、染色体及遗传学检查、经阴囊及直肠超声检查睾丸和输精管道,行睾丸显微取精术(micro-TESE,microsurgical testicular sperm extraction)或输精管附睾管端侧显微吻合术(VE,microsurgical vasoepididymostomy) 且术后病理证实为梗阻性或非梗阻性无精子症。健康对照组选取期间至我院男科检查证实睾丸发育良好、性激素水平正常、精液常规检查正常(或已有生育史)、超声检查未发现泌尿系统疾病,自愿参加本研究患者。 排除标准:有睾丸肿瘤、急性睾丸炎、急性阴囊肿胀、大量鞘膜腔积液、三周内行睾丸穿刺术患者除外。
二、仪器与方法
采用法国Supersonic 公司Aixplorer 实时二维剪切波弹性超声诊断仪,SL15-4 探头,频率为4-15 MHz,彩色编码范围为0-50 kPa。 患者取平卧位, 充分暴露阴囊,阴茎轻轻上提,保证阴囊皮肤未受牵拉,先行常规超声检查, 测量睾丸体积大小, 按公式体积=长×宽×高×0.71 计算体积,阴囊表面涂充分的耦合剂,纵切显示睾丸最大切面,微调整避开大血管及睾丸纵隔网,转换到弹性成像,检查过程中始终保持睾丸、探头互相垂直,避免压迫或移动睾丸。 如图1 所示,弹性成像取样框系统默认位于图像中心位置, 范围以尽量包含睾丸组织为宜(睾丸体积小于取样框最大径,则取样框与睾丸外缘相切包含整个睾丸; 若睾丸体积大于取样框最大径, 则如图1 所示取样框优先包含睾丸中心区域),静置3s 待图像稳定后冻结图像, 以图像填充90%,且睾丸中心图像填充相对均匀一致、无明显伪像为成功,启动Q-BOX 功能,以取样框中心为圆点,以1/2 取样框短径(图1 中距离为1.79 cm)为直径选择感兴趣区(图1 中测量取样框直径为9 mm), 此时显示Q-BOX 测量区域内的杨氏模量平均值(Mean)、最大值(Max)、最小值(Min)以及标准差(SD),同时显示剪切波平均速度(m/s)。
所有患者由具有5 年男科超声临床经验的高年资医师(操作者1)与有1 年男科超声临床经验的低年资医师(操作者2)分别存储3 帧图并测量3 次,共计6次, 两位操作者均于实验前接受4 周的超声弹性成像技术操作培训。
三、统计学方法
采用SPSS19.0 统计学软件进行统计学分析, 计数资料根据是否满足方差齐性,年龄、体积以均值±标准差表示,弹性用中位数(四分位数间距)表示,参考值范围以95%置信区间表示。 以组内相关系数(intraclass correlation coefficient,ICC) 评价观察者间信度与复测信度。 不同分组的杨氏模量值比较采用秩和检验,不同分组体积差异比较采用两独立样本t 检验。体积或弹性亚组组内差异比较采用卡方检验,以P<0.05 为差异有统计学意义(四组秩和检验两两比较时,P<0.0125 为差异有统计学意义)。 应用受试者工作特征曲线(receiver operating characteristic,ROC 曲线)分析取得最适合诊断临界点,利用Medcalc 软件比较ROC 曲线效能差异。
结 果
一、一般情况
本研究共收录210 人,排除逆行射精2 人、急性睾丸炎2 人、 混合性无精子症患者2 人、3 月内有穿刺史1 人、大量鞘膜腔积液3 人、弹性图像获取失败15 人,入组对象共计185 人,其中正常志愿者32 人,根据显微外科手术及术后病理证实,共58 例OA 患者,其中先天性双侧输精管缺如(Congenital Bilateral Absence of the Vas Deferens,CBAVD)13 例,附睾炎性梗阻38 例,输精管梗阻7 例;95 例NOA 患者, 因克氏症特有的病理及硬度改变,单独列为一组,共20 例;非克氏症的NOA 病例构成为Y 染色体AZF 微缺失4 例, 有隐睾下降固定病史5 例, 后天性睾丸炎3 例, 其他特发性NOA 共63 例,获得上述无精子患者、正常志愿者的睾丸体积及SWE 图像,杨氏模量值组内信度检测显示操作者1 的ICC 为0.867,操作者2 的ICC 为0.836,表明信度良好, 两位操作者弹性测值差异无统计学意义(P=0.231)。
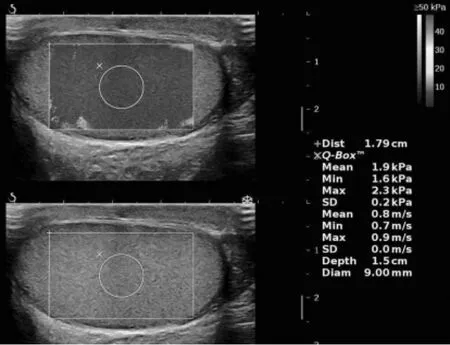
图1 正常志愿者睾丸纵切面SWE 图像
二、不同分组睾丸杨氏模量值比较
因非梗阻性无精子症(NOA)中克氏症患者睾丸特有的硬度特点,本研究将NOA 分为克氏症(KS NOA)和非克氏症(Non-KS NOA)两个亚组,不同分组间年龄、睾丸体积及睾丸弹性值见表1,各组间年龄无统计学差异(P>0.05),正常、OA、Non-KS NOA 及KS NOA组睾丸杨氏模量中位数(单位kPa)分别为1.8(1.6-2.0)、1.8(1.6-2.1)、1.6(1.2-1.8)和2.5(1.9-3.0),KS NOA 组患者睾丸弹性高于正常组、OA 组和Non-KS NOA 组,差异有统计学意义(P=0.001),OA 组高于非克氏症的NOA 组(P=0.007)与正常组比较无明显差异(P=0.7),非克氏症的NOA 组低于正常组(P=0.002)。
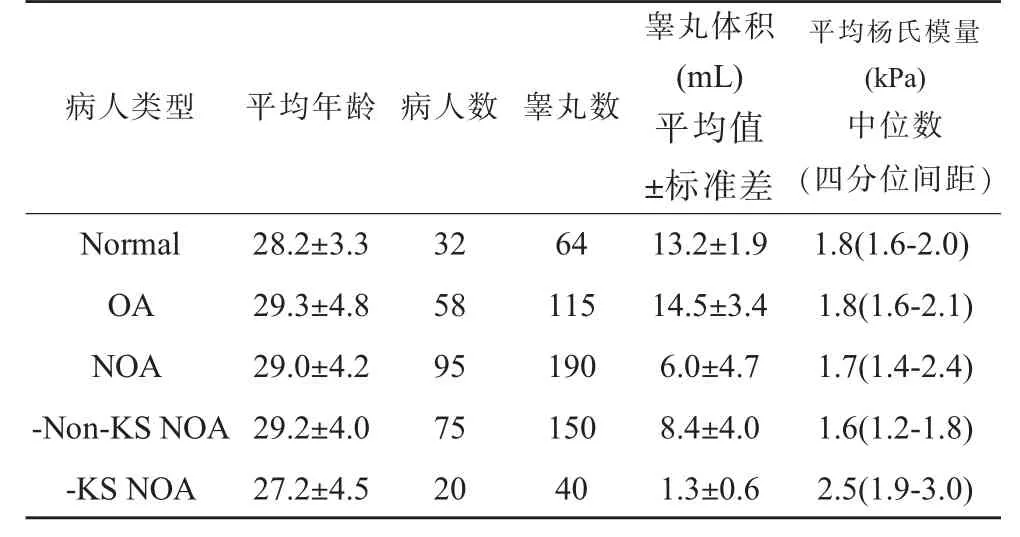
表1 不同分组睾丸体积及杨氏模量表
三、睾丸弹性联合体积鉴别价值探讨
如图2 所示,利用ROC 曲线得出杨氏模量值诊断OA 和Non-KS NOA 患者的曲线下面积Az=0.681(0.618-0.745),最佳截断值为1.7 kPa,以杨氏模量值≥1.7 kPa 诊断为OA 为标准, 敏感度=61.3%, 特异度=68.7%,约登指数=0.3。 利用体积鉴别OA 和Non-KS NOA 患者时,ROC 曲线下面积Az=0.886(0.849-0.923),最佳截断值为12 ml, 以体积≥1.2 ml 诊断为OA 为标准,敏感度=78.2%,特异度为81.3%,约登指数=0.595。睾丸体积的鉴别诊断能力高于睾丸杨氏模量值(P=0.000)。 睾丸体积和杨氏模量值联合诊断OA 和Non-KS NOA 患者,曲线下面积为Az=0.890(0.853-0.927),效能优于单一杨氏模量值(P=0.000),但与睾丸体积诊断效能无明显差异(P=0.465),以体积≥1.2 ml,且弹性值≥1.7 kPa 诊断为OA 为标准,敏感度=83.4%,特异度=81.9%,约登指数=0.653。
利用睾丸杨氏模量值及体积联合鉴别OA 及KS NOA, 结果示两者联合曲线下面积优于杨氏模量值(1.000 vs 0.799,P=0.001) 与体积无统计学差异(1.000 vs 0.996,P=0.201), 以体积≤3.6ml, 且弹性值≥2.3kpa诊断为KS NOA 为标准, 敏感度=99.16%, 特异度=100%,约登指数=0.99。
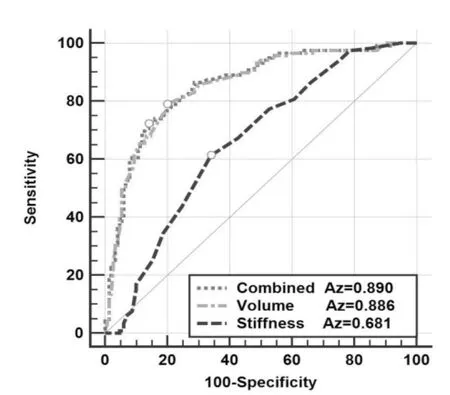
图2 睾丸体积、杨氏模量值及两个联合鉴别梗阻及非克氏症非梗阻患者的的ROC 曲线
为了进一步探讨弹性和体积的联合价值, 本研究将OA 及NOA 患者睾丸体积细化为5 组(如表2 所示), 结果示在5 个亚组中,1,2,4,5 组中OA 及NOA间体积均有统计学差异(P=0.000), 当睾丸体积小于10.0 ml 时,89.5%的患者是NOA 患者; 当睾丸体积大于等于12 ml 时,78.3%的患者是OA 患者。但睾丸体积在10.1-12.0 ml 区间内时,OA 及NOA 患者存在较大重叠,差异无统计学意义(P=0.612),我们比较此区间两组患者的睾丸杨氏模量,发现OA 组弹性值高于NOA 组患者(P=0.001),曲线下面积AUC 是0.788(0.655-0.921),以弹性值≥1.7 kPa 为OA 作为判定标准, 其敏感性为80%,特异性为62%,约登指数为0.409。如图3 所示,A 无精子症患者睾丸体积为10.2 ml(图A1),在10.1-12.0 ml区间,弹性杨氏模量值为1.8 kPa(图A2),最终手术和病理证实为梗阻性无精子症;B 无精子症患者体积11.9 ml(图B1), 弹性杨氏模量值为1.3 kPa(图B2),最终手术和病理证实为非梗阻性无精子症。 可见,在睾丸体积无法区分OA 和NOA 患者时,睾丸弹性值可以进行补充诊断。
另一方面, 本研究也将OA 和NOA 患者睾丸杨氏模量值细化为4 组,如表2 所示,可见第1,3,4 分组中,弹性对无精子症有鉴别价值, 当弹性≤1.2 kPa 时,88%的患者为NOA 患者,当弹性≥2.5 kPa 时,82.5%的患者为NOA 患者,主要为克氏症患者,当弹性介于1.3-1.7 kPa时,OA 和NOA 患者存在较大重叠,差异无统计学意义(P=0.325)。 但此区间内OA 患者睾丸体积远大于NOA患者睾丸体积(P=0.000),从而提高鉴别诊断价值。
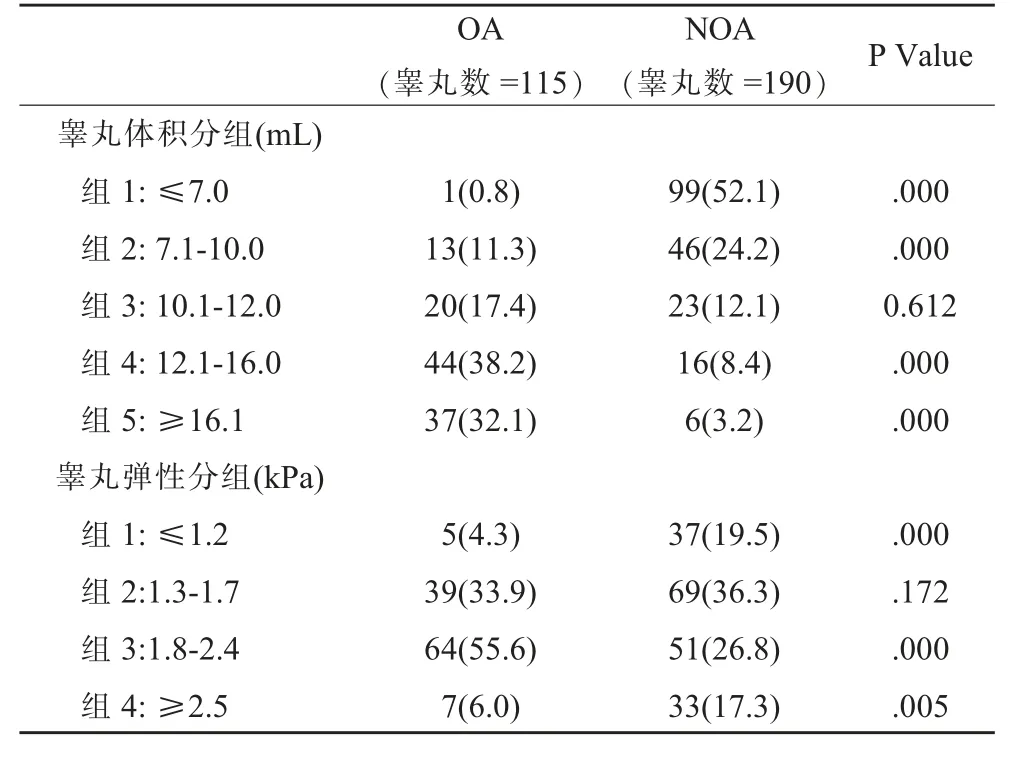
表2 梗阻性及非梗阻性无精子症患者睾丸杨氏模量及体积分布
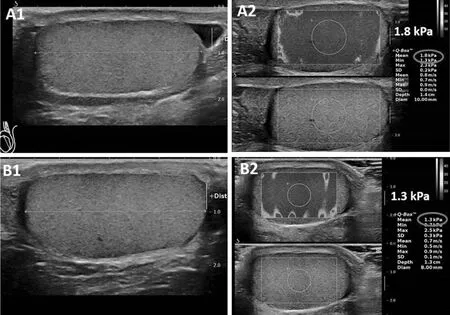
图3 睾丸体积介于10.1-12.0 mL 的OA(A)及NOA 患者的睾丸灰阶图(A1,B1)、睾丸E 成像图(A2,B2)
讨 论
不育不孕症作为生殖系统疾病影响着全世界约15%的人群[6],其中与男性因素相关者占50%[7],男性不育病因复杂,无精子症是其中尤为严重的情况[8]。 以往附睾穿刺及睾丸活检的病理学检查多是梗阻及非梗阻无精子鉴别诊断的金标准, 但睾丸本身的生精状况不完全均衡,生精可呈局灶性,同时睾丸/ 附睾活检位置选择的随机性很大,受手术者手法影响,组织获取情况无法保证。 随着显微外科技术的发展,睾丸显微取精术及输精管附睾管端侧吻合术作为无精子症患者的治疗手段,展示出创伤小,精子获得率高、可全面准确的评估鉴别无精子症病因等诸多优势[9,10]。 本研究以显微外科手术结果及术后病理进行无精子症的分组及回顾分析,比以往研究[10-12]有更加可靠的诊断“金标准”。
超声弹性成像是一项新技术, 主要有位移或应变成像、 点式剪切波测量及实时剪切波弹性成像(E 成像),有望通过探测睾丸组织各区域的不同硬度来评价睾丸生精功能[13]。本课题组前期评估了应变弹性成像在鉴别无精子症中的价值, 表明睾丸弹性硬度值可以对OA 及NOA 有鉴别能力, 且对无精子症的病理分型有一定预测作用[14,15]。 但应变弹性技术需要对探头施加压力, 弹性图像定性分级受到操作者手法及主观因素影响较大,重复性欠佳。 E 成像作为一种最新进展的弹性量化技术,采用“马赫圆锥”原理,可以获得组织定量杨氏模量值,不受主观因素的影响,其次不需要对探头施加压力, 避免不同操作者间的操作误差, 可重复性较好,研究表明[12,17]E 成像在睾丸组织硬度测量中可有较好的可行性及应用性, 可用于各类睾丸疾病的硬度测量及评估。
本研究结果显示, 不同操作者间杨氏模量的测值稳定性好,重复性高,非梗阻无精子症中克氏症患者的睾丸杨氏模量值高于正常、 梗阻及其他非梗阻患者(P=0.001),OA 组高于Non-KS NOA 组, 这与Rocher等人[12]的研究趋势一致。推测原因是克氏症的病理基础为睾丸间质增生、基底膜增厚,生精小管玻璃样变导致睾丸硬度增加[18]。非克氏症的非梗阻性患者睾丸弹性值低于梗阻性及正常患者,这与其睾丸体积小、精子发生低下、生精小管管腔窄、上皮组织薄导致睾丸不饱满而较软有关。
有研究表明, 睾丸体积大小与睾丸生精功能直接相关,有助于初步判断男性生育状态[19],对鉴别无精子症类型有一定价值。 本研究中, 当睾丸体积小于10ml时,89.5%的患者是非梗阻性无精子症的患者; 当睾丸体积大于等于12ml 时,78.3%的患者是梗阻性无精子症的患者,根据ROC 曲线分析,睾丸体积对无精子症的鉴别能力优于睾丸杨氏模量(P=0.000),这可能与睾丸杨氏模量值较小,各组测值重叠区域较大有关。
本研究通过细化睾丸体积及弹性的分组, 具体探讨了睾丸体积和弹性联合的最优条件。 在睾丸体积为10.1-12.0 mL 时无法有效的对梗阻和非梗阻进行鉴别,此时睾丸弹性值对梗阻和非梗阻起到很好的补充鉴别作用,同样在弹性值无法鉴别的亚组(1.3-1.7kPa),同时结合睾丸体积可以做出有效判断。
综上所述,E 成像检测睾丸组织弹性硬度稳定性高、重复性好,可以对无精子症进行鉴别诊断,但单独E成像杨氏模量值的鉴别效能要低于睾丸体积。 细化睾丸体积及E 成像分组,也成功的发现在单一体积或弹性无法鉴别时, 联合另一参数睾丸体积就可以很好的互补,提高鉴别诊断能力。 本研究以手术探查及组织病理学为金标准,对E 成像应用于无精子症鉴别诊断作出客观初步探究,有利于完整可靠诊断体系的建立,以期更好地服务于无精子症患者早期无创的超声鉴别诊断。

