利妥昔单抗治疗12例儿童免疫性脑病的疗效及安全性分析
李小晶 侯池 陈连凤 曾意茹 梁惠慈 田杨 朱海霞 彭炳蔚 吴汶霖 高媛媛 陈文雄
利妥昔单抗(rituximab,RTX)是一种人鼠嵌合性单克隆抗体,能特异性地与B细胞上的跨膜抗原CD20 结合,诱导B细胞凋亡[1]。最初批准用于治疗非何杰金氏B细胞淋巴瘤,目前逐渐被用于神经系统免疫相关性疾病(包括自身免疫性脑炎、中枢神经系统炎性脱髓鞘病、吉兰-巴雷综合征和重症肌无力等)中并显示出较好的疗效[2],目前该药在儿童中应用的研究较少。该研究回顾性分析了RTX对儿童难治性或复发性的免疫性脑病的疗效及安全性,以期为临床应用提供参考。
1 对象和方法
1.1 研究对象收集2016年9月1日至2018年12月31日在广州市妇女儿童医疗中心神经内科就诊的免疫性脑病患儿的临床资料。入组标准:(1)临床符合免疫性脑病诊断;(2)曾应用≥2个疗程的一线免疫治疗方案,包括大剂量静脉输注甲泼尼龙冲击治疗〔按体质量(10~15) mg/(kg·d)共3~5 d,其后每隔3 d剂量减半至2 mg/(kg·d)时改为泼尼松2 mg/(kg·d)口服〕联合静脉输注人免疫球蛋白治疗(按体质量2 g/kg,分3~5 d输注)和/或其他免疫抑制剂(霉酚酸酯 0.25 g/d,2周后加量至0.25 g/次,2次/d口服维持),治疗效果不佳;(3)除外遗传代谢病、肿瘤或系统免疫性疾病累及神经系统。患儿监护人均签署知情同意书,并通过广州市妇女儿童医疗中心医院伦理委员会(穗妇儿伦审批第2019052419364384号)批准。
1.2 方法记录患儿的一般资料及RTX治疗前后的临床资料,分别在RTX疗程结束3个月、6个月对所有患者进行随访。病程中使用国际通用的改良Rankin量表评分(modified Rankin scale,mRS)[3]评估患者在一线治疗前、RTX治疗前、RTX疗程结束3个月、RTX疗程结束6个月后的病情,并进行对比分析。免疫治疗前后mRS评分无改善或mRS评分≥4持续4周定义为疗效不佳。采用不良反应常见术语标准(Common Terminology Criteria for Adverse Events,CTCAE)对药物不良反应进行分级。
RTX治疗方案:RTX按体表面积375 mg/m2,每周1次,连用4周,或者每2周1次,共2次为1个疗程。RTX输注前预防性予口服氯雷他定、布洛芬及静脉输注小剂量甲泼尼龙〔2 mg/(kg·d),最大剂量不超过60 mg/次〕。RTX疗程结束后口服复方磺胺甲恶唑片预防感染〔15~20 mg/(kg·d),分3次口服,服用3 d间隔4 d,共服用3个月〕。RTX疗程结束后每隔1个月完成门诊一般状态及神经功能随访,每隔3个月返院复查,除完成一般状态及神经功能评估外,还包括抗体滴度、血CD19计数、脑电图及头颅MRI的复查。
1.3 统计学处理采用Excel 2019软件建立数据库,采用SPSS 26.0统计软件进行数据分析。使用Shapiiro-Wilk检验评估数据是否呈正态分布。对于计量资料,若服从正态分布,则用均数和标准差描述;如果资料是偏态分布,则采用中位数(上、下四分位数)描述。采用Wilcoxon检验进行治疗前后两个时间点的比较,以P<0.05为差异有统计学意义。采Friedman检验进行治疗前后多个时间点的比较,以P<0.05为差异有统计学意义;如果多组样本总体上差异存在统计学意义,进一步行两两比较,并使用Bonferroni法进行较正。
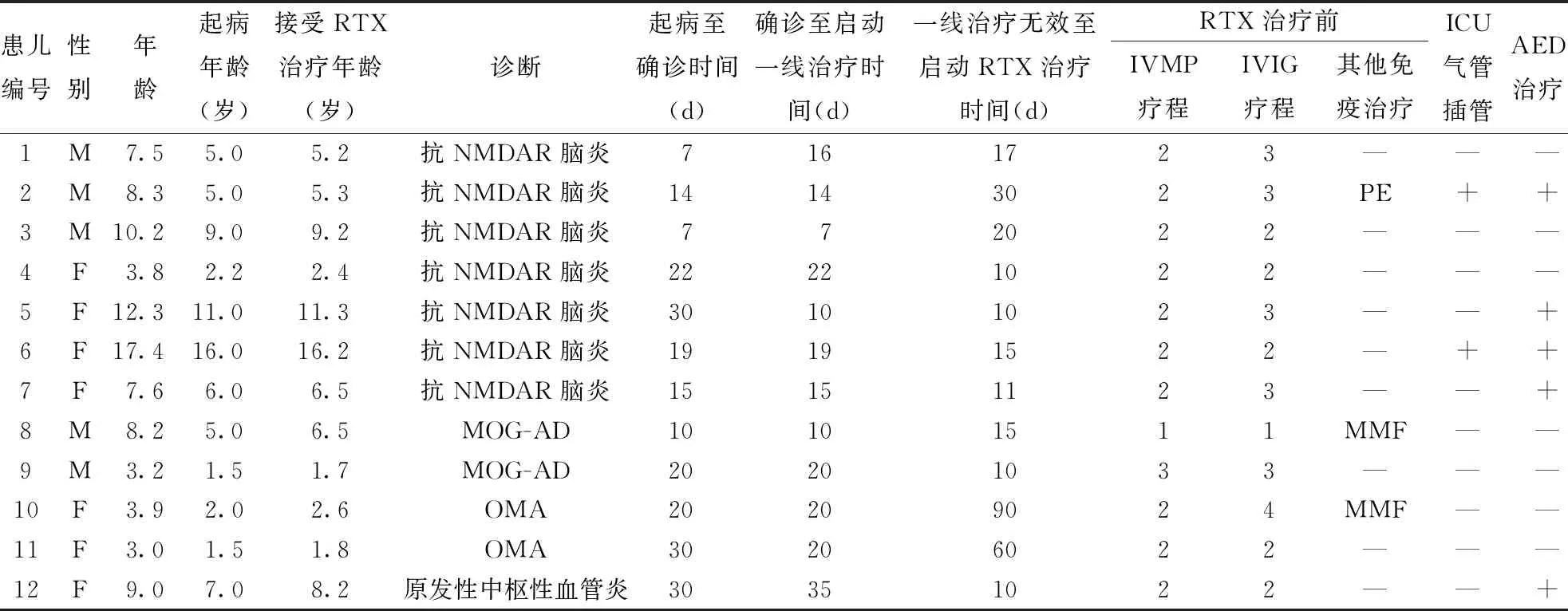
表1 12例患儿的一般临床资料及治疗情况
2 结果
2.1 一般临床资料患儿具体的一般临床资料及治疗情况见表1、表2。共12例患儿符合入组标准,其中男5例、女7例,平均起病年龄为(5.9±4.4)岁。其中NMDAR脑炎7例,髓鞘少突胶质细胞糖蛋白抗体相关疾病(myelin oligodendrocyte glycoprotein antibody associated diseases, MOG-AD)及急性播散性脑脊髓炎伴发视神经炎(acute disseminated encephalomyelitis followed by optic neuritis,ADEM-ON)各1例,眼阵挛-肌阵挛-共济失调综合征2例,原发性中枢神经系统血管炎1例。
2.2 临床表现7例NMDAR脑炎患儿中,急性期均有精神行为异常、抽搐、不自主运动、语言障碍(7/7例),其中睡眠障碍5例、意识障碍3例、自主神经功能紊乱3例。2例MOG抗体相关性疾病患儿均有脑病、运动障碍、共济失调的症状,其中1例有视力障碍。2例眼阵挛-肌阵挛-共济失调患儿均有眼阵挛-肌阵挛-共济失调及睡眠障碍。1例原发性中枢性血管炎患儿表现为球麻痹、运动障碍、抽搐。
2.3 病程从起病到明确诊断的时间为(18.7±8.4) d,从起病至使用一线药物治疗的时间为(20.7±9.9)d,一线治疗无效至启动RTX治疗的时间中位数(上、下四分位数)为15(10 d,27.5)d。2例患儿(患者8、10)在一线治疗结束后分别予霉酚酸酯口服3个月、6个月后各复发1次,末次复发一线治疗无效后予RTX治疗。1例患儿(患者9)诊断为MDEM,一线治疗3个疗程后病情仍急进性进展,遂予RTX治疗。所有患儿从使用RTX疗程结束至末次随访的时间为15.50(12.50,20.25)个月。具体见表1、表2。
2.4 辅助检查7例NMDAR抗体脑炎患儿接受RTX治疗前脑脊液NMDAR抗体均为阳性,2例MOG抗体相关疾病患儿一线治疗过程中血MOG抗体持续阳性。其余3例患儿未检测出相关抗体。急性期血CD19细胞数为345.96(280.99,1260.73) cell/μL,RTX疗程结束3个月CD19细胞数为2.15(0.78,3.43) cell/μL,RTX治疗疗程结束后3个月B细胞绝对计数明显下降(Z=-3.059,P<0.002)。8例患儿脑电图异常,主要表现为脑电图背景活动慢。9例患儿头颅MRI异常,以皮层及皮层下白质受累多见。RTX疗程结束3个月复查脑电图、头颅MRI均改善。RTX治疗前后CD19、脑电图及头颅MRI情况见表3。
2.5 预后及转归12例患儿接受一线治疗前mRS评分为4.50(4.00,5.00);一线免疫治疗结束后mRS评分为4.00(4.00,4.75),一线治疗前后mRS无明显改善(Z=-1.732,P=0.083)。RTX疗程结束3个月及6个月mRS评分分别为1.50(1.00,2.00)、1.00(1.00,2.00),与一线免疫治疗结束后的mRS评分比较明显减低(χ2=22.947,P<0.001)。RTX疗程结束6个月与RTX疗程结束3个月时mRS评分差异无统计学意义(Z=0.167,P=1),病情无明显改善。患儿的RTX治疗及预后情况见表2。
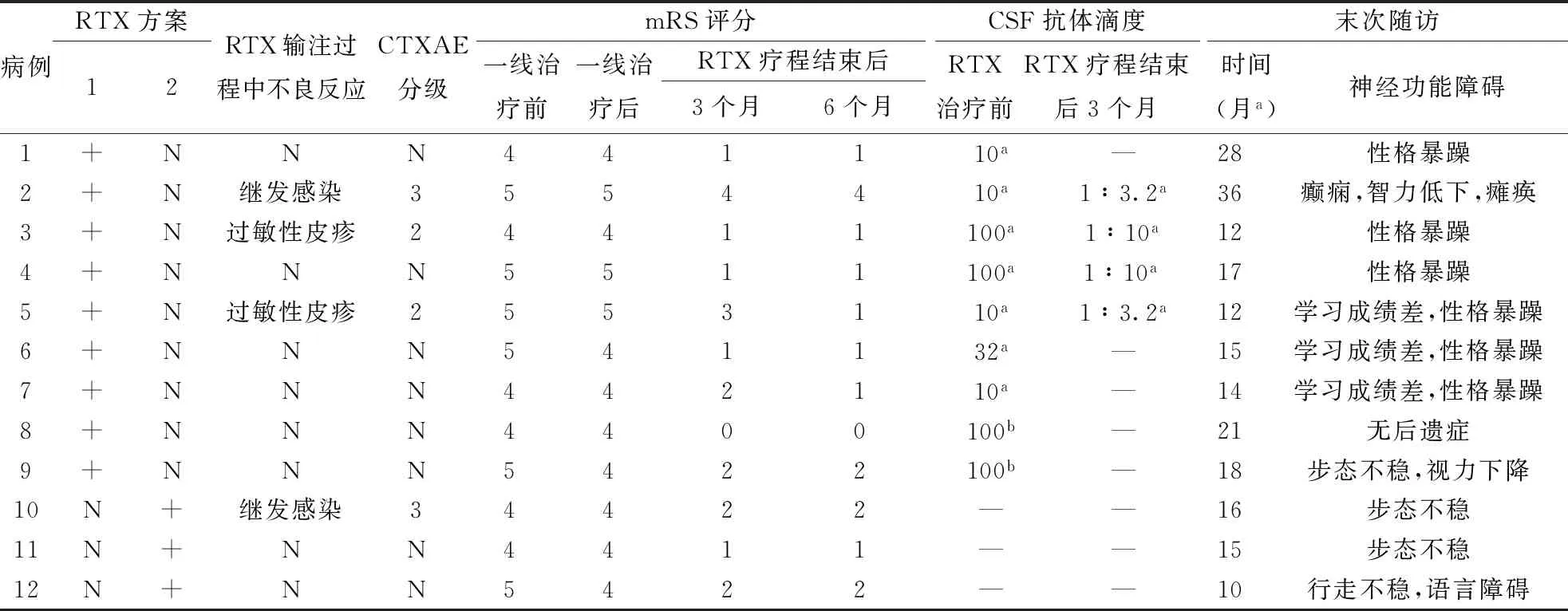
表2 12例患儿RTX治疗及转归
2.6 不良反应2例患儿在输注RTX 60 min内发生皮疹,为散在分布的红色斑丘疹,伴瘙痒,予盐酸异丙嗪肌注及减慢输注速度后,1例患儿皮疹于40 min后消退,1例患儿皮疹于60 min后消退。1例患儿在RTX输注后第2周发生呼吸道感染及深静脉导管感染,导管残端培养出人葡萄球菌,给予万古霉素输注后感染控制。1例患儿在RTX 1个疗程结束后发生反复呼吸道感染,给予人免疫球蛋白〔1 g/(kg·月)〕免疫支持及抗感染治疗后感染控制。
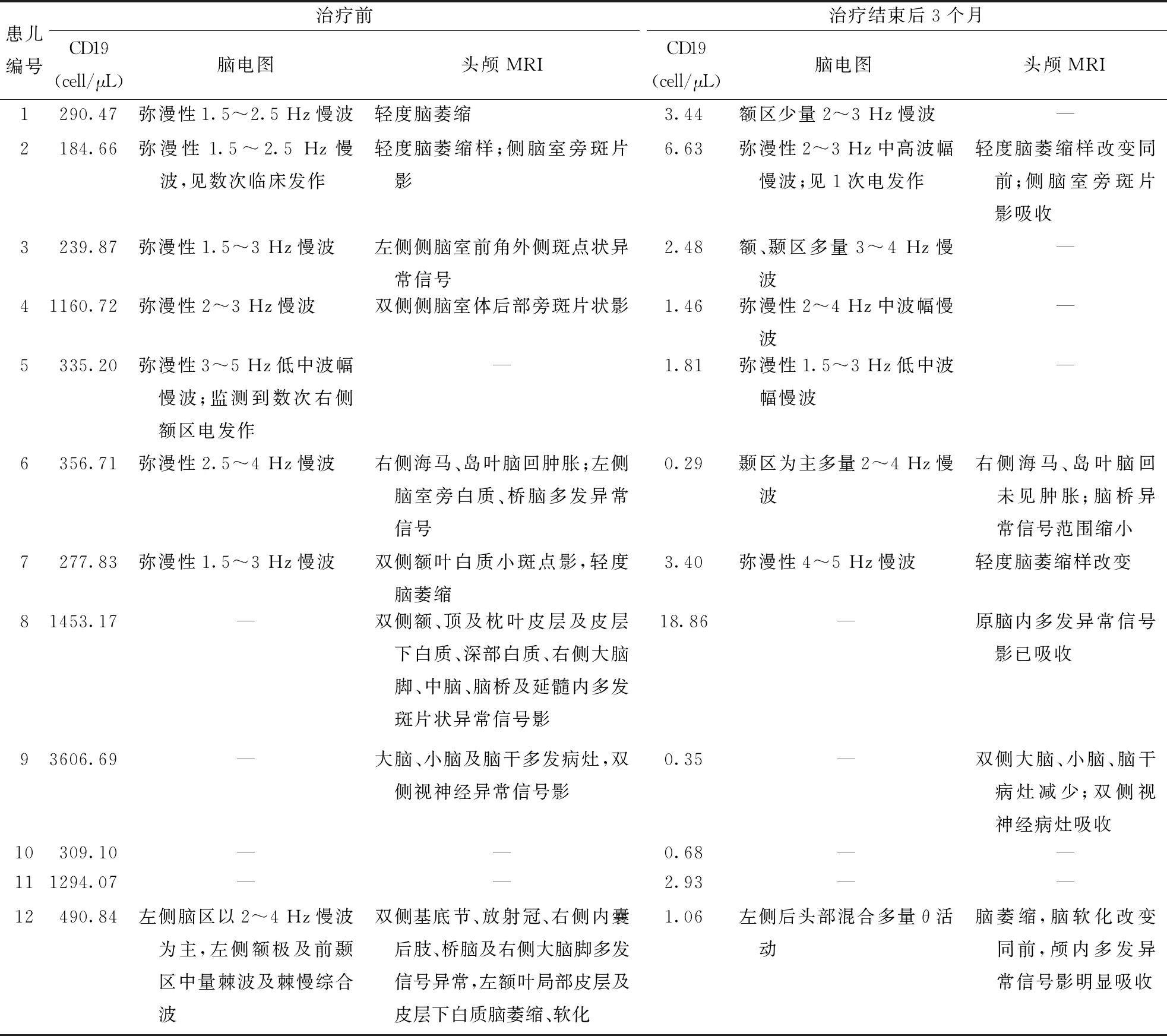
表3 12例患儿RTX治疗前后实验室检查结果
3 讨论
目前国际上对于儿童免疫性脑病的一线治疗药物是糖皮质激素(后文简称“激素”)、IVIG,而对于难治性或复发性的患儿,已有研究证据表明二线免疫抑制剂治疗效果较好[1],RTX是最常用到的二线免疫抑制药物之一。RTX为抗CD20单克隆抗体,可通过抗体介导的细胞毒性、补体激活和诱导细胞凋亡等方式消耗幼稚细胞和记忆性B细胞,从而降低复发率[4]。RTX对CD20阴性细胞,包括寿命较长的浆细胞无明显影响,免疫抑制作用较少。
抗NMDAR脑炎是一种较常见的自身免疫性脑炎,由抗NMDAR抗体介导,急性期病情危重,部分患儿可能需ICU治疗,但大部分患儿病程为单相且预后较好[2]。多数患儿一线免疫治疗包括激素及人免疫球蛋白治疗反应好,少数患儿需启动二线治疗包括RTX、环磷酰胺、霉酚酸酯等。目前RTX主要用于重症、难治性的抗NMDAR脑炎的治疗。本组7例抗NMDAR脑炎患儿,均对一线治疗无明显反应,病情严重,经RTX治疗后,6例患儿mRS评分明显改善。
MOG蛋白位于少突胶质细胞表面,MOG抗体介导的炎性脱髓鞘疾病包括ADEM、APQ4 IgG阴性的NMOSD、ADEM-ON及MDEM等。该病急性期多数对激素治疗反应良好,但部分患儿为复发病程。现有研究显示RTX主要用于该病的复发病例,可明显降低复发率,并可能改善预后,避免长期使用激素的不良反应[5]。本组中2例MOG抗体相关疾病患儿,均为复发病程,接受RTX治疗后未见复发,临床症状明显改善。
眼阵挛-肌阵挛-共济失调综合征是一种罕见的神经系统自身免疫性疾病,其发病机制尚不完全清楚,脑脊液中B细胞过度表达或“扩增”是其活动期的生物标记物,且与病情严重程度相关[6]。50%~80%的该病患儿可合并神经母细胞瘤[6],大多数在切除肿瘤后仍需接受免疫治疗。据报道RTX可有效控制该病复发,改善症状[7]。本组2例该病患儿经过多次一线免疫治疗后呈缓解-复发病程,接受RTX治疗后未再复发且症状明显改善。
原发性中枢性血管炎是一种免疫性炎症性疾病,病理表现为血管壁损伤及透壁性淋巴细胞浸润。免疫组化示CD3、CD4、CD8 T及CD20 B细胞阳性[8]。复发及病情进展快的患儿使用RTX治疗可取得较好疗效[9]。本组中1例该病患儿病情呈复发-进展,经多次一线免疫治疗无明显疗效,予RTX治疗后无复发,症状及影像学明显改善。
目前RTX在免疫性脑病的治疗上尚无公认的用药方案,临床用药以患者能耐受且有效为依据[4,10]。国内文献报道RTX治疗神经系统自身免疫性疾病不良反应轻微[4]。国外的文献显示RTX的不良反应主要包括过敏及继发感染[10]。该研究中患者不良反应较少,主要为过敏反应及感染。使用RTX前的预处理包括口服抗过敏药物、输注甲泼尼龙、及时有效的抗感染及免疫支持治疗,对防治这些不良事件的发生发展非常重要。
综上,本研究显示RTX对于儿童难治性或复发性的神经免疫性疾病可能是一种安全有效的治疗方法,疗效较好,安全性较好,未出现严重不良反应。

