肉桂精油纳米乳液的抑菌性和稳定性研究
侯克洪 冯 潇 高成成 汤晓智
(南京财经大学食品科学与工程学院;江苏省现代粮食流通与安全协同创新中心;江苏高校粮油质量安全控制及深加工重点实验室,南京 210023)
植物精油是从植物的花、叶、茎、根或果实中提取的含有挥发性芳香物质的浓缩亲脂液体,其中的活性成分抗菌性强,是良好的天然抗菌剂[1]。然而,精油的强挥发性和疏水性以及其对环境如氧气、光、稳定的高敏感性限制了精油在食品领域的应用。
利用纳米乳液包埋精油并应用于食品的抗菌保鲜已经有大量的报道[2-4]。纳米乳液载体的运载效应使被包埋的脂溶性成分的水溶解度显著提高,而且稳定性也有所提高。此外,由于液滴尺寸较小,颗粒光散射波较弱,使乳液呈现透明或仅轻度混浊状态,在饮料或某些食品中添加时不改变其光学性质[5]。然而,油水两相界面间较高的正自由能决定了纳米乳液是一种热力学不稳定性的体系,并可能因重力分离、凝聚、聚集、奥氏熟化等作用而发生破乳现象,因此如何制备具有较好稳定性的纳米乳液是目前研究的热点。改善纳米乳液的稳定性可通过控制其油/水相组成、粒径分布以及加入稳定剂,如乳化剂、品质改良剂或缓凝剂等实现[6]。
酪蛋白酸钠是常用的天然高分子乳化剂。酪蛋白酸钠已被报道可以降低界面张力,并且相对于球蛋白如乳清蛋白在界面处更易于展开,从而起到稳定乳液的效果[7-8]。羟丙基-β-环糊精(HPCD)是β-环糊精(β-CD)的醚化衍生物。羟丙基的引入部分打开了β-CD的分子内氢键,水溶性大大提高(>500 g/L,20 ℃)。与β-CD母体相比,HPCD在提高包埋物的溶解度、溶出速度、生物利用度和稳定性方面都有独特的作用,是目前研究及应用最为广泛的β-CD衍生物[9]。HPCD具有较β-CD更高的安全性,被认为是很有潜力的母体环糊精替代品[10]。然而,研究者往往更多关注其包合特性,反而忽略了其非包合方面的特性,比如其类似于表面活性剂的亲疏水特性[11]。由于HPCD 具有亲脂的内部空间和亲水的外部空间,可以将其理解为一个特殊的表面活性剂,水不溶性的精油可以进入亲脂的内部空间,与HPCD 形成水溶性复合体,从而增强乳液的稳定性。因此,本研究使用HPCD与酪蛋白酸钠共同乳化制备肉桂精油纳米乳液,研究HPCD和酪蛋白酸钠的添加量对乳液粒径的影响,并在此基础上,探究不同精油添加量下乳液的稳定性和抑菌性能,旨在为制备高稳定性且具备良好抑菌性能的精油纳米乳液提供参考。
1 材料与方法
1.1 材料与试剂
肉桂精油,食品级;羟丙基-β-环糊精,纯度97%;酪蛋白酸钠,食品级;尼罗红,纯度≥95%。
1.2 仪器与设备
ULTRA-TURRAX T18高速分散器;SCIENTZ-1500F 超声波分散仪;Nano-ZS90 纳米激光粒度仪;AxioScopeA1荧光显微镜;HWS型恒温恒湿箱;GHP-250智能光照培养箱; SpectralMax-M2e酶标仪。
1.3 方法
1.3.1 乳液的制备
室温下将HPCD溶解于纯水中,再添加酪蛋白酸钠充分溶解后,逐滴加入肉桂精油,继续搅拌2 h,高速分散器18 000 r/min条件下处理5 min,最后在450 W功率下,超声处理10 min。其中酪蛋白酸钠的质量分数为0.5%、1.0%、1.5%(m/m),肉桂精油的体积分数为1%、3%、6%、10%(V/V),HPCD的质量分数选择前期实验中效果最好的3%(m/m)。
1.3.2 平均粒径和多分散指数(PDI)分析
用纳米激光粒度仪测量乳液平均粒径和PDI。使用去离子水以1∶100稀释样品并充分搅拌以避免多次散射效应,根据米氏散射理论,选择折射率为1.456和吸收系数为0.001。
1.3.3 抗菌活性
参考Moraes-Lovison等[12]的方法,稍作修改,研究乳液对大肠杆菌(Escherichiacoli,E.coli)和金黄色葡萄球菌(Staphyloccocusaureus,S.aureus)的抗菌活性。使用LB肉汤,接种微生物后置于恒温振荡箱中,150 r/min、37 ℃下培养24 h,将菌浓度稀释至108CFU/mL。取1 mL稀释好的菌液与8.5 mL营养肉汤和0.5 mL样品乳液(对照组为0.5 mL无菌水,其他操作相同),混合振荡30 s,然后37 ℃下培养。每隔一段时间,通过平板计数法测定混合液的菌浓度。
1.3.4 最小抑菌浓度和最小杀菌浓度
参考Rakmai等[13]的方法,通过微量稀释法测定最小抑制浓度。将微生物浓度稀释至约为105CFU/mL备用,取0.5 mL的每种细菌接种物接种2.5 mL营养肉汤。然后将不同体积分数的精油(溶于10%的乙醇溶液)或纳米乳液加入管中,旋涡搅拌30 s。将混合液在37 ℃下培养24 h后未观察到可见微生物生长(OD600变化≤0.05)的最低浓度为精油和纳米乳液的最小抑菌浓度(MIC)。将在OD600下显示无浊度的培养液中的测试微生物培养液转移100 μL并涂布在PCA营养琼脂上,37 ℃培养24 h,不生长微生物的对应浓度作为最小杀菌浓度(MBC)。
1.3.5 储藏稳定性
将新鲜制备的乳液分别放在4、25、40 ℃环境下,储存28 d,每隔7 d测量粒径,进行拍照和荧光显微镜观察。
1.3.6 乳化指数
乳化指数间接表明了乳液的稳定性。参考Cheong等[14]的方法,乳液制备完成后,立即将10 mL纳米乳液转移到试管中密封,然后分别在4、25、40 ℃下储存。乳化指数通过公式测定:
乳化指数=(HL/HE)×100%
式中:HL为奶油层的高度;HE为乳剂的总高度。
1.3.7 荧光显微镜
用适量尼罗红溶液(0.1 mg/mL,溶于乙醇)对乳液预先染色,在荧光显微镜下观察被染色的油滴形态大小,记录图像。
1.4 数据统计与分析
采用SPSS 22软件对数据进行处理,数据以平均值±标准差表示。采用单因素方差分析分析组间差异性,以P<0.05表示差异显著。
2 结果与分析
2.1 粒度和电位测量
表1显示了质量分数为0.5%、1.0%、1.5%酪蛋白酸钠(SC)单独或与HPCD共同作用下不同肉桂精油含量的乳液粒径和PDI。由表1可知,酪蛋白酸钠可以用于稳定肉桂精油纳米乳液,当使用0.5%的酪蛋白酸钠时,乳液粒径范围在226.93~350.10 nm,PDI范围在0.20~0.31,但粒径和PDI随着精油浓度的增加而增加。表明在较低SC浓度下,随着精油浓度增加,没有足够的SC分子完全覆盖乳液液滴,乳液由于聚结而不稳定,其粒径和PDI有所增加[11]。当酪蛋白酸钠使用量由0.5%增加到1.0%时,可以看到在较低精油浓度时粒径无显著变化,但当精油体积分数增加到10%(V/V), 相对于0.5%的酪蛋白酸钠,1.0%酪蛋白酸钠稳定的精油乳液粒径显著降低。当继续增加酪蛋白酸钠到1.5%,乳液粒径反而有所上升。因为酪蛋白酸钠是一种柔性蛋白,通过降低界面张力,并在油水界面处展开来稳定乳液,当浓度过高时,酪蛋白酸钠分子游离在溶液中,无法吸附到界面处起到稳定乳液的作用,反而使乳液的粒径增加[7]。
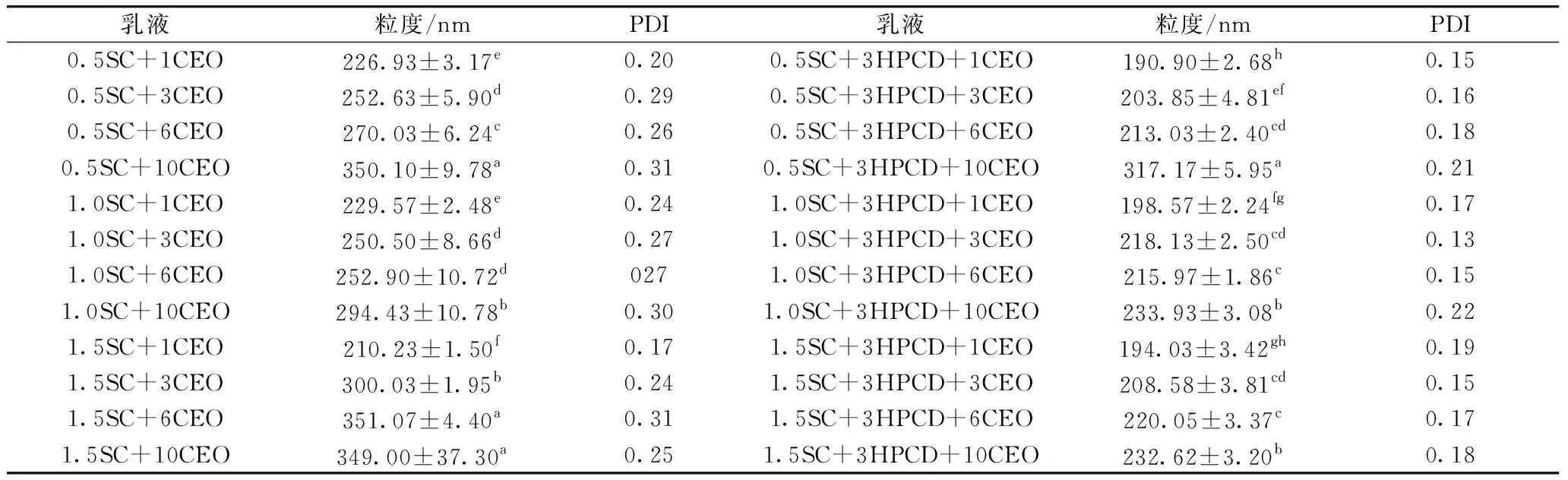
表1 不同SC浓度时不添加或添加HPCD乳液的粒径和PDI
HPCD的添加可以显著降低酪蛋白酸钠-精油乳液的粒径及PDI值,相较仅使用1%酪蛋白酸钠稳定的乳液粒径,当使用1%酪蛋白酸钠和3%HPCD共同稳定乳液时粒径降低到198.57~233.93 nm。其可能原因在于HPCD对精油的包合特性抑制了精油的聚集[13,15-16]。此外,HPCD包合精油生成的复合物,可能通过吸附在油滴表面增强其乳化稳定性,起到辅助其他乳化剂降低乳液粒径稳定乳液的效果。
2.2 抑菌生长曲线
1%酪蛋白酸钠和3%HPCD共同稳定的肉桂精油纳米乳液对大肠杆菌和金黄色葡萄球菌的抑菌曲线如图1所示。与对照组相比,添加纳米乳液后,大肠杆菌和金黄色葡萄球菌的生长受到明显抑制,并且随着精油添加量的增加,乳液对微生物的抑制作用也逐渐增强。精油纳米乳液的抑菌主要取决于基质中精油的浓度、粒径以及乳液中精油的释放速度。当乳液添加进营养基质中,由于水包油乳液的水溶性与分散性良好,纳米级粒径的精油液滴呈现较高的比表面积,增大了与微生物的接触机会,因此当与生物系统相互作用时呈现增强抑制的功能[17]。并且随着时间的推移精油从纳米乳液中持续释放,延长了精油作用于微生物的时间。当精油添加量为10%时,可以看到大肠杆菌的浓度降低了2.62 lg(CFU/mL),金黄色葡萄球菌的浓度降低了0.85 lg(CFU/mL),并在72 h内保持杀菌效果。
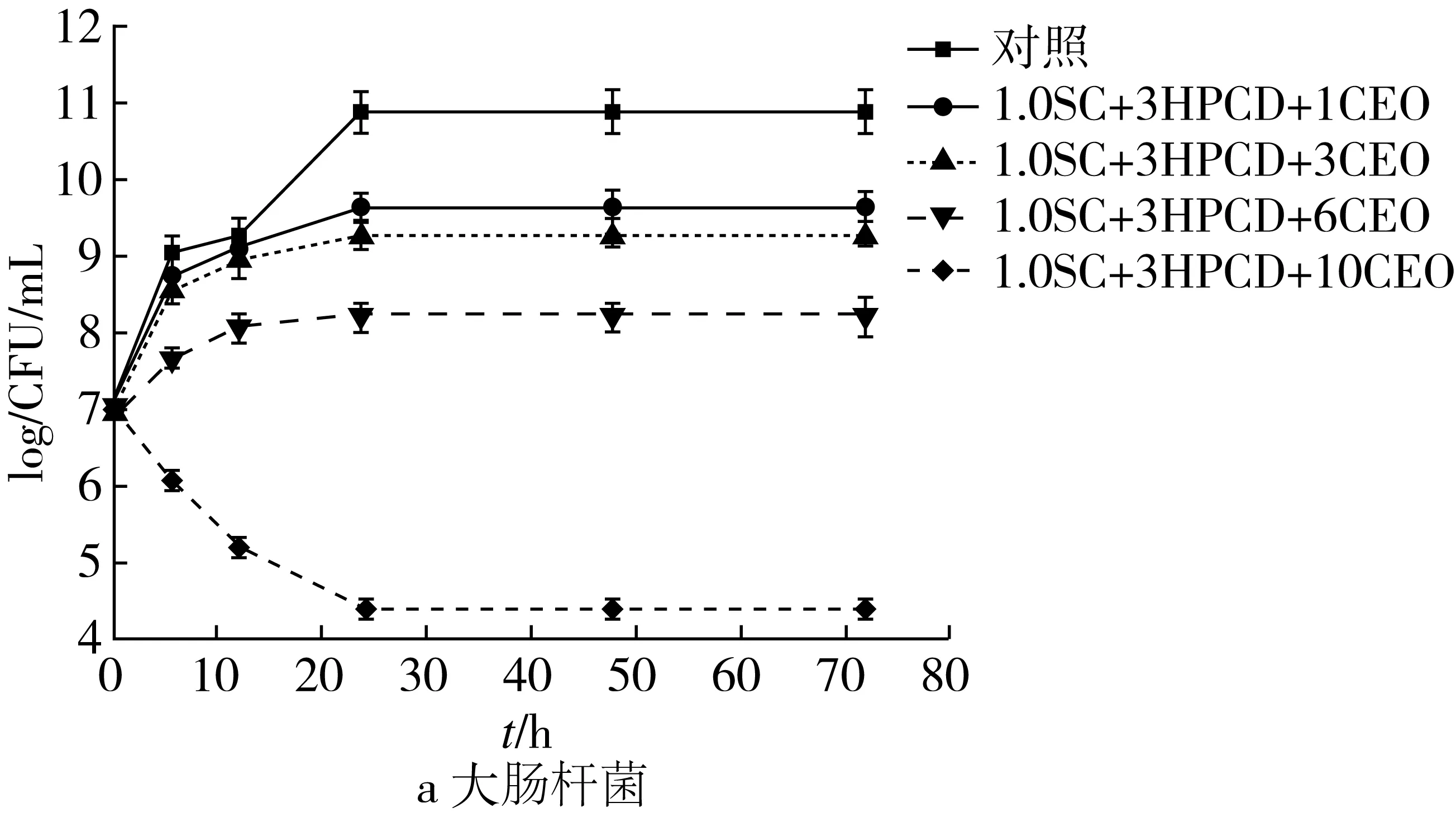
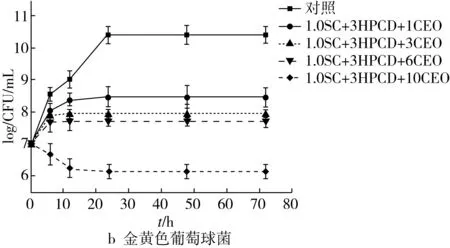
图1 乳液对大肠杆菌和金黄色葡萄球菌的抑菌生长曲线
肉桂精油纳米乳液对大肠杆菌的抑制作用强于金黄色葡萄球菌。革兰氏阴性菌比革兰氏阳性菌更敏感,可能是因为革兰氏阴性菌的外膜和内膜都有精油主要成分(肉桂醛)的靶位点,并且一旦外膜被破坏,细胞质膜就容易接近并破坏,造成细胞质外泄,从而达到更强杀菌效果[18]。
2.3 最小抑菌浓度(MIC)和最小杀菌浓度(MBC)
最小抑菌浓度(MIC)是指抗菌剂能抑制微生物生长的最低浓度,最小杀菌浓度(MBC)是指抗菌剂能杀死微生物的最低浓度,MIC和MBC都可以用来评价抗菌剂的抑菌和杀菌作用的强弱,其数值越小,代表抗菌剂的作用越强。如表2所示,与纯肉桂精油相比,肉桂精油纳米乳液的MIC和MBC均降低,表明精油以纳米乳液形式存在显著增强了其抑菌性,也意味着可以适当调整精油的使用量达到同样的抑菌效果,从而一定程度上降低精油特殊的风味对于食品体系的影响。精油纳米乳液比纯精油具有更好的水溶性、分散性以及更高的比表面积,增大了与微生物的接触机会,此外,具有纳米级别液滴的乳液有可能通过细菌外膜的孔蛋白进行转运,从而提高精油的递送效率并带来更高的抗微生物活性[19-20]。

表2 肉桂精油、HPCD和肉桂精油乳液的MIC和MBC
2.4 贮藏稳定性
4、25、40 ℃是食品加工贮藏中的几个常用温度。1%酪蛋白酸钠和3%HPCD共同稳定的肉桂精油纳米乳液在4、25、40 ℃下贮藏28 d的粒径变化如图2所示。当精油添加量为1%、3%和6%时,乳液的粒径在不同温度下储存均没有明显变化,表明在这些精油体积分数下纳米乳液的稳定性良好。当精油体积分数为10%时,在储存的最初7 d内,液滴的粒径大小增加迅速,但7 d后,粒径增长变缓,乳液趋于稳定。这可能是因为在O/W乳液体系中形成液滴时,新形成液滴在制备过程中获得过多的能量,可能需要一定时间达到热力学平衡[21]。由于奥斯特瓦尔德熟化等作用,小液滴向大液滴靠拢并发生聚集,粒径逐渐上升[22-23]。
2.5 乳化指数测定
乳化指数是表征乳液稳定性的方法,高乳化指数表明乳液由于粒径大、共轭、絮凝或聚集造成乳液不稳定。如图3所示,当精油添加量为1%和3%时,在4、25、40 ℃下28 d的储存期间内没有产生乳化层,说明乳液的稳定性良好,且一定范围内温度对乳液的稳定性无显著影响。当精油添加量增加至6%和10%时,随着储存时间的增加乳化指数有所增加。且温度越高,乳液的乳化指数增长越大,表明乳液的加工贮藏中温度依然对其稳定性有一定影响。
2.6 荧光显微镜
新鲜纳米乳液和25 ℃下储存28 d后纳米乳液的荧光显微镜图如图4~图5所示。新鲜制备的纳米乳液呈现出非常微小且均匀分布的油滴,但仍能观察到随着精油添加量的增加,精油的分布更加密集,并且液滴大小有一定的增长,这与表2中的数据相符。对比新鲜乳液和储存28 d的荧光图,肉眼可见的乳液油滴粒径有明显的增长,这与储藏过程粒径的变化趋势相一致。但从图5中可见,乳液中油滴仍然是分布相对均匀的,包括肉桂精油体积分数为10%时,表明1%酪蛋白酸钠和3%HPCD共同乳化的肉桂精油纳米乳液具备良好的稳定性。



注:a:1.0SC+3HPCD+1CEO;b:1.0SC+3HPCD+3CEO;c:1.0SC+3HPCD+6CEO;d:1.0SC+3HPCD+10CEO,下同。图4 新鲜乳液荧光显微图

图5 25 ℃下储存28 d乳液荧光显微图
3 结论
与单独使用酪蛋白酸钠稳定的乳液相比,HPCD与酪蛋白酸钠共同稳定的乳液具备更低的粒径及PDI值;1%酪蛋白酸钠和3%HPCD共同稳定的肉桂精油纳米乳液对大肠杆菌和金黄色葡萄球菌表现出良好的抗菌作用,以及相比精油自身更低的最小抑菌浓度(MIC)和最小杀菌浓度(MBC)。乳液在4、25、40 ℃下储存过程中的粒径、乳化指数、以及荧光显微镜图均表明1%酪蛋白酸钠和3%HPCD共同乳化的肉桂精油纳米乳液具备良好的稳定性。HPCD 具有亲脂的内部空间和亲水的外部基团,水不溶性的精油可以进入亲脂的内部空间,与HPCD 形成水溶性复合体,从而起到抑制精油的聚集,辅助其他乳化剂降低乳液粒径,增强乳液稳定性的效果。

