2011—2017年我国6个地区乳腺癌内分泌治疗药物应用分析
刘浩然,王萌萌,孙 慧,汤 静
(复旦大学附属妇产科医院药学部,上海 200011)
根据2018年恶性肿瘤数据年度报告,在女性人群中,乳腺癌无论是发病率还是死亡率均居首位[1]。乳腺癌生物学亚型多样,这些生物学亚型直接关系到治疗方案的选择,最常见的乳腺癌类型是激素受体阳性的乳腺癌。一项针对20岁以上女性侵袭性乳腺癌患者的研究结果发现,雌激素受体阳性的乳腺癌患者占79%[2]。《中国乳腺癌内分泌治疗专家共识(2015年版)》也提及,激素受体阳性的乳腺癌患者占60%以上[3]。对于激素受体阳性的乳腺癌患者,内分泌治疗可以改变激素依赖性肿瘤生长所需要的内分泌微环境,是缓解肿瘤进展及降低复发风险的重要手段[4]。《中国乳腺癌内分泌治疗专家共识(2015年版)》及美国国家综合癌症网络(national comprehensive cancer network,NCCN)指南均指出,对于绝经前激素受体阳性的早期乳腺癌患者、绝经后激素受体阳性的早期乳腺癌患者及转移性激素受体阳性乳腺癌患者,均可以考虑内分泌治疗。目前,乳腺癌内分泌治疗药物主要有以下5类:(1)选择性雌激素受体调节剂;(2)选择性雌激素受体下调剂;(3)芳香化酶抑制剂(aromatase inhibitor,AI);(4)卵巢功能抑制剂;(5)孕激素类药物。本研究通过对2011—2017年全国6个地区(北京、广州、杭州、天津、成都和上海)乳腺癌内分泌治疗药物的处方分析,揭示乳腺癌内分泌治疗药物的应用现状及发展趋势。
1 资料与方法
1.1 资料来源
本研究全部数据来源于《医院处方分析合作项目》,抽取北京、广州、杭州、天津、成都和上海6个地区参与该项目的医院作为研究对象。2011—2017年从上述医院共抽取约280个工作日,即每季度抽取10个工作日的处方作为研究样本,从中提取的信息包括临床诊断、处方编码、药品名称、规格、数量、用法、用量和用药金额等。
1.2 随机抽样方法
根据《医院处方分析合作项目》的规定抽取数据:按季度抽取,每月随机抽取3~4 d门诊处方和住院医嘱(只限周一至周五),周末节假日除外,每季度共抽取10 d,保证抽取数据中有两组周一至周五。
1.3 统计方法
使用Microsoft Excel/Sql Server等软件对收集到的数据进行统计和归类,计算用药频度(defined daily dose system,DDDs)及限定日费用(defined daily cost,DDC),并比较2011—2017年6个地区乳腺癌内分泌治疗药物的销售金额、DDDs、DDC及其增长情况。以限定日剂量(defined daily dose,DDD)来计算DDDs,限定日剂量指一个药品以主要适应证用于成年人的维持平均日剂量,DDD主要取自世界卫生组织“ATC&DDD Index 2018”。DDDs的含义为以DDD为单位的某药品的消耗量,DDDs=某药的总用量/DDD;DDDs越大,说明药物的使用频度越高,反映临床对该药的选择倾向性越大。DDC指患者使用某药的平均日费用,DDC=某药年销售金额/该药的DDDs。
1.4 分析评价相关指南依据
依据《中国乳腺癌内分泌治疗专家共识(2015年版)》《Breast Cancer 2018 NCCN Guidelines》《中国抗癌协会乳腺癌诊治指南与规范(2019年版)》及《中国早期乳腺癌卵巢功能抑制临床应用专家共识(2018年版)》,并结合数据汇总结果,对2011—2017年6个地区乳腺癌内分泌治疗药物的使用变化情况及未来发展趋势进行分析讨论。
2 结果
2.1 乳腺癌内分泌治疗药物销售金额及变化情况
2011—2017年6个地区乳腺癌内分泌治疗药物销售金额逐年增长,由2011年的1 191.53万元增至2017年3 406.93万元,与2011年相比,2017年增长了186%。
2.2 乳腺癌内分泌治疗药物的处方数、销售金额及其排序
2011—2017年6个地区乳腺癌患者使用的内分泌治疗药物中,第3代AI类药物来曲唑及阿那曲唑作为经典的内分泌治疗药物,其处方量排序及销售金额排序一直居前2位;他莫昔芬的处方量排序居第3位;依西美坦的销售金额排序居第3位;氟维司群及甲地孕酮无论是处方量排序还是销售金额排序均处于靠后的位置,见表1—2。

表1 2011—2017年我国6个地区乳腺癌内分泌治疗药物具体药品的处方数及排序Tab 1 Number of prescriptions and ranking of endocrine therapy drugs for breast cancer in 6 regions of China from 2011 to 2017
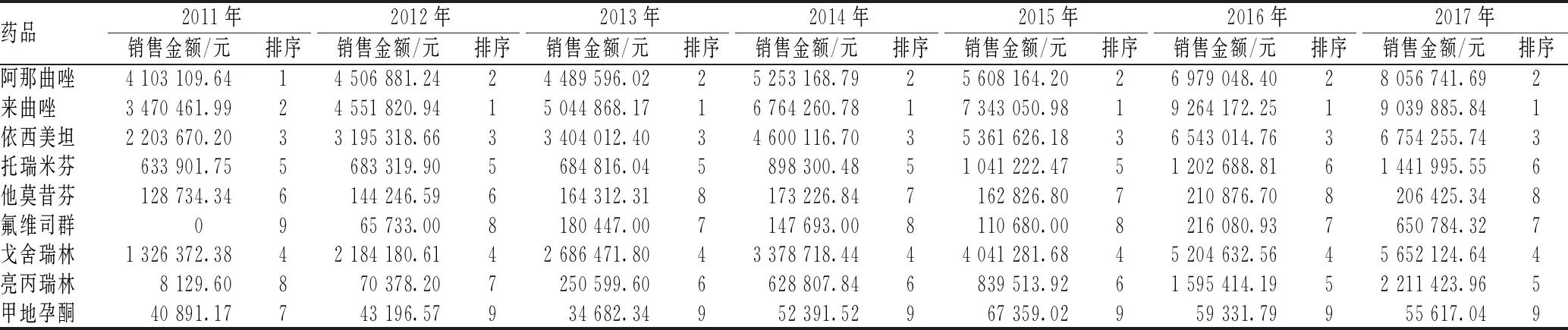
表2 2011—2017年我国6个地区乳腺癌内分泌治疗药物具体药品的销售金额及排序Tab 2 Consumption sum and ranking of endocrine therapy drugs for breast cancer in 6 regions of China from 2011 to 2017
2.3 乳腺癌内分泌治疗药物使用例次数占比及排序
2011—2017年6个地区乳腺癌患者使用的内分泌治疗药物中,第3代AI类药物来曲唑及阿那曲唑作为经典的内分泌治疗药物,使用例次数占比排序居前2位;他莫昔芬使用例次数占比排序居第3位;依西美坦使用例次数占比排序居第4位;氟维司群及甲地孕酮使用例次数占比排序均处于靠后的位置,见表3。
2.4 乳腺癌内分泌治疗药物的DDDs及排序
2011—2017年6个地区乳腺癌患者使用的内分泌治疗药物中,来曲唑、他莫昔芬及阿那曲唑的DDDs排序一直居前3位,紧随其后的是托瑞米芬及依西美坦,氟维司群、亮丙瑞林及甲地孕酮的DDDs排序较靠后;与2016年相比,2017年氟维司群的DDDs升高明显,增幅达469%,见表4。
2.5 乳腺癌内分泌治疗药物的DDC及排序
2011—2017年6个地区乳腺癌患者使用的内分泌治疗药物中,促黄体激素释放激素受体拮抗剂(亮丙瑞林及戈舍瑞林)及选择性雌激素受体下调剂(氟维司群)的治疗费用较高,患者经济负担较重;其中,亮丙瑞林的DDC排序一直居首位,氟维司群及戈舍瑞林紧随其后;与2016年相比,2017年氟维司群的DDC显著降低,降幅达47%;其他乳腺癌内分泌治疗药物的DDC变化不明显;乳腺癌内分泌治疗药物的DDC排序较为稳定,他莫昔芬的DDC排序一直居末位,见表5。
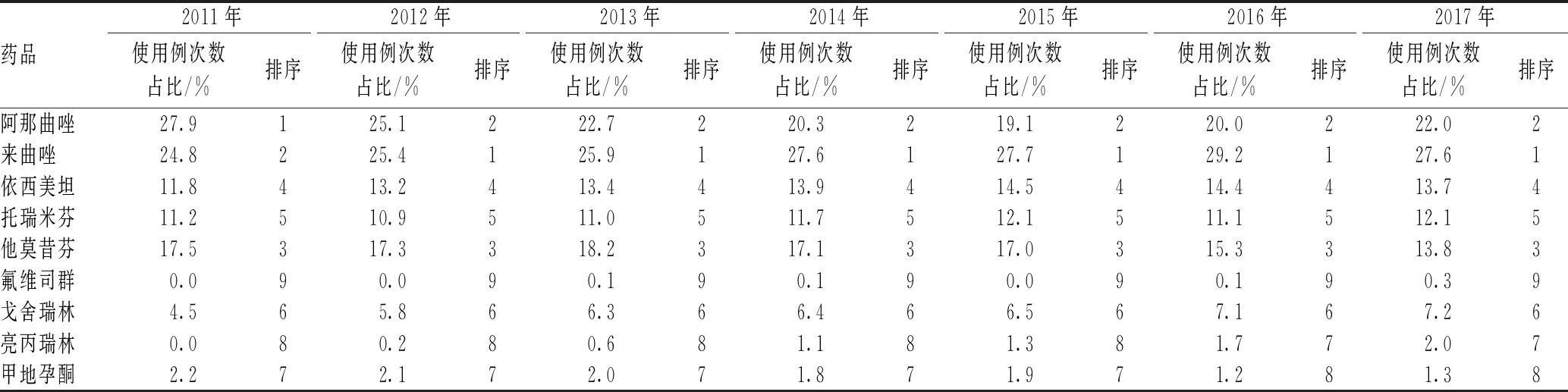
表3 2011—2017年我国6个地区乳腺癌内分泌治疗药物具体药品的使用例次数占比及排序Tab 3 Proportion of users and ranking of endocrine therapy drugs for breast cancer in 6 regions of China from 2011 to 2017
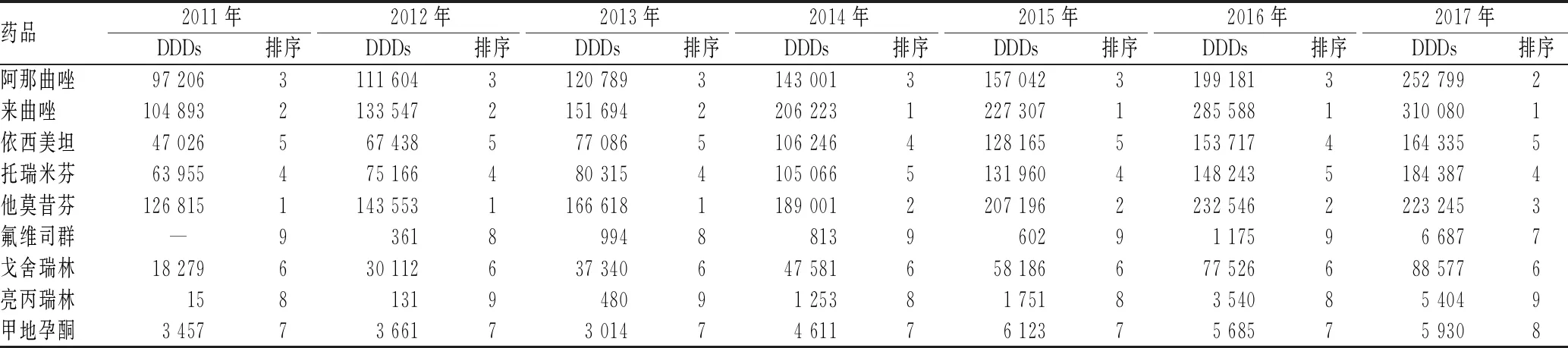
表4 2011—2017年我国6个地区乳腺癌内分泌治疗药物具体药品的DDDs及排序Tab 4 DDDs and ranking of endocrine therapy drugs for breast cancer in 6 regions of China from 2011 to 2017
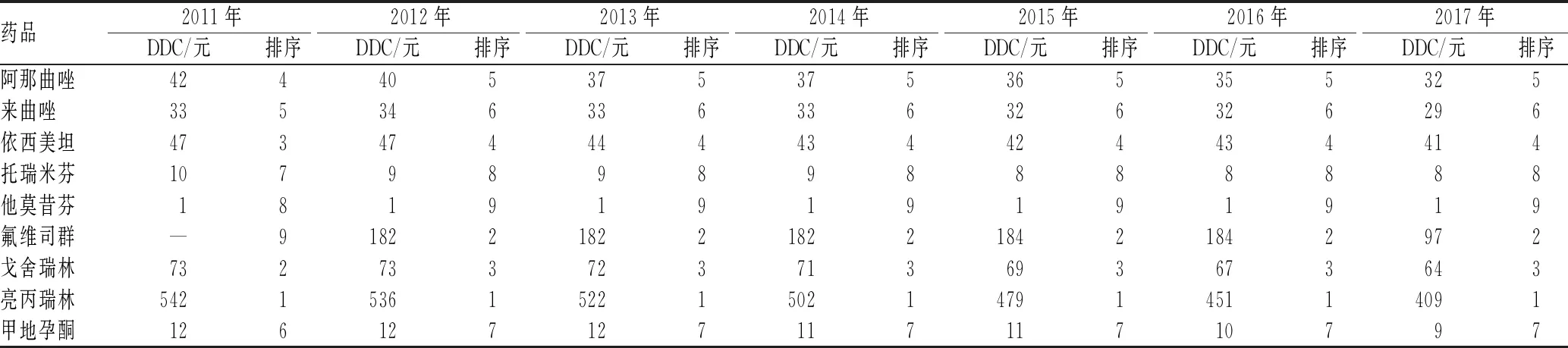
表5 2011—2017年我国6个地区乳腺癌内分泌治疗药物具体药品的DDC及排序Tab 5 DDC and ranking of endocrine therapy drugs for breast cancer in 6 regions of China from 2011 to 2017
3 讨论
对于激素受体阳性的乳腺癌患者,前面述及的指南及专家共识给出了内分泌治疗的指导意见。本研究抽取2011—2017年全国6个地区参与《医院处方分析合作项目》的医院收治的乳腺癌患者内分泌治疗药物的使用数据进行分析,结果显示,乳腺癌患者内分泌治疗药物处方数及总销售金额呈逐年增长趋势,下面就乳腺癌内分泌治疗的药物选择及调研数据进行讨论。
3.1 卵巢功能抑制剂
卵巢功能可通过促性腺激素释放激素激动剂(gonadotropin-releasing hormone agonists,GnRHa)进行抑制,如戈舍瑞林、亮丙瑞林,抽样结果显示, ≤50岁乳腺癌患者GnRHa使用例次数占比较>50岁乳腺癌患者高,≤50岁乳腺癌患者GnRHa使用例次数占比为85.4%,而使用内分泌治疗药物的≤50岁乳腺癌患者为36.3%。绝经前的乳腺癌患者在治疗过程中可能需要考虑到卵巢功能的保护,本次抽样调查中,≤30岁乳腺癌患者使用GnRHa例次数占比达38.04%。研究结果表明,卵巢功能抑制剂用于绝经前乳腺癌患者,能有效预防化疗引起的卵巢功能损伤,具有保护卵巢功能的作用[5]。因而,对于有保留生育功能需求的乳腺癌患者,可以使用GnRHa。
另外,卵巢功能抑制联合内分泌治疗可用于为绝经前女性使用AI类药物创造条件,或者作为他莫昔芬治疗的补充。小型研究结果显示,绝经前女性用GnRHa+AI治疗与绝经后女性单用AI治疗一样有效[6-7]。对于年轻乳腺癌患者,与单用他莫昔芬相比,他莫昔芬联合卵巢功能抑制剂可以显著降低复发风险[8]。研究结果已经证实,联合卵巢功能抑制剂的治疗方案可以使绝经前激素受体阳性的乳腺癌患者受益[9]。本次抽样调查中,联合用药方案有戈舍瑞林+他莫昔芬、戈舍瑞林+托瑞米芬、戈舍瑞林+来曲唑、亮丙瑞林+他莫昔芬、亮丙瑞林+来曲唑、亮丙瑞林+阿那曲唑和亮丙瑞林+依西美坦片等。本次抽样调查结果显示,使用GnRHa的乳腺癌患者中,81.7%的患者联合应用了他莫昔芬或AI类药物。
3.2 选择性雌激素受体调节剂
他莫昔芬是一种选择性雌激素受体调节剂,可通过竞争性地拮抗雌激素受体来抑制乳腺癌细胞的生长,是绝经前女性辅助治疗以及因任何原因而不适合AI治疗的绝经后女性的首选内分泌治疗药物。一项Meta分析对比了绝经前和绝经后接受他莫昔芬治疗5年的女性与未接受治疗的女性,发现第15年时,接受他莫昔芬治疗患者的乳腺癌复发风险显著降低(RR=0.61,95%CI=0.57~0.65)[10]。从本次抽样调查结果看,他莫昔芬治疗乳腺癌的DDC较低,其DDDs排序一直居前3位(见表3),可见患者使用的倾向性较大。托瑞米芬为非类固醇类三苯乙烯衍生物,与他莫昔芬相比,该药与雌激素受体结合后可产生雌激素样和(或)抗雌激素样作用。托瑞米芬可用于绝经后雌激素受体阳性或不详的转移性乳腺癌。研究结果发现,托瑞米芬与他莫昔芬治疗绝经前Luminal型乳腺癌的效果相当,均十分理想[11]。但与他莫昔芬相比,托瑞米芬的价格并没有优势(DDC高于他莫昔芬),因此,托瑞米芬的DDDs比他莫昔芬低。
3.3 AI
芳香化酶可以将外周雄激素转化为雌激素,而AI可通过抑制该酶活性或使该酶失活来降低血浆雌激素水平。常用的AI类药物有阿那曲唑、来曲唑及依西美坦。研究结果已发现,与他莫昔芬相比,AI治疗期间的复发率降低幅度更大,并且治疗期间和治疗后的乳腺癌死亡率均更低[12-13]。因此,对于绝经后乳腺癌患者,AI是优先选择的辅助治疗药物。从本次抽样调查结果看,使用AI的乳腺癌患者中,>45岁人群占比为91.4%。来曲唑、阿那曲唑的处方数排序均高于他莫昔芬,居前2位,2014年以后来曲唑的DDDs排序居首位。有证据表明,不同AI治疗的临床结局是相似的,如果患者对初始治疗AI的耐受性较差,并且其他副作用处理策略无效,则可以换用另一种AI[14-16]。本次抽样调查结果中,阿那曲唑的DDC高于来曲唑,其销售金额和DDDs低于来曲唑,说明患者更倾向于使用来曲唑,即在确保疗效的前提下,安全、经济的药物更易为患者所接受。临床研究结果显示,依西美坦用于治疗绝经后雌激素受体阳性的早期乳腺癌患者,疗效与阿那曲唑相当,但是不良事件多于阿那曲唑[15]。提示患者对依西美坦的依从性可能相对较差。同时,本次抽样调查结果显示,依西美坦的DDC高于来曲唑及阿那曲唑,因而,患者可能会从依从性及经济性2个方面考虑,更倾向于选择来曲唑或阿拉曲唑。本次抽样调查结果也表明,依西美坦的销售金额排序、DDDs排序和使用例次数排序均低于来曲唑及阿那曲唑。
3.4 选择性雌激素受体下调剂
氟维司群是一种雌激素受体拮抗剂,能够竞争性地结合、阻断及下调雌激素受体,理论上氟维司群可克服由他莫昔芬(减少雌激素的来源)导致的耐药[17]。尚无关于氟维司群单药治疗与氟维司群联合AI治疗的对比研究。Ⅲ期临床试验结果显示,一线治疗时,氟维司群单药治疗的益处优于AI单药治疗[18]。但部分患者可能倾向于口服AI,而非肌内注射氟维司群。从本次抽样调查结果看,氟维司群的DDC排序在内分泌治疗药物中居第2位,销售金额、使用例次数占比及DDDs均不高,可见氟维司群在乳腺癌内分泌治疗中的应用并不广泛。但值得一提的是,与2016年相比,2017年氟维司群的使用例次数、处方数和销售金额增长明显,DDC明显降低,DDDs明显升高(增幅达469%),在一定程度上说明氟维司群在乳腺癌内分泌治疗中的应用有所增加。
3.5 孕激素类药物
甲地孕酮是合成的黄体酮衍生物,用于辅助治疗乳腺癌,有研究结果显示,化疗时加用甲地孕酮可减轻化疗所致的不良反应,如胃肠道反应、骨髓抑制及糖代谢异常等,也有改善患者免疫功能的作用[19-20]。从本次抽样调查结果看,甲地孕酮的DDC并不高,其销售金额排序和DDDs排序却靠后,说明其较少应用于乳腺癌的辅助治疗。
综上所述,2011—2017年全国6个地区参加《医院处方分析合作项目》的医院乳腺癌患者内分泌治疗药物处方数及销售金额都呈逐年增长趋势,其中他莫昔芬的DDC仅1元,DDDs较高,患者接受度高。由此可见,疗效确切、经济实惠、副作用小、给药方便不仅可以作为临床医师选择合适药品的参考,也是提高产品市场竞争力的手段。

