(DdO)2DGA萃取Nd(Ⅲ)形成三相的研究
何喜红,卢 淳,叶国安,李林波,3,*,曹 智,王薪尧
(1.西安建筑科技大学 冶金工程学院,陕西 西安 710055;2.中国原子能科学研究院 放射化学研究所,北京 102413;3.陕西省冶金工程技术研究中心,陕西 西安 710055)
乏燃料后处理产生的高放废液(HLLW)有很强的放射性和很大的毒性,对人类和环境造成了长期的潜在危害,分离出其中的Am、Cm等次锕系元素进行嬗变,可大幅降低HLLW对环境造成的放射性危害[1]。为此,国内外开发了多个分离HLLW中锕系元素的流程,酰胺荚醚流程是其中有应用前景的流程之一[2]。
目前的酰胺荚醚流程中,采用N,N,N′N′-四辛基-3-氧戊二酰胺(TODGA)或N,N,N′N′-四(2-乙基己基) -3-氧戊二酰胺(TEHDGA)作为萃取剂[3-5]。这两种酰胺荚醚的萃取容量较小,在正十二烷等后处理常用稀释剂中易形成三相,其中三价镧系元素(Ln(Ⅲ))由于其化学性质与三价锕系元素(如Am(Ⅲ)、Cm(Ⅲ))相似,将随三价锕系元素进入有机相,而HLLW中Ln的含量较三价锕系元素约高1个数量级,因此,镧系元素是导致酰胺荚醚萃取过程形成三相的主要原因。镧系元素中,Nd是HLLW中含量最高的元素之一,且由于镧系元素的化学性质类似,文献[6-9]中常以Nd(Ⅲ)作为代表性的金属离子研究酰胺荚醚的三相行为,本文也选用Nd(Ⅲ)作为被萃离子。
为增加TODGA或TEHDGA的萃取容量,通常采用的方法是加入TBP、单酰胺或醇类作相改性剂,这种方法致使萃取体系复杂[3-5]。此外,还可通过增加烷基取代基碳链长度的方法,增加酰胺荚醚的萃取容量,如Sasaki等[10]设计合成了N,N,N′N′-四癸基-3-氧戊二酰胺(TDDGA)、N,N,N′N′-四(十二烷基)-3-氧戊二酰胺(TDdDGA)等对称酰胺荚醚萃取剂。与TODGA相比,这些长链酰胺荚醚的萃取容量增加,其中0.10 mol/L TDdDGA萃取Nd(Ⅲ)时,即使不加相改性剂,也不会出现三相,而相同萃取条件下,TODGA萃取Nd(Ⅲ)的极限有机相浓度(LOC)为6.4 mmol/L。但当酰胺荚醚的碳链长度增加时,会引起一些其他问题,如萃取剂黏度增加、分相速度变慢等。N,N′-二辛基-N,N′-二(十二烷基)-3-氧戊二酰胺((DdO)2DGA)是一种不对称酰胺荚醚,与TODGA相比,(DdO)2DGA中的2个取代基由正辛基变成了正十二烷基,萃取容量有可能增加;与TDdDGA相比,其分子量较小,萃取剂黏度较低。目前,还没有(DdO)2DGA的相关文献报道,本文拟对其萃取Nd(Ⅲ)的三相行为及三相形成前后(DdO)2DGA-Nd(Ⅲ)萃合物结构的变化进行研究,为(DdO)2DGA的应用提供数据支撑。
1 实验
1.1 主要试剂及仪器
(DdO)2DGA(结构如图1所示),纯度大于95%,青岛中盛宇达化工有限公司合成;正十二烷,分析纯,成都市科隆化学品有限公司;硝酸钕(Nd(NO3)3·6H2O)、硝酸铕(Eu(NO3)3·6H2O),分析纯,上海帝阳化工有限公司;硝酸锆(Zr(NO3)4·5H2O),分析纯,天津科密欧化学试剂有限公司;乙二胺四乙酸二钠(EDTA),分析纯,天津大茂化学试剂厂。
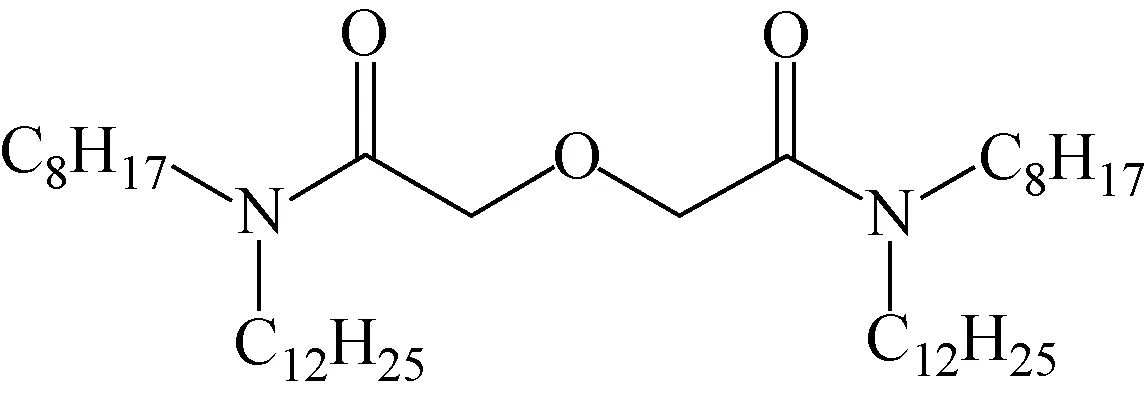
图1 (DdO)2DGA的结构Fig.1 Structure of (DdO)2DGA
TU1901型紫外-可见分光光度计,北京普析通用仪器有限责任公司;iS50型傅里叶全反射红外光谱仪,赛默飞世尔科技有限公司;Fluoromax-4型荧光光谱仪,美国Horiba公司;800B型低速离心机,上海安亭科学仪器厂;GL-88B型旋涡混合器,海门市其林贝尔仪器制造有限公司;DC-0506型低温恒温槽,江苏天翎仪器有限公司。
1.2 方法
1) 萃取实验
有机相为0.10 mol/L或0.20 mol/L (DdO)2-DGA-正十二烷溶液,萃取时,有机相先用对应浓度的硝酸溶液预平衡2次,即有机相与等体积的硝酸溶液振荡混合5 min,离心分相后,弃去水相,有机相再次与等体积的硝酸溶液混合、分相,其中,硝酸浓度与相应萃取实验中的酸度相同。
水相为具有一定硝酸浓度的Nd(NO3)3、Eu(NO3)3或Zr(NO3)4溶液,其中Nd(Ⅲ)、Eu(Ⅲ)的准确浓度采用EDTA滴定法确定,Zr(Ⅳ)的准确浓度采用ICP-AES确定,水相酸度采用标准NaOH溶液滴定得到。
萃取时,将预平衡过的有机相与水相在特定温度下混合5 min,离心分相,观察是否有三相出现以确定LOC,或取有机相、第三相进行光谱测量。
2) LOC测定
往离心管中加入1 mL 预平衡过的有机相和1 mL一定浓度的硝酸,然后加入一定体积的0.20 mol/L Nd(NO3)3溶液,进行萃取实验,观察是否出现三相,如没有出现,再逐步加入0.20 mol/L Nd(NO3)3溶液,重复萃取实验,直至三相出现,此时的有机相Nd(Ⅲ)浓度为(DdO)2DGA萃取Nd(Ⅲ)的LOC。采用EDTA滴定法测定三相出现时水相的Nd(Ⅲ)浓度,根据Nd(NO3)3溶液的加入总量计算水相体积,通过物料衡算计算有机相Nd(Ⅲ)浓度。
测定竞争离子存在条件下的LOC时,实验步骤与上述方法相同,只是将1 mL一定浓度的硝酸溶液改为一定浓度的硝酸铕或硝酸锆溶液(2种溶液的酸度均为3.0 mol/L),由于该条件下水相含有2种金属离子,其浓度的测量采用ICP-AES。
3) 光谱测定
LOC测量时生成三相的量很少,不足以进行光谱测定,为此采用高浓度的硝酸钕溶液(或硝酸铕溶液),即5 mL 0.10 mol/L (DdO)2DGA溶液与5 mL 0.20 mol/L Nd(NO3)3溶液(酸度为3.0 mol/L)进行萃取实验,取第三相进行光谱测定。为对比,制备未出现三相的样品,采用等体积的0.10 mol/L (DdO)2DGA和0.010 mol/L Nd(NO3)3(酸度为3.0 mol/L)进行萃取实验,取负载有机相作为两相体系的样品进行光谱测定。
红外吸收光谱采用ATR(衰减全反射)附件直接测定;紫外-可见吸收和荧光光谱测定时,样品封装在10 mm×3 mm的比色皿中进行扫描,其中测定荧光光谱的激发波长设定为395 nm,测定荧光寿命的激发波长和发射波长分别设定为395 nm和613 nm。
2 结果与讨论
2.1 (DdO)2DGA萃取Nd(Ⅲ) 形成三相的条件
(DdO)2DGA-正十二烷体系萃取Nd(Ⅲ)时,当负载有机相中的Nd(Ⅲ)浓度大于特定值时,有机相分裂,出现第三相。形成三相的难易可用LOC表征,影响LOC的因素包括酸度、温度、萃取剂浓度,以及共存离子浓度。
1) 酸度

图2 酸度对(DdO)2DGA萃取Nd(Ⅲ)的LOC的影响Fig.2 Influence of acidity on LOC of Nd(Ⅲ) in (DdO)2DGA
在温度为25 ℃、(DdO)2DGA浓度分别为0.10 mol/L和0.20 mol/L、无共存离子的条件下,酸度对LOC的影响如图2所示。由图2可见,LOC随酸度的增加而减小,这主要是由于(DdO)2DGA对硝酸有一定的萃取能力,随着酸度的增加,萃入有机相的硝酸浓度增加,萃取Nd(Ⅲ)的LOC将下降。相比之下,酸度从2.5 mol/L增加到 3.5 mol/L的过程中LOC下降较多,而酸度从3.0 mol/L增加到6.0 mol/L的过程中LOC变化较小。对于不同浓度的(DdO)2DGA,浓度越高,有机相的极性越大,LOC也越大,即越不易出现三相,但LOC随酸度的变化规律是一致的。与TODGA相比,(DdO)2DGA的2个烷基链由正辛基变成了正十二烷基,由于烷基链长度的增加,萃取容量也增加,如0.10 mol/L TODGA从3.0 mol/L 硝酸中萃取Nd(Ⅲ)的LOC为6.4 mmol/L[10],而对应条件下(DdO)2DGA的LOC为23 mmol/L,因此,采用(DdO)2DGA作萃取剂时,有机相可负载更高浓度金属离子而不出现三相。
2) 温度
在硝酸浓度为3.0 mol/L、(DdO)2DGA浓度分别为0.10 mol/L和0.20 mol/L、无共存离子的条件下,温度对LOC的影响示于图3。由图3可见,2种(DdO)2DGA浓度下,LOC均随温度的升高而增大,这主要是由于萃合物在正十二烷中的溶解度随温度而增加所致。为此,可通过适当升高温度的方法抑制三相的出现。

图3 温度对(DdO)2DGA萃取Nd(Ⅲ)的LOC的影响 Fig.3 Influence of temperature on LOC of Nd(Ⅲ) in (DdO)2DGA
3) 共存离子
酰胺荚醚对三、四价金属离子的萃取能力强,高放废液中的主要三价金属离子是三价锕系元素和Ln(Ⅲ),主要四价金属离子为Pu(Ⅳ)和Zr(Ⅳ),这些金属离子对酰胺荚醚萃取三相的形成都有贡献。为此,选择Eu(Ⅲ)和Zr(Ⅳ)作为代表性的共存离子,研究其对(DdO)2DGA萃取Nd(Ⅲ)的LOC的影响(实验条件为:硝酸浓度3.0 mol/L、(DdO)2DGA浓度0.10 mol/L、温度25 ℃),结果示于图4。由图4可见,Nd(Ⅲ)的LOC随有机相Zr(Ⅳ)和Eu(Ⅲ)浓度的增加线性下降,拟合方程分别为y=-1.42x+20.4(R2=0.989 9)和y=-1.09x+21.4(R2=0.981 6),即有机相Zr(Ⅳ)浓度每增加1 mmol/L,Nd(Ⅲ)的LOC下降约1.42 mmol/L,而有机相Eu(Ⅲ)浓度每增加1 mmol/L,Nd(Ⅲ)的LOC下降1.09 mmol/L。由此可见,Zr(Ⅳ)对LOC的影响更大,这主要是由于Zr(Ⅳ)的电荷更高,离子半径更小,形成的萃合物的极性更大,为此萃入有机相后更易出现三相。

图4 共存离子对(DdO)2DGA萃取Nd(Ⅲ)的LOC的影响Fig.4 Influence of coexisting ion on LOC of Nd(Ⅲ) in (DdO)2DGA
2.2 (DdO)2DGA萃取Nd(Ⅲ)形成三相的光谱分析

第三相和负载有机相的紫外-可见吸收光谱示于图6。Ln(Ⅲ)的紫外-可见吸收光谱是由4f电子的f-f跃迁形成的,配位环境的变化会引起吸收峰的改变,尤其是超灵敏吸收峰[12-13]。对于Nd(Ⅲ),超灵敏吸收峰处于500~600 nm之间。由图6可看出,负载有机相和第三相的光谱基本一致,超灵敏吸收峰也无明显变化,表明三相形成前后萃合物的配位形式没有改变,这与图5一致。
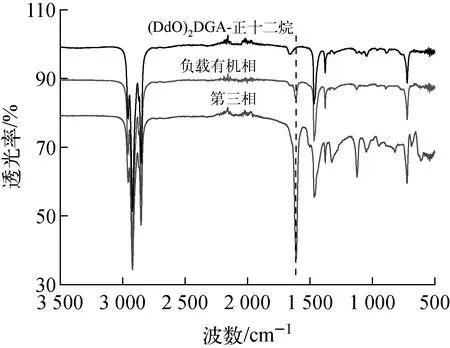
图5 (DdO)2DGA及其萃合物的红外谱Fig.5 Infrared spectrum of (DdO)2DGA and (DdO)2DGA-Nd(Ⅲ) complex

图6 (DdO)2DGA-Nd(Ⅲ)萃合物的紫外-可见吸收光谱Fig.6 UV-vis spectrum of (DdO)2DGA-Nd(Ⅲ) complex
为进一步研究形成三相前后萃合物结构的变化,测定了萃合物的荧光光谱和荧光寿命。由于Nd(Ⅲ)的荧光强度弱,不能直接测定,而Ln(Ⅲ)的化学性质相似,形成的配合物结构通常也一致,尤其是原子序数相近的Ln(Ⅲ),为此,常采用Eu(Ⅲ)代替Nd(Ⅲ)进行测定[14-15]。(DdO)2DGA-Eu(Ⅲ)萃合物的荧光光谱如图7所示。由图7可见,第三相和负载有机相的荧光光谱一致,均含有4个吸收带,分别位于592、613、648、698 nm处,表明三相形成前后萃合物的结构不变。
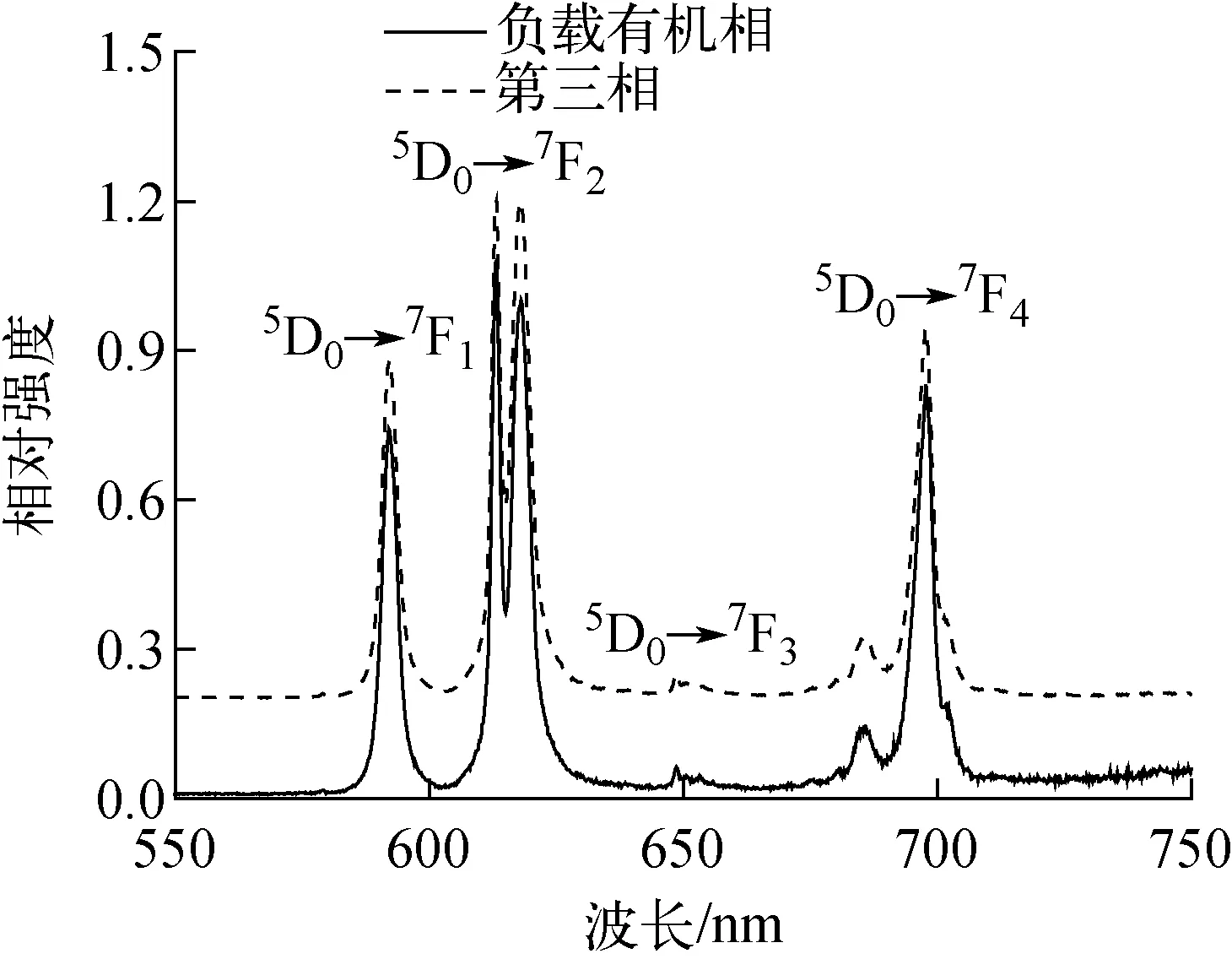
图7 (DdO)2DGA -Eu(Ⅲ)萃合物的荧光光谱Fig.7 Fluorescence spectrum of (DdO)2DGA-Eu(Ⅲ) complex

图8 (DdO)2DGA -Eu(Ⅲ)体系的荧光衰减曲线Fig.8 Fluorescence decay of (DdO)2DGA-Eu(Ⅲ) complex
萃合物的荧光寿命衰减曲线示于图8,可见两个体系的荧光寿命相差很小,且均符合一次指数函数的衰变规律,表明(DdO)2DGA与Eu(Ⅲ)只形成一种萃合物物种,且在三相形成前后不变。根据荧光衰减曲线拟合萃合物的荧光寿命,进一步采用Takaumi等[16]拟合的经验公式(式(1))计算Eu(Ⅲ)的内层配位水分子数,结果列于表1。对于第三相和负载有机相样品,配位水分子数均为0,即萃合物中水分子没有直接与金属离子键合。由于Eu(Ⅲ)和Nd(Ⅲ)的相似性,可推测(DdO)2DGA-Nd(Ⅲ)萃合物的结构在三相形成前后也无变化,且萃合物内配位层无水分子。
NH2O=1.05×10-3kobs-0.44=
1.05×10-3/τobs-0.44
(1)
式中:NH2O为配位水分子数;kobs为荧光衰减系数;τobs为荧光寿命。

表1 (DdO)2DGA-Eu(Ⅲ)萃合物的荧光寿命及配位水分子数Table 1 Fluorescence lifetime and hydration number of (DdO)2DGA-Eu(Ⅲ) complex
综合图5~7可知,(DdO)2DGA在萃取Nd(Ⅲ)形成三相前后,萃合物结构没有变化。文献[17-19]在研究TODGA等酰胺荚醚与Ln(Ⅲ)的配位结构时发现,酰胺荚醚与Ln(Ⅲ)的配位比为(3~4)∶1,水分子和硝酸根没有和Ln(Ⅲ)直接键合。本文的研究结果表明,(DdO)2DGA-Ln(Ⅲ)萃合物中,水分子也没有与Ln(Ⅲ)配位,且萃合物的光谱和寿命与文献[17-21]的结果相近,由此推测,在第三相及负载有机相中,也是3~4个(DdO)2DGA与Ln(Ⅲ)配位。
形成三相前后,(DdO)2DGA-Nd(Ⅲ)萃合物的结构没有变化,则说明(DdO)2DGA萃取三相的出现与萃合物/萃取剂的聚集行为相关。文献[22-24]研究了TODGA等酰胺荚醚在正十二烷中的聚集行为,发现酰胺荚醚萃取金属离子后以反胶束的形式存在,随着有机相金属离子浓度的升高,聚集体极性内核之间的相互作用增加,粒径逐渐增大,当增大到一定程度后,出现三相。由于(DdO)2DGA分子的骨架结构与TODGA相同,可推测(DdO)2DGA萃取Nd(Ⅲ)形成三相也主要是由于(DdO)2DGA-Nd(Ⅲ)萃合物的聚集形态改变所致。
3 结论
1) (DdO)2DGA萃取Nd(Ⅲ)时会有三相出现,但与TODGA相比,在相同萃取条件下,(DdO)2DGA萃取Nd(Ⅲ)的LOC有较大的增加。此外,降低酸度、升高温度、降低共存离子浓度,会增加(DdO)2DGA萃取Nd(Ⅲ)的LOC。
2) 形成三相前后,(DdO)2DGA-Nd(Ⅲ)萃合物的结构没有发生变化,三相的形成是由萃合物聚集形态改变所致。
——酸度

