肿瘤模型研究进展及应用
陈莹莹 吴玉亮 综述 程忠平 审校
随着国内肿瘤发病率和死亡率逐年攀升,肿瘤成为2010年以来的主要死因,是我国一个重大的公共卫生问题[1]。由于目前的肿瘤研究模型尚未模拟体内肿瘤,临床前的治疗研究与临床研究结局往往存在较大差距。构建理想的肿瘤研究模型为目前肿瘤研究领域的重点之一。目前,肿瘤模型包括自发瘤模型、动物诱癌模型、人源性肿瘤细胞系(patientderived tumor cell lines,PDC)、人源性肿瘤异种移植物(patient-derived tumor xenograft,PDX)、多细胞肿瘤球体模型和肿瘤类器官模型。PDC 在无限传代的过程中,基因组不可避免地发生了改变,且基于平面培养体系建立起来的肿瘤平面模型缺乏原始肿瘤的结构、异质性及肿瘤基质间的相互作用,从而限制了细胞系作为临床前模型的潜力[2]。PDX 的缺陷为培养时间长、成瘤率低、早期发生克隆选择[3]而改变了原始肿瘤的异质性,尚不能作为肿瘤研究的理想模型。随着3D培养技术逐渐成熟,建立了肿瘤3D培养模型,包括肿瘤悬浮球模型和肿瘤类器官模型。这两种模型不仅模拟了原始肿瘤的生长环境,而且很好地模拟了细胞-细胞和细胞-基质间的相互作用。但肿瘤悬浮球因其穿透性差、成像困难、药物筛选时的差异性大,从而限制了其在肿瘤研究方面的应用[4]。类器官作为最新的肿瘤研究模型,具有培养简单、成瘤率高、适合高通量药物筛选和遗传操作等优点,并且在最大程度上维持了原始肿瘤的结构和异质性,在肿瘤研究领域已大规模应用[5]。随着类器官在药物筛选领域的应用,临床上针对患者的个体化药物成为现实,进一步推动了精准医疗的发展[2]。
1 动物诱癌模型
在动物身上诱发出与人癌相类似的恶性肿瘤,称为癌模型,其目的在于获得与临床相对应的基础资料。动物诱癌模型是利用致癌物在动物模型体内诱发癌变的模型,如大肠癌、膀胱癌、口腔癌、肺癌、食管癌、胰腺癌、肝细胞癌和乳腺癌等[6]。王玉民等[7]使用wistar 大鼠研究了238钚诱发骨肉瘤及其剂量-效应相关模式,建立了稳定的骨肉瘤实验动物模型,并从骨肉瘤组织中,分离出骨肉瘤细胞系,建立了稳定的瘤细胞模型,组成了完善的骨肉瘤模型系统,提示在工业作业中向空气排放的有毒物质,可以导致骨肉瘤,威胁着人类的健康。动物癌模型的建立为环境和食物诱导癌症的防治提供了重要的理论依据,并且也为癌症的一级预防提供了方向[6]。
2 肿瘤细胞系模型
肿瘤细胞系是利用患者的肿瘤组织,在平面培养体系下建立起来的一种平面永生化细胞模型,具有易于构建、培养周期短、存活率高,能够进行高通量药物筛选的优点[5]。在20世纪70年代,有研究建立了第一个人类永生细胞系即HeLa宫颈癌细胞系。随着细胞遗传学、2D培养体系等技术的不断完善,细胞系作为应用最为方便、高效的肿瘤模型被广泛应用[8]。
随着研究的深入,细胞系模型的缺点也逐渐显露出来。在2D 培养条件下,由于缺乏肿瘤组织的免疫微环境和血管网络系统,细胞系模型并不能维持原始肿瘤细胞的遗传表型和遗传异质性,而且不能重现原始肿瘤组织的形态及功能[8]。随着肿瘤研究的深入展开,细胞系模型已逐渐不能满足研究人员的需求,与原始肿瘤更为相似的肿瘤模型成为了肿瘤研究的必备选项。
3 肿瘤异种移植物模型
PDX 是指将患者来源的肿瘤组织直接移植(原位或异位)到免疫缺陷的动物体内而得到的异种移植物。由于直接取肿瘤组织进行移植,肿瘤细胞及其细胞基质可以很大程度的保留下来,所以PDX 可以较大程度上维持原始肿瘤的异质性以及肿瘤与其周围基质间的相互作用,目前已用于临床前药物评估和生物标志物的鉴定[9]。
早在1775年,人类便尝试着将肿瘤组织移植到动物体内。之后,Toolan[10]研究证明了人类的肿瘤细胞能够在辐射过的小鼠和大鼠体内生长。此外,当X射线辐射过的宿主用免疫系统抑制因子可的松治疗时,肿瘤组织的增殖能力显著增加。随后,Phillips等[11]使用抗淋巴细胞的血清治疗宿主小鼠,尤其当与胸腺切除联合使用时,PDX 的存活比例会大大增加,这表明抑制免疫反应可以提高移植效率。
此后,免疫缺陷的小鼠模型也逐渐建立,使得肿瘤组织的移植效率大大增加。严重联合免疫缺陷(severe combined immunodificiency,SCID)小鼠、非肥胖糖尿病/重症联合免疫缺陷(non-obese diabetes/severe combined immunodificiency,NOD-SCID)小鼠等免疫缺陷小鼠模型被广泛用于肿瘤研究,使得PDX临床前模型的研究得到了飞速发展[12]。各种恶性肿瘤的PDX临床前模型也相继建立,包括结直肠癌、胰腺癌、乳腺癌、肺癌、皮肤癌、头颈部肿瘤、前列腺癌和卵巢癌[13]。然而由于移植时并不能将整个肿瘤组织移植到小鼠体内,免疫缺陷小鼠所培养的肿瘤移植物可能无法捕获原始肿瘤组织的全部遗传特性[14],与原始肿瘤仍具有一定的遗传差异性。
Morgan等[5]与对原发性非小细胞肺癌的PDX进行突变数的检测发现,仅有43%的突变被检测到,并且在PDX早期传代中发现4个原始肿瘤中不存在的突变,提示克隆选择和突变可能发生在肿瘤组织植入小鼠的早期过程中。因此,PDX尚未完全模拟体内肿瘤。除此之外,PDX移植成功率仍然非常有限,在不同癌症中差异很大[15]。且PDX的周期往往较长,遗传操作困难,造模成本往往非常高。研究者们期待成功率更高、周期更短、性价比更高、与体内原始肿瘤更为相似的肿瘤模型(表1)。
4 肿瘤3D培养模型
近年来,研究者们建立了一种3D培养系统,将细胞引入一个多孔生物相容性支架中[16],使细胞能够脱离平面而悬浮培养,以3D 的方式进行生长。体外3D 培养体系包括顶部矩阵、矩阵嵌入、矩阵封装、自旋器烧瓶、微型图板、超低吸附板、悬挂滴、磁悬浮和磁性3D打印等[4]。3D培养模型可分为全动物和器官外植体培养(包括胚胎)、细胞球体、微载体培养和组织工程研究模型,目前用于广泛的细胞生物学研究,包括肿瘤生物学、细胞黏附、细胞迁移和上皮形态的发生[17]。肿瘤3D 培养模型的建立,使肿瘤的治疗方法变得更为具体和个性化[18]。与2D 培养系统相比,3D 培养系统模拟了原始肿瘤的生长环境,使得肿瘤细胞可以由一种细胞或多种细胞形成肿瘤球体模型,从而更好地模拟了细胞-细胞和细胞-基质间的相互作用[19]。目前,常见的肿瘤3D 模型包括多细胞肿瘤球体(multicellular tumor spheroids,MCTS)模型和肿瘤类器官(patient derived tumor organoids,PDO)模型。
4.1 多细胞肿瘤球体模型
多细胞肿瘤球体模型(multicellular tumor spheroids,MCTS)是将患者来源的组织和细胞进行物理和酶促解离,形成单细胞悬浮液,然后将获得的单细胞悬浮液在在具有无血清培养基的低附着板中培养,形成多细胞肿瘤球体模型。该低附着板是由于覆盖一层薄层惰性底物(琼脂、琼脂糖或聚甲基丙烯酸羟乙酯(hydroxyethyl methacrylate,HEMA),使得细胞与培养皿之间的黏附性降低,促进了细胞与细胞之间的聚集和紧密生长,从而形成能够悬浮生长的多细胞肿瘤球体[20]。
MCTS被广泛用于肿瘤细胞的代谢[21]、侵袭和转移[22]及肿瘤相关信号通路[23]、抗癌药物的筛选[24]等研究。虽然肿瘤球体模型作为3D培养模型的先驱曾被广泛应用,但也面临着巨大的挑战。一方面,球体尺寸和均匀性一致性差,光散射差异以及抗体穿透性差,其成像困难,且用于药物筛选/敏感实验时差异性较大,限制了应用;另一方面,由松散排列的细胞形成的球体处理难度高,极易碎裂[4],操作难度高,不适合用于大规模实验。更重要的是,肿瘤球体模型虽然空间上很大程度模拟了原始肿瘤的三维结构,但仍缺乏肿瘤微环境与免疫系统的相互作用,限制了肿瘤球体模型在肿瘤研究中的应用。因此,类器官模型研究应运而生。
4.2 肿瘤类器官模型
类器官是指成体干细胞或胚胎干细胞在体外3D培养体系下,自组装形成能够反映原始组织(成体干细胞来源)或定向分化组织(胚胎干细胞来源)特性的具有3D结构的组织类似物[25]。在特殊的培养条件下,肿瘤类器官模型能在一定程度上模拟肿瘤微环境,为肿瘤的体外研究提供了与体内环境更为相似的研究平台(图1)。

表1 常见的肿瘤模型之间的比较
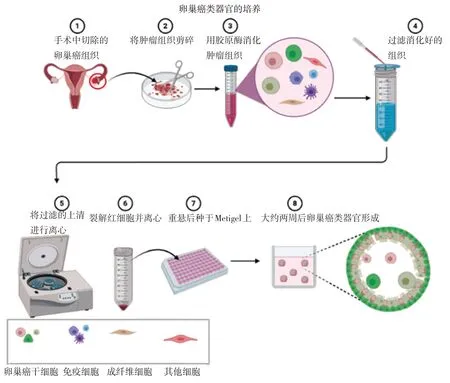
图1 卵巢癌类器官的培养过程
早在2009年,有研究通过在Lgr5+干细胞的Matrigel中加入R-spondin-1、表皮生长因子(epithelial growth factor,EGF)和Noggin,成功建立了mini-gut类器官培养体系[26]。在此培养体系基础上建立了成体干细胞来源的、能够自我更新、增殖并分化形成后代所必需的信号转导因子的小肠类器官。类器官在正常组织上的成功尝试与应用,使得类器官培养技术在肿瘤研究领域也快速发展,如结肠、胰腺、前列腺、乳腺、胃、肺、食管、膀胱、卵巢、肾脏、肝脏等肿瘤组织[13]。这些肿瘤类器官均具有一个非常重要的特征,能够部分或完全重现原始肿瘤的异质性[27],非常适合用于肿瘤研究。
Kopper 等[28]团队利用不同患者的卵巢癌组织分别培养了卵巢癌类器官,测序结果表明不同来源的卵巢癌类器官之间存在异质性。随后该研究使用卵巢癌化疗方案中常用的铂/紫杉醇类和非铂类药物测试化疗药物对患者来源的卵巢癌类器官体的敏感性,结果表明不同患者来源的卵巢癌类器官的药物反应是存在明显差异的,这与临床治疗中的个体差异相契合[28]。这提示类器官非常适用于精准医疗,能够在很大程度上解决由于个体差异而出现的不同患者对同一治疗方案的显著差异化问题,改善患者的预后[2]。源自患者的肿瘤类器官可用于高通量药物筛选和药物敏感试验,为个体化治疗提供了强有力的证据,为精准医疗的进一步发展提供了依据。
类器官在肿瘤机制研究也中有着较大的价值。肿瘤的发展是一个高度动态的过程,其突变通常因肿瘤细胞快速DNA复制而累积,包括染色体不稳定、微卫星不稳定以及表观遗传修饰的变化[2]。由于肿瘤的病因复杂、在发展的过程中受到多种因素的调控,所以应从多角度出发,对其发生机制进行研究,尤其是分子层面,如肿瘤的基因调控与信号转导。采用CRISPR-cas9介导的基因工程地在健康的人来源的结肠组织类器官上成功逐步重现了腺瘤-癌的发生发展过程[29-30],在肿瘤类器官上看到了巨大的研究价值。目前,研究证实结直肠癌的发生和WNT、TGFβ、TP53、PI3K/MAPK通路的突变有关[29]。后续的研究证实,这一系列的致癌突变能有效促进结直肠癌的生长、转移和定植[31]。
5 结语
目前,常用的肿瘤研究模型是PDC 和PDX,但因PDC 缺乏原始肿瘤的异质性,PDX 培养周期长、成瘤率低,应用存在一定的局限性。而3D 培养模型的建立为肿瘤研究提供了新的思路,体外3D 培养技术的产物更能模拟原始肿瘤的生长环境和形态,然而MCTS 因穿透性差、成像困难,而限制了其发展。肿瘤类器官作为一个新兴肿瘤研究模型,为肿瘤研究提供了新的平台。因其能在一定程度上保留肿瘤异质性,并能长期传代和冷冻保存,而被广泛用于肿瘤机制、精准医疗等领域的研究。但类器官仍存在局限性,且尚不能完全模拟肿瘤细胞与基质间的相互作用,也缺乏脉管系统,与体内肿瘤环境还有一定差距。随着精准医疗的逐步发展,相信肿瘤类器官能进一步发展,更大程度上模拟体内肿瘤,成为肿瘤个体化治疗的有力工具。

