异槲皮苷改善胰岛素抵抗作用机制网络药理学分析
张传艺,黄桂红








【摘要】目的:基于网络药理学方法探讨异槲皮苷改善胰岛素抵抗相关靶点之间的相互作用及其作用机制。 方法:通过TTD(Therapeutic Target Database)、swiss Target Prediction以及PubChem数据库找出异槲皮苷单成分基因靶点,再通过DisGeNET、Genecards、OMIM数据库设置筛选条件,优选分数及相关性高的胰岛素抵抗疾病靶点进行汇总,利用Venny软件找到异槲皮苷与胰岛素抵抗的共同靶点;利用STRING、DAVID、KEGG数据库进行PPI蛋白网络互做分析及富集(GO)分析和KEGG pathway分析;通过Cytoscape软件构建异槲皮苷改善胰岛素抵抗的“单成分-靶点-通路-疾病”的网络模型。结果:检索异槲皮苷基因靶点114个,检索胰岛素抵抗疾病靶点经筛选获取563个,异槲皮苷和胰岛素抵抗的共同靶点24个,其中核心靶点18个,预测核心靶点INSR、PI3K、AKT2、GSK-3为关键靶基因在 PI3K -Akt、mTOR、胰岛素抵抗、糖尿病心肌病等信号通路上参与糖异生途径、糖代谢、脂质代谢、抗炎等生物过程来发挥改善胰岛素抵抗的作用[1]。结论:异槲皮苷通过多靶点、多通路构建“单成分-靶点-通路”的机制改善胰岛素抵抗的发生与发展,为未来研究异槲皮苷影响关键靶基因在信号通路上mRNA和蛋白表达作用奠定基础。
【关键词】网络药理学 异槲皮苷 胰岛素抵抗 作用机制
【中图分类号】R587.1 【文献标识码】A 【DOI】10.12332/j.issn.2095-6525.2020.
异槲皮苷(isoquercitrin, IQ)又名罗布麻甲素 ,属于黄酮醇类化合物,广泛存在于砂仁、桑叶、罗布麻等多种药用植物当中 ,也可人工合成。异槲皮苷作为药用植物的有效成分具有许多药理作用,如抗炎、抗肿瘤、降血压、降血脂等[2]。异槲皮苷具有较大的药用价值和应用前景,值得深入开发研究。单一成分的化学药物可能特异性地作用于受体蛋白、生物膜通道、跨膜信号转导蛋白等多个不同类型的靶点。中药的复杂体系,使中药小分子与靶点之间的联系更加复杂。 网络药理学能从基因、分子水平去分析多种药物分子作用于不同靶点、细胞和器官的生物学行为,能系统地预测和揭示不同药物分子的作用及机制,帮助人们分析药物对疾病网络的干预与影响,更全面地了解药物治疗作用与疾病病理基础。[3]
现已有部分关于异槲皮苷通过影响某些信号通路上的基因靶点而改善某些疾病的报道,如异槲皮苷可抑制ERK激酶(MEK)/细胞外调节蛋白激酶(ERK)信号通路促进核因子E2相关因子1(Nrf1)表达,实现对糖尿病肾病(DN)肾脏纤维化的修复[4]。又如异槲皮苷有诱导Hep G2细胞凋亡的作用,其作用机制可能与对Raf/MEK/ERK信号通路中相关因子的干预有关[5]。一方面,本研究可以运用网络药理学提前构建出这些基因靶点的理论模型,为实验验证节约时间;另一方面,为未来更深入研究异槲皮苷可激活胰岛素抵抗等疾病相关信号通路上关键靶基因的mRNA和蛋白表达等作用延展实验提供一定的理论依据[6]。
1 材料与方法
1.1材料
TTD数据库(http://db.idrblab.net/ttd/)、Swiss Target Prediction数据库(http://www.swisstargetprediction.ch/)、PubChem数据库(https://pubchem.ncbi.nlm.nih.gov)、DisGeNET数据库(https://www.disgenet. org/)、Genecards数据库 (https://www.genecards.org/)、OMIM数据库(https://omim. org)、Venny作图软件(https://bioinfogp.cnb.csic.es/tools/venny/)、STRING数据库(https://string-db.org/)、DAVID数据库(https://david.ncifcrf.gov/)、KEGG数据库(https://www.kegg.jp/kegg/kegg3a.html)、 Cytoscape作图软件。
1.2方法
1.2.1异槲皮苷靶点的筛选
利用TTD数据库(http://db.idrblab.net/ttd/)、Swiss Target Prediction數据库(http://www.swisstargetprediction.ch/)以及 PubChem数据库(https://pubchem.ncbi.nlm.nih.gov)找到异槲皮苷的基因靶点并进行汇总。
1.2.2胰岛素抵抗靶基因的筛选
利用DisGeNET数据库(https://www.disgenet.org/)、Genecards数据库 (https://www.genecards.org/)、OMIM数据库(https://omim.org)输入关键词“insulin resistance”查找胰岛素抵抗发病基因,分别下载,其中筛选条件设置为:DisGeNET数据库(https://www.disgenet.org/)优选胰岛素抵抗分数≥0.1,Genecards数据库 (https://www.genecards.org/)优选胰岛素抵抗相关性≥20,最后将三个数据库中的所有基因整理汇总,作为胰岛素抵抗的疾病靶基因。
1.2.3成分-靶标网络的构建
利用Venny作图软件(https://bioinfogp.cnb.csic.es/tools/venny/),针对异槲皮苷有效靶点和胰岛素抵抗靶基因取交集,找到异槲皮苷和胰岛素抵抗的共有基因靶点,得到相应名称和个数。
1.2.4 PPI蛋白网络互做分析(Protein-Protein Interaction,PPI)
利用STRING数据库(https://string- db.org/),在“Multiple proteins”一栏输入共同靶点基因名称,选择人源基因(Homo sapines),得到PPI蛋白网络互做图,同时设置最低要求互动分数条件为 0.900及以上,得到PPI蛋白网络互做分析图,找出关键基因,再作图进一步分析。
1.2.5富集(GO)分析和KEGG分析
利用DAVID数据库(https://david.ncifcrf.gov/),选择“start Analysis”,在step1中输入异槲皮苷和胰岛素抵抗关键靶点,接着在step2中的“选择鉴别”一栏中选择“OFFICIAL_GENE_SYMBOL”,同时在step2a中设置筛选条件中种属选择智人(homo sapiens),在step3中选择基因列表。在“Functional Annotation Tool ”功能注释中仅勾选“Gene_Ontology ”中的“GOTERM_BP_DIRECT”、“GOTERM_CC_DIRECT”和“GOTERM_MF_DIRECT”以及“Pathways”中的“KEGG_PATHWAY”得到可视化表格并进行下载。
利用KEGG数据库(https://www.kegg.jp/kegg/kegg3a.html),在“KEGG mapping” 里找到“KEGG mapper”,点开进入,找到“Search&Color Pathway (and Brite, Module)”,输入关键靶点,筛选条件是种属为人,即选择“homo sapience pathway”。选择靶点数量较多出现在通路图上的进行分析,着重分析与胰岛素抵抗相关的通路和通路上的靶点。
1.2.6 药物-靶点-通路-疾病Cytoscape作图可视化分析利用Cytoscape作图软件绘制异槲皮苷和胰岛素抵抗“单成分药物-靶点-通路-疾病”的网络关系验证异槲皮苷改善胰岛素抵抗的作用机制。
2 结果
2.1异槲皮苷单成分靶点
通过TTD数据库(http://db.idrblab.net/ttd/)、Swiss Target Prediction数据库(http://www.swisstargetprediction.ch/)以及 PubChem数据库(https://pubchem.ncbi.nlm.nih.gov)找到异槲皮苷的基因靶点进行汇总,其中TTD数据库在“target”结果中搜索出2个靶基因,分别为“AKR1B1、ACE”;Swiss Target Prediction数据库画出异槲皮苷分子式图,如图1,搜索出“target”对应的基因名称“common name”下载;PubChem数据库搜索结果见“BioAssay Results’中的“target name”,筛选“active”基因,共计114个。
2.2胰岛素抵抗疾病靶点
通过DisGeNET数据库(https://www.disgenet.org/)、Genecards数据库 (https://www.genecards.org/)、OMIM数据库(https://omim.org)输入关键词“insulin resistance”查找胰岛素抵抗发病基因,分别下载,其中筛选条件设置为:DisGeNET数据库(https://www.disgenet.org/)优选胰岛素抵抗分数≥0.1;Genecards数据库 (https://www.genecards.org/)优选胰岛素抵抗相关性≥20;OMIM数据库(https://omim.org)整理首基因。最后将三个数据库中的所有基因删除重复项,整理汇总,作为胰岛素抵抗的疾病靶基因,共计563个。
2.3异槲皮苷与胰岛素抵抗共同靶点
通过Venny作图软件(https://bioinfogp.cnb.csic.es/tools/venny/),针对异槲皮苷有效靶点和胰岛素抵抗靶基因取交集,找到异槲皮苷和胰岛素抵抗的共有基因靶点,共计24个,将所有共同基因名称整理汇总,如图2。
2.4 PPI蛋白网络互做分析(Protein-Protein Interaction,PPI)结果
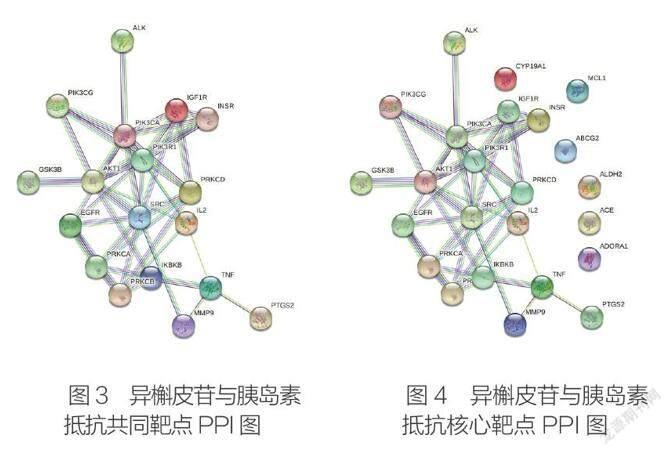
利用STRING数据库(https://string- db.org/),在“Multiple proteins”一栏输入24个共同靶点基因名称,选择人源基因(Homo sapines),得到PPI蛋白网络互做图,同时设置最低要求互动分数条件为 0.900及以上,得到PPI蛋白网络互做分析图,找出连线紧密的核心基因18个,再将18个核心蛋白在“Multiple proteins”一栏输入,继续重复上述步骤,得到最终PPI蛋白网络互做分析图,如图3,4。
2.5 富集(GO)分析和KEGG分析结果
利用DAVID数据库(https://david.ncifcrf.gov/)在“Start Analysis”页面中首先在“Enter Gene List”一栏中输入异槲皮苷和胰岛素抵抗的核心基因靶点名称,然后在“select Identifier”一栏中选择“OFFICIAL-GENE-SYMBOL”;在“List Type”选择“Gene List”;物种选择人源,于是得到异槲皮苷和胰岛素抵抗核心靶点的富集(GO)分析结果,其中生物学过程(BP)、细胞组分(CC)、分子功能(MF)的功能注释依次根据数量降序排列,分别取前10项作图分析,如图5,6,7;信号通路(PATHWAY)按P值升序,取前10个做饼状图,并进一步分析,如图8。接着利用KEGG數据库(https://www.kegg.jp/kegg/kegg3a.html)同样输入人源核心基因18个,首先验证DAVID数据库与KEGG数据库搜索得出的关键靶点数量较多的信号通路的疾病名称是否基本一致,再着重分析与胰岛素抵抗相关的信号通路,在胰岛素抵抗信号通路图上,肝脏细胞的关键靶点有TNFα、IKKβ、INSR、PI3K、AKT2、GSK- 3,如图10。
2.6异槲皮苷单成分-靶点-通路-疾病Cytoscape作图可视化分析结果
通过Cytoscape作图软件绘制异槲皮苷和胰岛素抵抗“单成分药物-靶点-通路-疾病”的网络关系验证异槲皮苷改善胰岛素抵抗的作用机制,其中通路筛选GO分析里“KEGG-pathway”中P值≤9.76E-10的信号通路,如图11。
3结论
胰岛素抵抗是细胞对胰岛素的作用产生抵抗的一种状态。胰岛素抵抗普遍存在于多种代谢性疾病中,包括代谢综合征(MS)、2型糖尿病、高血压、血脂紊乱、心脑血管疾病[7]。通过网络药理学理论验证出异槲皮苷改善胰岛素抵抗的信号通路包括PI3K -Akt、mTOR、胰岛素抵抗、糖尿病心肌病等[8],其中胰岛素抵抗信号通路尤为重要,在胰岛素抵抗信号通路上显示了多种作用机制:(a)通过丝氨酸/苏氨酸激酶(如JNK1和IKKB)和蛋白激酶C增加IRS(胰岛素受体底物)蛋白的磷酸化;(b)通过mTOR信号途径增加IRS-1蛋白酶体的降解;(c)降低信号分子的活化包括PI3K和AKT[9-10];(d)磷酸酶(包括PTPs、PTEN和PP2A)活性的增加。另外,胰岛素抵抗导致GLUT4易位减少,导致骨骼肌葡萄糖摄取和糖原合成增加,以及肝脏糖异生和糖原合成减少[11]。由胰岛素抵抗信号通路得知异槲皮苷改善胰岛素抵抗的主要途径之一是通过激活肝脏PI3K/AKT信号通路改善胰岛素抵抗,关键靶点包括INSR、PI3K、AKT2、GSK-3,可促进肝糖原的合成以及葡萄糖氧化分解,达到调节糖代谢、脂代谢紊乱的效果。而TNFα、IKKβ关键靶点可控制炎症因子的分泌[12]。
综上所述,本研究通过网络药理学对异槲皮苷改善胰岛素抵抗的药效成分、作用靶点及通路进行了分析,预测了异槲皮苷改善胰岛素抵抗的基因靶点与作用通路,现有实验表明异槲皮苷可以改善胰岛素抵抗[13]。实验结果显示了异槲皮苷可以通过多靶点、多通路改善胰岛素抵抗的特点,初步验证的结果则表明了网络药理预测的可行性,为异槲皮苷改善胰岛素抵抗的作用机制深入研究提供依据。
参考文献:
[1]ChenSH,LiuXN,PengY.MicroRNA-351 eases insulin resistance and liver gluconeogenesis via the PI3K/AKT pathway by inhibiting FLOT2 in mice of gestational diabetes mellitus. J Cell Mol Med. 2019 Sep;23(9):5895-5906. doi: 10.1111/jcmm.14079. Epub 2019 Jul 9. PMID: 31287224; PMCID: PMC6714143.
[2]陈燕,詹羽姣,李晨阳,徐芳,赵军.异槲皮苷的生物活性研究进展[J].中国现代中药,2018,20(12):1579-1582+1592.
[3]刘金彪,裴丽敏,李晓凤,杜武勋.网络药理学在单味中药研究中的应用及思考[J].湖南中医杂志,2019,35(10):122-124.
[4]陈杰彬,魏连波,李成杰,汪晓娟,聂晓莉.异槲皮苷对糖尿病肾病大鼠MEK/ERK/Nrf1信号通路及肾脏纤维化的影响[J].中国中西医结合肾病杂志,2020,21(10):853-856+941.
[5]蒋国君,刘天旭,黄桂红,巫亭,陶丽群,朱钊铭.异槲皮苷对HepG2细胞中Raf/MEK/ERK信号通路的干预作用[J].中国药理学通报,2017,33(10):1382-1387.
[6]甄云凤,冯静,唐勇,齐翠娟,甘可欣,费雯婕,温丰华,宋光耀.MicroRNA-802对胰岛素抵抗的骨骼肌细胞PI3K/Akt通路的影响[J].解放军医学杂志,2020,45(08):798-803.
[7]石光,石岩,孙晓波.从脾论治胰岛素抵抗[J].辽宁中医杂志,2014,41(02):251-252.
[8]Won YeongSeon,Kim JeongHo,Lizardo Rona Camille M,Min HyeJi,Cho HyunDong,Hong SeongMin,Seo KwonIl. The Flavonol Isoquercitrin Promotes Mitochondrial-Dependent Apoptosis in SK-Mel-2 Melanoma Cell via the PI3K/AKT/mTOR Pathway.[J]. Nutrients,2020,12(12).
[9]Qiu Z, Wang K, Jiang C, Su Y, Fan X, Li J, Xue S, Yao L. Trigonelline protects hippocampal neurons from oxygen-glucose deprivation-induced injury through activating the PI3K/Akt pathway. Chem Biol Interact. 2020 Feb 1;317:108946. doi: 10.1016/j.cbi.2020.108946. Epub 2020 Jan 11. PMID: 31935362.
[10]Guo Q, Chen Z, Santhanam RK, Xu L, Gao X, Ma Q, Xue Z, Chen H. Hypoglycemic effects of polysaccharides from corn silk (Maydis stigma) and their beneficial roles via regulating the PI3K/Akt signaling pathway in L6 skeletal muscle myotubes. Int J Biol Macromol. 2019 Jan;121:981-988. doi: 10.1016/j.ijbiomac.2018.10.100. Epub 2018 Oct 18. PMID: 30342127.[11]Huang F, Chen J, Wang J, Zhu P, Lin W. Palmitic Acid Induces MicroRNA-221 Expression to Decrease Glucose Uptake in HepG2 Cells via the PI3K/AKT/GLUT4 Pathway. Biomed Res Int. 2019 Nov 11;2019:8171989.
[12]孟利娜. 薏苡仁蛋白依賴IKK/NF-κB通道控制炎症及改善2型糖尿病胰岛素抵抗作用[D].合肥工业大学,2018.
[13]许光远,孙文,宋紫临,郭璇,吴丽丽,秦灵灵,侯丹,张茁,田硕,李响,刘铜华.异槲皮苷对小鼠肝脏脂肪酸代谢及相关基因表达的影响[J].天津中医药,2017,34(11):778-781.
[14]毛竹君,翁思颖,王磊,柴可夫.小檗碱调控IR-HepG2细胞miR-29a-3p及胰岛素受体信号通路的作用机制研究[J].中华中医药杂志,2018,33(12):5559-5562.
[15]张立雯,季涛,宿树兰,尚尔鑫,郭盛,郭建明,钱大玮,段金廒.桑叶黄酮类和生物碱类成分在正常和糖尿病大鼠体内的药代动力学研究[J].中国中药杂志,2017,42(21):4218-4225.
作者简介:
张传艺(1996-),女,汉族,重庆,在读硕士研究生,研究方向:药学。
*通讯作者:
黄桂红(1972-),女,药学部主任,主任药师,教授 ,硕士,硕士生导师,研究方向:抗糖尿病药物研究。

