微纳米气泡对实际烧结烟气中NOX和SO2催化氧化吸收的研究
杨天佑,孙红蕊,李登新
(1.东华大学 环境科技与工程学院,上海 201620;2.同济大学 环境科学与工程学院 污染控制与资源化研究国家重点实验室,上海 200082;3.上海污染控制与生态安全研究院,上海 200082)
众所周知,烧结烟气中颗粒物、SO2、NOX和二噁英[1-2]排放量分别约占钢铁生产总排放量的20%,60%[3],50%,90%,治理烧结烟气已迫在眉睫[4]。目前来看,我国大部分脱硫脱硝一体化技术设备复杂、操作难度大,因此寻求更加高效及环保的技术具有很好的现实意义。微纳米气泡具有水中停留时间长[5]、传质效率高、气泡表面电势差ζ高[6]、氧化性强等[7]突出性能,Jiang等[8]利用水、空气和NO混合产生微纳米气泡以达到吸收NO的目的,并在最佳条件下取得了69.18%的吸收效果。但近几年中,对于微纳米气泡吸收处理NO的研究多用模拟烟气[9-11],而实际烧结烟气污染物成分复杂、污染物浓度变化大、烟气量波动大等特点[12]会对脱硫脱硝一体化治理造成相对较大的困难。
目前未发现有关实际烟气经微纳米气泡催化氧化吸收处理多污染物的报道,因此本文在此基础上利用微纳米气泡催化氧化吸收实际烧结烟气中的NOX与SO2,探寻各种反应条件对其吸收效率的影响。
1 实验部分
1.1 材料与仪器
烧结料球团,由上海宝钢研究院提供;亚硝酸钠、氢氧化钠、氯化锰均为分析纯。
SG-GS1700刚玉管式炉,上海识捷电炉有限公司;LF02-PT微纳米气泡发生器;ICS-1100型离子色谱仪;MODEL 6010 便携式pH计;YB-2500A型粉碎机;Seitron C600型烟气分析仪。
1.2 实验方法
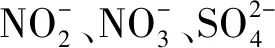

图1 微纳米气液分散体系处理烧结烟气实验装置图Fig.1 Experimental device for the treatment of sintered flue gas by micro-nano gas-liquid dispersion system1.管式炉;2.换热器;3.除尘器;4.质量流量计;5.烟气收集器;6.三通阀;7.烟气分析仪;8.储液罐;9.液体流量计;10.微纳米气泡发生装置;11.吸收反应器;12.集液箱;13.尾气吸收瓶
1.3 计算方法
NOX、SO2吸收效率计算公式:
(1)
(2)

式(2)中,ρ1、ρ2分别为NO、NO2的质量浓度,mg/L;M为N的相对原子质量;M1、M2分别为NO、NO2的分子质量;q2为气体流量,L/min;t为系统运行时间,min。计算SO2吸收效率时则只需以ρ1代入SO2的质量浓度,mg/L;M为S的相对原子质量;M1为SO2的相对分子质量;ρ2为0,其余不变。
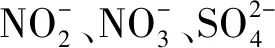
2 结果与讨论
2.1 烧结料燃烧温度对烟气吸收效率的影响
每次取1.00 g烧结料和1.23 g NaNO2在刚玉管式炉中燃烧20 min,控制其燃烧温度分别为800,850,900,950,1 000 ℃以得到不同性质的烧结烟气,结合微纳米气泡机(控制进水pH=7)生成微纳米气泡水,采用非循环生成的方式,系统运行5 min。考察得出不同燃烧温度条件下的烧结烟气中NOX、SO2的氧化吸收效率见图2。


图2 燃烧温度对NOX、SO2脱除率的影响Fig.2 Effect of temperature on removal rate of NOXand SO2
图2a为不同燃烧温度下产生气体中NOX、SO2的浓度,由图可知,800 ℃时NOX的浓度很低,850 ℃则达到最高,随后逐渐下降,而SO2的浓度则基本稳定。由图2b可知,从800 ℃升到850 ℃后,NOX的吸收效率有了显著的提高,并在850~950 ℃之间吸收效率基本稳定,到达1 000 ℃后开始出现下降的趋势。NOX、SO2在被微纳米气液分散体系吸收的过程中从气相转入了液相,然后与微纳米气泡破裂时产生的·OH发生氧化反应以达到去除的目的[14]。而800 ℃并未达到烧结料与NaNO2能够完全发生燃烧反应的温度,NOX浓度极低,其它气体含量则相对较高,因此会对NOX与·OH的反应造成影响,导致NOX的吸收效率不高。温度升高后,烟气中NOX的浓度明显升高,更易与·OH发生反应,吸收效率也随之提高。与之相对SO2的吸收效率则一直处于很高的状态,有研究表明,当[SO2] <10.71 mg/L时,SO2几乎可以完全吸收[15],因此在后续实验过程中不再赘述SO2的吸收效率。
2.2 烧结料燃烧时间对烟气吸收效率的影响
图3是取1.00 g烧结料和1.23 g NaNO2在刚玉管式炉中以850 ℃分别燃烧10,15,20,25,30 min后所得烟气经微纳米气液分散体系(控制进水pH=7)处理后NOX、SO2的吸收效率图。


图3 燃烧时间对NOX、SO2脱除率的影响Fig.3 Effect of time on removal rate of NOX and SO2
由图3可知,NOX的吸收效率差别不大,且与NOX的浓度趋势大致符合,原因可能是燃烧时间的不同并未对烟气中各气体的含量与浓度产生较大差异。择其最优值,在后续实验过程中燃烧时间均取20 min。
2.3 烧结料与NaNO2比例对烟气吸收效率的影响
图4是在850 ℃、20 min的条件下,取不同质量0.50,1.00,2.00,3.00,4.00 g的烧结料与1.23 g NaNO2一同燃烧后产生烟气经微纳米气液分散体系(控制进水pH=7)处理后NOX、SO2的吸收效率图。


图4 烧结料与NaNO2比例对NOX、SO2脱除率的影响Fig.4 Effect of the proportion of sinter and NaNO2 on removal rate of NOX and SO2
由图4可知,当烧结料的质量从0.50 g增至1.00 g时,NOX的浓度变化不大,但吸收效率却有所提高,这可能是因为烧结料中含有Fe等金属元素,当吸收系统溶液中存在Fe2+时,部分Fe2+会被·OH和O2氧化为Fe3+,这两种价态的铁离子能与溶于水中的SO2、NO以及·OH反应生成络合物,与SO2反应生成的络合物还能继续与NO2反应,Fe2+也能直接与NO2反应,所以NOX的吸收效率会提高。而当烧结料继续增加时,大量的离子与NOX络合导致NOX在气液两相间的传质速率降低,影响了NOX吸收效率[13],因此后续实验中取1.00 g烧结料为宜。
2.4 pH对烟气吸收效率的影响
图5是1.00 g烧结料与1.23 g NaNO2在850 ℃燃烧20 min后所产生的烟气经微纳米气液分散体系分别控制进水pH=3,5,7,9,11条件下的NOX、SO2吸收效率图。

图5 pH对NOX、SO2脱除率的影响Fig.5 Effect of pH on removal rate of NOX and SO2
由图5可知,NOX的吸收效率随着pH的增加而增加,并在pH=5时达到最高值59.3%。而继续增加pH后吸收效率会逐渐降低。其原因可能是在低pH的条件下,NO2、SO2作为酸性气体在水中溶解度会降低;且水中含有大量的H+以及SO2溶于水释放出的H+会与气泡表面的OH-结合,这会导致气泡的Zeta电位降低,气泡稳定性变差,水中的停留时间变短,因此NOX的吸收效率较低。而在pH=5时,微纳米气泡的传质效率最高,对NOX的吸收最有利。随着溶液碱度的升高,水中OH-增多,这会与气泡表面的OH-相互排斥,使得气泡在水中的运动加剧,导致气泡破裂,NOX的吸收效率也就随之降低。
2.5 Mn2+对烟气吸收效率的影响
图6是1.00 g烧结料与1.23 g NaNO2在850 ℃燃烧20 min后所产生的烟气经微纳米气液分散体系,进水是由MnCl2·4H2O配制的Mn2+浓度分别为0.5,1,2,3,4 mmol/L的溶液(控制其pH=5),吸收处理得到的NOX、SO2吸收效率图。
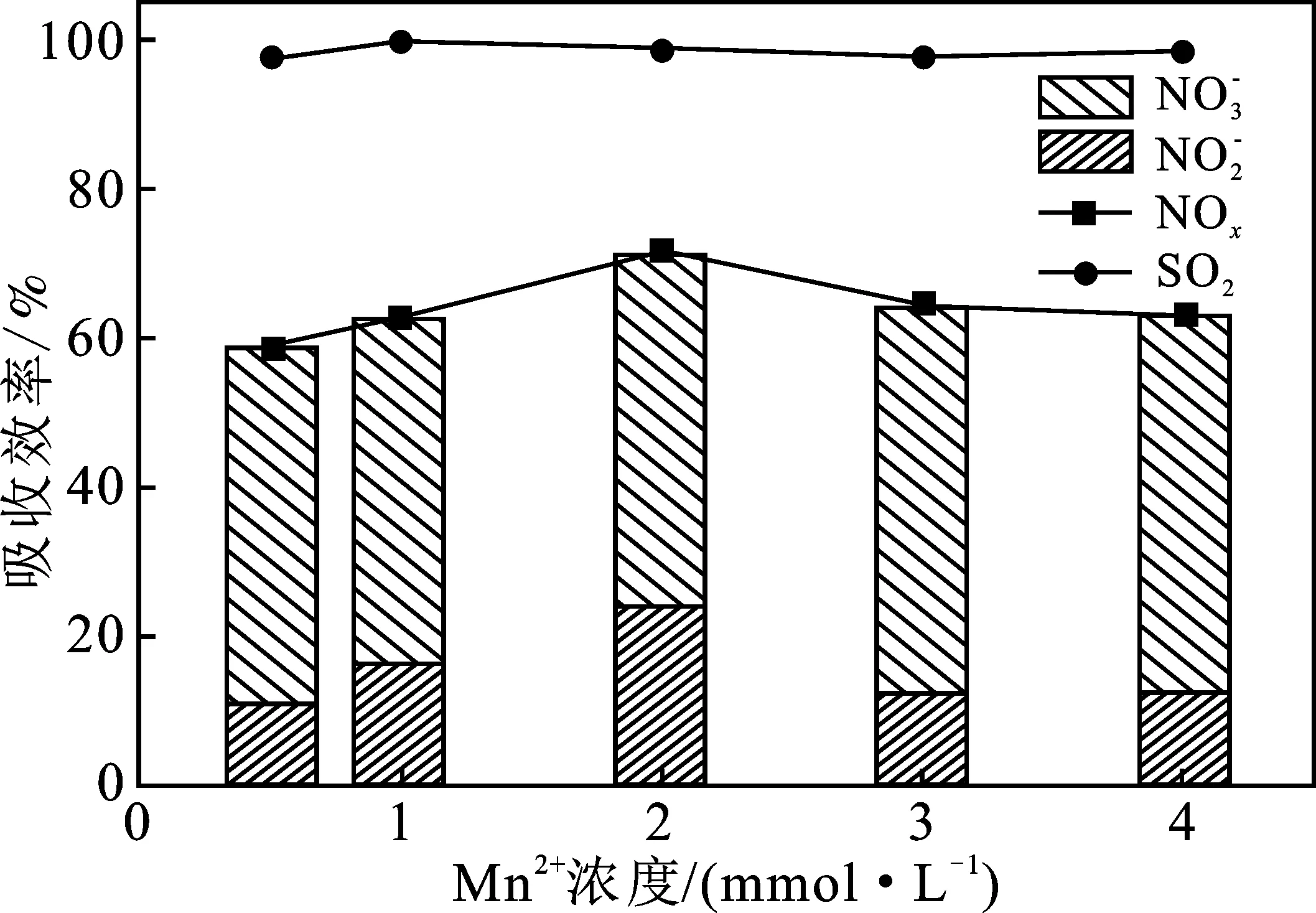
图6 Mn2+对NOX、SO2脱除率的影响Fig.6 Effect of Mn2+on removal rate of NOX and SO2
由图6可知,在微纳米气液体系中加入Mn2+后,在离子浓度较低(<2 mmol/L)时,NOX的吸收效率随着Mn2+浓度的增加而升高,并在2 mmol/L时达到峰值71.7%。其原因可能是在液相中加Mn2+后,微纳米气泡破裂产生的自由基会使Mn在Mn2+、MnO2+、Mn3+之间相互转化,Mn2+就起到催化剂的作用加快了NOX的吸收。离子浓度继续增加后,NOX吸收效率反而下降,这可能是因为Mn2+和NO发生了络合反应,络合之后的离子催化效率降低。
2.6 添加聚氯乙烯塑料燃烧对烟气吸收效率的影响
图7是添加不同质量的聚氯乙烯塑料(0.5,1.0,1.5,2.0,2.5 g)与1.00 g烧结料和1.23 g NaNO2在850 ℃燃烧20 min后所产生的烟气经微纳米气液分散体系(蒸馏水,并控制进水pH=5)处理后NOX、SO2的吸收效率图。

图7 塑料质量对NOX、SO2脱除率的影响Fig.7 Effect of plastic weight on removal rate of NOX and SO2
由图7可知,NOX的吸收效率随着塑料的添加呈现下降的趋势。这可能是因为聚氯乙烯塑料燃烧产生的气体中含有HCl的成分,HCl溶于水后产生Cl-,由于Cl-的水合能较低,容易吸附在气泡界面处,当气泡表面堆积大量的Cl-后,气泡的传质效率会降低,从而影响了NOX的吸收效率。
3 结论
(1)1.00 g烧结料与1.23 g NaNO2在850 ℃的温度下燃烧20 min得到的烟气经微纳米气液分散体系处理,在控制进水pH=5的条件下NOX的吸收效率能达到59.3%,SO2几乎全部被吸收。
(2)在最佳处理条件下,将微纳米气泡机进水替换为Mn2+溶液后,NOX的吸收效率显著提高,并且在Mn2+的摩尔浓度为2 mmol/L时效率最高,达到71.7%。
(3)聚氯乙烯塑料的添加会影响对NOX的吸收效率,燃料中塑料的含量越多,吸收效率下降得也就越多。

