5,5′-联四唑-1,1′-二氧铅盐的热分解
杨彩云
摘 要:以5,5′-联四唑-1,1′-二氧钠盐和硝酸铅为原料通过复分解反应制备了5,5′-联四唑-1,1′-二氧铅盐([Pb(BTO)(H2O)2]),考察了[Pb(BTO)(H2O)2]的热分解性能,获得在绝热条件下的分解动力学参数,绝热温升为2.1 ℃;初始放热温升速率为5.13 ℃/min。
关键词:5,5′-联四唑-1,1′-二氧铅盐;合成;绝热分解
中图分类号:TJ55 文献标识码:A
引言
Niko Fischer等[1]首次报道了多氮化合物5,5′-联四唑-1,1′-二羟基二水合物(BTO)及衍生物,并对爆炸性能进行预测。王杰群等[2]研究了二水合5,5′-联四唑-1,1′-二氧铅盐[Pb(BTO)(H2O)2]的热分解性能和非等温条件下的动力学。关于[Pb(BTO)(H2O)2]的结构和热性能虽有文献报道[3],本文采用新方法制备了[Pb(BTO)(H2O)2],利用绝热加速量热仪(ARC)等热分析仪研究[Pb(BTO)(H2O)2]的热稳定性,为安全生产和使用提供基础数据。
1.实验部分
1.1 实验样品及仪器
本实验所使用DSC-TG分析仪由日本岛津公司制造,样品质量约3 mg左右,空气氛围,样品盘采用三氧化二铝坩埚,参比坩埚使用空坩埚,操作温度为25~600 ℃,升温速率为5 ℃/min。
1.2 [Pb(BTO)(H2O)2]的合成
250 mL带温度计的三口烧瓶固定在水浴中,向三口烧瓶中加入水100 mL,四水合5,5′-联四唑-1,1′-二氧钠盐2.86 g(10 mmol),开启搅拌,升温至80 ℃使料液完全混合均匀。将硝酸铅5g(15.1 mmol)溶于30 mL水的溶液加入三口瓶,硝酸铅水溶液加完后保温1 h,缓慢降至室温,过滤,滤饼用水洗涤3次。自然晾干得到淡粉白色的[Pb(BTO)(H2O)2]晶体3.5g,收率85.17%。
红外(IR)(KBr,υ/cm-1):3436(w)、1610(m)、1553(w)、1440(w)、1253(w)、1187(m)、1013(w)、750(s)、667(w);元素分析(w/%):[Pb(BTO)(H2O)2](Mr=411.2),理论值,C 5.83,H 0.97,N 27.24;实测值,C 5.77,H 0.94,N 27.21。
2.结果与讨论
加速量热仪选择加热速率以“加热-等待-探测(H-W-S)”的模式操作,样品分解反应放出的热量不仅用于自身的加热,而且还要加热样品球,所以测试结果是样品和样品球组成的整个反应系统。
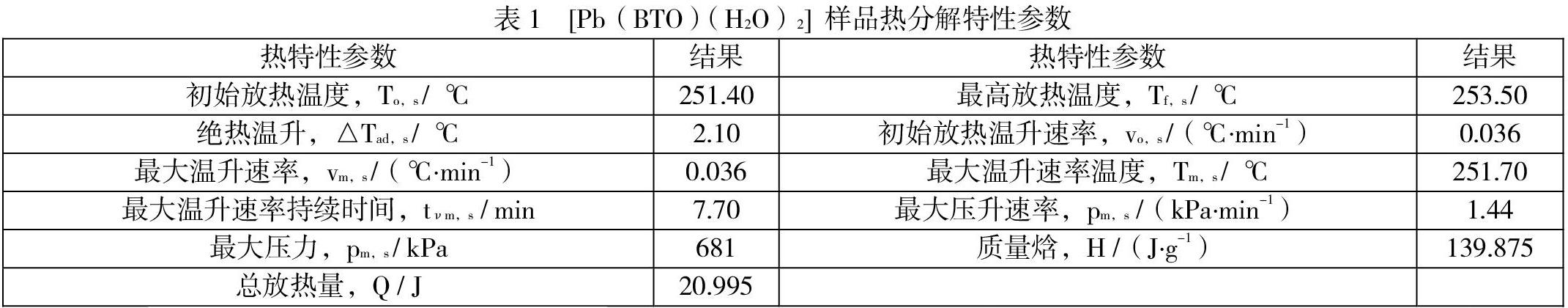
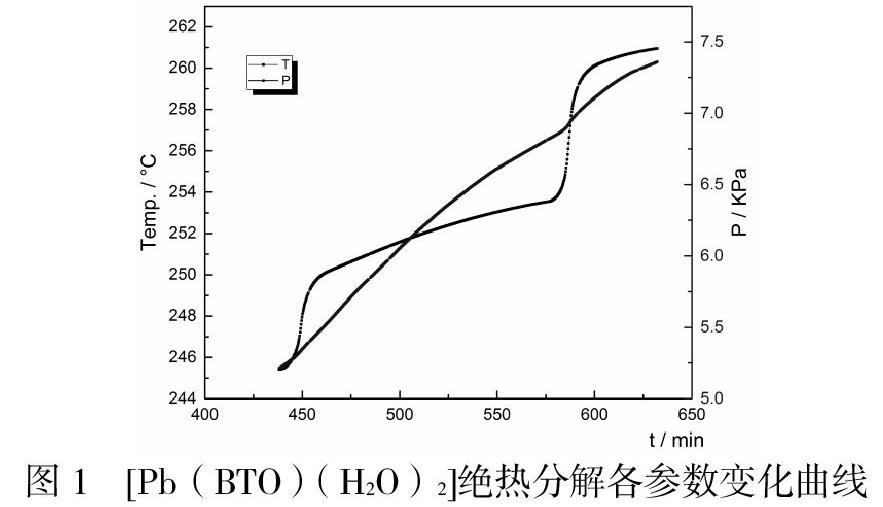
由图1可知,试样经过加热-等待-搜寻的运行周期后在251.40 ℃探测到样品开始分解放热反应,[Pb(BTO)(H2O)2]在绝热分解阶段温度随着时间的延长而缓慢增加。表1可知,251.40℃时样品开始分解放热,对应的温升速率为0.036℃/min,初始分解压力为598.57kPa,随后温升速率在7.70min内维持0.036℃/min不变,而压升速率开始缓慢下降,此時温度与压力继续升高,温度最高升至253.50℃,压力达到最大值681 kPa。
3.结论
以5,5′-联四唑-1,1′-二氧钠盐和硝酸铅为原料通过复分解反应制备了[Pb(BTO)(H2O)2],采用红外光谱、元素分析对结构进行了表征,以ARC研究了[Pb(BTO)(H2O)2]在绝热条件下的热行为,绝热分解过程的初始放热温度为251.40℃,绝热温升为2.1℃。
参考文献
[1] FISCHER Niko,KLAP?TKE Thomas M,REYMANN Marius,et al. Nitrogen-rich salts of 1H,1′H-5,5′-bitetrazole-1,1′-diol:energetic materials with high thermal stability [J]. European Journal of Inorganic Chemistry,2013,2013(12):2167?2180.
[2] 王杰群,王鹏程,陆明,等.1,1-二羟基-5,5-联四唑金属盐的制备及热分解动力学[J]. 含能含能材料,2016,24(6):538?543.
[3] SU Qiang,WANG Xiaojun,SHU Qinghai,et al. Synthesis,crystal structure and properties of energetic complexes constructed from transition metal cations(Fe、Co、Cu and Pb)and BTO2?[J]. Journal of Heterocyclic Chemistry,2017,54(6):3227?3234.

