介入栓塞治疗反复出血的杜氏溃疡1例
陈 东 刘 武 雷小林
攀枝花学院附属医院肿瘤科,四川省攀枝花市 617000
杜氏溃疡(杜氏病,Dieulafoy病,黏膜下恒径动脉破裂出血)是一种罕见的急性消化道大出血疾病,以动脉畸形破裂为特征,易反复出血。攀枝花学院附属医院曾有1例介入栓塞治疗上消化道反复出血的杜氏溃疡病例,现介绍如下。
1 病例资料
患者男性,44岁。因“黑便7d,呕血1次伴头晕、乏力”于2017年3月3日首次至消化科就诊。既往史无特殊。平素饮食不规律,常饮酒(具体次数和量描述不清)。查体:心率:150次/min,血压87/60mmHg(1mmHg=0.133kPa),贫血貌,睑结膜苍白,扶入病房;余无特殊。辅助检查:血常规提示血红蛋白60g/L,血尿素氮11.68mmol/L,肝肾功能、电解质、凝血功能、肿瘤标志物等检验结果无明显异常。予抑酸、止血、补充血容量、降低胃肠道血流量、输血治疗,嘱患者绝对卧床、暂禁食。入院第2天,患者生命体征平稳,胃镜见:胃小弯侧可见一约0.6cm×0.7cm浅表溃疡,表面覆盖白苔,周边黏膜见少许充血痕,喷洒去甲肾上腺素后未见明显活动性出血。胃镜诊断:杜氏溃疡可能性大。继续予抑酸、止血、补充血容量、降低胃肠道血流量等治疗后,患者好转出院。
2019年9月20日,患者因“黑便4d,头晕乏力2+h”再次入院。查体:轻度贫血貌,余无特殊。辅助检查:红细胞数2.3×1012/L,血红蛋白72g/L,血尿素氮13.59mmol/L,肝功能、电解质、凝血功能、肿瘤标志物等检验结果无明显异常。行胃镜示(图1):胃体下段小弯侧可见一直径约7mm孤立性黏膜缺损,周围黏膜无明显炎症表现,黏膜缺损中央可见血管残端,未见明显活动性出血。胃镜诊断:杜氏溃疡。予抑酸护胃、止血、输血、补液扩容等治疗。入院第4天,黑便转黄,头晕乏力较前好转。入院第5天,患者再次出现黑便1次。肿瘤科介入医生会诊后建议行腹腔动脉造影。完善检查,无血管介入禁忌证,第6天行腹腔干、肠系膜、胃十二指肠、胃左动脉造影及栓塞术(图2),胃左动脉灌注药物:注射用白眉蛇毒血凝酶2个单位,以明胶海绵颗粒栓塞(图3)。手术顺利。术后股动脉穿刺处压迫10min后加压包扎,嘱患者制动12h。继续予抑酸护胃、止血、营养支持、补液扩容等治疗。患者黑便转黄,红细胞数3.7×1012/L,血红蛋白113g/L,病情好转出院。每2个月电话随访至今,未再出现消化道出血。
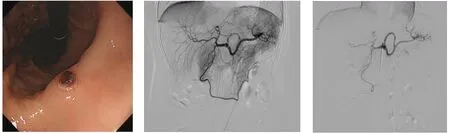
图1 胃镜可见裸露的血管残端 图2 胃左动脉远端可见造影剂泄露 图3 栓塞后,未见出血征象
2 讨论
杜氏溃疡的解剖学基础是黏膜下恒径小动脉畸形,以消化道黏膜下多见,亦可见于支气管黏膜,本文主要讨论消化道的杜氏溃疡。正常情况下黏膜小动脉逐渐分支并变细,直径0.1~0.2mm,末梢形成黏膜下毛细血管网。杜氏溃疡的黏膜下小动脉无分支,保持恒定直径,1~4mm,是正常黏膜下毛细血管直径的10倍,该小动脉增多、迂曲,其搏动产生的机械压力使上面的黏膜变薄受损;小动脉常穿过受损的黏膜,孤立、突出于消化道黏膜表面。杜氏溃疡分布于消化道的任何部位[1-2],但常见部位主要是沿胃小弯靠近食管与胃连接处,范围约6cm。本患者溃疡病灶位于胃小弯附近,属于上述常见部位。
杜氏溃疡多见于成人,儿童案例[3-4]较少出现。杜氏溃疡的病因以及出血诱因尚不明确,大出血以男性多见,且多并发心血管疾病、慢性肾病、糖尿病、嗜酒史、NSAID药物史;生理性应激也可诱发出血。该溃疡出血具有自限性,但常反复发作。近年一项回顾性研究[5]分析了111例杜氏病再出血的风险因素,Logistic 回归多因素分析结果提示,输血为治疗后再出血的独立危险因素。本案例中患者素平饮食不规律,因工作原因,社交活动常饮酒;此外,在治疗过程中患者也有输血史,与上述研究结果相符,可能与患者本身动脉性出血,扩充血容量后血管压力增大有关。
杜氏溃疡的诊断具有一定难度,由于其病灶小,间歇性出血,易与其他血管畸形疾病混淆,如动脉瘤、Mallory-Weiss综合征等。在无活动性出血时,病灶可呈乳头状凸起,或者无明显溃疡的裸露血管。在活动喷射性出血时病灶易被发现;但当其被血凝块或活动性出血覆盖时,诊断将出现困难。仅49%的杜氏溃疡患者在首次内镜检查时被发现,33%的患者需再次内镜检查,18%的患者为精确诊断甚至需要手术探查。在缺乏炎性黏膜病变和溃疡病灶时,内镜易漏诊。因此,当患者出现来源不明的胃肠道出血时,应考虑该病。本例亦属于再次内镜检查才明确诊断的情况,患者2017年的胃镜下病灶特征不明显,为浅表溃疡,表面覆盖白苔;2019年再次入院时,胃镜可见7mm孤立性黏膜缺损,其中央可见血管残端,病灶特征明显,才进一步明确诊断。
内镜是诊断杜氏溃疡的常见手段,其优势包括费用低、可重复性强、诊断和治疗同步进行等。但也有局限性:(1)消化道内积血或血凝块掩盖病灶,导致视野不清,内镜可能漏诊;(2)出血间歇期时,若病灶位置特殊,难以发现;(3)胃底检查时,需行U型反转,若患者配合度不佳,检查难度增大;(4)检查过程中患者可能出现恶心、呕吐等不适,耐受性低;(5)大出血且生命体征不平稳的患者无法配合,并且无痛胃镜时全身麻醉风险高。
杜氏溃疡的内镜下治疗方法诸多,例如双极电凝治疗、热探头凝固治疗或止血夹,随后联合注射肾上腺素等止血药物。其他疗法还包括,内镜下套扎术、氩等离子凝固术、内镜下组织胶注射术等。各类方法疗效不一,国内外都有相应的成功案例,不再赘述。但内镜下多种方法联合止血后,患者有仍有再次出血的风险[5-7]。喷洒或注射止血药物法在临床较为常见,其暂时止血率高,但易再次出血。本例中患者内镜下仅喷洒止血药物,再出血风险高。
作为动脉破裂的出血性疾病,杜氏溃疡亦属于血管介入的诊治范畴,国内外已有应用动脉栓塞治疗杜氏溃疡再出血的报道。对于以下情况,血管介入是另一种有效的诊治方法:(1)患者处于急性出血期或休克状态,一般情况差,无法耐受或配合;(2)内镜止血失败,再出血的患者;(3)内镜难以到达、位置特殊的病灶。相对于内镜,介入栓塞治疗的优势在于:(1)视野不受消化道内积血或血凝块等因素的干扰,对出血部位和靶血管定位更精准;(2)不受消化道部位的限制;(3)即便在出血间歇期,未见明确出血点,迂曲、扩张的血管可为诊断提供依据;(4)操作时间相对较短,患者耐受性较好;(5)对患者一般情况的要求较低,禁忌证相对较少(除凝血功能异常为绝对禁忌证)。本例介入手术时间约40min,手术过程中耐受性良好,术后亦无特殊不适。但介入治疗也有一定局限性:(1)因设备及耗材昂贵,未能普及于基层医院;(2)被栓塞的动脉,可能会建立侧支循环,发生再通,最终再次出血;(3)术后患者需要制动12h;(4)有一定的风险,如造影剂过敏、血管损伤、异位栓塞等。
内镜与血管介入各有优势,两者结合可以提高杜氏溃疡的诊治效果。因内镜具有较强的普遍性、费用低廉,暂时止血率高,适合作为首选方案;但在内镜检查或治疗后,对于出血原因不明或再次出血的患者,介入治疗是另一安全有效的手段,可作为内镜诊治失败后的补救措施。此外,手术切除病灶虽然有效,但创伤大、恢复慢、影响患者生活质量,盲目手术切除可能未切除出血病灶,导致治疗无效。因此,仅对于内镜和介入难以控制的出血,才考虑手术治疗。
综上所述,内镜和血管介入治疗均为杜氏溃疡重要的诊治手段,两者联合使用有利于杜氏溃疡的早发现和早治疗,尤其是对于内镜诊断不明确或治疗失败的患者,应立即考虑介入治疗,以防病情恶化。若以上两种保守治疗均不理想,则考虑手术治疗。相信随着介入技术和设备的日新月异,介入治疗会逐渐发展至基层医院,为杜氏溃疡等难治的消化道出血疾病提供及时且准确的救治,最终降低杜氏溃疡患者的再出血风险,使其获益。

