基于CT定量心外膜脂肪组织与冠状动脉疾病的关系:Meta分析
程 勇,樊建坤,陈澜菁,漆万银,李 艳,傅建梅,兰永树
(西南医科大学附属医院放射科,四川 泸州 646000)
心外膜脂肪组织(epicardial adipose tissue, EAT)指沉积于心肌和脏层心包之间的内脏脂肪组织,主要见于心房心室沟和心室间沟及冠状动脉主要分支周围[1-2]。EAT具有内分泌和旁分泌功能,生理状态下可保护心脏,但代谢障碍时沉积的EAT可能分泌肿瘤坏死因子-α、白细胞介素-6、瘦素等促炎因子和细胞因子,促进冠状动脉疾病(coronary artery disease, CAD)发生发展[3-4]。既往研究[5-6]采用影像学方法定量EAT,并探究其与CAD、心肌桥、心肌缺血、心脏结构和功能等之间的关系。本研究应用Meta分析系统评价基于CT定量的EAT与CAD的关系。
1 资料与方法
1.1 文献检索 检索中国知网、万方医学网、维普网及PubMed、Medline、Web of science数据库中关于评估CT定量EAT与CAD之间关系的病例对照研究,检索时间自建库至2019年12月31日。中文检索词:心外膜脂肪组织厚度、心外膜脂肪组织容积、冠状动脉疾病、冠心病、冠状动脉粥样硬化和阻塞性冠状动脉疾病;英文检索词:epicardial adipose tissue、epicardial fat、subepicardial adipose tissue、subepicardial fat、coronary artery disease、coronary heart disease、atherosclerosis、coronary stenosis、obstructive coronary artery disease、computer assisted tomography、computer tomography、computed tomography coronary angiography、cardiac computed tomography、coronary artery calcium score、coronary angiography。
1.2 纳入及排除标准 纳入标准:①CT测量EAT厚度或容积,探究其与CAD之间关系的病例对照研究;②根据冠状动脉(以下简称冠脉)狭窄程度分为CAD组(冠脉狭窄≥50%)和非CAD组(冠脉狭窄<50%);③采用冠脉造影(coronary angiography, CAG)或CTA判定冠脉狭窄程度;④以±s表示测量EAT结果;⑤同一作者发表多篇文献时,纳入样本量最大者。排除标准:①无法提取数据,语言非中文或英文;②综述、会议论文、病例报道等无具体数据的文献;③以特定人群如糖尿病、肥胖、透析患者等为研究对象。
1.3 数据提取 由2名影像科医师根据纳入及排除标准独立阅读文献,提取第一作者、发表年、样本量、病例-对照例数、EAT测量方法和结果、测量EAT容积时脂肪阈值、CAD诊断标准和方式等信息;并进行交叉验证,提取信息不一致时经协商决定。
1.4 文献质量评价 由上述2名医师采用Newcastle-Ottawa Scale(NOS)量表分别评价文献质量,包括研究对象、组间可比性及暴露因素等,总分10分,将>5分者纳入Meta分析;有异议时经讨论决定。
1.5 统计学分析 采用 Stata 12.0 统计分析软件,以I2和Q检验分析文献的异质性。I2≥50%且P<0.1表明各研究间异质性较大,选择随机效应模型合并,并根据潜在异质性来源进行回归及亚组分析(原文未报告相应变量的文献不纳入分析),反之采用固定效应模型。以标准化均数差(standardized mean difference, SMD)和95%CI为合并统计量,Egger线性回归检测发表偏倚。P<0.05为差异有统计学意义。
2 结果
2.1 文献检索及数据提取 经数据库检索去重后获得848篇相关文献,经筛选最终纳入19篇文献[7-25],中文8篇、英文11篇(图1);其中2篇[14,19]同时测量EAT厚度和容积,3篇[23-25]仅测量厚度,14篇[7-13,15-18,20-22]仅测量容积。纳入文献总样本量为12 563例,CAD组5 129例,非CAD组7 434例。纳入文献中,有研究者[13-14,16,18-19,23,25]同时采用不同方法或在不同位置测量EAT而得出多组数据,将其编号后均纳入分析。文献质量评分6~8分。见表1、2。
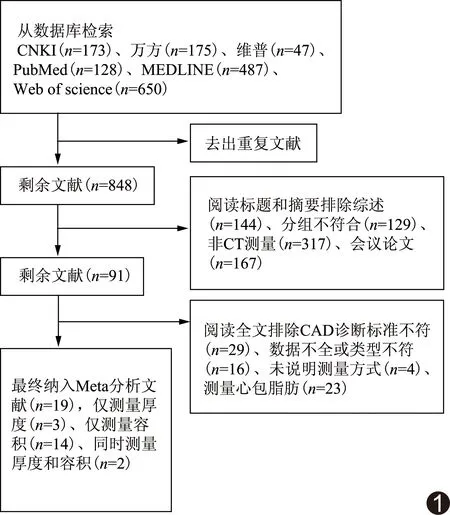
图1 文献筛选流程及结果
2.2 Meta分析
2.2.1 异质性检验 测量EAT厚度[14,19,23-25]和容积[7-22]相关文献的异质性检验结果分别为I2=86.4%、P<0.01和I2=93.4%、P<0.01,即均存在异质性,故以随机效应模型进行合并。
2.2.2 模型合并和敏感性分析 EAT厚度与CAD相关性的合并效应量SMD=0.46,95%CI(0.26,0.66),Z=4.51,P<0.01,见图2;EAT容积与CAD相关性的合并效应量SMD=0.65,95%CI(0.46,0.86),Z=6.58,P<0.01,见图3;CAD组EAT厚度和容积均高于非CAD组(P均<0.01)。敏感性分析结果显示,任意一篇文献对合并模型结果均不会造成显著影响,即Meta分析结果稳定。
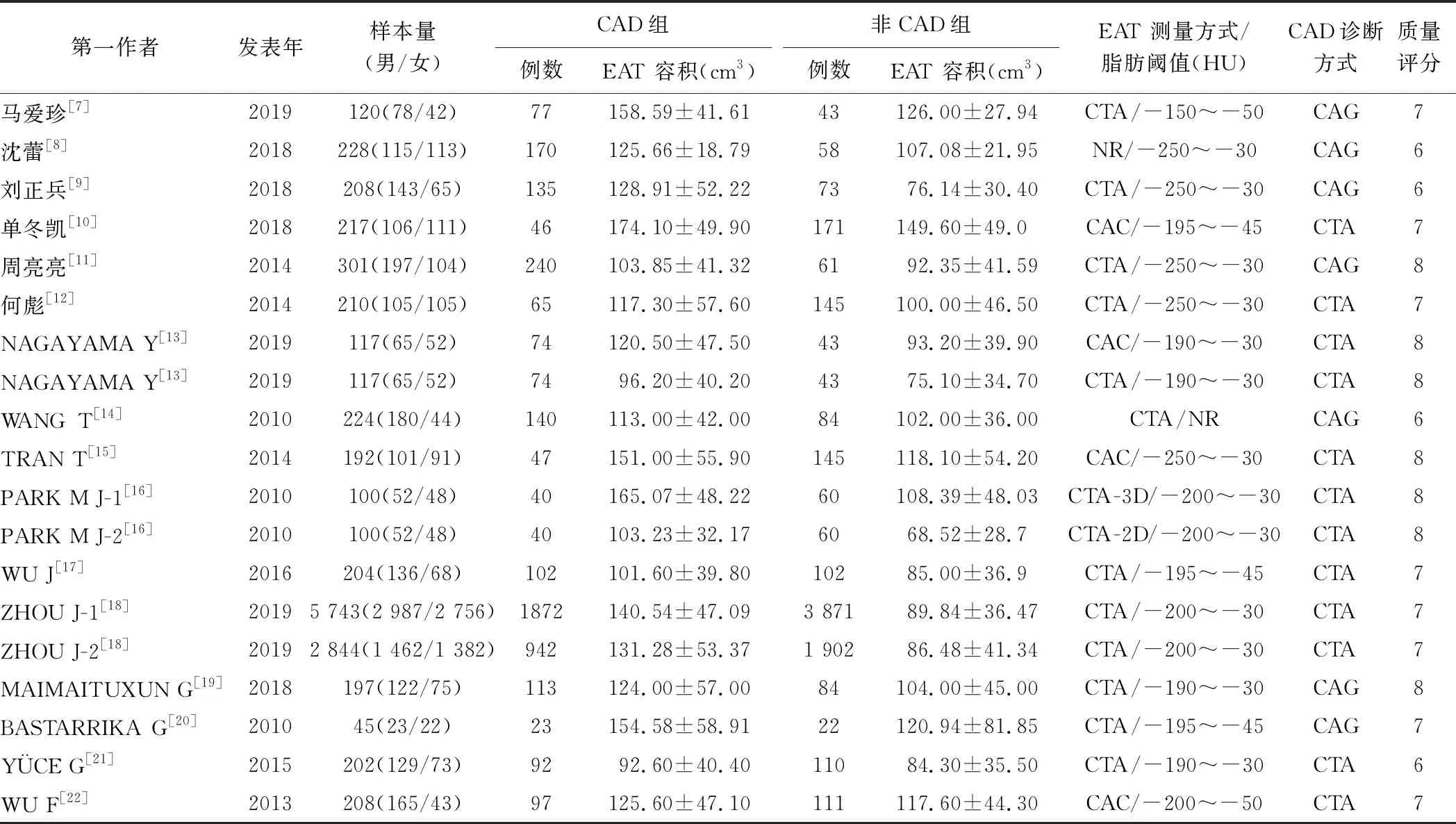
表1 CT测量EAT容积纳入文献特征
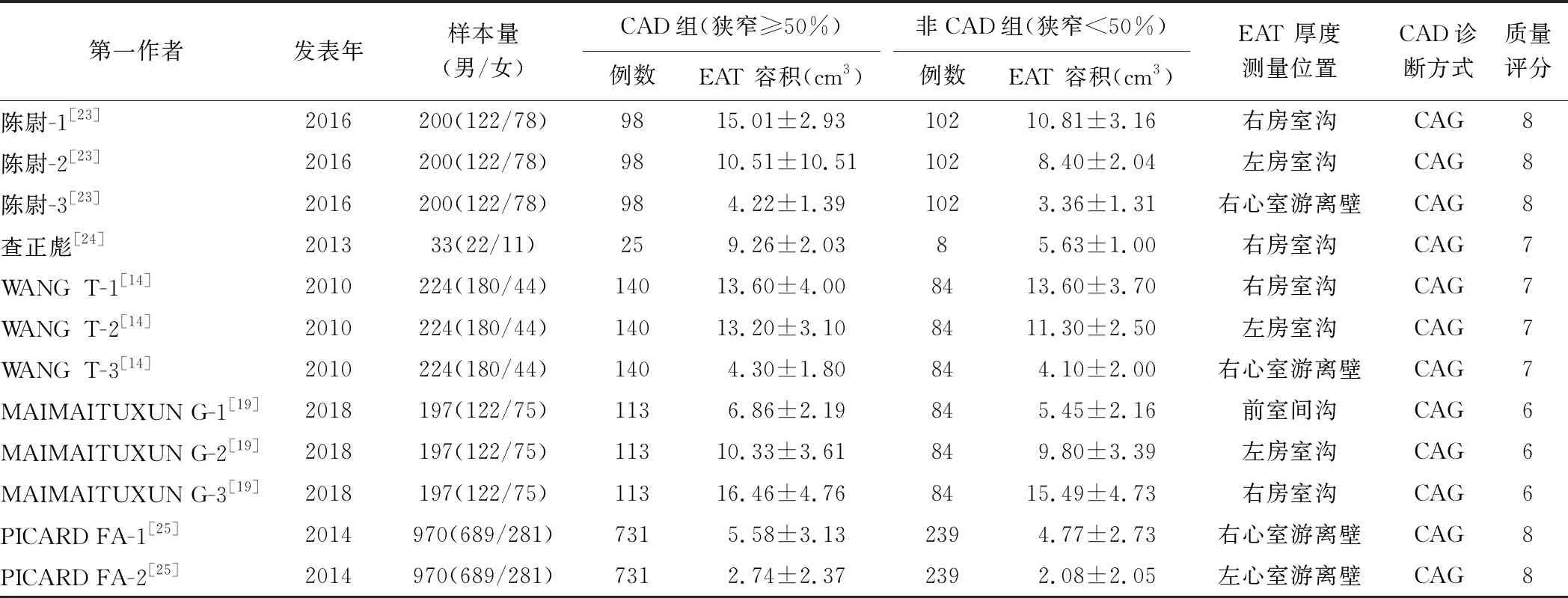
表2 CT测量EAT厚度纳入文献特征
2.2.3 回归及亚组分析 以发表年(t=0.37、P=0.72)和测量位置(t=-0.76、P=0.47)为协变量对测量EAT厚度的文献[14,19,23-25]进行回归分析,以发表年(t=1.21,P=0.25)、CAD诊断方式(t=0.80,P=0.44)、EAT容积测量方式(t=-1.63,P=0.13)及容积测量时设定的脂肪阈值(t=1.06,P=1.31)为协变量对测量EAT容积的文献[7-22]进行回归分析,差异均无统计学意义,表明以上因素均非文献异质性的主要来源。对以上作为协变量的因素分别进行亚组分析的结果见表3。
2.2.4 发表偏倚 经Egger线性回归分析,EAT厚度相关文献[14,19,23-25]不存在发表偏倚(t=1.73,P>0.1);EAT容积相关文献[7-22]存在发表偏倚(t=-4.49,P<0.01)。
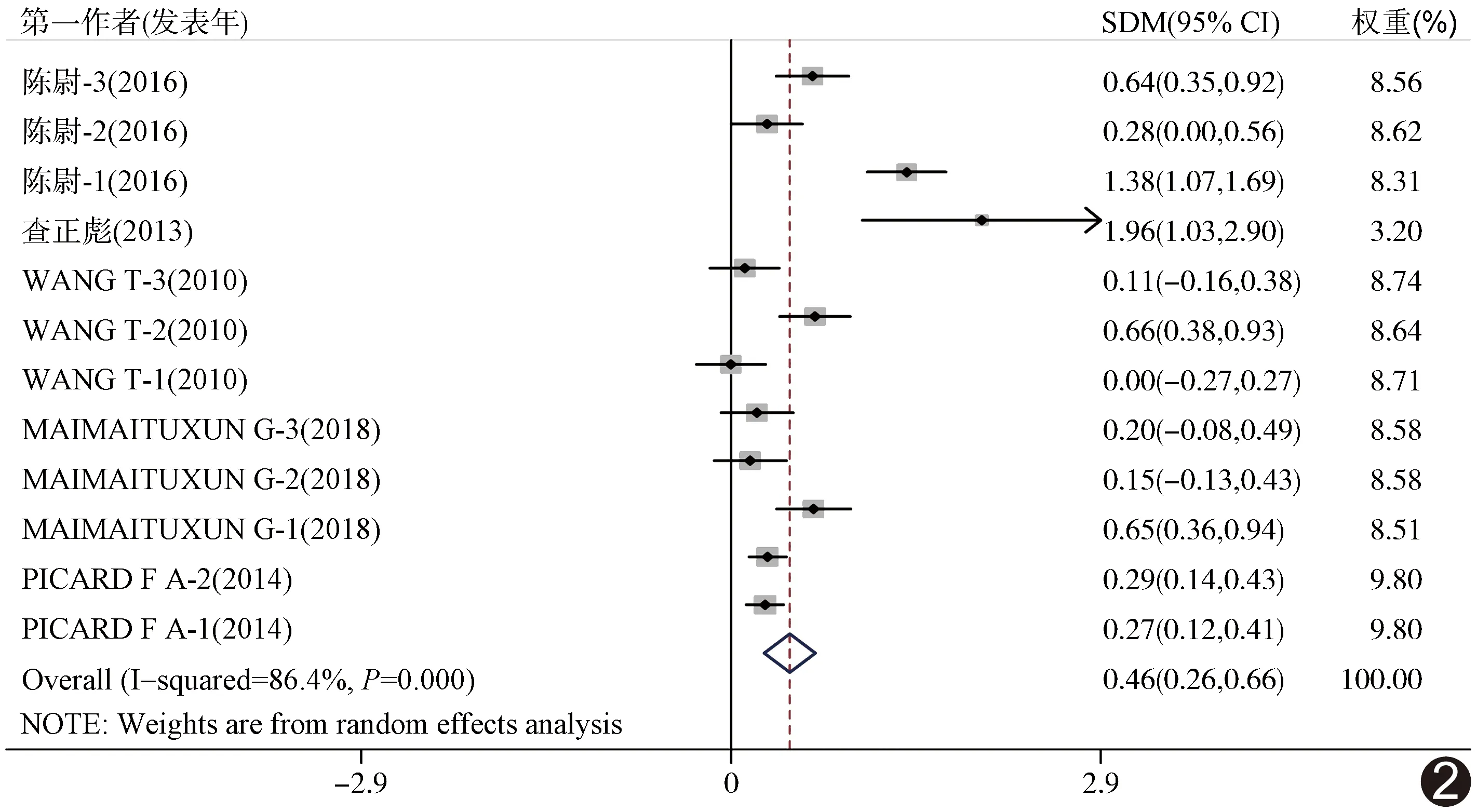
图2 EAT厚度与CAD关系的森林图
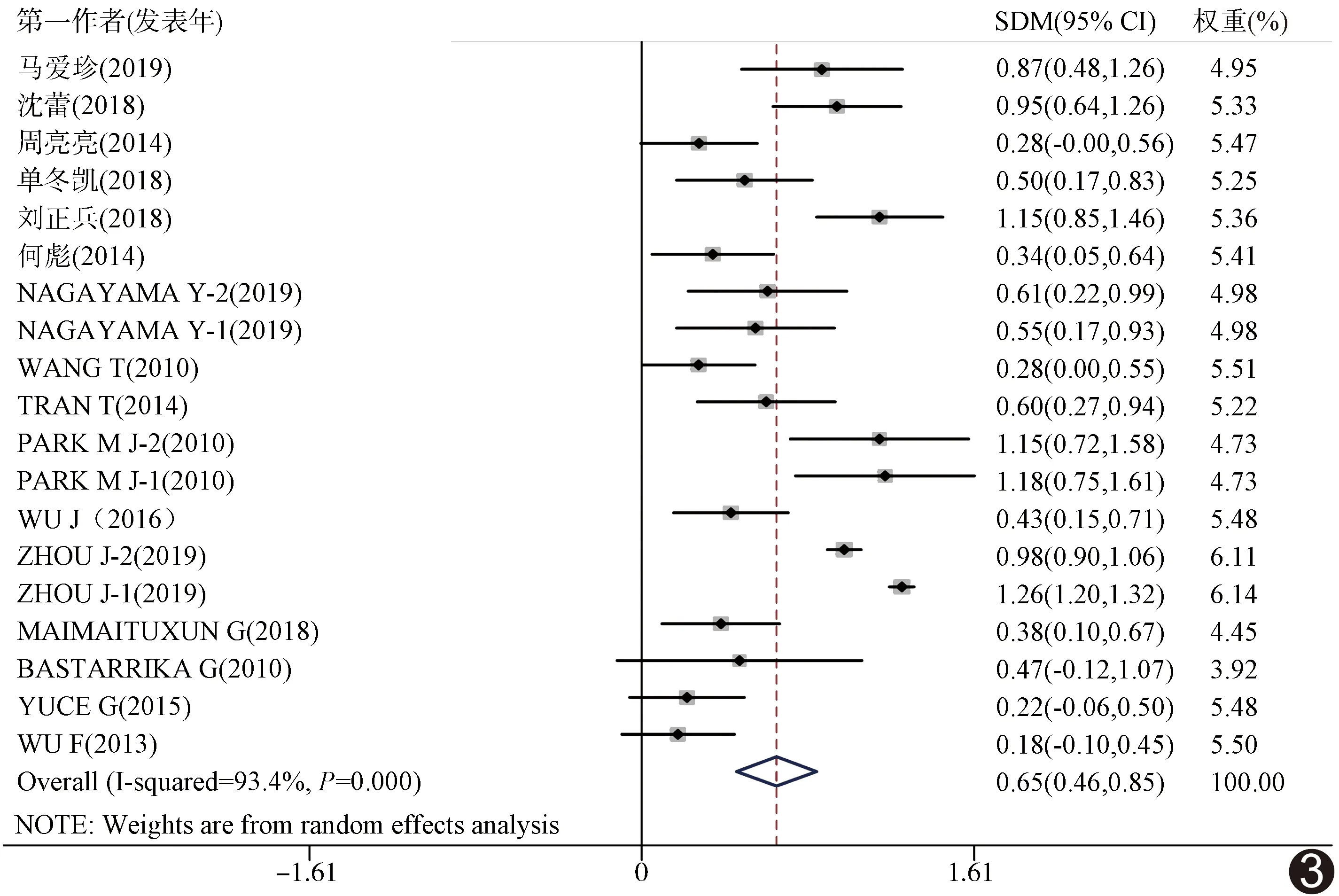
图3 EAT容积与CAD关系的森林图
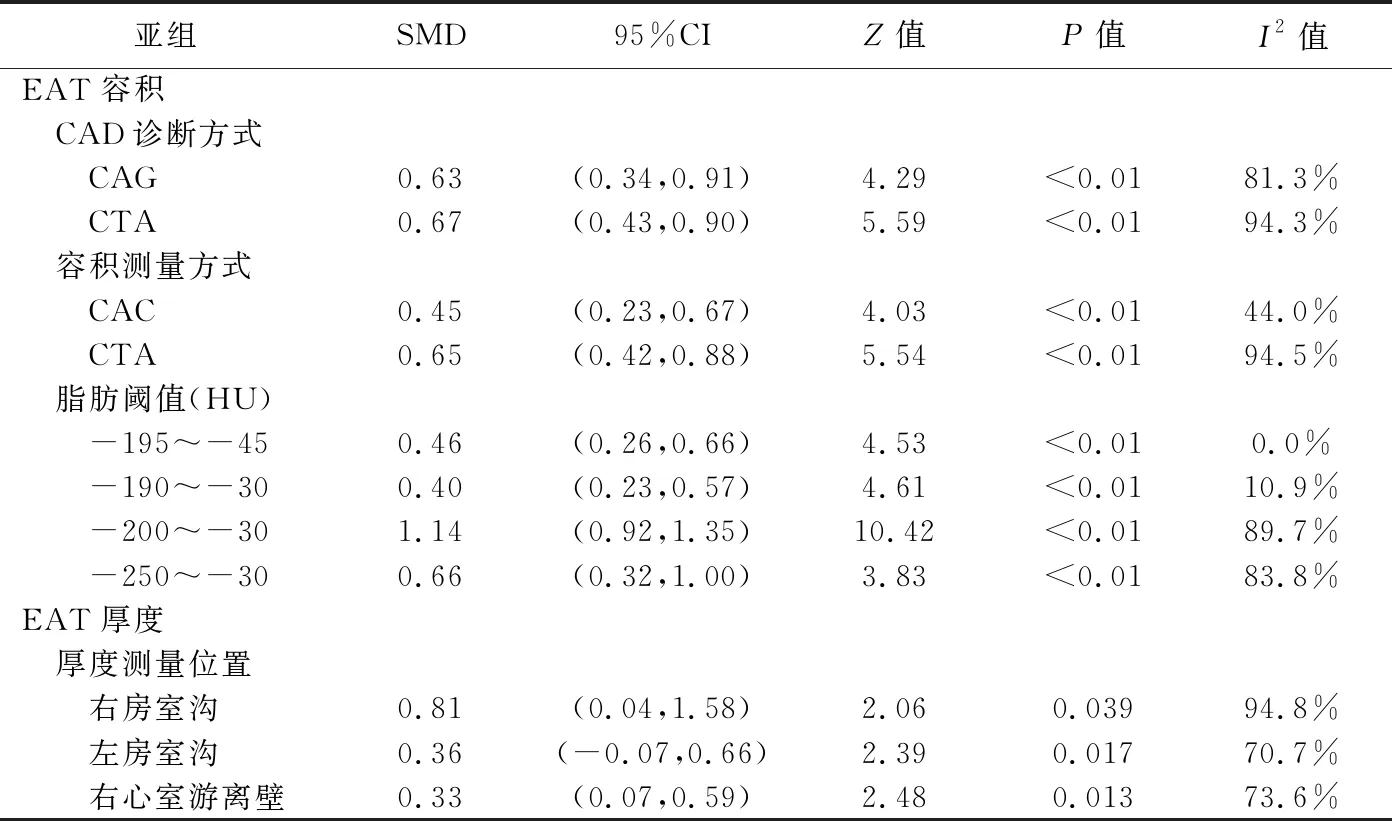
表3 EAT容积及厚度文献异质性亚组分析结果
3 讨论
心血管疾病是导致人群死亡的主要原因,其中CAD患病人数仅次于脑卒中[26]。测量EAT有助于分析CAD严重程度及预后,抑制EAT形成可阻止心房纤颤及心力衰竭发生、发展[27]。目前主要采用影像学方法如超声、CT、MRI对EAT进行定量分析。超声测量EAT厚度方便快捷、成本低、无辐射,但受医师经验影响较大,医师间测量结果存在一定差异。MR检查费用较高,且心脏MRI普及程度有限。CT扫描较为普及,且测量EAT受人为影响相对较小。
本研究结中CAD组EAT厚度和容积均高于非CAD组,表明EAT与CAD发生有关。纳入文献质量评分均>5分,但EAT厚度及容积纳入文献之间的异质性均较大。对文献发表年、CAD诊断方式、EAT厚度测量位置、容积测量时脂肪阈值等进行回归分析,结果显示以上因素均非异质性的主要来源;进一步亚组分析结果提示测量EAT容积时设定的脂肪阈值并不影响EAT与CAD之间的关系;而测量EAT厚度位置的合并效应值也说明测量位置并不影响EAT厚度与CAD的关系。本研究纳入文献虽然存在异质性和发表偏倚,但任意单一文献对合并模型结果的影响均不大,提示结果稳定;详细阅读原文,发现EAT沉积还可能与体质量指数(body mass index, BMI)有关,但多数文献未说明研究对象的BMI,且部分文献甚至未提及BMI,无法对BMI进行回归分析和亚组分析。测量EAT容积与CAD关系的文献存在发表偏倚,原因可能为纳入文献数量有限,且阴性结果研究较少。本研究纳入文献均为病例对照研究,证据等级较低,故需谨慎看待合并效应结果。
综上所述, CT定量测量EAT与CAD之间存在相关性,可能对预测CAD发生发展具有重要意义;但EAT能否成为CAD新的治疗靶点以及能否采用EAT预测评估CAD发生发展尚需进一步研究。