改性吸附剂去除废水中磷的应用研究进展
崔婉莹,艾恒雨,张世豪,魏金枝
(哈尔滨理工大学化学与环境工程学院,黑龙江哈尔滨150040)
磷被认为是导致水体富营养化的主要限制因子[1],随着磷化工的发展,水体富营养化越来越严重,减轻水体富营养化程度对保障饮用水安全意义重大,减少含磷废水的排放并对其进行有效治理是减少水体磷污染的重要途径[2]。目前常用的除磷方法有化学沉淀法、生物法、吸附法、离子交换法和膜分离方法,其中生物法和化学沉淀法应用较为广泛[3]。化学沉淀法除磷具有效果佳、效率高、操作简便等优点,但是除磷过程需投加大量药剂,所需成本较高,且除磷后产生的污泥含水量大,处理困难,易造成二次污染[4]。生物除磷法较化学除磷法成本低、产泥量少、除磷范围广,但对操作条件严格,且在除磷过程中受多种因素影响,导致出水质量不稳定,总磷往往无法达到排放标准,需配合深度处理进一步去除[5]。吸附法除磷则无上述问题,且具有工艺简单、操作简便、高效低耗、吸附容量大、污染少、吸附剂的性能稳定易再生等特点,可用于回收磷酸盐[6-7]。
废水中磷的存在状态取决于废水的类型,常见的有正磷酸盐、聚合磷酸盐和有机磷。自然氧化和生物氧化过程能够将更复杂形式的磷转化为正磷酸盐,常规二级生物处理出水中90%以上的磷酸盐以正磷酸盐形式存在,因而废水除磷主要是去除废水中的正磷酸盐。正磷酸盐在水溶液中可能存在4种形态,即H3PO4、、、。4 种形态存在,在接近中性pH 条件下,主要以和态间存在平衡关系,不同的pH 条件下,以不同形形式存在。
吸附法除磷的效果在很大程度上依赖于吸附剂本身和吸附反应条件。吸附材料应同时具有高吸附容量、高吸附速率、对吸附物质的高选择性、吸附过程无污染物质溶出、性能稳定、廉价易得且容易再生等特点[8]。溶液pH和溶液中的共存阴离子是吸附法除磷不可忽视的影响因素,pH 不仅影响吸附材料的表面电荷,还影响溶液中磷的存在形态,进而影响磷的去除效率[9]。在中性条件下,水中的共存阴离子在吸附过程中会有一定的竞争作用。由于吸附剂具有不同的表面性能及电化学特性,尽管在同一吸附条件下,不同类型吸附材料的吸附除磷性能也存在较大差异[10],故吸附剂是整个吸附工艺的核心,有必要深入研究不同吸附剂的除磷效果。本文将目前研究较多的除磷吸附剂分为4类,即改性硅酸盐类吸附剂、改性金属氧化物类吸附剂、改性固体废弃物类吸附剂和聚合物类吸附剂,分析了各类吸附剂的特点、除磷机理和存在的问题,以利于在不同原水条件下,有针对性地选择吸附除磷材料,提出除磷吸附剂未来的研究方向。
1 改性硅酸盐类吸附剂
天然硅酸盐类吸附剂具有孔隙多、比表面积大、耐酸和耐腐蚀的特性,且材料易于获得,被用作多种物质的吸附剂,但天然吸附剂也存在对磷的吸附容量小、吸附不具备选择性等不足,为此研究者对硅藻土、沸石和凹凸棒石等天然硅酸盐类吸附剂进行了改性。
1.1 改性硅藻土
硅藻土是一种生物硅质岩,由硅藻遗骸堆积形成,因其具有特殊的多孔构造和较大的比表面积,被作为吸附材料广泛应用于废水处理领域[11]。硅藻土是一种天然吸附材料,主要成分是SiO2,其表面富含硅羟基,同时含有大量氢键,因羟基和氢键的存在使得硅藻土具有表面活性和吸附能力[12]。天然硅藻土表面是带有电荷的,可能带有正电荷也可能带有负电荷,这主要取决于溶液的pH。因为在硅藻土表面存在着Si-O 和Al-O 键的水解断裂反应,水解断裂后生成的R-OH 具有两性性质,可与H+和OH-进一步发生反应,如式(1)、式(2)所示。
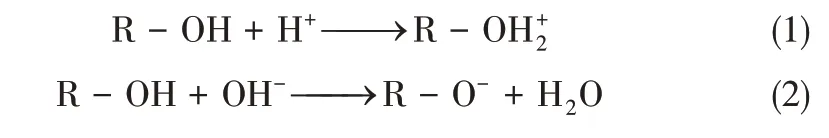
硅藻土的零电荷点约为2,故只有当溶液pH小于2时,硅藻土表面才带有正电荷。由于静电排斥作用,带负电的表面不利于磷酸根离子的吸附,因此需要进行特定的改性,将其表面电荷由负转变为正,从而改善对磷酸根阴离子的吸附性能。
多数水化金属离子会发生水解反应,配位水分子给出质子变成OH-,与金属离子结合生成羟基氧化物,这类羟基氧化物具有较高的零电荷点。因而将适当的金属阳离子加入硅藻土中,可以提高硅藻土的整体零电荷点,使其在中性溶液中带有正电荷,更有利于磷酸根离子的吸附。同时嵌在硅藻土表面的纳米态羟基氧化物,增大了硅藻土的比表面积,进一步提升了硅藻土的吸附性能。范艺等[13]以氧化锆为改性剂,通过交联法制得改性硅藻土,大大提升了硅藻土的比表面积,硅藻土经氧化锆改性后比表面积增加至75.22m2/g,是原硅藻土的5.37倍。吸附热力学实验研究表明,吸附过程符合Langmuir 模型,经计算最大吸附容量为10.56mg/g。Xiong 等[14]采用廉价的FeCl2改性硅藻土,对硅藻土表面进行氢氧化钠处理以及亚铁酸盐沉积,制备改性硅藻土。经氢氧化钠处理,硅藻土表面部分二氧化硅溶解在氢氧化钠溶液中,溶解硅有助于稳定的二价铁氧体形成。这些稳定的纳米级铁氧体沉积在硅藻土的大孔和中孔中提升了硅藻土的比表面积,同时提高了硅藻土的整体零电荷点,进而提升了吸附剂对磷的吸附性能。实验测得,改性后硅藻土比表面积为221.1m2/g,较原硅藻土高出8.5 倍;零电荷点值从原硅藻土的5.8 提高至10。在pH=4 时吸附效果最佳,饱和吸附容量达37.3mg/g。Wu 等[15]采用水合镧氧化物改性硅藻土去除低浓度含磷废水,实验表明,0.1mol/L LaCl3处理的硅藻土吸附效果最好,对含磷量低于2mg/L的废水,最大吸附容量达58.7mg/g。且La-硅藻土吸附含磷废水后平衡pH 为7.26,在实际工程应用中,处理后的水体不需调节pH 即可排放。废水其他共存离子对磷的吸附过程没有明显的影响,且吸附过程中没有出现明显的La 浸出。在解吸再生实验中,采用NaOHNaCl 混合物对La-硅藻土进行连续8次吸附解吸循环实验,磷吸附能力仍保持在88%以上,是一种能够有效处理低磷废水且可循环使用的理想吸附剂。
对于金属改性硅藻土除磷的吸附过程中,pH是影响吸附效果的主要因素,因为溶液pH 影响着吸附剂表面带电荷情况,同时影响着溶液中磷酸盐的存在状态。以镧改性硅藻土为例,不同离子形式的磷酸盐吸附到改性硅藻土上的过程可用图1 表示。硅藻土经镧改性后,在其表面形成了镧氧化物,镧氧化物具有较高的零电荷点,当溶液pH 低于零电荷点时,镧氧化物表面即带正电。它去除水中磷酸盐的机制包括3种,即配位交换、静电作用和路易斯酸碱作用。在酸性条件下,镧改性硅藻土表面被质子化,通过静电力形成外球复合物,经配位交换形成内球复合物。在碱性条件下,镧改性硅藻土的表面去质子化并带负电,静电排斥起作用,同时削弱配位交换。此时,镧活性位点与磷酸根离子中的氧阴离子之间的路易斯酸碱作用可能形成La-O络合,可在较高pH下去除磷酸盐。
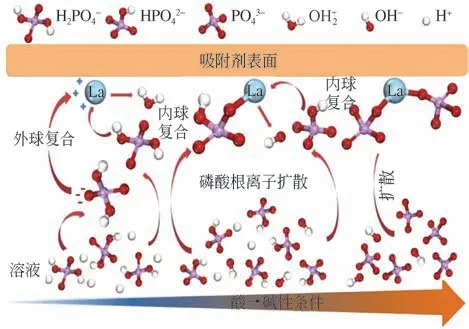
图1 镧改性硅藻土吸附除磷机理[15]
除了将金属阳离子加入硅藻土改性外,制备复合式改性硅藻土吸附剂也能显著提升硅藻土对磷的吸附性能。纳米分子筛的磷吸附性能较好且具有较大的比表面积,但沉降性能较差,硅藻土可协助其沉降,基于这一特性将二者复合制备吸附剂,可解决两种吸附剂单独除磷时存在的不足。段宁等[16]以硅藻土和沸石为原料,加入黏结剂和造孔剂,制备复合颗粒吸附剂。采用最佳配比硅藻土∶沸石(质量比)为6∶4,经700℃焙烧90min。用此复合吸附剂处理5mg/L的含磷废水,在投加量为20g/L时,能够去除94%以上的磷酸盐。高耀文等[17]以废弃钢渣和硅藻土为原料,加入黏结剂NaSiO2制备复合吸附剂除磷,复合吸附剂产生了新的晶相,吸附进行1h 后基本达到稳定,复合吸附剂对磷的吸附更符合准二级反应动力学模型,计算理论饱和吸附容量为1.428mg/g。
1.2 改性沸石
沸石是一种架状铝硅酸盐[18],由通过氧桥相互连接的Si 或Al 原子组成,具有四面体骨架结构,从而形成很多形状规则、大小一定的空穴和孔道,使得沸石具有巨大的比表面积,且沸石廉价易得,是一种较理想的吸附材料。但是沸石的硅铝架结构的电负性,决定了其具有从溶液中回收大多数阳离子污染物的能力,其对阴离子污染物的交换能力较低[19]。同时沸石具有很强的亲水性,沸石的孔隙常含有大量沸石水和杂质,降低了沸石的吸附性能,故而沸石需要经过改性增强磷酸盐吸附能力。多项研究表明,对于沸石的改性可以通过酸、碱和盐改性提高其交换容量,通过金属氧化物等改变其性质,增强对磷酸盐阴离子的吸附能力。
程婷[20]采用酸改性沸石,探究不同种类的酸以及酸的浓度对磷酸盐吸附性能的影响。研究表明,盐酸改性要优于硫酸改性,4mol/L的盐酸改性效果最佳,对于5mg/L 的含磷溶液,磷酸盐去除率达50.50%。李辉等[21]采用酸碱盐分别改性沸石。结果表明,盐改性沸石除磷效果最佳,经20%MgCl2浸泡后,在500℃下煅烧2h后制备的改性沸石,吸附160min后,可去除78%的磷酸盐。
通过掺入金属可以大大增强沸石对磷酸盐的吸附能力。崔有为等[22]采用浸渍法,以镧和铈为改性剂改性沸石。研究结果表明,镧、铈改性沸石对磷的最大吸附容量分别为0.3127mg/g 和0.3329mg/g,接近原沸石(0.0398mg/g)的10 倍。李海芳[23]对比镧、锆改性沸石对磷酸盐吸附性能的影响,发现,经镧、锆改性后沸石对磷的去除率分别为75.5%和74.4%,吸附性能大幅度提高。此外,在对吸附剂进行镧改性基础上进行焙烧处理,当焙烧温度达到400℃时,其吸附除磷效率可进一步提高,达到86%。稀土元素镧用于改性沸石,明显提升了沸石对磷的吸附性能,但吸附性能多受pH 的限制。为克服镧改性吸附剂只能在较窄酸性范围内有效的现象,Shi 等[24]通过共沉淀法将La 与Mg 和Al 结合到沸石上,制备了一种新的掺入镧的三元(氢) 氧化物纳米复合材料(MALZ),研究其对磷吸附性能的影响。研究结果表明该吸附剂对pH 变化具有优良的耐受性,磷酸盐吸附容量在pH 为4~10 的范围内无明显变化,且吸附后的平衡pH 接近中性。在pH 为6.6 时MALZ(12.5%La,质量分数)对磷酸盐的最大吸附容量达80.8mg/g。为了进一步评价MALZ 除磷的实际应用效果,进行了固定床柱连续吸附实验,在7.5mL/min 的流速下,MALZ 的有效处理体积为4800BV(3600mL)。沸石经稀土金属改性后对磷酸盐的吸附主要包含两方面,一是静电引力作用,二是经稀土金属改性后产生了新的晶体[LnAl(SO4)2(C2O4)·12H2O],在吸附磷酸盐的过程中,镧、铈、和锆改性沸石表面均形成了含有羟基的官能团,磷酸根离子与羟基离子进行交换,再与镧、铈和锆离子进行配位,进而去除磷酸盐。
上述Ce3+、La3+和Al3+等多价金属改性的天然矿物具有良好的磷酸盐吸附能力,但为了减少这些金属释放到环境中对水生物种有毒害作用和水质恶化的风险,并且减少化学药剂的成本,Mitrogiannis等[25]使用Ca(OH)2改性天然沸石。研究表明,用0.25mol/L Ca(OH)2预处理天然沸石,处理10mg/L的含磷废水,磷酸盐的去除率从1.7%增加到97.6%。当Ca(OH)2浓度过高时(高于1mol/L),会导致Ca(OH)2颗粒沉淀和聚集,这是因为Ca(OH)2水溶性低,导致吸附剂孔堵塞,阻碍Ca(OH)2扩散到内表面结合位点。Ca(OH)2改性沸石对较高的P 浓度(200mg/L)废水也具有良好的吸附能力(7.57mg/g)。在吸附过程中,Ca(OH)2改性沸石具有酸碱耐受性,初始溶液pH 从4 增加到9 并不影响磷酸盐的去除率。Ca(OH)2改性沸石吸附剂除磷过程主要如下,当溶液初始pH 范围为4~9 时,pH<pHPZC,吸附剂表面质子化并带正电荷,有利于对、两种磷酸盐的静电引力。在酸性条件下,吸附剂表面羟基进行质子化,、与吸附剂表面之间形成外球面表面络合物,如式(3)、式(4)所示。
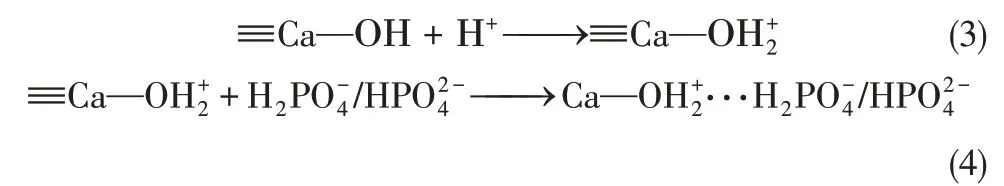
在吸附一段时间后,溶液pH 会增加(仍低于pHPZC),吸附磷酸盐后吸附剂的pHPZC也降低了,此时配体交换机制起主导作用,在配体交换过程中,一价和二价磷酸盐阴离子取代了位于吸附剂表面的基团,形成了内球表面复合物,如式(5)、式(6)所示。
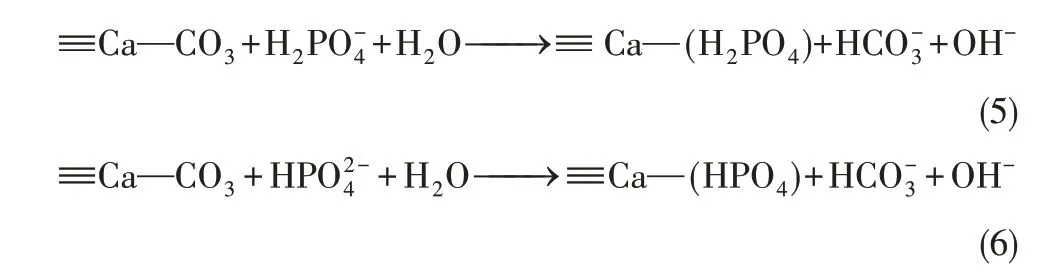
此时,由于碳酸盐基团被释放到溶液中,导致pH 升高,吸附剂表面正电荷减少,静电吸引作用减弱,但同时释放到溶液中的Ca2+与磷酸盐离子结合形成沉淀,在碱性条件下静电吸引减少的磷吸附与吸附剂表面的磷酸钙沉淀抵消。故初始溶液pH从4增加到9并不影响Ca(OH)2改性沸石对磷酸盐的去除率。
1.3 改性凹凸棒石
凹凸棒石是一种具有纤维形态的水合铝镁硅酸盐矿物,具有悬浮液黏度高、比表面积大、吸附能力强等特点[26]。通过改性能有效提高凹凸棒石对磷酸盐的吸附能力,例如经酸改性可以除去表面的碳酸盐,经碱焙烧改性,可以除去孔道内的结晶水,均进一步增大其比表面积,焙烧改性可以去除孔道内外存在的自由水、结晶水等,增加了交换容量。
张建民等[27]对凹凸棒石进行酸、碱改性处理。研究发现,酸改性后凹凸棒石的比表面积有不同程度的提升,9%HCl改性的凹凸棒石除磷效果最佳,酸浓度过低,改性效果不明显,酸浓度过大,会破坏凹凸棒石的结构,降低其吸附性能。碱改性凹凸棒石吸附能力也得到提升,但是吸附时间较长。最后对凹凸棒石进行酸碱复合改性,先经碱焙烧改性,再经9%HCl 改性,最终磷酸盐去除率达99%以上。而余荣台等[28]采用碱干法改性代替常用的碱湿法改性凹凸棒石,将固体氢氧化钠与凹凸棒石按摩尔比为1∶1 混合,经500℃煅烧2h,除磷率达92%,采用碱干法改性除磷的效果要优于碱湿法改性。潘敏等[29]进一步探究了不同焙烧温度对热改性凹凸棒石除磷性能的影响,选取了200~900℃下8个不同温度进行焙烧。研究表明,焙烧温度低于400℃时,热改性对凹凸棒石除磷效果的影响不明显;焙烧温度为700℃时,除磷效果最佳,吸附容量达13.52mg/g;当焙烧温度高于700℃时,凹凸棒石结构被破坏,可能堵塞部分微孔,导致吸附性能降低。
天然富含钙的凹凸棒石是一种特殊的凹凸棒石,因含钙量高而被关注,对其进行盐、热复合改性处理,能提升对磷酸盐的吸附性能。Yin 等[30]以天然富含钙的凹凸棒石(NCAP)为原料,通过混合盐改性(NaCl 和MgCl2)和高温焙烧组合法对其进行改性,制得混合盐、热处理的改良NCAP,探究其对磷的吸附性能。研究表明,将NCAP加热至700℃或更高的温度时,可以大大提高磷酸盐与NCAP 的结合能力,在5min内,改性NCAP 可除去97.2%的磷酸盐,且对磷含量在5~600mg/L范围内的废水,去除率均超过90%,磷酸盐去除过程受pH影响很小。柱吸附实验结果表明,对磷酸盐的吸附有很大的影响,NCAP-NM 对富营养化河水的有效处理体积是1440BV。Yin等[31]将水合铝加入到多孔热处理的富钙凹凸棒石(TCAP)中,增强对磷的吸附能力。TCAP 先经700℃煅烧2h,然后浸渍在AlCl3溶液中经烘干后制成1~2mm 的颗粒。结果表明,浓度为2mol/L 的AlCl3浸渍可显著提高TCAP 的磷吸附能力,在pH 为7 时,铝改性TCAP达到最大磷吸附容量8.79mg/g,约为TCAP磷吸附容量的两倍,且在pH 为4~11 内均具有实用的吸附效益。
将富含钙的凹凸棒石加热到700℃或更高的温度,可以大幅度提升凹凸棒石的磷酸盐结合能力,这主要是较高的煅烧温度下形成碱性钙质材料所致。氧化钙、氢氧化钙和钙镁硅化合物等活性Ca物质可迅速将Ca2+释放到溶液中,与和结合,形成Ca-P 沉淀。磷酸盐吸附在富、含钙质凹凸棒石上的机理如图2所示。此外,高温焙烧形成碱性钙质材料,导致零电荷点的显著提高,在很宽pH 范围内改性富含钙的凹凸棒石表面均携带正电荷,故废水处理期间磷去除效率受溶液pH影响很小。吸附过程中几乎不受阴离子的影响,但的存在会明显影响到磷酸盐的吸附,这是因为水中的会与磷酸盐竞争,形成含有Ca2+的沉淀物。然而,高浓度的HCO3-废水不常见,因此改性凹凸棒石在实际应用中,磷酸盐的吸附容量不会受到显著影响。
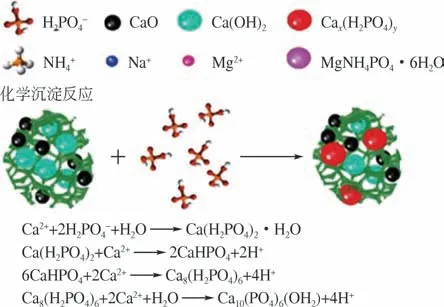
图2 富含钙质凹凸棒石上磷吸附机理[30]
2 改性金属氧化物类吸附剂
金属氧化物/氢氧化物吸附剂是目前国内外很成功的吸附氧阴离子的吸附剂。因为它们对磷酸盐具有特殊的亲和力,目前已有较多的金属氧化物及氢氧化物被用于磷酸盐吸附研究,Al、Fe、Ca、Mg、La、Ce 等金属多被用于合成吸附剂,其中稀土元素La和Ce因为具有较高的磷酸盐吸附容量成为改性除磷吸附剂的首选。
2.1 改性铁(氢)氧化物
基于铁(氢)氧化物的吸附剂常被用于废水吸附除磷,因为这种吸附剂不仅无毒且价廉,还具有环境友好性和化学稳定性。铁氧化物主要有赤铁矿、磁铁矿、磁赤铁矿和铁酸盐。铁氢氧化物种类较多,一般包括针铁矿、水铁矿、纤铁矿和四方纤铁矿等,它们的结构和稳定性各异,彼此之间在一定条件下可互相转化。目前,各种铁基吸附剂,如铁矿物、合成铁基材料和掺杂于活性炭、石英砂等载体上的铁(氢)氧化物,已广泛应用于废水除磷。
赤铁矿是自然界中分布极广的一种铁矿物,对于难处理的低品位矿石,是作为吸附剂的良好材料。Zhou等[32]采用低品位高磷鲕状赤铁矿处理酸浸磷酸盐废水,磷吸附在60min内达到平衡,总磷去除率为92.27%,是一种经济型吸附剂,但是吸附高度依赖于pH和吸附剂量,在pH=5.5下观察到最大的磷去除率。Ajmal 等[33]评估了3 种合成(氢)氧化铁吸附剂(水铁矿、针铁矿和磁铁矿)对磷的吸附性能。研究表明,水铁矿是3种合成(氢)氧化铁吸附剂中磷吸附性能最好的,最大磷吸附容量达66.6mg/g,其次是磁铁矿,再次是针铁矿。合成(氢)氧化铁吸附剂去除水中的磷主要是通过氧化铁吸附剂表面与磷酸盐间产生的静电吸引力。磷酸盐的吸附过程是可逆的,可以在中性及碱性环境中以不同的速率进行解吸,良好的解吸能力有利于实际应用中吸附剂的再利用。
铁氢氧化物自身带有羟基官能团,且具有较大的比表面积,是一种对磷、重金属等均具有良好吸附性能的吸附材料。Saha等[34]以氯化铁和氢氧化钠为原料制备颗粒状氢氧化铁(GFH),研究表明,GFH 对低浓度磷酸盐具有很高的吸附能力。吸附效率随着溶液pH 的增加而降低,随着温度的升高而提高。在pH 为3 时,磷酸盐去除效率最高。孙丽华等[35]用氢氧化钠改性铁盐,利用产生的羟基氧化铁去除磷酸盐,实验按不同比例混合NaOH 和FeCl3,探究不同摩尔比对吸附性能的影响。结果表明,FeCl3和NaOH 的摩尔比为1∶3 时,吸附剂对磷吸附性能最好,且在pH为4~9内均具有实用价值。郑晓英等[36]以自行制备的FeOOH 为吸附剂,处理低浓度含磷废水。实验结果表明,在投加量为0.03g/L、pH=6条件下处理0.5mg/L的含磷废水,可以将磷酸盐浓度降至0.008mg/L。羟基氧化铁中α,β,γ-FeOOH 的结构具有多种不同的形态,也具有不同的理化性质,进而具有不同的去污效果。众多学者对羟基氧化铁制备过程的影响因素进行探究,寻求最佳的羟基氧化铁合成条件,以达到最佳的磷酸盐去除效果,主要的影响因素有反应物种类和浓度(铁盐、沉淀剂的种类和浓度),制备条件(pH 和温度等),表面活性剂和阴、阳离子调节剂[37]。继续研究羟基氧化铁净化污染物的作用机理以及影响羟基氧化铁制备过程的主要因素,进而制备出具有不同特性的羟基氧化铁,增强其降解污染物的能力,在实际工程应用中具有重要意义。
尽管金属(氢)氧化物具有良好的吸附性能,且Fe3O4等材料具有磁性,能够分离吸附剂。然而,小于15nm 的纳米颗粒的磁分离可能是无效的,对于这种纳米吸附材料,在水处理后从溶液中分离是困难和昂贵的,基于这一情况,纳米金属(氢)氧化物吸附剂的大规模应用受到限制,因此,寻找适宜的载体制备复合吸附剂十分重要和急迫。Zhu等[38]制备了α-Fe2O3/Fe3O4包覆竹炭(HPA-Fe/C-B)的新型磁性层状多孔吸附剂,并对其磷酸盐去除能力展开研究。在25℃和pH=3 的反应条件下,粉状HPA-Fe/C-B 吸附剂(dg=0.11mm)处理初始磷浓度分别为2mg/L、5mg/L 和10mg/L 的废水,吸附分别在60min、720min 和1080min 时达到平衡,最大磷去除率分别为99.2%、97.5%和84.4%,HPA-Fe/C-B的磷吸附能力优于文献报道的纳米和微米尺寸的氧化铁颗粒。Yuan 等[39]采用改进的共沉淀法以Fe3O4和废FCC(催化裂化)催化剂为原料制备磁性复合吸附剂[FCC4@(Fe)1-O]处理含磷废水。结果表明,FCC4@(Fe)1-O(废FCC 催化剂与Fe3O4质量比为4∶1)对磷的吸附性能较好,吸附机理主要是磷酸盐取代表面羟基与Fe 和La 配位,并通过配位交换形成内环磷酸配合物,吸附过程受共存离子影响小,且不受pH 影响。胡小莲等[40]采用共沉淀法以生物炭为载体,制备了生物炭负载Fe3O4的复合吸附材料,解决了Fe3O4作为吸附剂应用时存在的不稳定、易团聚等现象,研究表明,吸附剂投加量为400mg/L、调节pH 至3 时,对50mg/L 的含磷废水去除率达92.14%。
2.2 复合金属氧化物
近年来,采用含有两种(或更多种)不同金属氧化物的复合吸附剂吸附除磷引起许多学者关注。考虑到这些金属氧化物复合材料不仅可以继承其母体单组分氧化物的优点,还可以表现出对磷酸盐吸附能力增强的协同作用,因此多金属氧化物的合成一直在发展。
经过对单元素及复合金属氧化物的除磷研究发现,稀土元素具有优异的磷酸盐吸附容量,且吸附过程受pH 影响小,抗干扰能力强,但是分离过程较困难。铁的吸附能力较差,但廉价易得且易分离,将二者结合制备复合吸附剂,可以解决稀土金属和铁单独使用时存在的问题。李永球[41]制备了磁性锆/铁复合吸附剂去除磷,在克服了磷和锆氧化物分离困难的同时也解决了铁氧化物吸附容量不理想的问题。研究表明,当铁和锆的摩尔比为1∶2时制备的吸附剂,比表面积为282.02m2/g,对磷的平衡吸附容量为21.3mg/g,且该吸附剂具有较强的磁性,吸附后可在外磁场作用下快速分离,采用0.1mol/L NaOH 溶液对吸附后的吸附剂进行解吸,解吸率达85%,经3次循环后,磷的去除率仍维持在70%以上,在处理含磷废水方面具有潜在价值,但不足之处是磷的吸附过程易受到HCO3-的影响。Wang等[42]用水热法合成Fe-La吸附剂去除磷。研究表明,在pH=8.5条件下,制备的La和Fe摩尔比为3∶1的Fe-La复合吸附剂吸附性能最好,比表面积达113.13m2/g,计算最大吸附容量为89.14mg/g。吸附过程形成金属磷酸盐沉淀,几乎不受其他共存离子的影响,且在较宽pH范围内均具有实用价值。
为了进一步节约成本,一些研究学者选择更为廉价的金属氧化物或利用废弃尾矿石进行复配,也取得了良好的磷酸盐去除效果。Li等[43]以白云石和锯末为原料,在不同温度下共热解制备了一种新型CaO-MgO 杂化碳复合材料,去除水中磷酸盐。白云石和锯末在900℃下共热解生成了富含碳、CaO和MgO 颗粒的复合物,由Langmuir 模型计算的最大磷吸附容量为207mg/g。合成的复合吸附剂在很宽的pH范围(3~11)内均能有效去除磷酸盐。此外,进行了盆栽实验,将负载磷酸盐的复合吸附剂用作磷基肥料的替代品,结果表明,芸苔幼苗地上部分的平均生长高度和平均鲜重均显著高于对照组,再生后的复合磷酸盐具有替代磷酸盐肥料的潜力。Liu等[44]以锰矿尾矿为原料,采用消解-共沉淀法合成了复合金属氧化物(CMOMO)吸附剂。经检测分析,CMOMO 比表面积为307.21m2/g,pHIEP为5.4,主要成分为非晶态的FeOOH、MnO2和AlOOH。磷的最大吸附容量随着温度的升高而增大,随着pH 的升高(4~10)或离子强度的降低(1~0.01mol/L)而降低。
对于两种(或多种)不同金属氧化物的复合,最重要的是找到金属之间合适的比例,使得吸附能力最大化,或能够有效利用昂贵的金属。Lin 等[45]建议将Mg(OH)2掺入ZrO2中,利用Mg(OH)2组分溶出的Mg2+增强了磷酸盐在ZrO2组分上的吸附。实验通过共沉淀法将摩尔比为2∶1的Mg(OH)2和ZrO2混合制备吸附剂,新型复合吸附剂具有更高的比表面积(195.9m2/g),是单组分Mg(OH)2的2.3 倍,pHZPC也更高(pHzpc=10.2),吸附容量分别比单组分ZrO2和Mg(OH)2高1.8 倍和4.3 倍。杨雪等[46]采用共沉淀法,以铜、铁和铝盐为原料,按铜、铁、铝摩尔比为1∶1∶4制备了三元复合吸附剂,探究其对磷的吸附性能。研究表明,在中性条件下磷的吸附性能最佳,最大吸附容量达62.6mg/g,磷酸盐的去除主要是吸附剂表面的羟基与磷酸盐反应生成表面络合物。溶出实验显示,在中性偏酸性条件下,铜、铁和铝离子没有明显的溶出量,但吸附过程会受到共存阴离子的干扰。
复合金属氧化物对磷酸盐的吸附受pH的影响,但影响程度随吸附剂的不同而有很大差异。以Mg(OH)2和ZrO2混合制备的复合吸附剂,pH 在4~10范围内对除磷效率的影响可忽略不计[45]。氧化锰掺杂铝氧化物吸附磷酸盐,在pH范围为5~6之间达到最大吸收[47]。磁性锆/铁复合吸附剂除磷效率随着pH 的增加而降低,由pH=1.5 的99.75%减小至pH=10 的41.06%[41]。这些结果反映出的吸附机理似乎是一致的。金属氧化物类材料的吸附过程可描述为图3所示。即金属氧化物吸附磷酸盐主要基于配位交换的内球吸附(2~4)和静电吸引(1)。当pH 低于零电荷点时,金属类吸附剂表面带正电荷,与带负电的之间存在静电吸引,此时去除机制为配位体交换和静电吸引;当pH 等于零电荷点时,不存在静电作用,此时去除机制是配位交换;当pH 高于零电荷点时,金属类吸附剂表面带负电,其与带负电的之间有静电斥力,此时,配位交换是主要吸附机制。吸附剂和被吸附物之间的最大静电吸引力应该发生在吸附剂带正电而被吸附物为负的pH 范围内的某处(低于吸附剂的pHZPC),故而吸附剂在强酸或中酸性甚至中性条件下,磷酸盐的吸附容量最大。同时又由于碱性条件有利于配体交换反应,而由于竞争作用过量的OH-不利于磷酸盐的吸附,故而某些情况下磷酸盐的吸附容量随pH的变化不大。
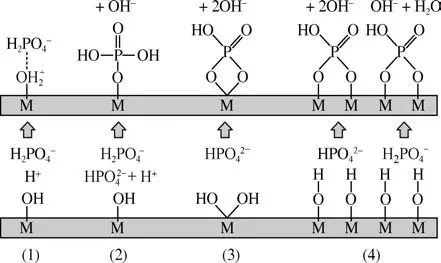
图3 金属类吸附剂吸附过程[48]
而对于金属氧化物类吸附剂除磷选择性方面,除受碳酸盐种类的影响外,几乎不受其他离子如硝酸盐、硫酸盐、氯化物的影响。对磷酸盐的吸附有很高的选择性。碳酸盐对磷酸盐的吸附会产生影响。一方面是碳酸盐的引入导致溶液pH 的增加,另一方面是由于争夺表面位点抑制了磷酸盐吸收,两种物质都被吸附在吸附剂表面。
2.3 改性层状羟基氧化物
层状双金属氢氧化物(LDHs)是一类通常用于有效去除阴离子的材料,也称为类水滑石化合物或阴离子黏土,水滑石是一种层状双金属氢氧化物。LDHs 具有相当大的比表面积和很高的阴离子交换容量。
通过改变二价和三价阳离子、层间阴离子和化学计量系数,可以合成范围广泛的LDHs。在各种合成方法中,通常优选的是共沉淀法。王镜渊等[49]以ZnCl2、CaCl2、FeCl3·6H2O 三种物质按不同比例混合制备层状双金属氢氧化物(LDHs),实验中FeCl3·6H2O 用 量 为0.5mol/L 保 持 不 变,ZnCl2、CaCl2的用量随x 的变化而发生改变,制得ZnxCa(2-x)-Fe系LDHs,探究不同配比对磷吸附性能的影响。结果表明,ZnxCa(2-x)-Fe 系LDHs 在酸性、碱性环境中均具有良好的磷吸附性能,在酸性废水中,主要通过离子、配位交换和静电吸引力除磷,在碱性废水中,主要依靠化学沉淀去除磷。经计算ZnxCa(2-x)-Fe 系LDHs 中的Zn2.0-Fe 和Ca2.0-Fe 吸附剂对磷最大吸附容量可达95.23mg/g 和228.31mg/g。Triantafyllidis 等[50]先合成母体Mg-Al 水滑石样品,然后加入不同量的Fe(Ⅲ)进一步改性LDHs,最后再进行煅烧改性,探究制备的各LDHs样品对磷的吸附能力。实验结果表明,其中Fe3+完全取代Al3+的LDHs(Mg∶Fe∶Al=3∶1∶0)经煅烧后制备的吸附材料除磷效果最佳,吸附容量达350mg/g。煅烧后的吸附材料吸附过程主要是混合金属氧化物的再水化和离子同时插入中间层以重建LDHs 结构,而未煅烧的吸附材料主要是通过层间阴离子的交换去除磷酸盐。
通常制备的LDHs 都是超细粉末,导致吸附时反应床阻力较大。为解决这一问题,可将LDHs固定在多孔基质上。Jia 等[51]以羧甲基纤维素钠作为稳定剂,将Mg-Al-Fe 层状双氢氧化物在混合甲酰胺/N,N-二甲基酰胺(DMF)溶剂中快速剥离,并结合到聚醚砜膜中,获得混合膜基质,应用于废水除磷。研究表明,该膜对磷的吸附在2h 内达到平衡,吸附容量为5.61mg/g,同时具有良好的解吸再生能力。
为了节约资源和废物再利用,LDHs 的制备原料也可以来源于工业废渣。Hu 等[52]使用工业残渣硼泥和赤泥在碱性条件下制备的层状双氢氧化物吸附剂(BR-LDHs)用于吸附磷酸盐。二价金属与三价金属的适当比例是形成LDHs 晶体结构的关键。研究表明,当硼泥与赤泥的质量比为4∶1,NaOH 浓度为4mol/L 时,成功制备了OBR-LDHs。OBR-LDHs上的磷酸盐去除率达到93%。
LDHs 除具有高比表面积外,还具有相对较快的磷酸盐吸附速度,对磷酸盐的吸附在2h 甚至更短时间内即可达到平衡[51,53-54]。文献[55]还报道了LDHs具有良好的解吸再生能力,基于Mg-Fe-Cl的LDHs 吸附剂,在磷酸盐的解吸实验中,经过6 个吸附-解吸过程中,解吸百分率约为91%。不同的LDHs 吸附剂吸附磷酸盐最佳pH 有所不同,磁性Fe3O4/Zn-Al-Fe-La-LDHs 吸附剂在酸性条件下对磷的吸附性能明显优于碱性条件[56],而钙基LDHs吸附剂在pH为3.5~10.5范围内对磷酸盐的吸附几乎是稳定的(98%)[57]。因此在实际运行中,应注意选取适宜的运行pH,还要考虑LDHs的化学稳定性,因为有研究指出金属可能在酸性或碱性环境中溶解[58]。
这些层状羟基氧化物吸附磷的过程也涉及静电吸引、离子交换、配位交换的协同作用。除此之外,吸附机理还包含通过离子交换与层间阴离子进行交换,以及对于煅烧后的LDHs 的再水化和氧阴离子同时插入中间层以重建LDHs 结构来吸附磷酸盐。因此,以OBR-LDHs 吸附磷酸盐为例,LDHs对磷酸盐的吸附过程可用图4表示。
3 改性固体废弃物类吸附剂
许多工业副产品是需要处理的废物,对它们进行合理有益的使用,可以节省处置成本,防止污染环境。目前,已有部分工业副产品用于处理水体中的污染物(如磷酸盐),它们大多是钢铁业(如钢渣)、采矿业(如赤泥)、发电厂(如粉煤灰)和污水处理厂(污泥)的副产品,它们的有效成分是具有化学反应性能的Fe 和Al 氧化物/氢氧化物、铝硅酸盐或碳酸盐等,可以通过配体交换、表面沉淀等与磷酸盐发生反应。这些物质去除磷酸盐的方法和去除效率取决于它们的物理化学特性。
3.1 改性钢渣
目前,我国钢渣主要用于冶金工业和建筑材料,但利用率不到22%,若这些钢渣不能得到妥善处理,将会占用越来越多的土地,危害环境[59]。钢渣主要由钙、铁、硅、镁和少量铝、锰、磷等氧化物组成,具有孔径结构和较大的比表面积,价格低廉,吸附性能稳定、效果良好,可用来处理废水,实现以废治废。
杨合等[60]采用钢渣除磷,探究反应条件对除磷性能的影响。结果表明,减小粒径,增大投加量,有利于磷酸盐的去除。溶液pH 对钢渣除磷影响较显著,酸性条件更利于钢渣除磷,pH=4 时除磷效果最佳,去除率达70.09%,较中性条件下的磷去除率高出15.43%。王莉红等[61]探究pH 对钢渣除磷效果影响,也得出相似结论,在pH 为4~7.5 时钢渣对磷酸盐有较好的去除效率。
钢渣去除磷酸盐主要是吸附和沉淀两方面的作用,其中化学沉淀起主导作用。酸性条件下,钢渣会产生Ca2+、Fe3+等离子,与磷酸根结合产生难溶性沉淀,同时酸性条件下产生的铁系、铝系氧化物对磷酸盐有一定的吸附作用;在碱性条件下,磷酸根主要通过与氧化镁或氧化钙形成沉淀去除。当溶液pH过低时,钢渣产生的Ca2+、Fe3+等离子因溶解度较大,较难附着在钢渣表面,不利于磷酸盐的吸附,而当溶液pH 为碱性条件时,OH-浓度增加,可能与竞争吸附位点,且金属氧化物溶解也减慢,限制了沉淀过程,故钢渣除磷过程受pH 影响较明显。
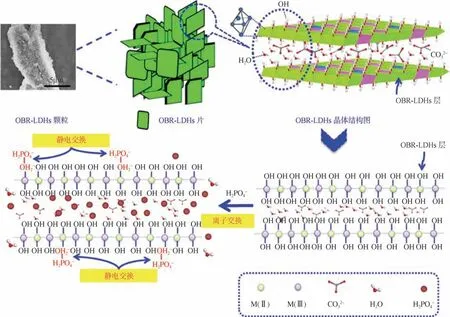
图4 LDHs吸附剂吸附磷酸盐的过程[52]
与普通钢渣相比,改性钢渣对磷酸盐的吸附能力更强,通过碱改性或高温煅烧等方式处理后,可以进一步增加比表面积,扩大适用的pH 范围。李延波等[62]采用水热法改性钢渣,显著提高了钢渣对磷酸盐的去除率,处理10mg/L 的含磷废水,吸附2h 能够将磷浓度降低至0.1mg/L,且适宜的pH范围更广,在pH=5~11 范围内,除磷效率均可达到99%。Yu 等[63]采用不同的改性方式活化钢渣,包括于800℃下加热1h 的热改性,浸入3mol/L NaOH 溶液、1mol/L NaNO3溶液和蒸馏水中24h 并于800℃加热1h的碱、盐、水改性。与未改性钢渣相比,经碱、盐、水、热改性后,钢渣的吸附容量分别提升了191%、107%、125%和118%,盐、水、热改性的吸附容量差异不明显,说明加热是决定改性效果的关键,碱改性进一步提升了磷酸盐去除率,并随着碱度的增加,磷酸盐去除率也在增加。尽管碱改性效果最佳,但会增加额外费用,且产生的废液和渗滤液对环境不利,综上考虑,认为热改性钢渣是提高磷吸附能力最合适、最经济的方法。
基于工程应用角度考虑,部分学者研究了钢渣在长期运行下的除磷稳定性并寻求更为经济的改性手段。Bowden等[64]使用碱性氧钢炉渣(BOS)去除废水中的磷,在pH=4~12 时均能保持磷吸附容量约在9mg/g,通过连续流动柱实验发现,对于进水浓度低的含磷废水(1~50mg/L),运行406天,去除率达62%,对于进水浓度高的含磷废水(100~300mg/L),运行306天,最大吸附容量达8.39mg/g。Li等[65]采用高功率球磨技术对钢渣进行改性,得到更细的粒径和更高的比表面积。通过批量实验探究其吸附性能,结果表明,对浓度为5mg/L的含磷废水吸附1h,磷去除率达96%,吸附过程主要是化学沉淀,去除效果与pH 和Ca2+浓度呈正相关。此外将改性钢渣与石英砂、水泥混合制备成水泥填料,在700h 连续流动实验中,对磷去除率为98.2%。
3.2 改性赤泥
赤泥(RM)是在氧化铝生产过程中苛性碱消化铝土矿后形成的细颗粒废渣,主要由氧化铝、氧化铁、二氧化硅、氧化钛和氢氧化物的细颗粒组成。由于在氧化铝精炼过程中会残留部分氢氧化钠溶液,因此赤泥是一种高碱性废料,pH 为10~13[66]。经众多研究学者发现,赤泥本身对磷酸盐的吸附性能较低,通过酸处理、热处理或采用海水中和,可以提高赤泥的吸附能力。如Liu 等[67]对赤泥采用热处理或酸-热处理活化。不同的活化方式导致磷酸盐的去除率不同,在700℃煅烧2h的热处理赤泥样品的磷酸盐吸附容量达19.1mg/g,80℃下0.25mol/L HCl处理2h的酸-热处理赤泥样品的磷酸盐吸附容量为26.4mg/g,经酸-热处理的赤泥对磷酸盐的去除效果更为显著。Huang 等[68]采用酸(HCl 和HNO3)处理和酸-热处理来改性赤泥,探究赤泥对磷酸盐的吸附性能。实验结果发现,相较于原赤泥样品,所有活化后的赤泥样品都显示出更高的磷酸盐吸附能力,其中HCl改性赤泥对磷酸盐吸附能力最强,在温度为40℃、pH=5.5 条件下,最大磷吸附容量为0.58mg/g,约是原赤泥(0.23mg/g)的2.5倍。
采用酸、热处理活化赤泥,均能提升赤泥的磷酸盐吸附性能,经酸处理后,中和了氢氧根离子,减少了碱性赤泥表面上的负电荷,可促进带负电荷的在溶液中的吸附。经焙烧处理后,赤泥颗粒表面形成带有-OH 官能团结构的物质,可通过配位交换反应对水体中的磷酸根产生吸附作用,但应控制活化过程中的酸浓度和焙烧温度。适当浓度的酸活化赤泥能够增强赤泥中金属氧化物表面的正电荷,有利于磷酸盐在活性赤泥表面的吸附,同时酸性条件下,钙和其他酸溶性盐部分溶解,在酸化过程中会出现粗大的外部孔隙和新的孔隙,可见用适当浓度的HCl 处理可以改善样品的比表面积,从而增加除磷量。适当的煅烧温度会导致孔隙中的水排出,增加赤泥的比表面积,增强对磷酸盐的吸附能力,但过高煅烧温度吸附能力反而下降,可能是过高的温度导致某些羟基、方解石的分解,降低了有效吸附位点及高温导致颗粒烧结降低了与磷酸盐的接触面积。Ye 等[69]使用人工神经网络和响应面法研究了HCl 浓度、温度和活化时间对赤泥磷吸附的作用。结果表明,酸活化可显著提高赤泥的磷吸附性能,HCl浓度对活化赤泥吸附磷的影响显著。
酸和热处理已被证明能有效提高赤泥对磷酸盐的吸附能力,但是这种改性方法较昂贵、耗能高,海水或石膏处理赤泥提供了相对便宜的替代处理方法,不仅增强了磷酸盐吸附性能,也助于改善物理化学性质。石膏或海水处理赤泥可显著提升磷吸附性能力的主要原因是海水和石膏处理后,Ca2+和Mg2+浓度提高,大部分以磷酸镁[Mg3(PO4)2]和磷酸钙[Ca3(PO4)2] 的形式从溶液中除去。Cusack等[70]采用石膏和海水处理赤泥,考察改性赤泥对磷酸盐的吸附性能。研究表明,经石膏和海水处理后,赤泥的比表面积和孔隙率均增加,有助于提升对磷的吸附性能,主要机理是石膏和海水在吸附过程中产生的沉淀作用及Ca 作为絮凝剂的絮凝作用。吸附符合Langmuir 模型,计算最大吸附容量为0.345~2.73mg/g。
赤泥本身是细碎的,若要将赤泥应用于废水柱处理需要对其进行造粒,但由于赤泥的黏结性不足以使其粒化,因此一些研究人员使用添加剂来制备粒状赤泥,通常造粒方法是通过将赤泥与淀粉和膨润土以不同的比例混合经焙烧制得,这些操作条件将决定生产的粒状材料对磷酸盐的吸附能力。王春丽等[71]采用原料赤泥和一些辅助材料粉煤灰、膨润土、碳酸氢钠等按不同配比混合制成赤泥吸附剂,探究不同配比对除磷效果的影响。研究表明,影响磷的吸附性能的主要因素是赤泥的比例,当赤泥(焙烧活化后)、粉煤灰、碳酸氢钠、膨润土的质量比为16∶2∶1∶3 时制备的吸附剂除磷效果最佳,在pH=8 条件下,吸附8h 后对浓度为6.0mg/L 的含磷废水去除率为83.7%。经检测分析,赤泥活化后,其表面形成官能团-OH,与磷酸根进行配位交换去除磷。张婧等[72]在此基础上通过改变碳酸氢钠比例进一步优化改性赤泥吸附剂,研究表明,采用赤泥、粉煤灰、碳酸氢钠、膨润土的质量比为16∶2∶3∶2时吸附效果更好,吸附容量增加17%,吸附平衡时间缩短33%。
3.3 改性污泥
净水厂除浊过程中产生的含铁、铝污泥是净水厂的废物,但对磷却有很好的吸附能力,用净水厂污泥处理含磷废水,可实现以废治废,提高环保效益和经济效益。对于水厂的铁、铝污泥,除磷机制主要是配位交换和化学沉淀,在较低pH 下有利于吸附的进行,此条件下污泥表面羟基被质子化,产生静电引力,有利于和的去除。
李一兵等[73]对给水厂排出的废弃铝污泥进行风干、研磨、过筛处理后,用于废水除磷。粒径为0.15~0.3mm 的污泥颗粒除磷效果最好,在投加量为15g/L时,处理10mg/L的含磷废水,吸附100min接近饱和,去除率达90.93%。在pH=2~10时均能发挥良好的吸附性能,过高的pH(高于污泥零电荷点)下,污泥表面带负电荷,静电斥力作用下不利于磷酸盐的吸附。一些研究通过加入不同的添加剂制备颗粒污泥,增强其使用范围。邢孟等[74]将铝污泥、膨润土和碳酸钙按不同配比混合,再进行焙烧处理制备热改性颗粒污泥,吸附废水中的磷酸盐。改性污泥对磷酸盐的去除率较原污泥高1.2%~3.2%,最佳去除条件下,磷酸盐的最大吸附容量为0.69mg/g,吸附效果良好,且制备出可工程应用的颗粒态污泥,解决了堵塞等问题。朱宏伟等[75]以铝污泥、粉煤灰、硅酸钠为原料烧制颗粒污泥,烧制后的颗粒污泥具有较强的机械强度和抗冲刷能力,持续振荡24h 后,平均磨损率仅有1.49%。颗粒污泥中Fe3+、Ca2+、Al3+等金属含量也增多,利于沉淀效应去除磷酸盐,最高去除率可达94.92%。动态吸附实验中,水力停留时间6h,出水磷酸盐浓度仅为0.1mg/L。铝污泥对磷酸盐有一定的吸附效果,但需要投加大量的铝污泥才能实现可观的吸附容量。利用铁等金属对铝污泥进行改性,可以改善这一问题。王信等[76]以铁盐改性铝污泥,由Langmuir 方程计算最大吸附容量可达24.6mg/g。杨杭炽[77]以氯化铁和硫酸锆组合改性污泥,最佳铁、锆比为3∶7,吸附200min 后,磷酸盐吸附容量达46.76mg/g。
相较于铝污泥,铁污泥同样具有良好的絮凝效果,且铁盐的残留不会对健康造成危害。Song等[78]将水厂铁污泥经加热、研磨、筛分和煅烧处理后用于吸附水中磷酸盐。通过序批式吸附柱实验表明,吸附过程符合Thomas 模型,对30mg/L 的磷酸盐吸附容量可达30mg/g。吸附过程主要是磷酸盐阴离子与羟基离子的交换反应,低pH 更利于反应进行,在pH=5.5 时,达到最大吸附容量。铁污泥对磷酸盐的优异结合效率,为水厂废弃物及工程湿地底物的处置提供了良好的潜在解决途径。此外,Yang 等[79]研究经酸性混凝剂回收后的净水厂污泥(DWSR)对水中磷酸盐的吸附性能,批量实验表明,DWSR 对磷酸盐有优异的吸附能力,对磷的去除率接近100%,且DWSR 对高浓度含磷废水去除效果远高于原水厂污泥(DWS),对含磷浓度为400mg/L 的废水,DWSR 的磷去除能力是DWS 的近5 倍,但对于低浓度含磷废水,DWS 处理效果更好。金属浸出实验结果表明,DWSR中可溶性Al/Fe 不产生任何安全风险,但DWSR吸附具有较强的pH 依赖性,最适pH 范围较窄,为4~6。
4 聚合物类吸附剂
聚合物是具有多种用途的大分子,例如用作除磷树脂。它们由烃或其他有机单体的长链和网络组成,并可根据目标污染物是阳离子还是阴离子而官能化以与带负电荷或正电荷的基团进行离子交换。对于阴离子污染物,理想的官能团有、、和 S+。阴离子交换剂的聚合物基质通常由交联的苯乙烯组成,也可以由苯乙烯-二乙烯基苯、聚乙烯醇/藻酸钠或脂族交联聚合物,或通过改性天然材料制成。通过不同种聚合物的组合,可以增强材料的机械强度,促进亲水性和孔隙率等。Luo 等[80]合成了一种新的藻酸盐衍生珠,在藻酸盐-Zr4+互穿网络(PNIPAM/SA-Zr)结构中渗透N-异丙基丙烯酰胺,以聚乙二醇(PEG)为成孔剂,合成PEG 修饰的PNIPAM/SA-Zr 珠用作新型生物吸附剂,具有互穿网络结构的大孔结构、热敏性,且机械强度和稳定性均优于天然生物材料藻酸盐。实验结果表明,当PEG 与单体(海藻酸钠和N-异丙基丙烯酰胺)的摩尔比为1∶2、pH 为2 时达到最佳吸附容量,为36.06mg/g,负载珠吸附磷后在热刺激下表现出更快的解吸速率,在5 个连续循环内保持良好的解吸效率和可重复使用性,吸附过程主要通过路易斯酸-碱相互作用的静电吸引、配位交换和内球络合将磷吸附到衍生珠上。吸附柱实验表明,吸附在珠子上的磷酸盐总量随着流速的增加而降低,故在固定床塔中除磷需要较慢的流速和较长的接触时间。
但是,阴离子交换树脂存在的问题是有其他阴离子共存时对磷酸盐的选择性低。当聚合物基质为疏水性时,该树脂对硝酸盐或硫酸盐具有更高的亲和力,对于亲水性树脂,尽管与氯化物或硝酸盐的竞争得到了改善,但在硫酸盐存在的情况下,由于较高的化合价而影响了选择性,磷酸盐吸收受到显著抑制。水中硫酸盐是阻碍阴离子交换剂成功吸附磷酸盐的重要影响因素,通过在聚合物基质中掺入纳米颗粒(即水合金属氧化物)可以有效改善阴离子交换剂对磷酸盐的选择性。因为金属氧化物通过配体交换和内球络合物的形成与磷酸盐发生相互作用,而其他阴离子如氯离子、硝酸根或硫酸根只能形成外球络合物。此外,复合吸附剂有利于提升工程纳米粒子在吸附中的应用潜力,因为粉末状纳米粒子存在水力性能差、耐磨性差、分离困难等问题。
Zhou 等[81]合成了具有互穿网络(IPN)结构的新型聚乙烯醇/海藻酸钠/氢氧化镧(PVA-SALH)水凝胶珠,用于处理废水中的磷。结果表明,在酸性条件下(pH=4)吸附效果最好,最大磷吸附容量为7.89mg/g,吸附过程主要受化学吸附控制,当有其他共存阴离子存在时,吸附剂表现出对磷的选择性吸附。在5 次吸附-解吸运行后,吸附剂对磷的吸附能力保持在第1 次运行的75%以上,柱测试实验显示,吸附穿透时间约为90min。Lin 等[82]以壳聚糖和氯化镧为原料通过共沉淀、乙醇脱水制备出醇凝胶珠,再通过超临界二氧化碳干燥技术制备出复合气凝胶珠,用于吸附废水中的磷酸盐。实验结果表明,当壳聚糖与氯化镧的质量比为2∶1 时制备的复合气凝胶珠比表面积最大,达172.74m2/g,平衡时磷吸附容量达148.33mg/g,吸附过程为化学吸附,是一种具有较大磷吸附潜力的合成吸附剂。张小娜等[83]制备羟甲基魔芋葡甘聚糖,然后负载金属镧得到载镧羟甲基魔芋葡甘聚糖凝胶微球吸附剂(CMKGM-La),用于废水除磷。实验结果表明,当pH 为4 时,CMKGM-La 吸附处理10mg/L 的含磷废水,去除率可达95.45%。吸附过程主要是硬酸离子La3+与磷发生配位反应,同时La 还是稀土金属,对阴离子有静电引力,进而使磷酸盐吸附在CMKGM-La 上。Yuan 等[84]研究负载在分子筛上的氢氧化铈(CHMS)对磷酸盐的吸附。结果表明,CHMS 的最佳负载量是0.4%,CHMS 在较宽的pH 范围内(4~11)内具有实用的吸附效率,吸附过程主要是化学吸附和多层吸附,吸附过程几乎不受共存离子的干扰,并且在吸附过程后检测不到残留的铈离子。故而,CHMS 是一种适用于去除磷酸盐的吸附剂,且不会对环境产生不利影响。Ding 等[85]为了减少连续操作期间硅酸钙水合物(CSH)粉末的损失,采用质量比为1∶10的CSH 与8%的聚乙烯醇(PVA)溶液制备新型固定化材料PVA-CSH,来去除废水中的磷。实验结果表明,PVA-CSH 具有多孔网格结构,CSH粉末和固定化PVA-CSH 的平衡吸附容量分别为22.95mg/gCSH 和22.85mg/gCSH,PVA-CSH 中CSH的量与CSH 粉末一致,证实PVA-CSH 的除磷性能不受PVA 固定的影响。为了评价PVA-CSH 的实用性,连续流动装置处理205L 废水,运行7 天,PVA-CSH 的出水浊度在整个运行期间为(0.11±0.03)NTU,从第4 天到第7 天,PVA-CSH的除磷能力优于CSH。
聚合物类吸附剂多以负载稀土金属为主,其作用机理因pH 不同而不同,酸性条件下,金属与磷酸盐离子发生配位反应,且稀土金属对阴离子有较强的静电吸附能力,同时,在酸性条件下基底材料上羟基质子化,使羟基带正电,增加了磷的吸附位点,质子化的羟基与磷通过静电吸引方式结合在吸附剂上得以去除,作用机理可用图5(a)表示;碱性条件下,稀土金属活性位点和磷酸氧阴离子之间存在路易斯酸性反应,从而使磷结合在吸附剂上,作用机理可用图5(b)表示。
不同种类吸附材料在不同的实验条件下对水中磷的吸附性能存在差别,除磷吸附剂的吸附特性汇总如表1。由表可知,吸附剂的吸附特性受改性方法、操作条件和含磷溶液pH 的影响,一般在酸性条件下吸附效果较好,最大吸附容量因操作条件不同而存在较大差异。
5 结语
吸附法具有环境友好、高效低耗等特点,在废水处理中有明显的优越性,也是去除低浓度含磷废水的最有效方法之一。吸附除磷的工程应用中,应结合不同吸附剂的特点,根据废水水质和水厂工艺条件,选择不同类型的除磷吸附剂:①改性硅酸盐类吸附剂来源广、价格低,是吸附除磷的潜在优良材料,但由于吸附能力的限制,其处理对象主要是污水厂未达标的二沉池出水和含磷浓度较低的湖水;②改性金属及其氧化物类吸附材料,对磷的吸附容量高,吸附速度很快,选取合适的金属以一定的比例复配,可以增强对磷酸盐的吸附能力,铁氧化物类吸附剂在吸附后可以采用磁分离,适用于固液密度差较小的废水混合物除磷;③改性固体废弃物类吸附材料的应用可以缓解固体废弃物的环境污染问题,实现废物资源化,将固体废弃物材料应用于当地的污水处理中,还可以降低运输成本;④聚合物类吸附材料在磷的吸附容量和选择性方面具有优越性,聚合物还可以充当具有高磷酸盐吸附力的纳米材料的载体,可提升纳米粒子吸附磷酸盐的工程应用能力。
为了进一步缓解磷资源短缺问题,应在吸附除磷的同时尽量做到解吸回收磷,为此,吸附材料的研究工作还可以从以下几方面开展:①广泛研究低成本的磷酸盐吸附材料,如生物质材料等;②进一步探究吸附剂对磷酸盐的选择性,特别是基于碳酸盐矿物、活性炭和生物炭的吸附剂,目前对此类吸附剂少有评估;③通过使用酸、碱和盐来解吸被吸附的磷酸盐,并添加CaCl2或Ca(OH)2后可作为磷肥农用,但需进一步验证吸附剂中某些物质浸出的潜在危害性。
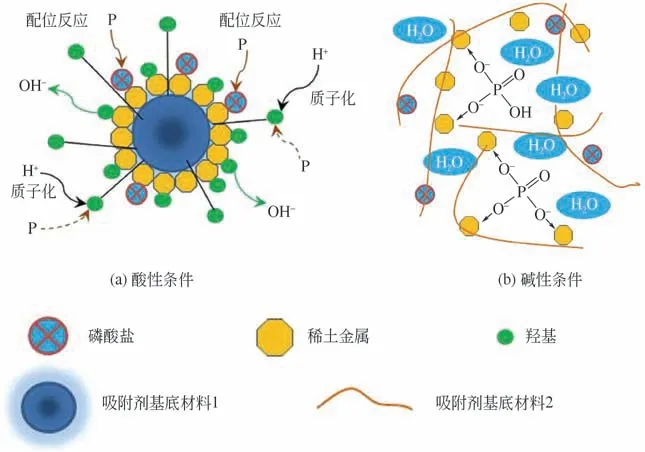
图5 聚合物类吸附剂的磷吸附机理
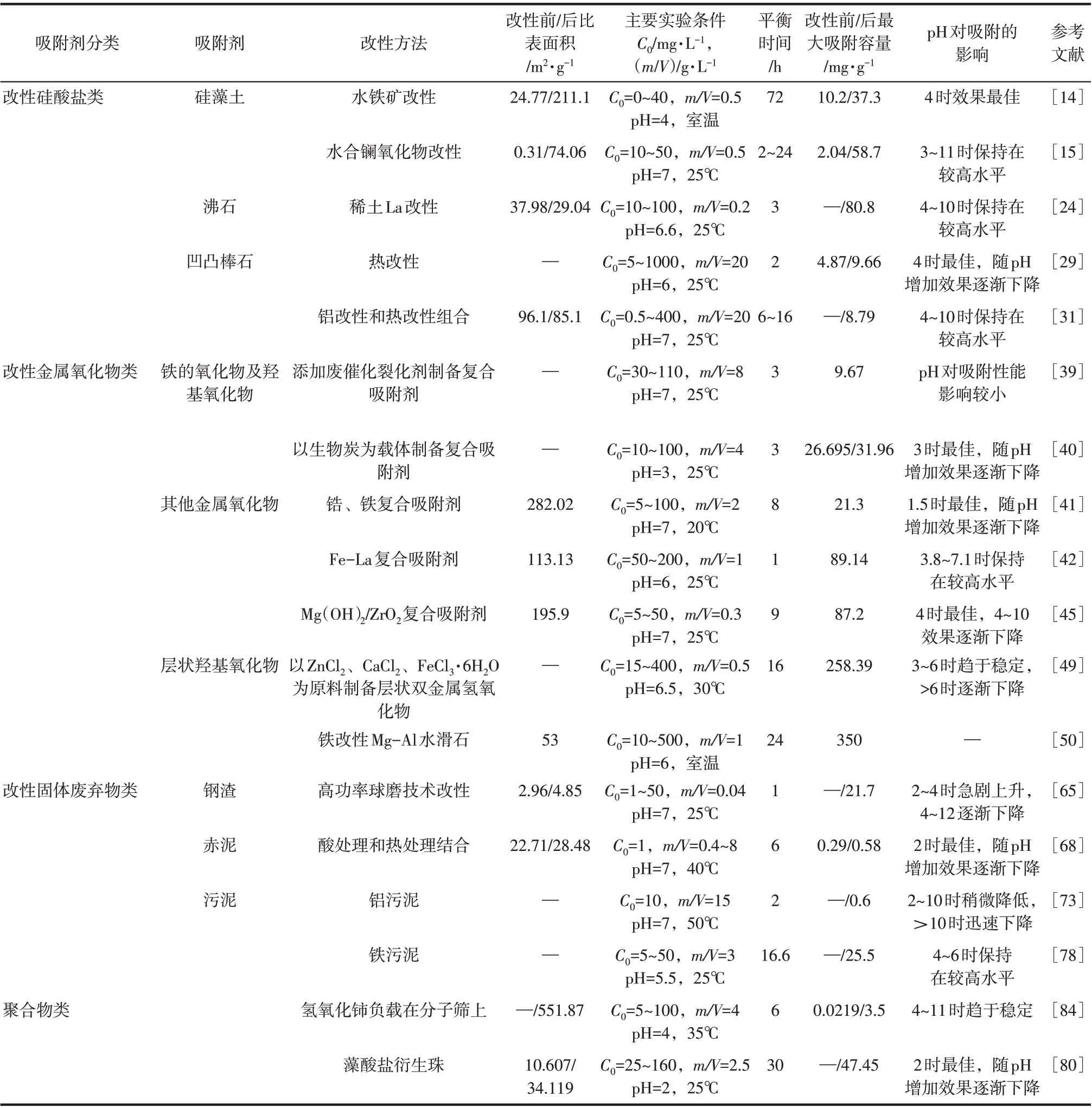
表1 不同类型吸附剂对磷的吸附特性

