一例非典型Ⅱ型牙本质发育不全患者的临床表型及患牙超微结构分析
李 强,黄 昕,李晓聪,田 晴,陈 栋
1)郑州大学第一附属医院口腔美容科 郑州 450052 2)郑州大学医学科学院 郑州 450052 3)郑州市牙博仕口腔门诊部 郑州 450000 4)濮阳市人民医院口腔科 河南濮阳 457099
Ⅱ型牙本质发育不全(dentinogenisis imperfecta type Ⅱ,DGI-Ⅱ)亦称遗传性乳光牙本质,是较为常见的牙本质发育异常类疾病,呈常染色体显性遗传,发病率为1/8 000~1/6 000,男女患病率均等,乳恒牙均可受累[1-2]。此类患者牙齿常呈琥珀色或蓝灰色,明显半透明改变[3];釉质易剥脱,继而暴露的牙本质易磨损,牙冠变短,严重者接近牙槽嵴顶[4-5];X射线片显示球形牙冠,颈部紧缩,根短呈圆锥形,髓腔及根管变窄或完全消失[6];部分患者还可伴高频神经性听力丧失,但不伴有成骨不全症状[7]。本文报道1例非典型DGI-Ⅱ患者,经家系基因检测发现其与先证者存在相同的突变,并进行相关临床调查,探讨该患者临床表型与患牙超微结构的关系,现报道如下。
1 临床资料
1.1一般情况患者,男,28岁,无临床主诉,因其7岁女儿全口牙齿严重磨耗影响功能就诊于郑州大学第一附属医院口腔美容科。其女(先证者)牙齿呈蓝灰色半透明,全口牙齿釉质剥脱,磨耗平齐龈缘,影像学显示牙齿呈球形牙冠,颈部缩窄,髓腔及根管闭锁;临床诊断为DGI-Ⅱ(图1A~F)。知情同意后患者作为正常家系成员进行常规口腔检查并采集静脉外周血。患者既往体健,无骨折史、传染性疾病史或其他严重系统性疾病史,否认家族类似遗传疾病。
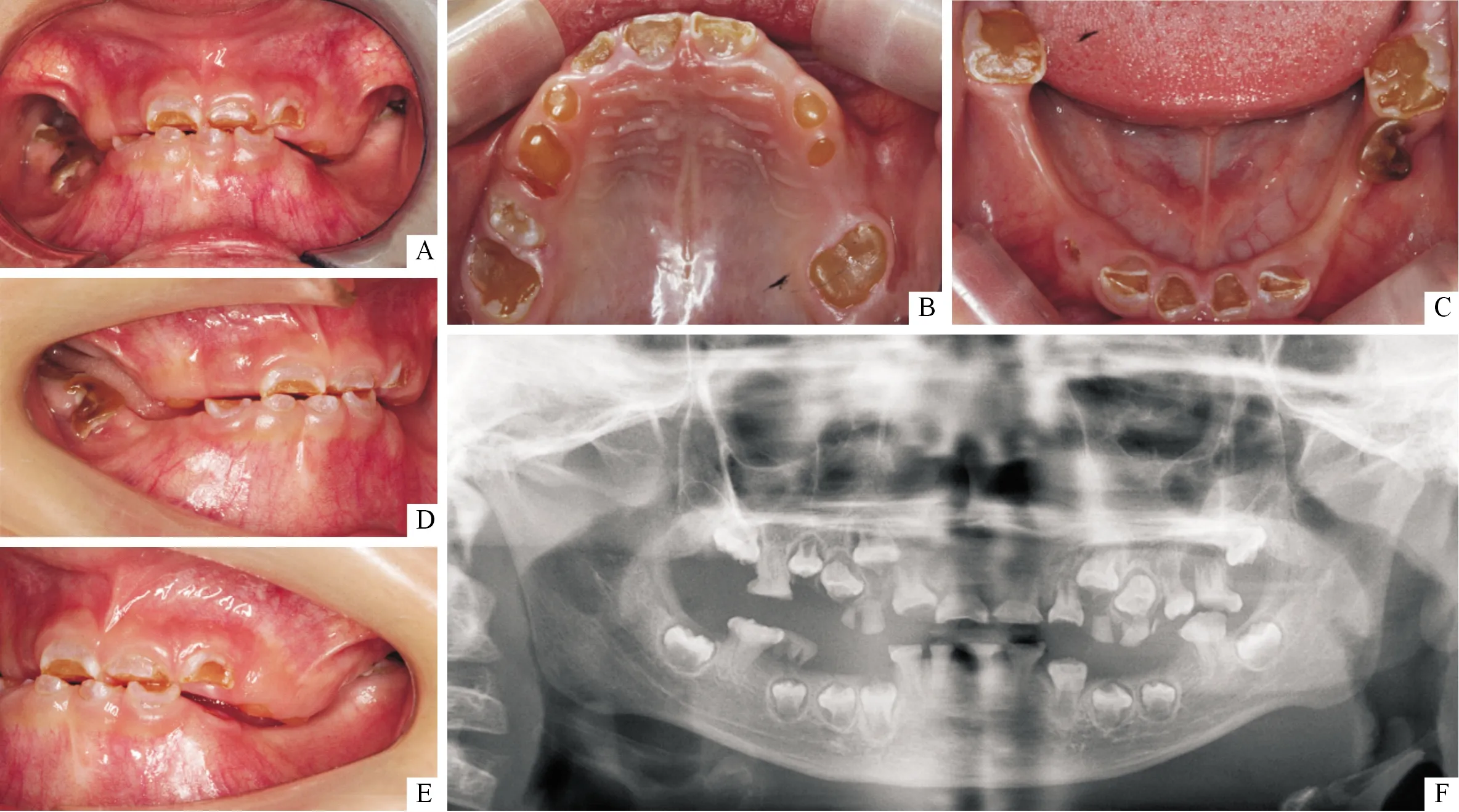
A:正面牙合像;B:上颌牙合面像;C:下颌牙合面像;D:右侧牙合像;E:左侧牙合像;F:全口曲面体层X射线片
1.2临床检查患者身高、体型发育正常,全身营养状况良好,皮肤光滑有弹性,未查及蓝色巩膜,听力无异常。颌面部左右对称,面形协调。全口牙齿颜色未见明显异常,中切牙轻度磨耗,部分牙齿唇面和牙合面的釉质轻微剥脱,31-32牙冠融合,26-27烤瓷冠修复,38水平近中阻生,X射线检查清晰可见髓腔及根管影像(图2A~F)。
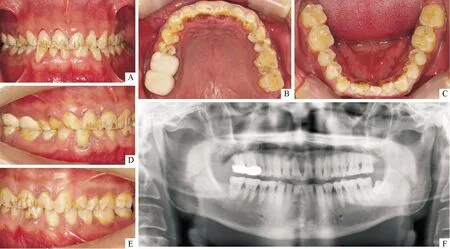
A:正面牙合像;B:上颌牙合面像;C:下颌牙合面像;D:右侧牙合像;E:左侧牙合像;F:全口曲面体层X射线片
1.3基因检测抽提患者和先证者外周静脉血送英潍捷基(上海)贸易有限公司进行DNA测序,发现先证者及患者的牙本质涎磷蛋白(dentin sialophosphoprotein,DSPP)基因第2号外显子均存在c.50C>T(p.P17L)杂合错义突变[8],该突变位于蛋白的高度保守区,且为有害突变(可导致蛋白三级结构发生改变),最终确诊为与DSPP基因突变相关的DGI-Ⅱ家系。
1.4患牙组织学观察拔除患者38阻生磨牙,未见典型的乳光牙临床表型,拔出后立即放入体积分数2.5%戊二醛溶液中固定、备用。正常对照牙为郑州大学河南省口腔医院牙槽外科门诊拔除的同龄男性且处于同一发育阶段的阻生磨牙(样本牙冠形态正常完好、无龋坏、无裂纹)。研究对象均已签署知情同意书,研究方案已通过郑州大学第一附属医院伦理委员会审查。
1.4.1 扫描电镜(scanning electron microscope, SEM)分析 见图3、4。与正常对照牙相比,患牙釉质内可见裂隙,釉柱排列不规则,且釉牙本质界呈弧度微小的波浪状(未见典型的连续扇贝状结构);其牙本质小管分布不均匀,部分区域小管相对密集,其余部位排列稀疏。另可见牙本质小管闭塞及管间牙本质增厚,致管径大小不一且形状不规则。

A、B:正常对照牙釉柱排列规则,釉牙本质界呈扇贝状;C、D:患牙釉柱走向紊乱,釉质内见裂隙(箭头示),釉牙本质界较平直

A、B:低倍镜下(×500)牙本质小管分布极度不均匀,部分区域排列密集,部分区域排列稀疏;C、D:高倍镜下(×1 000)见牙本质小管排列不一,部分小管闭塞,管间牙本质增厚致管径变小
1.4.2 能谱分析 将患牙和正常对照牙标本通过与SEM联机的色散能分光计进行成分分析。选择2个牙齿的牙釉质、牙本质各10个区域进行C、N、O、Ca、P等元素分析,结果详见表1~2。发现患牙的牙釉质Ca含量降低,Ca/P值下降;牙本质中N、O比重下降而Ca、P比重升高,但Ca/P值较正常组差异无统计学意义。

表1 正常对照牙与患牙牙釉质的元素质量百分比比较(n=10) %
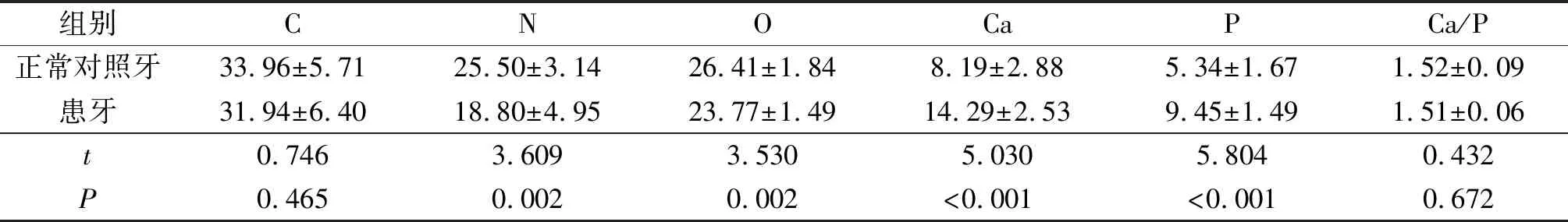
表2 正常对照牙与患牙牙本质的元素质量百分比比较(n=10) %
1.4.3 显微硬度分析 将正常对照牙和患牙标本置于HV-1000Z型显微硬度计测试台,选择牙釉质、牙本质各10个点,以负荷1.961 N、10 s的压力作用于牙齿表面,记录各点的维氏硬度值(Vickers hardness,HV),发现患牙釉质硬度降低(表3);牙釉质菱形压痕面积小于牙本质;而两组牙齿表面压痕面积相差较小(图5)。

A:正常对照牙釉质压痕;B:患牙牙釉质压痕;C:正常对照牙本质压痕;D:患牙牙本质压痕
2 讨论
DGI-Ⅱ作为一种常染色体显性遗传病,不但极大影响患者的咀嚼功能,同时也对其容貌、社交及心理健康造成影响。现已有多位学者[7, 9-14]研究证实其致病基因为DSPP,位于4q21,基因全长8 343 bp,共有5个外显子和4个内含子。DSPP蛋白的酶切产物为牙本质涎蛋白(dentin sialoprotein,DSP)和牙本质磷蛋白(dentin phosphoprotein,DPP)[15],目前已报道[16]的突变位点达40个,其中位于DSP区域的17个位点大多为无义或错义突变,位于DPP区域的23个位点为移码突变。但是也有学者[3]未能在DSPP基因上检测到致病突变,这提示该类疾病的致病机制仍需进一步研究。
众多学者[17-20]报道了DGI-Ⅱ的牙本质结构异常,即牙本质小管分布不均匀、管径大小不一且排列紊乱,认为患牙易发釉质剥脱、重度磨耗是位于釉质内层的异常牙本质(釉牙本质界缺乏连续的扇贝状结构)所致。本文观察到非典型临床表型患牙不仅牙本质结构改变,同时见釉质裂纹并伴釉柱走向不规则,釉牙本质界缺乏扇贝形嵌合且邻近的牙本质内小管稀疏,这与Wieczorek等[21-22]的描述一致,表明DGI-Ⅱ患者的牙釉质、牙本质及釉牙本质界的正常发育均受影响,牙齿釉质剥脱不耐磨可能受多因素影响。能谱分析及硬度测试结果显示:患牙釉质内Ca含量下降,Ca/P值降低,硬度下降为正常牙齿的0.625倍,进一步证实牙釉质发育异常,存在矿化不良;牙本质中Ca、P含量增加而Ca/P值差异无统计学意义,硬度测试结果差异也无统计学意义。席戈等[23]利用X射线能量色谱仪和纳米压痕仪研究发现,乳光牙的牙本质Ca含量升高,与本文结果类似;而牙齿Ca/P值增高,显微硬度降低,与本文结果不一致,推测可能与实验检测方法及患者疾病程度的差异有关,需要进一步的研究。
由于我国人口基数庞大,在临床接诊中时常会遇到此类患者。这些患者或呈牙釉质广泛剥脱、牙齿严重磨损、髓腔及根管闭锁等典型的临床表型,或仅为牙齿轻度磨耗等其他的非典型表现。因此仅将牙齿的临床表现及影像特点作为此类疾病的诊断依据[24]容易带来家系患者的漏诊,不利于发现基因突变的全部罹患患者。段小红[25]详细介绍了此类疾病的研究策略:正确诊断,明确候选基因,确定基因变异位置。因此,患者初诊时明确诊断至关重要。本文对一例未经临床表型确诊的漏诊DGI-Ⅱ患者,经基因检测确认后再对患牙进行组织学观察,发现其发生典型病理改变:牙本质小管分布不均匀、管径大小不一且排列不规则。
DGI-Ⅱ具有牙釉质广泛剥脱、牙齿严重磨损、髓腔及根管闭锁等特点。不仅影响咀嚼功能和美观,磨损严重时还可继发根尖周炎,但因根管系统的异常,根管治疗极为困难,因此预防牙齿磨耗显得尤为重要。目前在临床中该类疾病暂无特殊有效治疗方法,皆为综合的对症治疗,以期最大程度和最长时间的保留牙齿。由于该疾病乳恒牙均可受累,故乳牙罹患时,应早期做好恒牙预防措施,以免造成新萌恒牙的严重磨耗,做到预防重于治疗。

