艾拉莫德与羟氯喹联合用于干燥综合征治疗的效果分析
贾旭强
(定西市人民医院,甘肃 定西 743000)
干燥综合征的发生、进展过程,受多种因素影响,共同参与、综合作用,其主要特征体现在外分泌腺淋巴细胞浸润,可见免疫功能异常改变、自身抗体产生数量骤增等[1]。流行病学调查显示:国内人群患病率约0.77%,好发年龄段40~50岁,将其归为结缔组织病,其患病率仅次于类风湿关节炎[2]。羟氯喹是常用药物,使用率高,通过调节IgG水平、乙酰胆碱酯酶活性等作用途径,消除症状,促进腺体分泌。行单药治疗,则效果不佳[3]。艾拉莫德为抗风湿药,其作用路径主要是经由B淋巴细胞实现,兼能阻碍免疫球蛋白合成、炎症因子产生[4]。基于此,本研究联合艾拉莫德与羟氯喹,将其用于治疗干燥综合征,现报告如下。
1 临床资料与方法
1.1 临床资料
研究对象为2017年9月~2019年9月期间于定西市人民医院风湿免疫科就诊的干燥综合征患者86例,依据随机数字表法将其分成2组,对照组43例,男6例,女37例,年龄32~69岁,平均年龄(50.47±9.11)岁,病程6个月~7年,平均病程(4.51±1.46)年;研究组 43例,男6例,女37例,年龄32~69岁,平均年龄(50.47±9.11)岁,病程6个月~7年,平均病程(4.51±1.46)年。2组上述资料比较,差异无统计学意义(P>0.05)。
1.2 纳入与排除标准
纳入标准:①均确诊为干燥综合征[5];②既往未曾行头颈部放射治疗;③患者知情本次研究且已签署同意书。
排除标准:①合并免疫系统疾患,如红斑狼疮等;②过敏体质,或对本研究涉及药物存在过敏情况;③患有严重脏器与系统疾患。
1.3 治疗方法
对照组服用甲泼尼龙片(生产厂家:天津天药药业股份有限公司,批准文号:国药准字H20020224,规格:4mg)+羟氯喹(生产厂家:上海上药中西制药有限公司,批准文号:国药准字H19990263,规格:0.1g),具体方案:①甲泼尼龙片,晨服,8mg/次,1 次/d;②羟氯喹,早、晚各 1 次,0.2g/次,2 次/d。
研究组服用甲泼尼龙片+羟氯喹+艾拉莫德(生产厂家:先声药业有限公司,批准文号:国药准字H20110084,规格:25mg),具体方案:①甲泼尼龙片,同对照组一致;②羟氯喹,同对照组一致;③艾拉莫德,25mg/次,2 次/d。
2组用药周期:12周。
1.4 观察指标
1)对比血清学指标。选取血清学指标共四项,即①免疫球蛋白 G(Immunoglobulin G,IgG),测定方法:速率散射比浊法;②红细胞沉降率(Erythrocyte Sedimentation Rate,ESR),测定方法: 魏氏法;③血小板(Blood Platelet,PLT),测定方法:全自动血液分析仪(型号:BC-6800,厂家:深圳迈瑞);④类风湿因子(Rheumatoid Factor,RF),测定方法:免疫比浊法。
2)对比干燥综合征自我感受(EULAR Sjogren's Syndrome PatientReported Index,ESSPRI)、干燥综合征疾病活动度 (EULAR Sjogren's Syndrome PatientReported Index,ESSDAI)评分。ESSPRI用于评价症状(共3项,即:肢体疼痛、疲乏、干燥)的主观感受情况,ESSPRI评分范围0~10分,ESSPRI评分越接近10分,则症状越严重。ESSDAI用于评估机体脏器与系统功能病变状况,以判断疾病进展情况,轻度:0分≤ESSDAI评分<5分;中度:5分≤ESSDAI评分<14分;重度:ESSDAI评分≥14分。
3)对比不良反应发生率。两组是否出现下述不良反应,即:胃肠道反应、皮疹、瘙痒、肝功能异常、白细胞降低,计算各组总发生率。
1.5 统计学处理
数据分析用SPSS22.0,血清学指标、ESSPRI评分、ESSDAI评分用均数±标准差表示,比较用t检验;不良反应发生率用百分数表示,行χ2检验,检验水准α=0.05,P<0.05差异有统计学意义。
2 结果
2.1 对比血清学指标
对比治疗前两组血清IgG、ESR、PLT、RF水平,差异无统计学意义(P>0.05),治疗后两组血清IgG、ESR、RF 水平均低于治疗前(P<0.05),血清 PLT 水平均高于治疗前 (P<0.05),且治疗后研究组血清IgG、ESR、RF 水平均低于对照组(P<0.05),血清 PLT水平高于对照组(P<0.05)。见表 1。
表1 对比血清学指标 (±s)
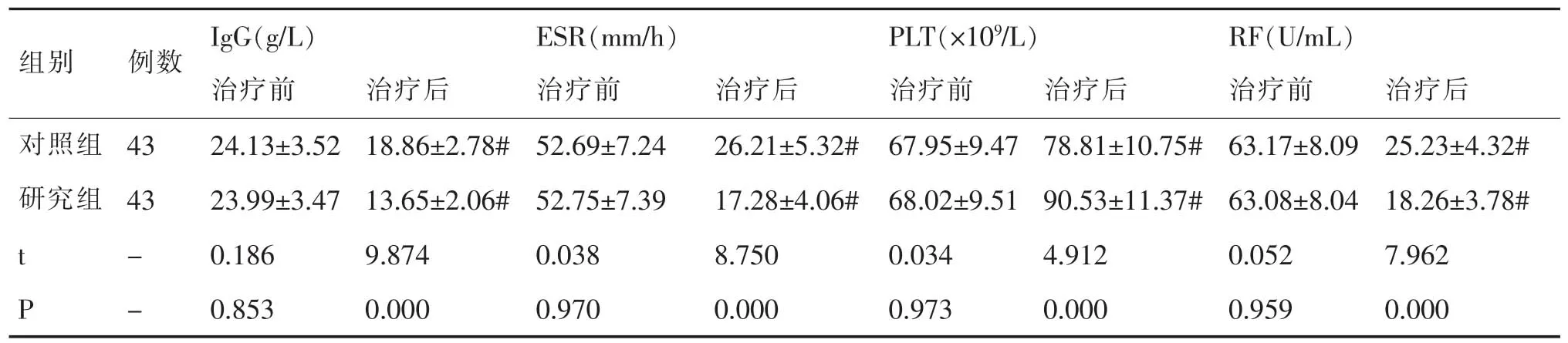
表1 对比血清学指标 (±s)
注:与同组治疗前对比,#P<0.05
组别 例数 IgG(g/L) ESR(mm/h) PLT(×109/L) RF(U/mL)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组 43 24.13±3.52 18.86±2.78# 52.69±7.24 26.21±5.32# 67.95±9.47 78.81±10.75# 63.17±8.09 25.23±4.32#研究组 43 23.99±3.47 13.65±2.06# 52.75±7.39 17.28±4.06# 68.02±9.51 90.53±11.37# 63.08±8.04 18.26±3.78#t - 0.186 9.874 0.038 8.750 0.034 4.912 0.052 7.962 P - 0.853 0.000 0.970 0.000 0.973 0.000 0.959 0.000
2.2 对比 ESSPRI、ESSDAI评分
对比治疗前两组ESSPRI、ESSDAI评分,差异无统计学意义 (P>0.05),治疗后两组 ESSPRI、ESSDAI评分均低于治疗前(P<0.05),且治疗后研究组 ESSPRI、ESSDAI评分均低于对照组 (P<0.05)。见表 2。
表2 对比ESSPRI、ESSDAI评分 (±s,分)
注:与同组治疗前对比,#P<0.05
组别 例数 ESSPRI ESSDAI治疗前 治疗后 治疗前 治疗后对照组 43 6.97±1.73 4.54±1.19# 13.05±2.64 8.44±1.93#研究组 43 6.89±1.68 2.71±0.76# 12.98±2.59 6.51±1.56#t-0.218 8.499 0.124 5.100 P-0.828 0.000 0.902 0.000
2.3 对比不良反应发生率
对比两组不良反应发生率,差异无统计学意义(P>0.05)。见表 3。
3 讨论
干燥综合征发病率高,危害颇大,患病后,可累及机体多个脏器、系统,将其归为结缔组织病,其症状多样,主要为外分泌腺功能受损症状,比如眼内干涩、泪少等[6]。研究发现,在干燥综合征发生、进展过程中,自身免疫耐受异常是不可或缺的环节之一。其临床治疗需多个科室共同协作,尚缺乏特异性药物,现行治疗主要包括两类,即局部治疗、系统治疗,前者包括人工泪液、口腔浸润剂及其他,后者包括免疫制剂、糖皮质激素及其他。以上治疗,其目标均是减轻症状、控制病情[7]。
在干燥综合征临床治疗中,糖皮质激素仍为基本药物,本研究使用甲泼尼龙片,其可直接抑制免疫细胞,产生抗炎作用、免疫抑制作用,给药后短时间内即可起效,因药效持续短暂、疗效局限,故在实际治疗中多采取联合用药方案。羟氯喹是目前临床治疗干燥综合征的常用药物,使用率高,可抑制乙酰胆碱酯酶活性,可调节IgG水平,可减轻症状,关节疼、肌肉痛、干燥等有关症状均减轻[8]。行“糖皮质激素+羟氯喹”治疗,病情整体控制效果仍欠佳,易反复,在合并顽固并发症情况下,治疗效果并不明显。
艾拉莫德主要用于治疗类风湿性关节炎,其作用途径多样,包括:(1)可选择性抑制环氧化酶-2,可直接作用炎性部位,阻碍组织中前列腺素产生,且能发挥一定抑制作用,阻止缓激肽释放;(2)直接作用单核细胞分泌进程,通过产生抑制作用,减少白细胞介素-1、白细胞介素-6;(3)抑制抗原特异性T细胞增殖;(4)阻碍血清B淋巴细胞分泌进程,以有效调节IgG等水平;(5)作用破骨细胞、成骨细胞,既能对前者分化起到抑制效果,亦能对后者增生起到促进效果;(6)既可阻碍滑膜成纤维细胞增殖,亦可对细胞因子分泌产生抑制[9]。根据此药物作用路径,可见其同样适用于治疗干燥综合征。
本研究结果显示:(1)治疗后研究组血清IgG、ESR、RF水平均低于对照组,血清PLT水平高于对照组。(2)治疗后研究组ESSPRI、ESSDAI评分均低于对照组。(3)对比两组不良反应发生率,差异无统计学意义。提示,联合艾拉莫德与羟氯喹,将其用于治疗干燥综合征,通过有效调节血清学指标,可减轻病情,且安全性高。

