ZIF-8/C60复合物衍生电催化剂的制备及其水氧化性能
董沛沛,刘 倩,师丽娟,Noureen Syed,王 潇,陈俊生,冯伟航,王 海,黄剑锋,2,冯永强,2*
(1.陕西科技大学 材料科学与工程学院,陕西 西安 710021;2.陕西科技大学 陕西省无机材料绿色制备与功能化重点实验室 教育部轻化工助剂化学与技术重点实验室,陕西 西安 710021)
0 引言
随着能源危机和环境问题的日益突出,开发清洁、无污染的新型可再生能源成为当今社会被广泛关注的热点问题[1-3].氢气由于其能量密度高、环境友好的特点被认为是可再生能源的首选.从技术角度而言,氢气可通过电解水获取.电解水过程分为阳极析氧反应(OER)和阴极析氢反应(HER)两个半反应[4,5].目前,析氧反应严重依赖于成本高昂的贵金属催化剂,如IrO2、RuO2等,这极大地限制了电解水技术的大规模应用[6,7].因此,开发廉价高效的阳极析氧反应催化剂具有重要的研究价值.
沸石咪唑酯类框架结构(ZIFs)是一种典型的多孔聚合物,具有孔隙可调、比表面积大、稳定性好等特点.ZIFs材料通过碳化处理或与其他纳米材料进行复合可以获得结构多样、性能可控的多级结构,在能源存储、光电催化、生物医药等领域广泛应用[8].清华大学李亚栋课题组[9]报道了一种由ZIF-8@ZIF-67衍生化而来的氮掺杂碳纳米管包覆CoP核壳结构,碳纳米管与CoP之间的快速电荷转移有效提升了该复合材料的电化学性能,使其成为高效的电解水产氢、产氧双功能催化剂.中国科技大学杨上峰课题组利用球磨法将富勒烯C60嵌入到ZIF-8的三维孔道内,碳化后发现富勒烯碳笼有效扩大了ZIF-8衍生而来的多孔碳的孔道,这为锂离子的输运提供了有利条件,使其成为一种新型的锂离子电池负极材料[10].
本论文采用一种简单易行的共沉淀法,以氮,氮-二甲基甲酰胺(DMF)为溶剂,一步法制备了ZIF-8/C60纳米复合材料,如图1所示.研究发现,溶剂对形成复合材料具有重要影响,碳化处理后所得多孔碳材料表现出优异的电解水析氧性能,在10 mA cm-2电流密度时析氧过电位仅0.42 V,并且表现出良好的循环稳定性.

图1 ZIF-8/C60复合物结构示意图
1 实验部分
1.1 实验试剂
六水合硝酸锌Zn(NO3)2·6H2O,二甲基咪唑C4H6N2,氮,氮-二甲基甲酰胺(DMF),氢氧化钾(KOH),异丙醇(IPA),无水乙醇(C2H5OH)均为天津市天力化学试剂有限公司提供,富勒烯从厦门福纳新材料科技有限公司采购,所用试剂均为分析纯,去离子水(DI)为实验室自制.
1.2 仪器设备
扫描电镜(S-4800),日本日立公司;X射线衍射仪(RAXIS RAPIP IP),日本Rigaku公司;透射电子显微镜(FEI Tecnai G2 F20 S-TWIN),美国FEI公司;拉曼光谱(Renishaw-invia),德国Renishaw公司;电化学工作站(CHI660E),上海辰华仪器有限公司.
1.3 ZIF-8、ZIF-8/C60前驱体的制备
将100 mg富勒烯(C60)、10 mL DMF超声30 min充分溶解,配制为A液;4 mmol二甲基咪唑、1.2 mmol Zn(NO3)2·6H2O和10 mL DMF配制为B液,将B液缓慢滴入A液并在室温下混合搅拌24 h,反应完成后离心洗涤,依次用DMF、乙醇各洗三次,干燥,得到ZIF-8/C60复合物.ZIF-8的制备方法除了不加入富勒烯,其他与ZIF-8/C60类似.
1.4 ZIF-8、ZIF-8/C60碳化处理
取100 mg的ZIF-8/C60放入管式炉,以10 ℃/min的速率升温至1 000 ℃,通氮气保护,保温2 h,所得产物记为ZIF-8/C60-C.以相同的方法碳化处理ZIF-8,所得产物记为ZIF-8-C.
1.5 电化学测试
电极制备:将5 mg催化剂粉末和5 mg炭黑粉末分散在500μL IPA/DI水(v/v=4∶1)中超声至形成均匀的墨水状分散液.将2μL分散液滴在玻碳电极表面上(Φ=3 cm),待分散液晾干后在其表面滴加2μL Nafion溶液,并在空气中干燥.
线性扫描伏安(LSV)测试:根据Ecal=E-iR方程,对测试进行IR校正.扫描速率设定为5 mV·s-1,扫描电压范围是0.163~0.8 V.
塔菲尔斜率(Tafel):将LSV曲线绘制为电压和电流密度的对数关系图,以获得Tafel斜率图.通过方程η=a+blogj对Tafel斜率图的线性部分进行拟合到的Tafel斜率值b,其中η表示过电势,a表示截距[11].
循环伏安测试(CV):在无法拉第电流区域以2~12 mV·s-1的扫描速率记录循环伏安区曲线,电压区间为0.05~0.15 V.双层电容(Cdl)是通过阴阳极电流密度之差(Δj)与扫描速率的关系曲线所拟合出的.
电化学阻抗谱(EIS):开路电势为起始电势,振幅0.01 V,频率范围为0.1 Hz~100 KHz.
所有测试均采用三电极体系,饱和甘汞电极(SCE)为参比电极,石墨棒为对电极,所有电位均采用式(1)转化为可逆氢电极(RHE)表示[5]:
E=E(SCE)+0.241 5+0.059pH
(1)
2 结果与讨论
2.1 ZIF-8/C60复合物的制备及表征
本文采用一种液相共沉淀法制备ZIF-8/C60复合物.以DMF为溶剂,分别配置富勒烯溶液和ZIF-8前驱液,充分溶解后将两者混合,室温搅拌24 h,反应完毕后离心洗涤即可.图2为所得产物的形貌表征结果.从图2(a)可以看出,ZIF-8为微米级别的多面体晶粒.当与富勒烯原位复合后,晶粒尺寸变小,变成几百纳米的颗粒(图2(b)、(c)),这可能是由于富勒烯分子进入到ZIF-8的孔道内扰乱了ZIF-8晶核的长大.若以水为溶剂进行反应,则无法得到均一的复合物,说明溶剂对形成ZIF-8/C60复合物具有重要影响.从图2(d)的高分辨透射电镜照片可以看出,所得复合物结晶性较好,图中所示晶面间距d=0.48 nm对应于ZIF-8晶体(222)晶面,这与文献报道结果一致[9].

(a)ZIF-8的SEM (b)ZIF-8/C60的SEM
图3所示为所得样品的XRD图.从图3可以清晰地看到,ZIF-8与C60复合后表现出较好结晶性,图3曲线a中2θ位于10.87 °、17.73 °、20.81 °、21.70 °的衍射峰归属于C60的(111)、(022)、(113)、(222)晶面(JCPDS 96-901-1074)[12].值得注意的是,这几个衍射峰相比于曲线b中纯C60的衍射峰都出现了微小的右移,说明C60分子与ZIF-8之间存在晶格相互作用.

图3 ZIF-8/C60,C60及ZIF-8的XRD图
2.2 ZIF-8/C60-C催化剂的制备及表征
将所得ZIF-8/C60复合物在高温进行碳化处理,可以增加催化剂的孔隙度,增大比表面积,暴露更多的催化活性位点[13].图4(a)、(c)分别为ZIF-8/C60在1 000 ℃碳化后所得催化剂的SEM、TEM照片,可以看出高温煅烧后晶粒尺寸明显变小,约为50~100 nm.从图4(b)可以看出,ZIF-8/C60-C和ZIF-8-C均无明显的衍射峰,只在22 °附件出现一个大包峰,说明碳化处理后样品转变为无定形碳.图4(d)的高分辨透射图进一步证明无定型碳的形成.这是由于碳化过程在提高样品导电性的同时破坏了ZIF-8和C60原有的晶体结构.已有研究报道,非晶化区域可以提供催化活性位点,有利于催化性能的提升[14].

(a)ZIF-8/C60-C的SEM (b)ZIF-8/C60-C与ZIF-8-C的XRD
进一步,对所得催化剂进行了拉曼光谱表征.通常,拉曼光谱在1 340 cm-1和1 580 cm-1附近的振动峰分别归属于晶格缺陷(D峰)和石墨化(G峰)[15].两者的比值ID/IG可以反映出催化剂的石墨化程度.从图5可以看出,ZIF-8/C60-C和ZIF-8-C的D峰和G峰出现在1 343和1 589 cm-1,对应的ID/IG比值依次为0.990和0.998,较小的ID/IG比值说明ZIF-8/C60-C具有较高的石墨化程度,这有利于提升催化剂的导电性.
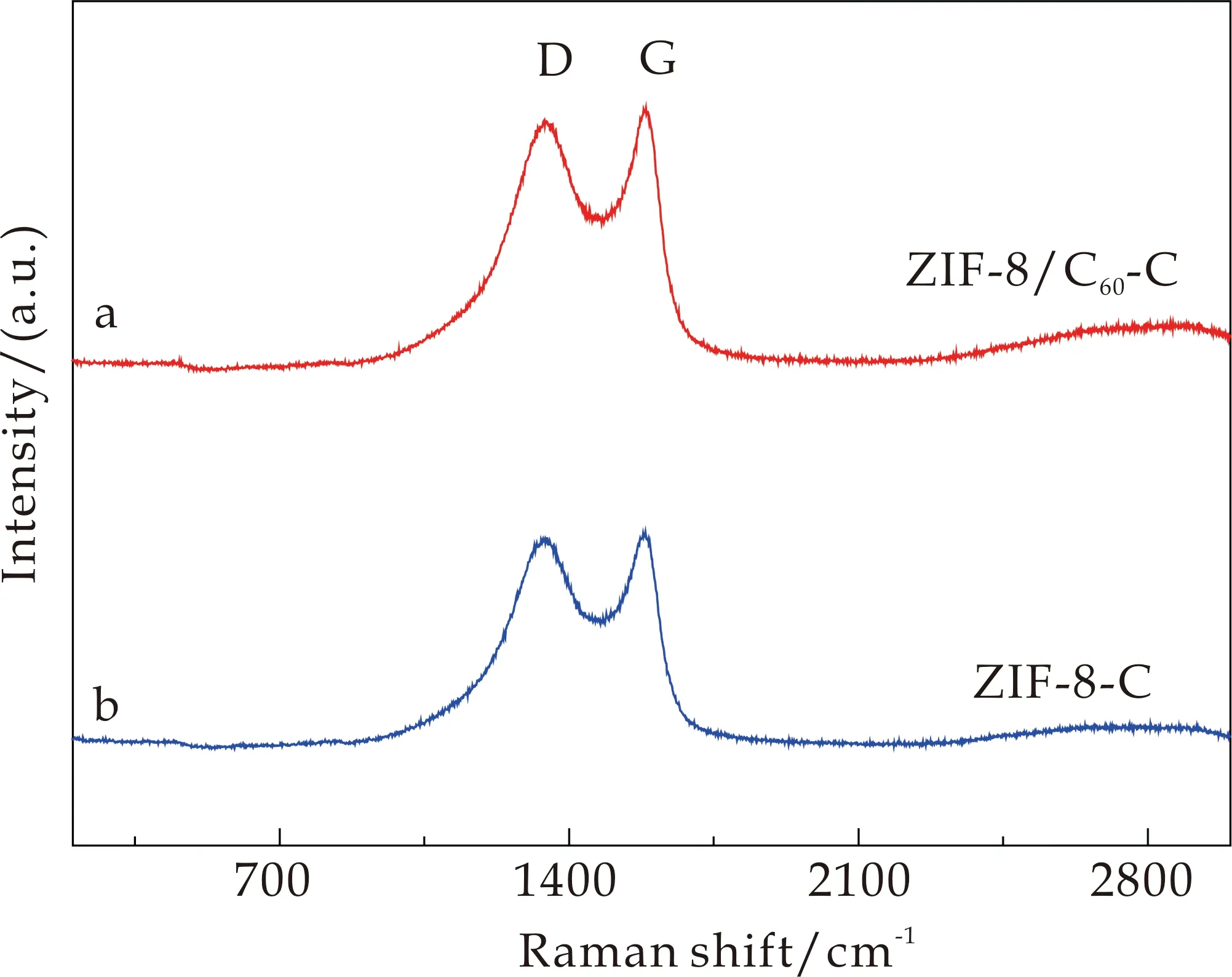
图5 ZIF-8/C60-C和ZIF-8-C的拉曼谱图
催化剂的亲水性决定了催化剂表面吸附水分子的能力,对于电极表面动力学具有重要影响.图6为ZIF-8/C60-C和ZIF-8-C的接触角测试结果.从图6可以看出,两者都有较好的亲水性,水滴可以在两者表面铺展,从铺展的速度可以看出前者只需0.720 s即可在催化剂表面铺展,而后者则需要1.968 s,这从侧面证明了ZIF-8/C60-C具有更佳的水分子吸附能力[16].

(a)ZIF-8-C (b)ZIF-8/C60-C图6 接触角测试图
2.3 OER性能测试
OER性能测试采用典型的三电极体系,以饱和甘汞电极作为参比电极,石墨棒作为对电极,电解液采用浓度为1 M的KOH水溶液,测试结果如图7所示.
图7(a)为LSV曲线.从图可以看出,对于ZIF-8-C和ZIF-8/C60,当外加电压大于1.6 V时才可观察到极小的极化电流,而ZIF-8/C60-C在1.5 V即表现出一定的极化电流.当电流密度为10 mA cm-2(商用太阳能电池所能提供的最小电流密度)[17],ZIF-8/C60-C所需过电位为0.42 V,而ZIF-8-C则需要0.61 V,说明ZIF-8/C60-C电解水析氧过程耗能更低.
同时,发现碳化温度对电极过电位亦有影响.如图7(b)所示,当温度为1 100 ℃或900 ℃时,电极表面过电位均升高,这是由于温度过高,材料的三维孔道结构被破坏;温度过低不能有效石墨化,材料的导电性降低.
对LSV曲线进行对数转化可以获得Tafel曲线,如图7(c)所示.Tafel曲线的斜率越小,表明催化剂具有越快的电极表面动力学.从图可以看出,ZIF-8/C60-C具有最小的Tafel斜率(56 mV dec-1),而ZIF-8-C和ZIF-8/C60的Tafel斜率分别为89 mV dec-1和116 mV dec-1.电化学活性面积(ECSA)是表征催化剂活性的另一个指标,它可以从循环伏安扫描曲线的电流密度与扫速进行线性拟合得到[9].
图7(d)为ZIF-8/C60-C、ZIF-8-C和ZIF-8/C60三个样品循环伏安曲线的电流密度与扫速关系图,其中ZIF-8/C60-C具有最大的斜率即双电层电容值Cdl(30 mF cm-2).根据式(2)可知(其中,Cs为比电容,S为有效电极面积,通常取值20~60μF)[18]:较大的比电容意味着较大的电化学活性面积.
ECSA=Cdl/Cs*S
(2)
由此计算得ZIF-8/C60-C、ZIF-8-C和ZIF-8/C60三个样品的ECSA分别为56.55 cm2、33.57 cm2、24.74 cm2,因此,ZIF-8/C60-C催化剂相比于ZIF-8-C和ZIF-8/C60具有更大的电化学活性面积,说明富勒烯碳笼不仅使催化剂的晶粒度变小,碳化后石墨化程度提高,并且暴露了更多的催化活性位点.
图7(e)为电化学阻抗谱(EIS),从谱图可以得出ZIF-8/C60-C、ZIF-8-C和ZIF-8/C60三者的电荷转移电阻(Rct)分别为15.2 Ω、23.5 Ω和56.3 Ω,较小的电阻表明ZIF-8/C60-C催化剂具有更快的电荷传输能力,这也进一步证实了其优异的催化性能.
催化剂的稳定性是评价其使用寿命的一个指标[19].从图7(f)可以看出,ZIF-8/C60-C催化剂的极化曲线在2 000圈CV扫描后基本没有明显的衰退,说明该催化剂具有良好的催化稳定性.电流-时间曲线(图7(g))表明该催化剂在循环使用6个小时后催化性能依然没有下降,进一步证明了该催化剂性能稳定性.

(a)三个样品的LSV曲线
3 结论
本文通过共沉淀法制备了ZIF-8/C60复合物,经过高温煅烧获得了多孔碳电催化剂ZIF-8/C60-C,研究了该催化剂在碱性电解水析氧反应中的催化性能.
结果表明,相比于ZIF-8-C和ZIF-8/C60,ZIF-8/C60-C具有最小的析氧过电位,最小的Tafel斜率,当电流密度为10 mA cm-2时,其所需过电位仅为0.42 V.电化学阻抗谱研究发现ZIF-8/C60-C良好的催化性能得益于其较小的电荷转移电阻,说明富勒烯的引入改善了复合材料的导电性.
同时,富勒烯还增大了ZIF-8/C60-C的电化学活性面积,暴露了更多的活性位点,证明富勒烯在制备ZIF-8/C60-C复合电催化剂中具有重要的协同催化效应.此外,该催化剂表现出了良好的循环稳定性,可以连续稳定工作6 h,这有利于该催化剂的市场化应用.本论文的研究结果可为制备碳基纳米复合电催化剂提供有益的参考和借鉴.

