HPLC法测定疏肝胶囊中丹参素的含量
杨建刚,李吟平,麻纪斌,张俏
(1.陕西医药控股医药研究院有限公司,陕西 西安 710075;2.陕西中药研究所,陕西 西安 712000)
疏肝胶囊由山楂、丹参、泽泻、决明子等药材经过提取、浓缩、精制而制成的复方制剂,具有降脂护肝、改善肝脏代谢的功效,其中丹参为方中君药,现代药理研究表明,丹参对具有动脉硬化实验动物有降低肝脂的作用[1-2]。丹参中有效成分有丹参酮ⅡA、丹参素等[3-4]。丹参酮ⅡA、丹参素都可以作为本复方制剂中丹参的含量控制指标。但丹参素相对于丹参酮ⅡA更稳定,并同样具有扩张冠脉、降血脂、加强脂质代谢的作用[5]。故选用更稳定的丹参素作为复方制剂中丹参的控制指标。本研究通过对疏肝胶囊中丹参素检测方法进行验证,确保检测准确,进而保证疏肝胶囊质量可控。
1 实验部分
1.1 试剂与仪器
甲醇,色谱纯;甲醇、冰醋酸、盐酸、无水乙醇均为分析纯;丹参素钠(批号0752—9907,含量测定用),中国药品生物制品鉴定所。
Waters e2695高效液相色谱仪;AG-135电子天平;Cary50紫外分光光度计;H5150D超声波。
1.2 溶液配制
1.2.1 对照品溶液的制备 称取经干燥过的丹参素钠对照品适量,至棕色量瓶中,加色谱纯甲醇溶解,定容,制成每1 mL含0.08 mg(相当于每1 mL含丹参素0.072 mg)的溶液,作为对照品溶液。
1.2.2 供试品溶液的制备 取疏肝胶囊内容物研细,精密称取2.0 g,置50 mL棕色量瓶中,加水适量,超声30 min,放冷,过滤于50 mL棕色量瓶,加水至刻度,摇匀,作为供试品溶液。
1.2.3 阴性对照溶液的制备 按疏肝胶囊处方比例及工艺参数制备缺少丹参药材的样品,按照供试品溶液制备方法制成阴性对照溶液。按检测丹参素的色谱条件测定,结果显示阴性对照溶液在丹参素色谱峰相应的保留时间处无色谱峰,表明疏肝胶囊样品丹参素检测杂质无干扰。
1.3 实验方法
1.3.1 色谱条件 色谱柱为Kromasil C18(150 mm×4.6 mm,5 μm),流动相为甲醇-0.4%醋酸溶液(5∶95),流速1.0 mL/min,检测波长280 nm,柱温30 ℃,进样量10 μL。理论板数按丹参素峰计算应不低于2 000。
1.3.2 测定法 按照检测丹参素的色谱条件,分别吸取丹参素对照品溶液与疏肝胶囊供试品溶液各适量于2 mL进样瓶中,采用自动进样,进样量10 μL,记录相应色谱图,按外标法以峰面积计算样品含量。对照品和供试品高效液相色谱图见图1。
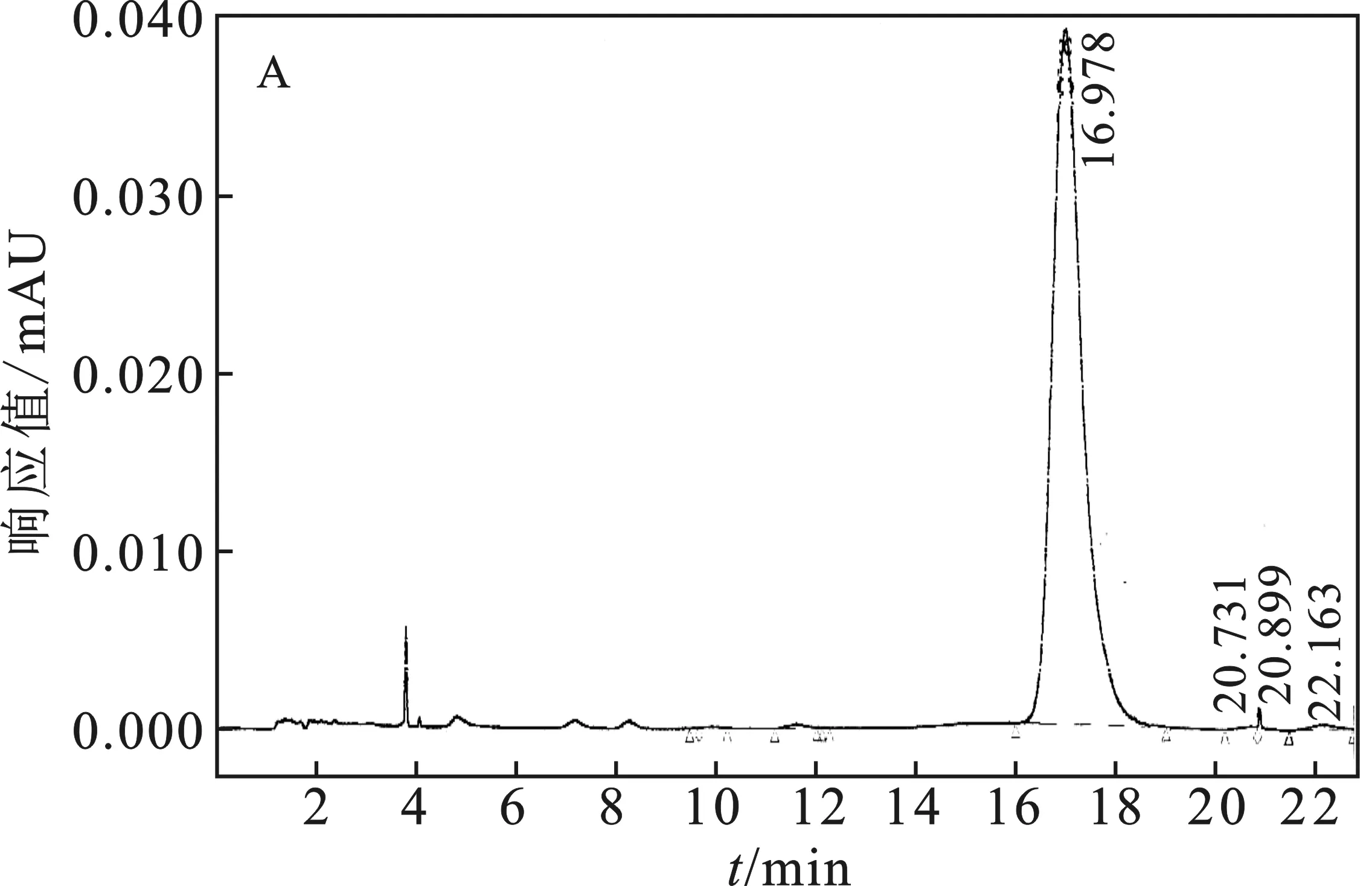

图1 标准品、供试品和阴性对照色谱图Fig.1 Standard(A),sample(B) and negative control chromatogram A.标准品色谱图;B.供试品色谱图
2 结果与讨论
2.1 扫描波长确定
取丹参素钠对照品适量,用甲醇配制对照品溶液(0.80 mg/mL),以甲醇为空白,进行波长扫描,最大吸收波长为280 nm。故本方法选择280 nm为丹参素钠检测波长。
2.2 流动相选择
试用了甲醇-水(50∶50)、乙腈-水(5∶95)等为流动相检测丹参素,色谱峰与相邻峰分离度<1.5,最终本方法选用甲醇-0.4%醋酸溶液(5∶95)为流动相,分离效果很好,分离度>1.5。
2.3 丹参素测定的方法学验证
2.3.1 线性关系的考察 精密称取丹参素钠对照品14.00 mg(相当于丹参素12.60 mg),用蒸馏水溶解并定容于50 mL棕色量瓶中(丹参素0.252 mg/mL),作为储备液。分别吸取1.0,2.0,3.0,5.0,8 mL于 10 mL 容量瓶中,用水定容,作为丹参素标准系列溶液进行高效液相检测,结果见表1。以丹参素色谱峰对应的浓度(X)为横坐标,对应峰面积(Y)为纵坐标,丹参素回归方程为Y=6.167×106X-4.337×103,相关系数r=0.999 9(n=5)。结果表明,丹参素对照品在0.025 2~0.201 6 mg/mL浓度范围,丹参素对照品浓度与峰面积之间呈现良好线性关系。

表1 丹参素线性实验Table 1 Danshensu linear test
2.3.2 精密度实验 吸取丹参素对照品溶液与疏肝胶囊供试品溶液各适量分别于2 mL进样瓶中,采用自动进样,进样量10 μL,对照品溶液和供试品溶液分别连续进样5次,记录峰面积,计算RSD值,结果见表2、表3。
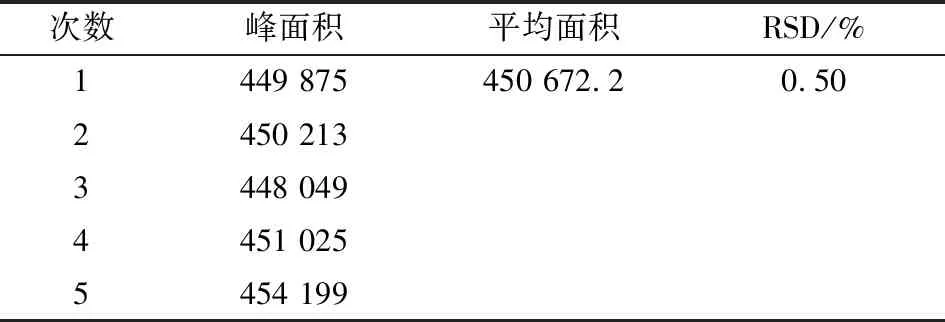
表2 丹参素对照品溶液精密度Table 2 Precision of Danshensu control solution
由表2可知,丹参素钠标准溶液精密度实验良好,RSD 0.50%。
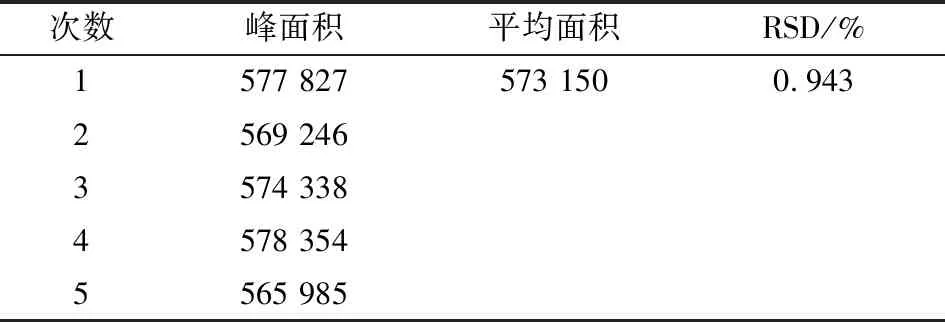
表3 疏肝胶囊供试品溶液精密度Table 3 Precision of test solution of Shugan capsule
由表3可知,疏肝胶囊供试品溶液精密度实验良好,RSD 0.94%。
2.3.3 溶液稳定性实验 吸取丹参素对照品溶液与疏肝胶囊供试品溶液各适量分别于2 mL进样瓶中,采用自动进样,进样量10 μL,对照品溶液和供试品溶液分别在0,1,2,6,12 h进样,记录峰面积,计算RSD值,结果见表4、表5。

表4 丹参素对照品溶液稳定性实验Table 4 Stability test of Danshensu control solution
由表4可知,丹参素钠标准溶液在12 h内稳定,RSD
1.06%。
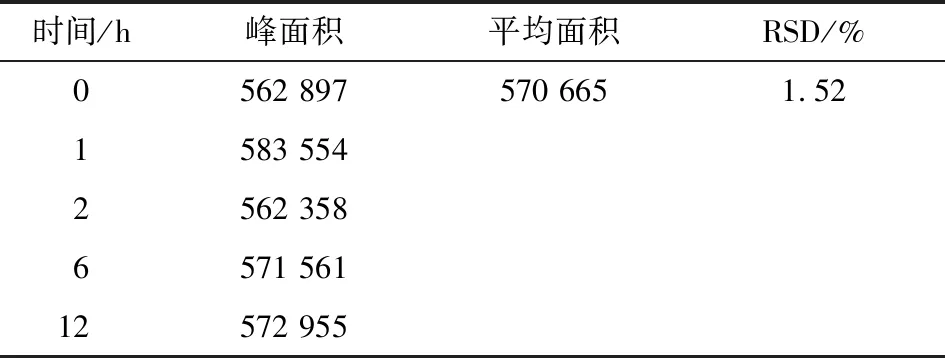
表5 疏肝胶囊供试品溶液稳定性实验Table 5 Stability test of test solution of Shugan capsule
由表5可知,疏肝胶囊供试品溶液在12 h内稳定,RSD
1.52%。
2.3.4 重现性实验 取批号20190321疏肝胶囊样品,取出内容物研细,分别配制5份供试品溶液,色谱条件进行测试,记录峰面积,按照外标法计算供试品含量,结果见表6。
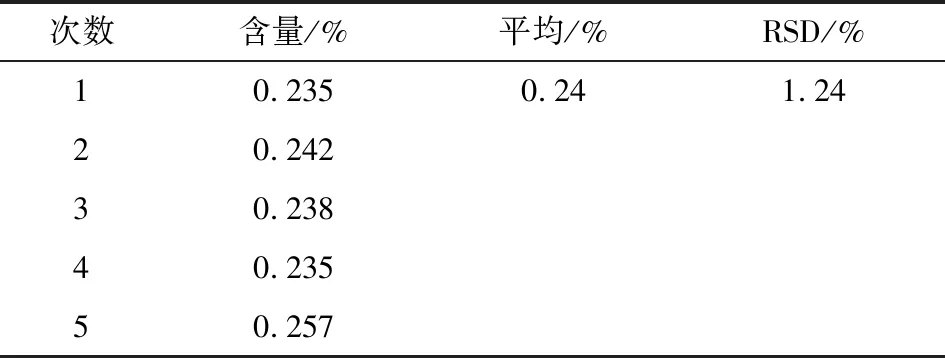
表6 重现性实验Table 6 Reproducibility test
由表6可知,疏肝胶囊供试品中丹参素平均含量为0.24%,RSD
1.24%,重现性良好。
2.3.5 加样回收实验 取疏肝胶囊样品(批号20190321,含量0.24%),取出内容物,研细,配制供试品储备液,浓度0.094 4 mg/mL,精密量取疏肝胶囊储备液5 mL于10 mL棕色容量瓶中(量取6份分别于6个10 mL棕色容量瓶中),同时分别精密加入对照品溶液(丹参素0.252 mg/mL)2 mL,加水稀释并定容。按色谱检测方法进行6次回收实验,记录峰面积,用外标法计算每份溶液丹参素总量,并分别计算每份溶液回收率,结果见表7。
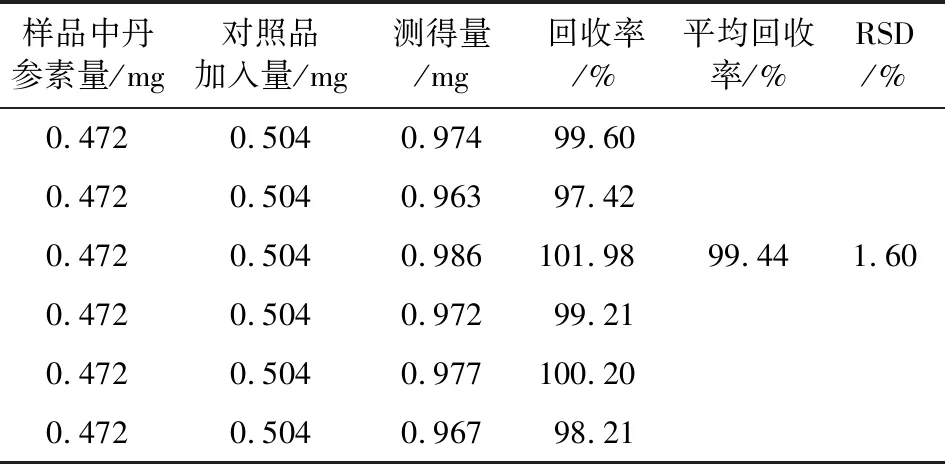
表7 回收率实验结果(n=6)Table 7 Results of recovery experiment
由表7可知,丹参素含量的回收率在97.42%~101.98%之间,RSD值1.60%,回收率良好。
2.4 三批疏肝胶囊含量测定
经过方法学的验证实验,证明该方法可以用于疏肝胶囊中丹参素含量的测定,因此按色谱条件,对20181025,20190321,20190416三批成品测定,结果见表8。
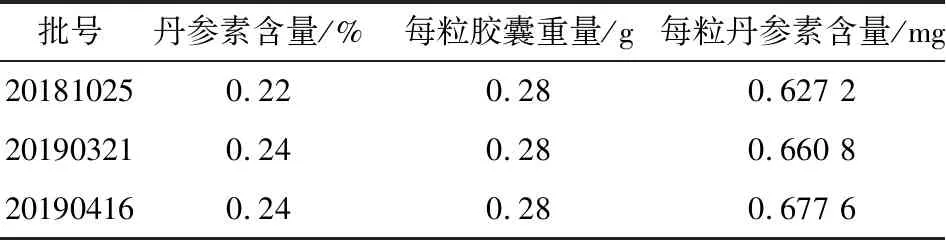
表8 三批样品含量测定Table 8 Determination of three batches of samples
由表8可知,三批成品丹参素含量稳定。
3 结论
采用高效液相色谱测定疏肝胶囊中丹参素的含量,色谱柱为Kromasil C18(150 mm×4.6 mm,5 μm),流动相为甲醇-0.4%醋酸溶液(5∶95),流速1.0 mL/min,柱温30 ℃,检测波长为280 nm。疏肝胶囊供试品溶液在12 h内稳定。方法的检测结果准确,操作简便,重现性好,可用于疏肝胶囊中丹参素的质量控制。

