聚合物类阻垢剂在海水中的可生物降解性
周筝,李亚红,赵小芳,樊利华
(自然资源部天津海水淡化与综合利用研究所,天津 300192)
可生物降解性是评价阻垢剂环境友好性的重要指标之一。目前对阻垢剂生物降解性的研究一般采用活性污泥或花园土为接种物,以淡水配制实验培养基,缺少直接以海水利用工程废水排放受纳水体——海水为实验介质的研究报道。但早在1981年de kreuk and Hanstveit[1]就指出,化学品在淡水和海水介质中的生物降解性可能存在差异。为此,直接以海水利用工程废水排放受纳水体——海水为实验介质和接种物,开展阻垢剂在海水中的生物降解性研究,还是有其必要性的,其可以更为直观地反映阻垢剂对海洋环境的影响,相关研究结果也可为今后开展海水利用工程排放阻垢剂海洋环境风险评价提供数据支持。
1 实验部分
1.1 材料与仪器
受试物为5种聚合物类阻垢剂,分别是聚天冬氨酸(PASP)、聚环氧琥珀酸(PESA)、聚丙烯酸(PAA)、聚环氧琥珀酸接枝聚丙烯酸(PESA-g-PAA)、丙烯酸-丙烯磺酸共聚物(AA-SAS)均为工业品;海水样品,采样于浙江宁海电厂取水口附近海域。
Multi N/C总有机碳/化合态氨分析仪。
1.2 接种物的制备方法
海水样品依次经滤纸、0.45 μm微孔膜过滤后,采用0.22 μm微孔膜过滤浓缩法,对海水样品进行浓缩,制备细菌浓缩液作为接种物。将浓缩接种物和未浓缩的海水样品同时置于黑暗下,于(20±2)℃振荡培养1周,以去除样品中的有机物。按照GB 17378.6—2007,采用平皿计数法测定样品中的细菌含量。按照GB 17378.4—2007,采用总有机碳/化合态氨分析仪检测样品中的TOC含量。
1.3 生物降解实验
OECD 301B适用于淡水体系,采用活性污泥和蒸馏水制备接种物和实验培养基,评估的是有机化学品的完全矿化能力。本文模拟海水环境,评估有机化学品在海水中降解为CO2的能力,对OECD 301B进行了部分修改,即以含菌量104~105CFU/mL的浓缩海水作为接种物,以海水配制实验培养基,按20%接种量配制含菌实验液3 L。将受试物定量加入到3 L实验液中,控制有机碳浓度为20 mg/L。将水样于(25±2)℃下避光放置,以50 mL/min的速度向水样中连续通入脱CO2的空气,并用0.012 5 mol/L的Ba(OH)2溶液分级吸收水样产生的CO2。定时用0.1 mol/L的HCl溶液滴定吸收瓶中Ba(OH)2的剩余量,计算CO2的产生量。同时设不加受试物的含菌水样作空白对照。每一实验组和空白组均设置双平行样。
1.4 非生物降解实验
以邻苯二甲酸氢钾为参比物。向无菌海水中定量加入邻苯二甲酸氢钾,使其有机碳浓度为 20 mg/L。将水样于(25±2)℃下避光、密闭放置 3 d。分别于放置前、后用0.1 mol/L标准NaOH溶液滴定水样中邻苯二甲酸氢钾的浓度。实验设两个平行样。无菌海水的制备方法如下:采用0.22 μm微孔滤膜对1.2节中除有机物的海水样品进行2次过滤除菌处理后,保存于经高温高压灭菌的容器中备用。过滤水采用吖啶橙荧光检测,达到无菌要求。
1.5 数据处理
取平行样的平均值作为实验结果,计算有机物的生物降解率:
(1)
式中Dt——至t时刻有机物的生物降解率,%;
mt——至t时刻产生的CO2累积量,mg;
m0——初始加入的TOC量,mg;
3.67——以C转换成CO2的系数,44/12。
有机物在环境中的降解通常遵循一级动力学方程,即降解残留率和降解时间之间存在方程(2)的关系:
ln(1-Dt)=-kt
(2)
t1/2=ln2/k
(3)
其中,k为降解速率常数,t为反应时间。降解速率常数(k)和半衰期(t1/2)通常被用来表征有机物降解难易程度。
2 结果与讨论
2.1 参比物在海水中的降解性
用无菌蒸馏水配制的有机碳浓度为20 mg/L的邻苯二甲酸氢钾溶液在避光、密闭保存一段时间后,用标准氢氧化钠溶液测定最初和结束时的邻苯二甲酸氢钾浓度,结果显示,邻苯二甲酸氢钾在无接种菌和避光的情况下,3 d内的降解率为0.41%,几乎不发生降解,因此可以采用邻苯二甲酸氢钾作为参照物,进行生物降解评价方法研究。
经有机物去除处理后,浓缩海水和未浓缩海水的含菌量分别为4.3×106CFU/mL和1.4×104CFU/mL,DOC含量分别为1.013 mg/L和 0.715 mg/L。分别配制含菌量约为105CFU/mL和106CFU/mL的实验液,评估参比物邻苯二甲酸氢钾在海水中的生物降解性,结果见图1。
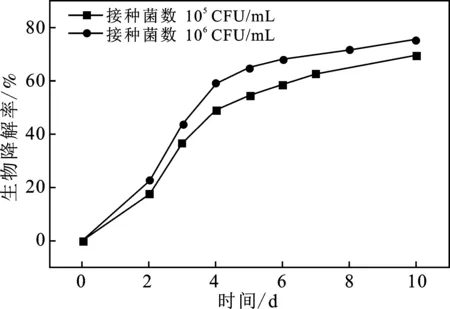
图1 邻苯二甲酸氢钾在海水中的生物降解性Fig.1 Biodegradation of potassium biphthalate in seawater
由图1可知,当海水中的细菌接种量达到105~106CFU/mL时,邻苯二甲酸氢钾10 d时的生物降解率均可达60%以上,说明本实验体系满足OECD 301B的质量控制要求,实验方法可行。
2.2 受试阻垢剂在海水中的生物降解性
由图2可知,5种受试阻垢剂在海水中均发生了生物降解。PASP、PESA、PESA-g-PAA和AA-SAS在海水中经历的降解停滞期3~5 d。至28 d实验结束时,仅有PASP的生物降解率>60%,达到严格定义上的通过水平,具有快速降解性;PESA在实验延长至31 d时降解率达到60%;其余3种受试阻垢剂至28 d实验结束时降解率均低于35%,说明其在海水中均不具有快速生物降解性[2]。PASP和 PESA 在分子主链上分别插入了N和O原子,因此其在海水中的生物降解率明显高于其他3种受试阻垢剂。按照OECD 301B对受试阻垢剂在海水中的生物降解性进行评价,结果见表1。
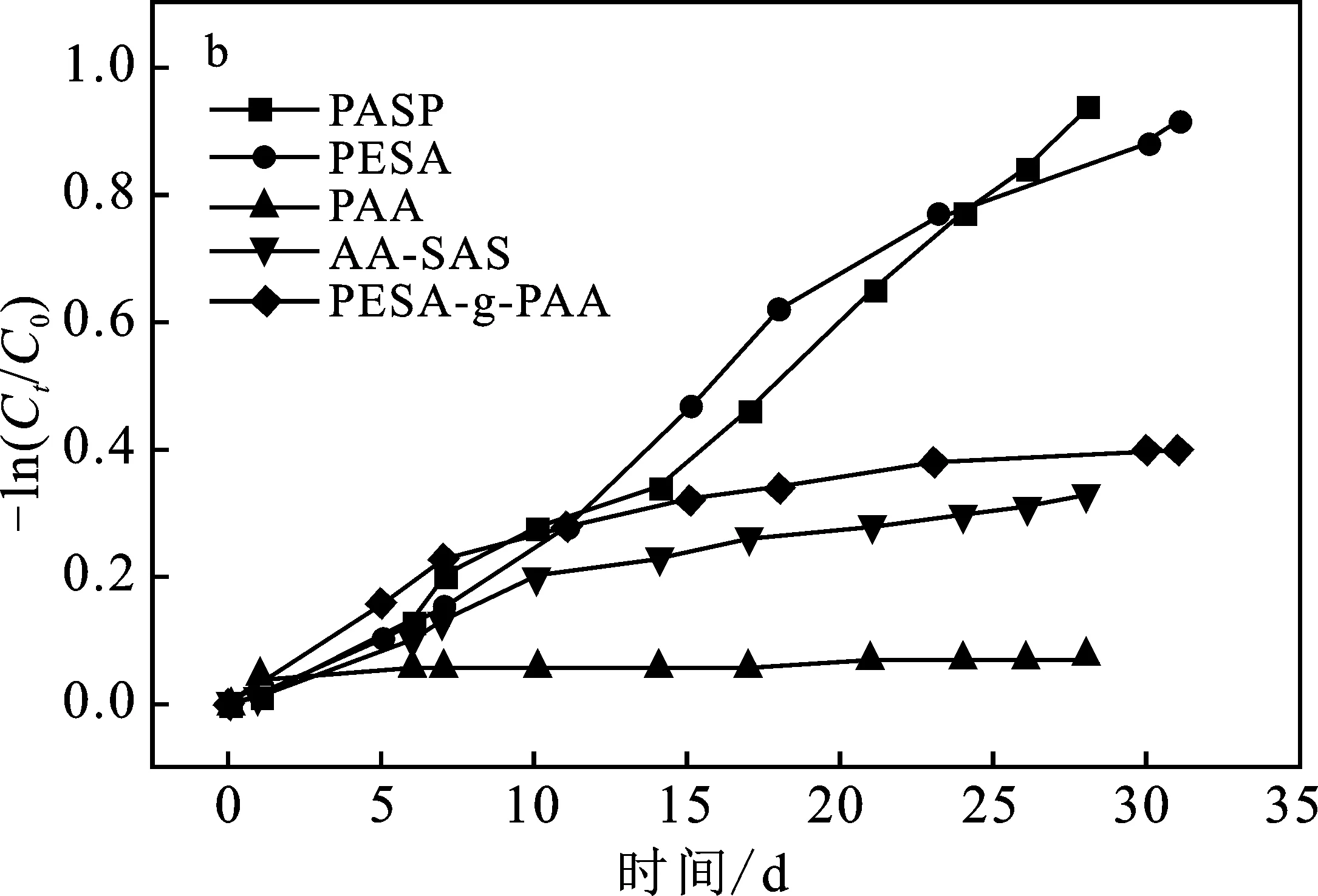
图2 受试阻垢剂在海水中的生物降解性Fig.2 Biodegradability of tested scale inhibitors in seawater a.生物降解率;b.降解残留率
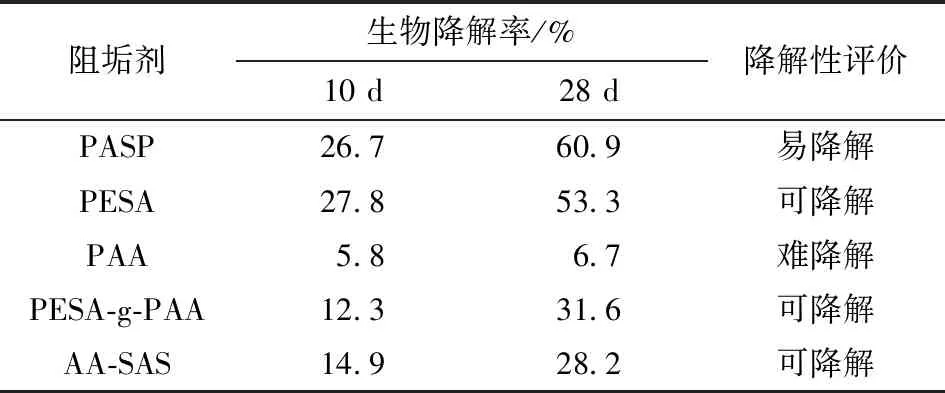
表1 受试阻垢剂在海水中的生物降解性评价Table 1 Biodegradability of tested scale inhibitors in seawater
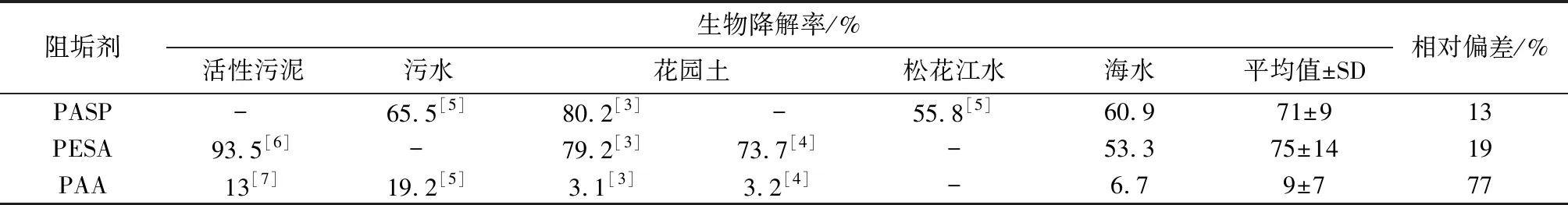
表2 三种受试阻垢剂在淡水和海水中的生物降解性比较Table 2 Comparison of biodegradability of tested scale inhibitors in fresh water and seawater
由表2可知,PASP、PESA和PAA在海水中的生物降解性评价结果与文献报道在淡水中的基本一致[3-7],但其降解率低于文献报道实验结果。黄远星等曾对10种不同来源的PASP的生物降解性进行实验评价,结果显示各种PASP的降解率相对偏差达22%[8]。陶虎春等分别采集松花江水和污水处理厂污水制备接种物,研究不同来源接种物对相同来源的PASP的降解率,实验结果相对偏差约11%[5]。杨莹琴等研究结果显示,营养盐中N/P比显著影响PESA的生物降解率[4]。同样采用花园土制备接种物,PESA在不同实验室的生物降解率相差5.5%。由此可见,受试物来源、接种物来源和实验培养基等因素均可对化学品的生物降解性产生影响,其中尤以受试物的来源影响显著,其次是接种物的来源。活性污泥是一种优良的微生物接种物,含有包括细菌、原生动物和藻类在内的丰富的微生物群体,对不同碳源具有良好的适应性和耐受性。相对来说,本文所用接种物经多次过滤处理后,其中的微生物种群多样性和生物体完整性都可能遭到破坏,导致其生物活性下降,造成其对有机物的利用能力下降。此外,季节和海域的差异,也可能导致海水样品差异较大,最终导致实验结果出现较高偏差和较低生物降解率[9]。综上,考虑到不同海水样品的差异性,寻找一种如同活性污泥一样,微生物组成相对稳定的海水接种物将更有利于研究有机物在海水中的生物降解性。
2.3 受试阻垢剂在海水中的降解动力学
对图2b进行回归分析发现,除PAA外,其余4种受试阻垢剂在海水中的生物降解曲线均符合一级动力学模型,其拟合方程及拟合度R2见表3。由降解速率常数(k)和半衰期(t1/2)可知,5种阻垢剂在天然海水中的降解从易到难的顺序是PASP>PESA>PESA-g-PAA>AA-SAS>PAA。其中,PASP和PESA的降解速率相当,kPASP∶kPESA=1.02,半衰期基本相同;PAA是5种阻垢剂中降解速率最慢的化合物,k值仅是PASP和PESA的1/10,其线性拟合度较低。kAA-SAS∶kPAA=5,说明AA-SAS的生物降解速率约是PAA的2倍,丙烯磺酸的生物降解性要好于丙烯酸。

表3 受试阻垢剂在海水中的降解动力学参数Table 3 Biodegradation kinetic parameter of tested scale inhibitors in seawater
2.4 接枝改性对聚合物阻垢剂生物降解性的影响
官能团的单一往往导致性能单一,因此近年来,为提高PASP和PESA的性能,改善其对不同垢物的抑制作用,PASP和PESA合成改性研究渐成热点。赵军平研究显示,在PASP中引入磺酸基后,接枝改性共聚物对磷酸钙垢的阻垢效果得到明显改善,且磺酸基引入量越多,阻垢性能越好,但生物降解性却逐渐降低,磺酸基与PASP的比例在0.2时生物降解率下降约30%,比例在1时下降约50%[10]。本次实验中所用PESA-g-PAA是在PESA分子中引入PAA,这一改性虽有效改善了PESA对CaCO3和CaSO4的阻垢性能[11],但却同时影响了PESA的生物降解性,降解率降低约21.7%,降解速率降低约50%(见表1和表2)。由此可见,接枝改性虽然有效改善了易降解阻垢剂PASP和PESA的阻垢性能,但对其生物降解性的影响也很明显,影响程度受引入的功能性官能团的类型和数量制约,被引入的官能团降解性越好,影响越小;引入数量越少,影响越小。换言之,接枝改性仅是单体的键合,但不能改变单体本身的生物降解性。改性PASP和PESA的生物降解性仍然主要由PASP和PESA贡献,因此,PASP和PESA在接枝改性产物中的占比越高,其生物降解性受影响越小。这也说明,在对易降解阻垢剂PASP和PESA进行结构改性研究中,应注意寻求性能改善和生物降解性损失之间的平衡,不能仅关注性能改善而忽略对其生物降解性的影响,尽量保持改性PASP和PESA仍具有良好的生物降解性。
3 结论
(1)以浓缩海水制备接种物,以天然海水配制实验培养基,修改OECD 301B方法,测得的受试阻垢剂的生物降解性评价结果与文献相同,但降解率略低于文献结果,其原因可能在于采用的接种物不同。文献采用的接种物活性污泥是一种具有优良生物活性的多种群微生物群体,本文采用的浓缩海水在物种多样性和生物活性等方面可能因多次过滤处理而受到破坏,最终导致其对有机物的利用率下降,有机物的生物降解率随之下降。
(2)5种受试阻垢剂在海水中均具有一定的生物降解性,降解曲线均符合一级动力学模型。其中,聚合主链中分别插入N和O的PASP和PESA在海水中的生物降解率和降解速率常数均高于仅以 C—C 键聚合的PAA,说明N和O原子的插入,可有效改变有机物的生物降解性,PASP和PESA在海水中的生物降解性优于PAA。
(3)聚合物的完全矿化很大程度上依赖于聚合单体自身的生物降解性,改性PASP和PESA的生物降解性仍然主要由PASP和PESA贡献。因此,在对PASP和PESA进行改性研究中,应注意控制PASP和PESA的比例,尽可能保持改性PASP和PESA的良好生物降解性。

