清瘟解毒口服液质量控制试验
王 彬,章荣叶,汤赛飞,罗成江,陈晓林,林仙军
(1.浙江省动物疫病预防控制中心,浙江 杭州 311101 ;2.浙江省台州市农业综合行政执法队,浙江 台州 317700;3.浙江建安检测研究院有限公司,浙江 杭州 310006)
清瘟解毒口服液由地黄、栀子、黄芩、连翘、玄参和板蓝根通过一定的工艺制得[1],其主要活性成分有黄芩苷、栀子苷、连翘苷等,具有清热解毒的功效,临床主要用于鸡外感发热[2]。该品种检测标准收载于《兽药质量标准(2017年版)》中药卷[3],仅采用薄层色谱法分别鉴别黄芩苷、连翘苷和栀子苷3种物质,需要采用3种不同的鉴别方法,操作繁琐,既耗时耗力,又只能定性,不能准确测定其含量,无法满足对产品质量控制的要求。
高效液相色谱法快捷、准确、灵敏度高,定性和定量均准确。高效液相色谱-二极管阵列检测器法(HPLC-DAD)因其结合了光谱扫描和数据库功能,定性更准确,在中兽药质量控制中将发挥更大的优势。目前,国内有学者采用高效液相色谱法分别测定清瘟解毒口服液中的黄芩苷[4]和连翘苷的含量[4-5],未见同时对清瘟解毒口服液中黄芩苷、栀子苷和连翘苷3种有效成分进行检测的文献报道。本试验采用HPLC-DAD法对清瘟解毒口服液中栀子苷、黄芩苷和连翘苷同时检测的方法进行了研究,为清瘟解毒口服液质量控制提供数据。
1 仪器与材料
1.1 仪器 高效液相色谱仪,Agilent 1260,配Agilent 1260 Infinity G4212A型DAD检测器;AG-285电子天平(Mettler公司);DELTA320 pH计(Mettler公司);KQ-500E型超声波清洗器(昆山市超声仪器有限公司)。
1.2 试剂与材料 甲醇为分析纯;乙腈为色谱纯;磷酸、盐酸、氢氧化钠、30%双氧水均为分析纯;试验用水为milli-Q超纯水。黄芩苷对照品,来源中国兽医药品监察所,批号:Z0271705,含量96.8%;栀子苷对照品,来源中国食品药品检定研究院,批号:110749-201115,含量99.7%;连翘苷对照品,来源中国食品药品检定研究院,批号:110821-201514,含量93.5%。清瘟解毒口服液,100 mL/瓶,来源浙江施比龙生物科技有限公司,批号分别为20180101、20180102和20180103。
2 方法与结果
2.1 对照品溶液的配制 取黄芩苷对照品5.50 mg、连翘苷对照品9.90 mg和栀子苷对照品5.50 mg,置50 mL量瓶中,加甲醇适量,超声处理使溶解并稀释至刻度,摇匀制成对照品储备液。
2.2 供试品溶液的配制 量取供试品1.00 mL于100 mL量瓶中,用50%甲醇溶液适量稀释,超声处理5 min,再用50%甲醇溶液稀释至刻度,摇匀,作为供试品溶液。
2.3 色谱条件及系统适应性试验 采用Agilent Eclipse XDB-C18色谱柱(250 mm×4.6 mm,5 μm),流动相:0.05%磷酸溶液(A)和乙腈(B),梯度洗脱程序见表1;进样量10 μL,柱温30 ℃,流速为1.0 mL/min,用二极管阵列检测器进行扫描,扫描范围为190~400 nm,记录230 nm波长处的色谱图。该色谱条件下黄芩苷、连翘苷和栀子苷峰分离良好。对照品溶液典型色谱图见图1,光谱图分别见图2~4;供试品溶液典型色谱图见图5,光谱图分别见图6~8。
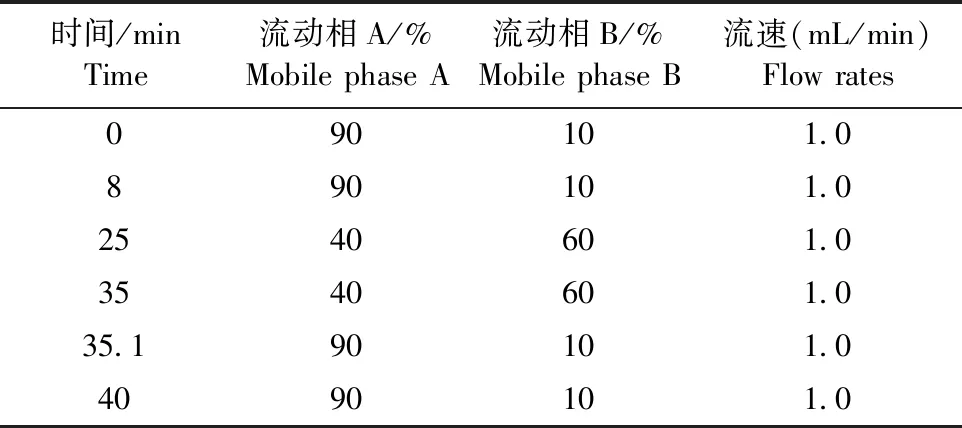
表1 流动相梯度洗脱程序表Table 1 Gradient mobile phase for HPLC
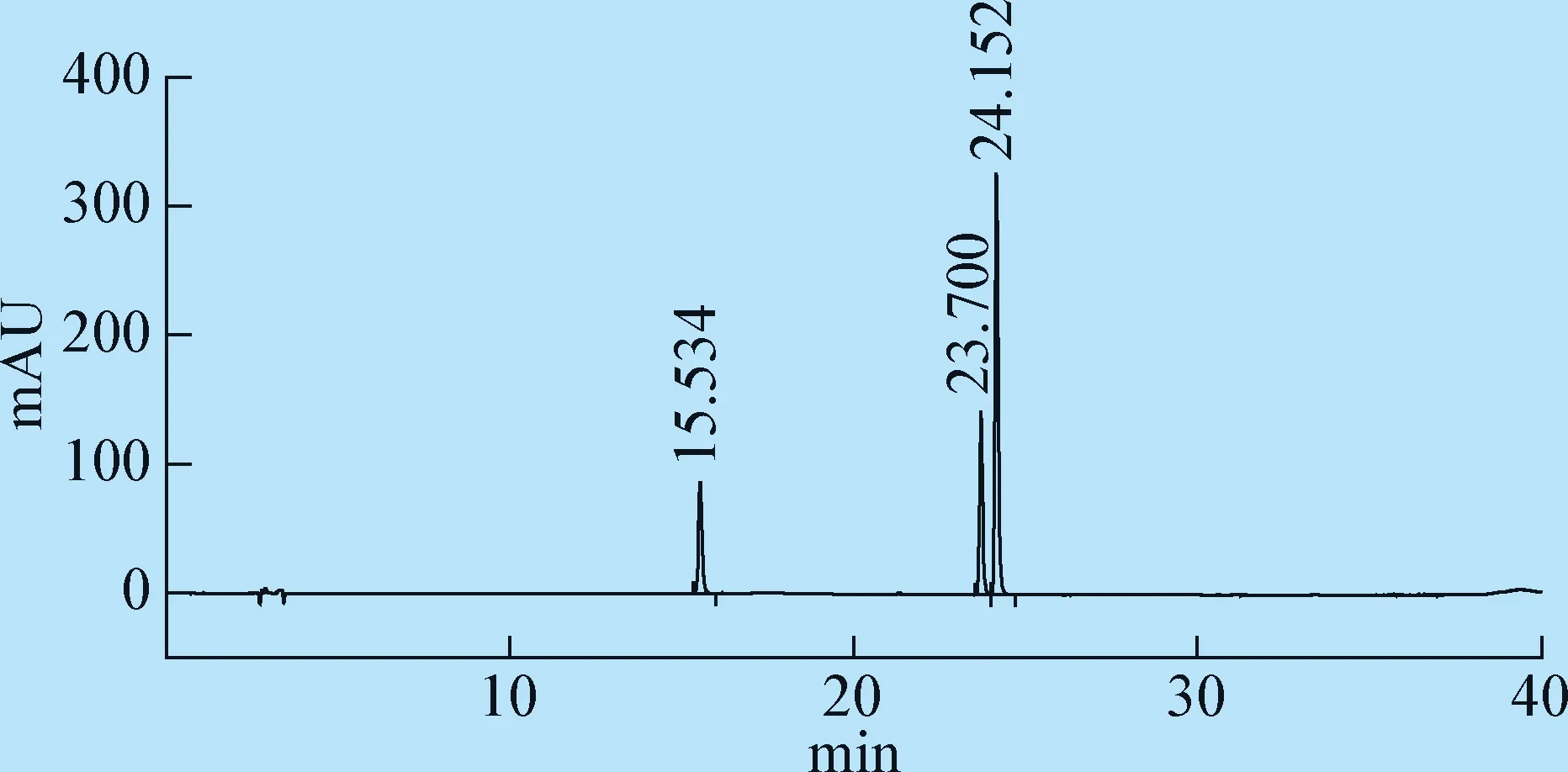
图1 黄芩苷、连翘苷和栀子苷对照品溶液色谱图Fig.1 Chromatogram of mix standard solution注:出峰顺序依次为栀子苷、黄芩苷和连翘苷Note:The order of peak was asminoidin,baicalin and phillyrin
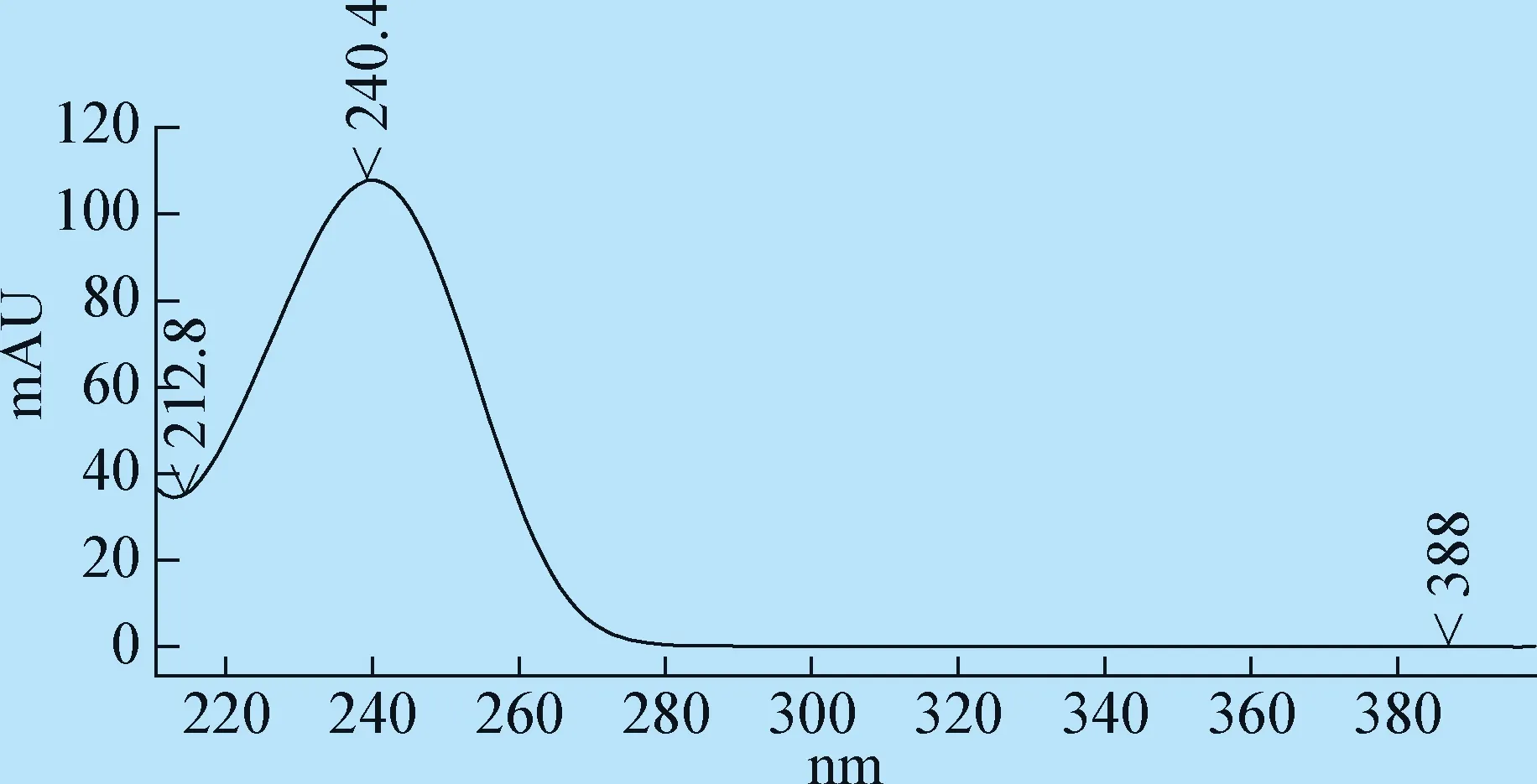
图2 栀子苷对照品溶液光谱图Fig.2 Spectroscopy of asminoidin solution

图3 黄芩苷对照品溶液光谱图Fig.3 Spectroscopy of baicalin solution

图4 连翘苷对照品溶液光谱图Fig.4 Spectroscopy of phillyrin solution
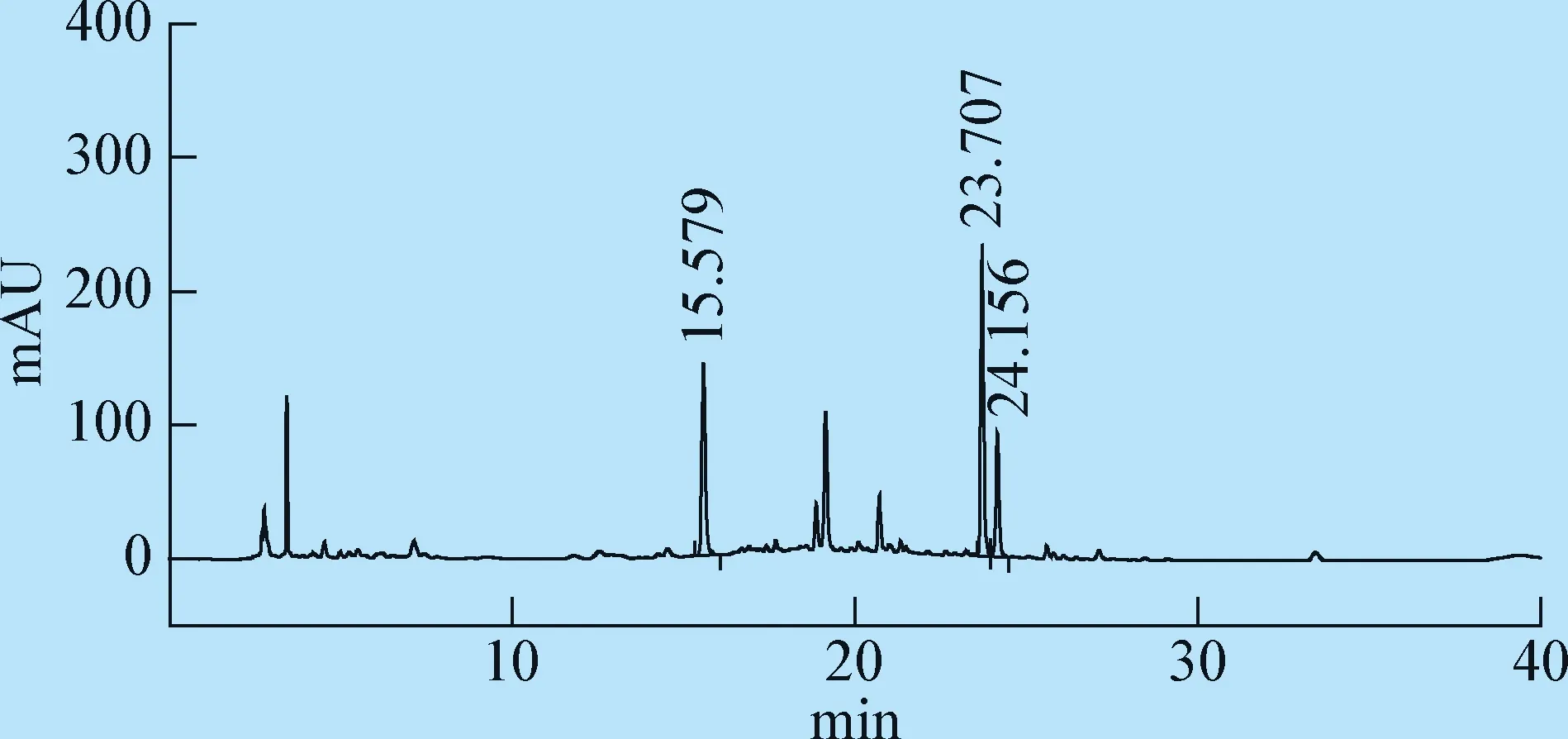
图5 清瘟解毒口服液色谱图Fig.5 Chromatogram of Qingwen jiedu oral liquid 注:出峰顺序依次为栀子苷、黄芩苷和连翘苷Note:The order of peak was asminoidin,baicalin and phillyrin
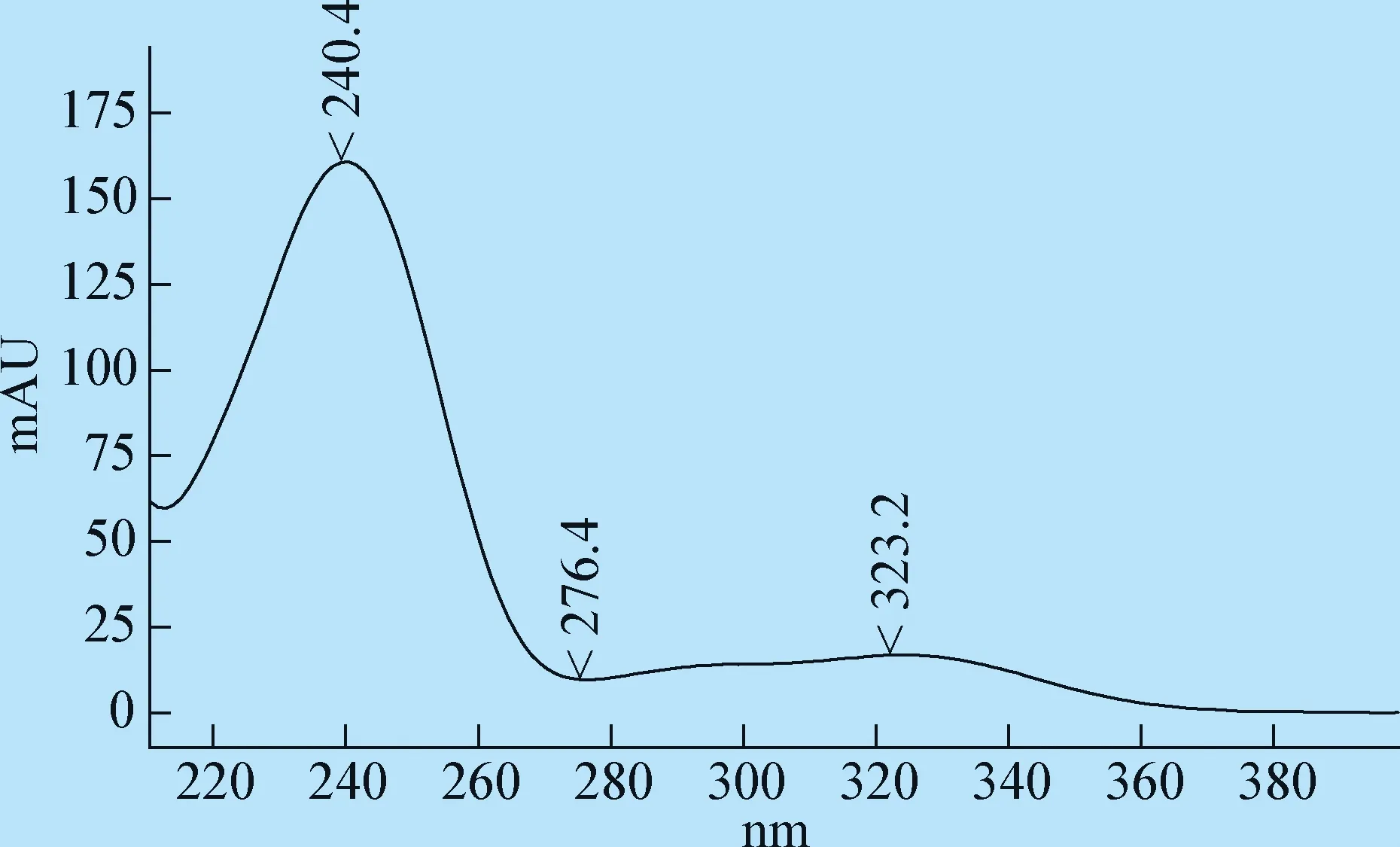
图6 清瘟解毒口服液中栀子苷光谱图Fig.6 Spectroscopy of asminoidin solution in Qingwen jiedu oral liquid
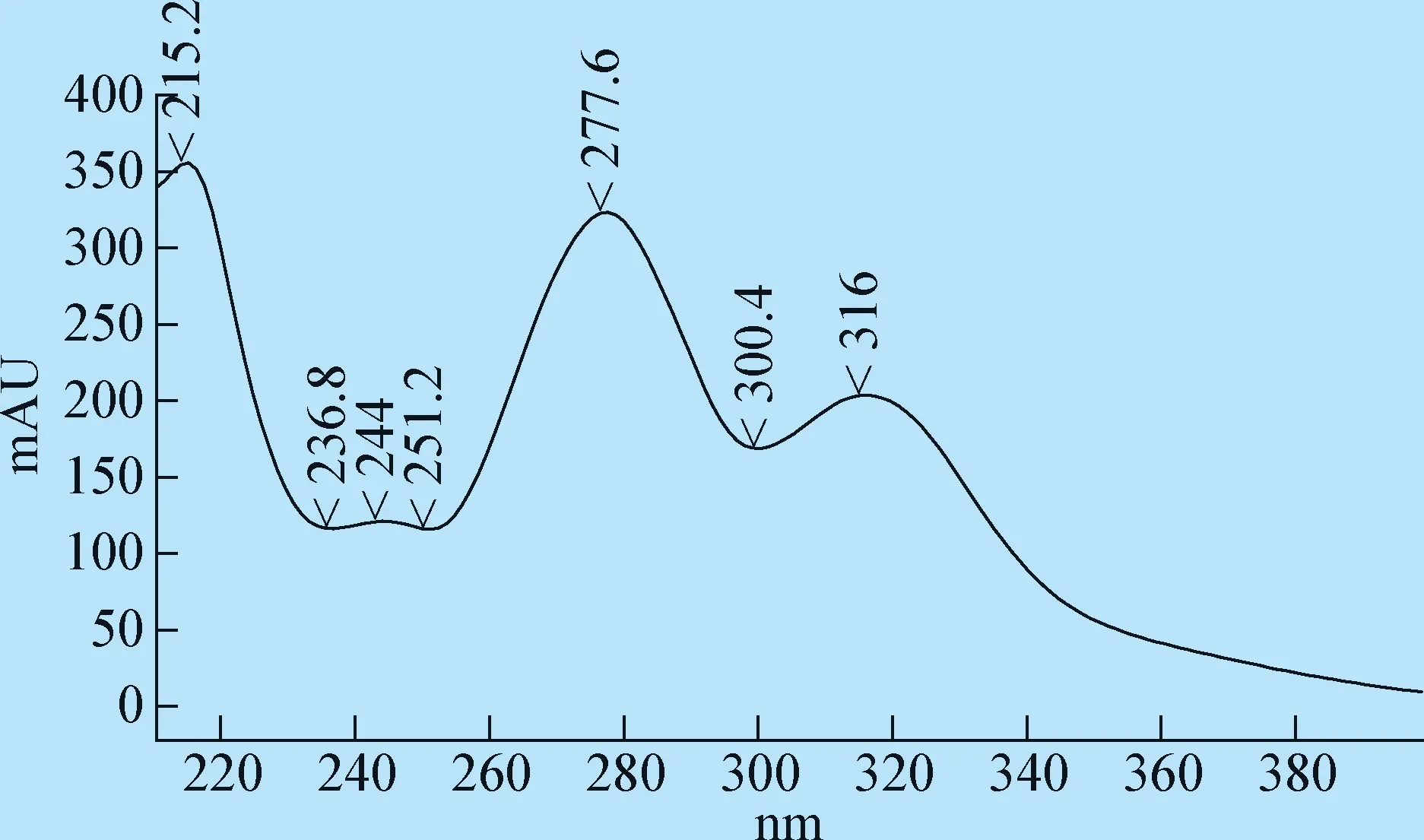
图7 清瘟解毒口服液中黄芩苷光谱图Fig.7 Spectroscopy of baicalin solution in Qingwen jiedu oral liquid
2.4 方法学考察
2.4.1 线性范围考察 精密量取对照品储备液适量,用50%甲醇分别稀释2、5、10、20倍和50倍。制成相应浓度的系列标准品溶液,从低浓度到高浓度依次进样分析,以浓度(X)为横坐标,峰面积(Y)为纵坐标,绘制标准曲线,得线性方程和相关系数结果见表2。
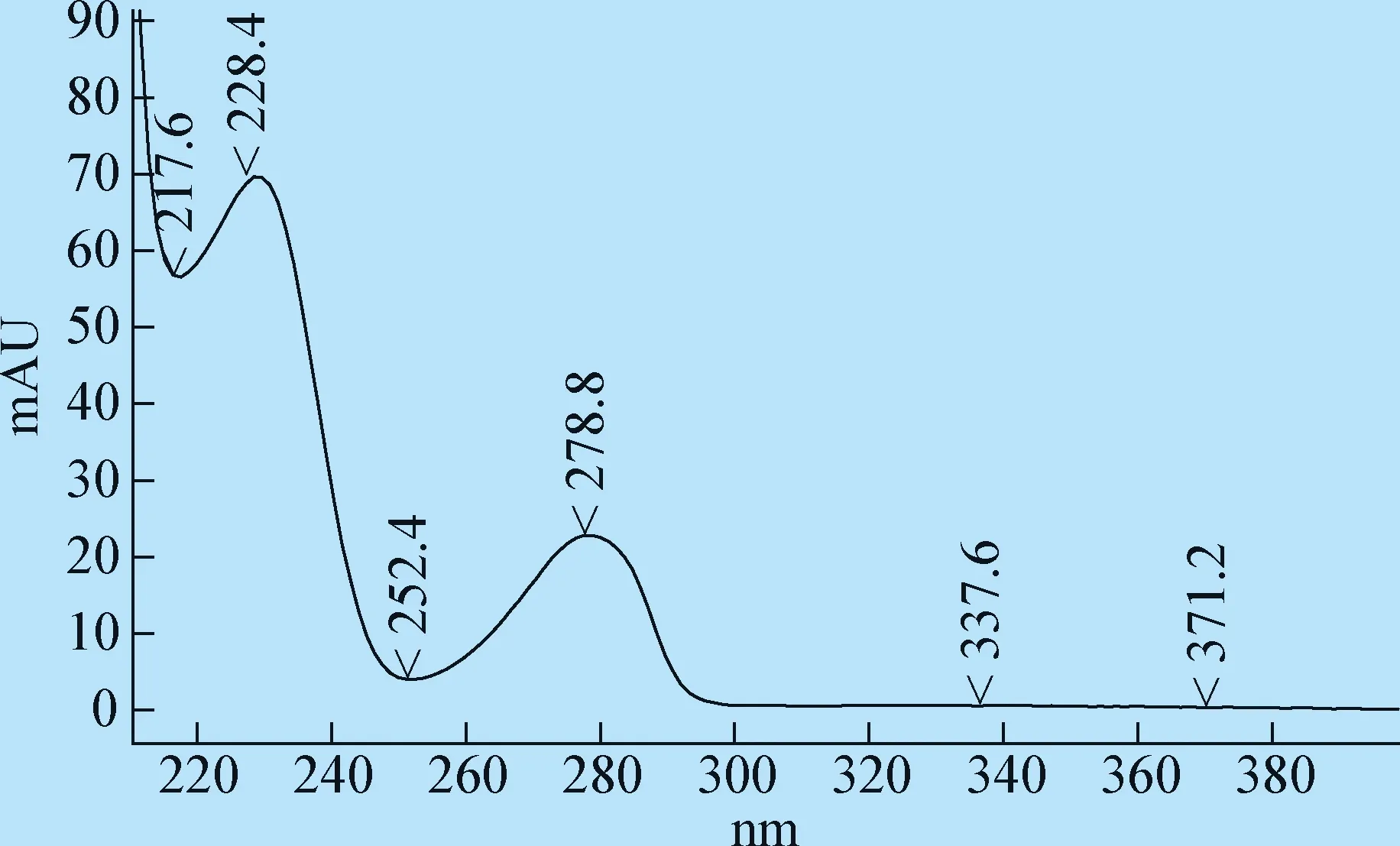
图8 清瘟解毒口服液中连翘苷光谱图Fig.8 Spectroscopy of phillyrin solution in Qingwen jiedu oral liquid
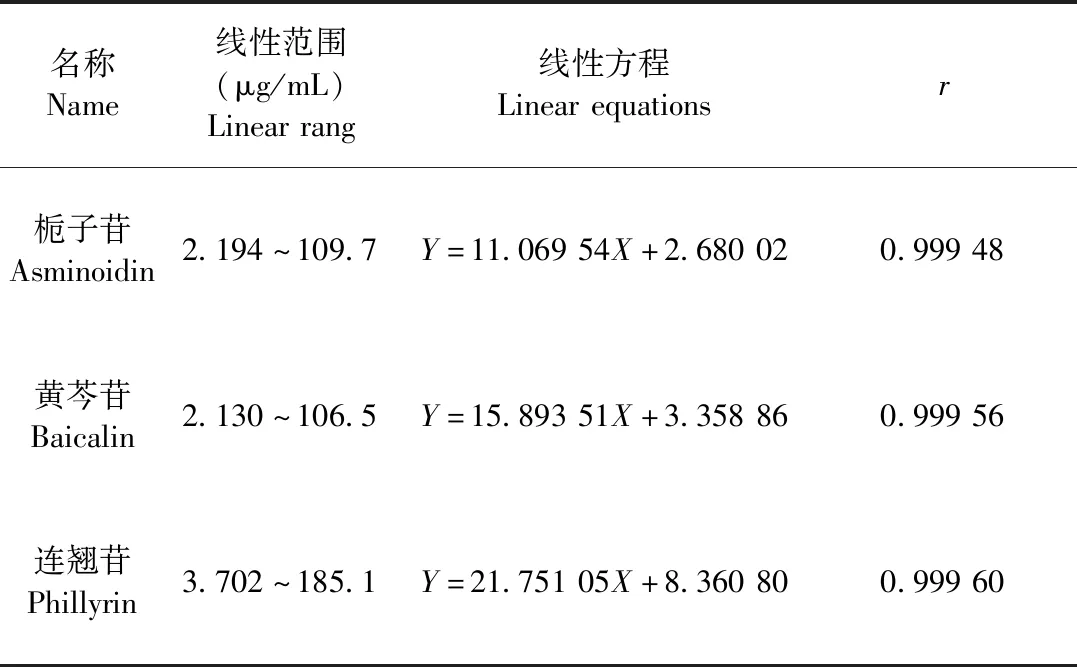
表2 栀子苷、黄芩苷和连翘苷标准曲线Table 2 Standard curve of baicalin,asminoidin and phillyrin
2.4.2 精密度试验 取批号为20180101清瘟解毒口服液供试品溶液,按上述色谱条件重复连续进样6次,测得栀子苷峰面积相对标准偏差为0.8%,测得黄芩苷峰面积相对标准偏差为0.5%,测得连翘苷峰面积相对标准偏差为1.2%。表明此方法的仪器精密度符合要求。
2.4.3 稳定性试验 取批号为20180101清瘟解毒口服液供试品溶液,分别于0、2、4、6、12 h和24 h进行测定,测得栀子苷峰面积相对标准偏差为0.6%,测得黄芩苷峰面积相对标准偏差为0.9%,测得连翘苷峰面积相对标准偏差为1.3%。表明供试品溶液稳定性良好。
2.4.4 方法专属性 取20180101清瘟解毒口服液各1 mL,置100 mL量瓶中,分别加1 mol/L盐酸溶液、1 mol/L氢氧化钠溶液和5%过氧化氢溶液各1 mL,放置1 h[6],用50%甲醇溶液定容,依法测定。栀子苷、黄芩苷和连翘苷在盐酸溶液和过氧化氢溶液均稳定,峰面积减少在3%以内;在氢氧化钠溶液中,连翘苷稳定,峰面积减少在3%以内,栀子苷减少了95%,黄芩苷减少了90%。
2.4.5 加样回收率试验 取栀子苷、黄芩苷和连翘苷各适量,加甲醇配制成约1 mg/mL的加样回收率试验溶液。另取批号为20180101的清瘟解毒口服液样品6份,各1.00 mL,分别精密加入加样回收率试验溶液各5 mL,置100 mL量瓶中,按照2.2项下方法制备供试品溶液,按“2.3”项下条件检测,结果扣除清瘟解毒口服液样品原有相应组分的量,计算平均回收率及RSD,结果见表3。
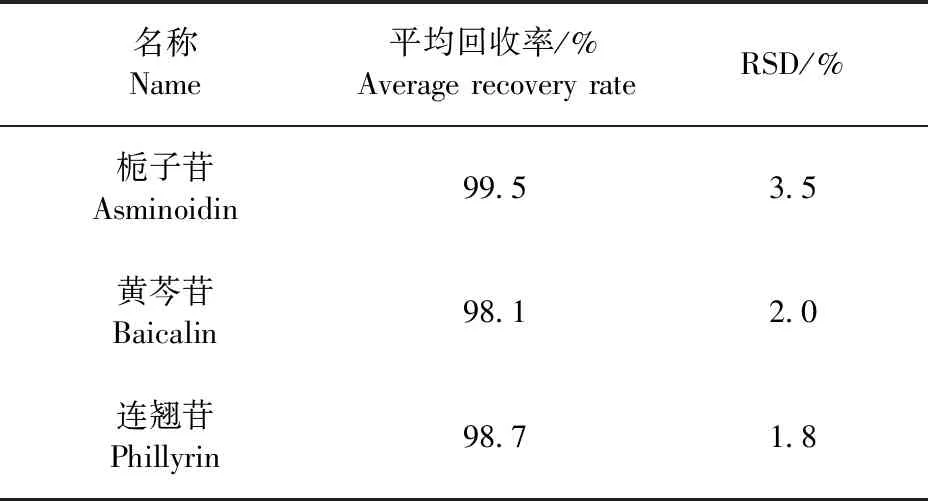
表3 栀子苷、黄芩苷和连翘苷回收率试验结果Table 3 Recovery of baicalin,asminoidin and phillyrin
2.4.6 实际样品的测定 取批号为20180101、20180102和20180103的清瘟解毒口服液3个平行,各1.00 mL,按照2.2项下方法配制供试品溶液,依法检测,记录色谱图,按外标法计算黄芩苷、连翘苷和栀子苷含量,结果见表4。
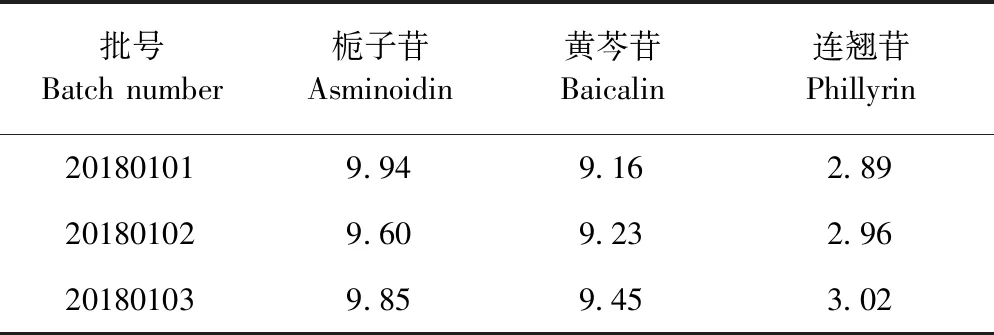
表4 样品中含量测定结果Table 4 Recovery of baicalin,asminoidin and phillyrin (mg/mL,n=3)
3 讨论
3.1 稀释溶剂的选择 本试验选择了甲醇、50%甲醇、20%甲醇等稀释溶剂进行测定,结果表明,稀释溶剂为甲醇时,栀子苷峰较宽,理论板数偏小,而用50%甲醇溶液稀释时,3种药物峰形尖锐、对称,分离度好。黄芩苷在甲醇中较易溶解,50%甲醇溶液的溶解度临界浓度在0.1 mg/mL左右,超声加热后可以溶解,冷却后有时会析出,导致浓度不准。因此,在对照品储备液的配制过程中,第一步是需要用甲醇溶剂,再用50%甲醇溶液稀释至需要的浓度,甲醇的含量需要保持50%左右,甲醇浓度太低不利于溶解,甲醇浓度太高峰形可能会不好。因此本试验选择50%甲醇溶液为提取溶剂。
3.2 检测波长 本试验采用DAD检测器对栀子苷、黄芩苷和连翘苷进行全波长扫描,结果发现,栀子苷在240 nm波长有最大吸收,黄芩苷在215 nm、277 nm、316 nm波长处有最大吸收,连翘苷在278 nm和220~240 nm处有最大吸收,综合考虑每个药物的响应值及杂质干扰因素,选择230 nm作为检测波长。
3.3 流动相的选择 参考《兽药质量标准2017年版》中黄芩苷的流动相,考察了乙腈和不同浓度磷酸溶液作为流动相。比较了乙腈与0.01%磷酸溶液、0.05%磷酸溶液、0.2%磷酸溶液和0.4%磷酸溶液作为流动相,各流动相保留时间和峰形一致,而乙腈-0.4%磷酸溶液pH值为1.5,乙腈-0.2%磷酸溶液pH值为1.7,pH值小于2.0对色谱柱损害较大;而乙腈-0.05%磷酸溶液pH值为2.3左右。因此,选择0.05%磷酸溶液-乙腈作为流动相,调节流动相比例,3种有效成分分离较好,保留时间比较合适。最后,确定梯度洗脱程序。
4 结论
本文采用HPLC-DAD法同时对清瘟解毒口服液中栀子苷、黄芩苷和连翘苷进行检测,对稀释溶剂、检测波长、专属性和色谱条件等进行试验,方法定性定量准确,可用于清瘟解毒口服液中3种有效成分的含量检测。

